
- DAZ.online
- DAZ / AZ
- DAZ 16/2014
- Neuer Wirkstoff bei PAH
Arzneimittel und Therapie
Neuer Wirkstoff bei PAH
Macitentan als neue Option bei pulmonaler Hypertonie
Die pulmonal-arterielle Hypertonie zeichnet sich durch einen Umbau (remodelling) kleiner Pulmonalarterien aus, welcher zu einem Anstieg des pulmonalen Gefäßwiderstandes (PVR) und Blutdruck des Lungenkreislaufs führt und in einer Rechtsherzinsuffizienz und schließlich dem Tod mündet. Eine PAH kann idiopathisch (IPAH), familiär (FPAH), Arzneimittel- oder Toxin-induziert oder mit anderen Erkrankungen (z.B. einer HIV-Infektion) einer portalen Hypertonie oder Kollagenosen (APAH) assoziiert sein. Betroffene sind je nach Schweregrad der Erkrankung eingeschränkt in ihrer körperlichen Leistungsfähigkeit, leiden oft auch in Ruhe unter Atemnot, ermüden schnell, neigen zu Schwindel- und Ohnmachtsanfällen (Synkopen), haben Thoraxschmerzen und entwickeln aufgrund der Rechtsherzinsuffizienz periphere Ödeme. Langwierige Krankenhausaufenthalte sind bei den Patienten keine Seltenheit und noch vor zehn Jahren betrug die Drei-Jahres-Überlebensrate nach Diagnosestellung nur 58%.
Therapieoptionen
Zu den bisherigen Therapieoptionen zur Verbesserung der körperlichen Leistungsfähigkeit und Lebenserwartung zählen Prostacyclin-Analoga (Prostanoide: Epoprostenol, Iloprost, Treprostinil), Phosphodiesterase-5-Hemmer (PDE-5-Hemmer: Sildenafil und Tadalafil) und Endothelin-Rezeptorantagonisten (ERA: Bosentan und Ambrisentan), die je nach Schweregrad der Erkrankung miteinander kombiniert werden. Der neue orale Endothelin-Rezeptorantagonist Macitentan ist in Monotherapie oder in Kombination mit anderen Wirkstoffen zur Langzeitbehandlung der PAH bei erwachsenen Patienten mit funktioneller WHO-/NYHA-Klasse II bis III zugelassen. Vor zwei Wochen erhielt zudem mit Riociguat ein Vertreter einer neuen Wirkstoffklasse (Stimulator der löslichen Guanylatcyclase (sGC)) die europaweite Zulassung. In der Pipeline steckt zudem noch der Prostacyclin-IP-Rezeptoragonist Selexipag, welcher derzeit noch eine Phase-III-Studie durchläuft.
Wirkmechanismus
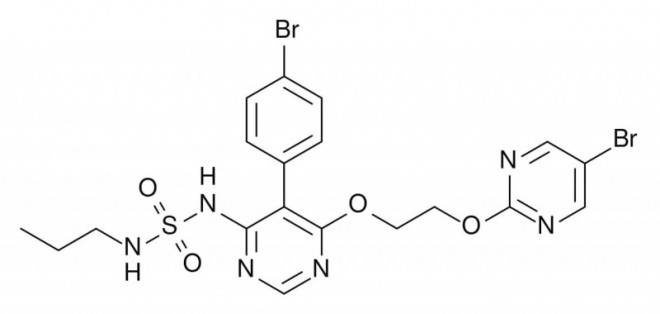
Der starke Vasokonstriktor Endothelin 1 spielt eine große Rolle im Krankheitsgeschehen der PAH, wirkt nach Rezeptorstimulation proliferativ auf glatte Gefäßmuskelzellen und wird bei Erkrankten vermehrt ausgeschüttet. Macitentan ist ein dualer Endothelin-Rezeptorantagonist und wirkt sowohl auf den Typ A als auch auf den Typ B des Endothelin-1-Rezeptors, die auf Gefäßendothel- und glatten Muskelzellen exprimiert sind.
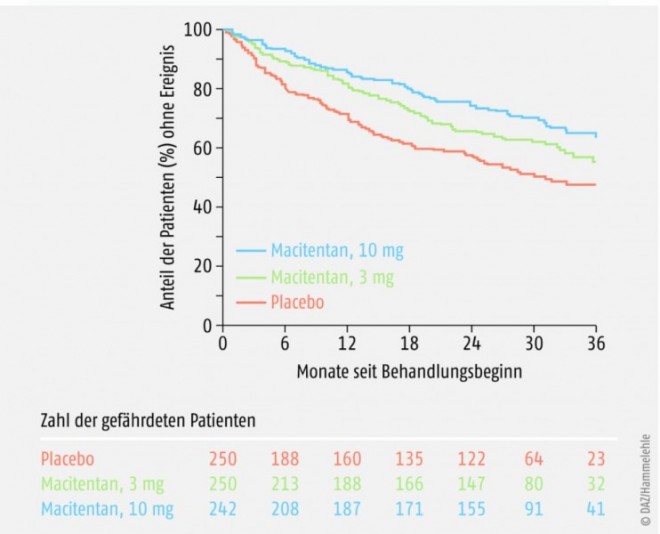
Macitentan zeigte in der zulassungsrelevanten Phase-III-Studie SERAPHIN (Study with an Endothelin Receptor Antagonist in Pulmonary arterial Hypertension to Improve clinical outcome) eine Reduktion des Morbiditäts- und Mortalitätsrisikos gegenüber Placebo und verzögerte die Krankheitsprogression. Die in 39 Ländern mit insgesamt 742 Studienteilnehmern größte placebokontrollierte Doppelblindstudie, die bei PAH-Patienten bis dato durchgeführt wurde, verglich die Effektivität von Macitentan in der Wirkstärke 3 mg und 10 mg mit Placebo. Der primäre Studienendpunkt war die Zeit bis zum Eintreten des ersten PAH-bedingten Morbiditäts- oder Mortalitätsereignisses (definiert als Verschlechterung der PAH in mehreren Parametern, Beginn einer i.v.- oder s.c.-Prostanoid-Therapie, Lungentransplantation, Tod jeglicher Art). Sekundäre Studienendpunkte umfassten Veränderungen sechs Monate nach Therapiebeginn in der Sechs-Minuten-Gehstrecke (6MWD) und der WHO-Funktionsklasse sowie die Analyse PAH-bedingter Todesfälle und Hospitalisierungen. Die durchschnittliche Behandlungsdauer betrug 115 Wochen.
Verbesserte Lungenfunktion und körperliche Leistungsfähigkeit
Der primäre Studienendpunkt eines PAH-bedingten Morbiditäts- oder Mortalitätsereignisses wurde bei 46,4% in der Placebogruppe, bei 38,0% in der Macitentan-3-mg-Gruppe und bei 31,4% in der Macitentan-10-mg-Gruppe beobachtet (siehe Abb. 1). Die Behandlung mit 10 mg Macitentan erwirkte demzufolge eine 45%-ige Reduktion des relativen Risikos für das Auftreten eines PAH-bedingten Morbiditäts- oder Mortalitätsereignisses verglichen mit Placebo (HR 0,55; 97,5% CI, 0,32 bis 0,76; p <0,001). 3 mg Macitentan reduzierten das Risiko gegenüber Placebo um 30%. Ausschlaggebend war, dass es unter Macitentan (dosisabhängig) seltener zu einer Verschlechterung der PAH kam. Das Risiko eines PAH-bedingten Todes oder einer PAH-bedingten Hospitalisierung wurde um 50% gegenüber Placebo gesenkt (HR 0,50; 97,5% CI, 0,34 bis 0,75; p <0,001), wobei ungefähr jeder Dritte in der Placebo-Gruppe und jeder Fünfte in der Macitentan-10-mg-Gruppe ein solches Ereignis (meist Hospitalisierung) aufwies. In der Sechs-Minuten-Gehstrecke wurden signifikante Verbesserung unter 10 mg Macitentan gegenüber Placebo gemessen. Es ist jedoch fraglich, ob die durchschnittliche Verbesserung gegenüber Placebo in Form von 22 Metern eine klinische Relevanz hat, wenn man betrachtet, dass die durchschnittliche 6MWD 360 Meter betrug. Wichtiger erscheint eher, dass nach sechsmonatiger Behandlung 22% der Patienten unter Macitentan und 13% der Patienten unter Placebo eine Niedrigstufung in der WHO-Funktionsklasse zeigten.
Studienkritik
Die von Actelion Pharmaceuticals gesponsorte zulassungsrelevante Studie muss sich Kritik gefallen lassen. So kann die Möglichkeit eines Bias nicht ganz ausgeschlossen werden, wenn man bedenkt, dass die Konzeptionierung und statistische Analyse durch das pharmazeutische Unternehmen selbst erfolgte (überprüft durch zwei unabhängige Statistiker) und ein vom Unternehmen bezahlter, professioneller Medizinautor die Erstfassung des Manuskripts erstellte. Ein weiterer Kritikpunkt ist ethischer Natur. Die Autoren der Studie rühmen sich damit, dass eine derartige Langzeitstudie bei PAH noch nie durchgeführt wurde und dass zum Beispiel andere Wirkstoffe auf Basis von 12- bzw. 16-wöchigen Studien zugelassen wurden. Doch sind Langzeitstudien bei PAH, die einen Wirkstoff gegen Placebo testen, überhaupt ethisch zu vertreten? Schließlich handelt es sich um eine Erkrankung, die unbehandelt mit kurzer Überlebensdauer assoziiert ist. Die Autoren entgegnen dieser Kritik mit der Aussage, dass positive Vota von Ethikkommissionen vorlagen und dass Studienmedikation in manchen Ländern der Welt die einzig verfügbare Therapieoption darstellt.
Auf Anzeichen einer Leberschädigung achten
Die Initiierung und Überwachung der Therapie sollte einem in der Behandlung der PAH erfahrenen Arzt vorbehalten sein. 10 mg Macitentan werden einmal täglich, möglichst immer zur gleichen Zeit, zu oder unabhängig von den Mahlzeiten eingenommen. Bei älteren Patienten und bei Patienten mit beeinträchtigter Nieren- oder Leberfunktion ist keine Dosisanpassung erforderlich. Jedoch wird die Anwendung bei dialysepflichtigen Patienten nicht empfohlen und bei Patienten mit schweren Leberfunktionsstörungen ist die Gabe kontraindiziert.
In der zulassungsrelevanten SERAPHIN-Studie entwickelten 14% der Probanden unter Macitentan eine Nasopharyngitis, ebenfalls 14% Kopfschmerzen und 13% eine Anämie (4% mit einem Hb-Wert <8 g/dl). Aufgrund anämischer Beschwerden brachen drei Teilnehmer die Studie ab (jeweils ein Patient pro Gruppe). Besonders aufmerksam wurde jedoch das potenzielle Auftreten erhöhter Leberenzymwerte (Alanin-Aminotransferase [ALT] und Aspartat-Aminotransferase [AST]) verfolgt, da unter der Vorgängersubstanz Bosentan 13% der Probanden Transaminasewerte von mehr als dem Dreifachen des oberen Normwertes entwickelten und unter dem mittlerweile vom Markt genommenen Sitaxentan fatale Hepatotoxizitäten auftraten. Das Sicherheitsprofil von Macitentan kann in diesem Punkt als verbessert angesehen werden, da nur 3,4% der Patienten eine derartige Erhöhung zeigten (interessanterweise auch 4,5% der Patienten unter Placebo). Dennoch werden monatliche Kontrollen der Leber-Aminotransferase-Werte empfohlen, unter Bosentan sind sie hingegen verpflichtend. Vor der Behandlung mit Macitentan muss zudem eine schwere Leberfunktionsstörung und eine klinisch signifikante Erhöhung der Leber-Aminotransferase-Werte auf mehr als das Dreifache des oberen Normwertes ausgeschlossen werden.
Nicht für Schwangere
Macitentan erwies sich im Tierversuch als teratogen, weshalb vor Beginn der Behandlung eine bestehende Schwangerschaft ausgeschlossen werden muss. Frauen im gebärfähigen Alter sollten unter der Therapie mit Macitentan und einen Monat darüber hinaus sichere Verhütungsmethoden praktizieren (zum Beispiel orales Kontrazeptivum plus Kondom). Es wird empfohlen, monatliche Schwangerschaftstests durchzuführen, um eine eingetretene Schwangerschaft frühzeitig erkennen zu können. In den USA geht man hier einen Schritt weiter. Alle Frauen, die sich für eine Therapie mit Macitentan entscheiden, müssen in einem von der FDA geforderten Programm zur „Risikoevaluation und -abschwächung“ (Risk Evaluation and Mitigation Strategy [REMS]) registriert werden (www.opsumitrems.com). Auch Ärzte und Apotheker müssen sich in den USA zertifizieren lassen, um Opsumit® verschreiben oder abgeben zu dürfen. Ziel des REMS-Programms ist, über die teratogenen Eigenschaften von Macitentan aufzuklären und eine Exposition mit möglichen nachteiligen Auswirkungen auf Feten zu vermeiden. Innerhalb des Programms sind daher monatliche Schwangerschaftstests für Frauen im gebärfähigen Alter verpflichtend. In Europa wurde ein Risikomanagementplan implementiert.
Steckbrief
Handelsname: Opsumit
Hersteller: Actelion Pharmaceuticals Deutschland GmbH
Einführungsdatum: 1. Februar 2014
Zusammensetzung: 1 Filmtablette enthält 10 mg Macitentan
Stoffklasse: andere Antihypertonika, ATC-Code: C02KX 04Indikation: als Mono- oder Kombinationstherapie zur Langzeitbehandlung der pulmonalen arteriellen Hypertonie (PAH) bei erwachsenen Patienten mit funktioneller WHO-/NYHA-Klasse II bis III
Dosierung: einmal täglich 10 mg zu oder unabhängig von den Mahlzeiten
Gegenanzeigen: Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile; Schwangerschaft; Frauen im gebärfähigen Alter, die keine zuverlässigen Verhütungsmethoden anwenden; Stillzeit; Patienten mit schwerer Leberfunktionsstörung (mit oder ohne Zirrhose); vor Behandlungsbeginn bestehende Erhöhung der Leber-Aminotransferasewerte (Aspartat-Aminotransferase (AST) und/oder Alanin-Aminotransferase (ALT) > 3 x oberer Normwert (ONW)
Nebenwirkungen: sehr häufig: Nasopharyngitis, Bronchitis, Anämie, Kopfschmerzen; häufig: Pharyngitis, Influenza, Harnwegsinfekt, Hypotonie
Wechselwirkungen: Die Cytochrom-P450-Enyzme CYP3A4, CYP2C8, CYP2C9 und CYP2C19 sind in die Metabolisierung von Macitentan sowie die Bildung seiner Metabolite involviert, Macitentan und sein aktiver Metabolit entfalten keinen klinisch relevanten inhibitorischen oder induzierenden Effekt auf die Cytochrom-P450-Enyzme, sie sind keine Inhibitoren der hepatischen oder renalen Wiederaufnahme-Transporter und sie sind keine Inhibitoren hepatischer oder renaler Efflux-Pumpen.
Warnhinweise und Vorsichtsmaßnahmen: Ein Anstieg der Leber-Aminotransferasewerte (AST, ALT) wurde mit einer PAH und Endothelin-Rezeptor-Antagonisten (ERA) assoziiert. Eine Therapie mit Macitentan darf nicht bei Patienten mit schwerer Leberfunktionsstörung oder erhöhten Aminotransferasewerten (> 3 x ONW) begonnen werden und wird bei Patienten mit mittlerer Leberfunktionsstörung nicht empfohlen. Wie auch bei der Behandlung mit anderen ERAs, war die Behandlung mit Macitentan mit einem Abfall der Hämoglobinkonzentration assoziiert; unter Macitentan wurden Fälle von Anämie berichtet, die eine Bluttransfusion erforderten, eine Behandlung mit Macitentan wird bei Patienten mit schwerer Anämie nicht empfohlen.
Fazit
Für Patienten mit pulmonal-arterieller Hypertonie steht mit Macitentan nun ein weiterer Wirkstoff zur Milderung des dramatischen Krankheitsbildes mit leicht verbessertem Sicherheitsprofil zur Verfügung. Die Zulassung von Opsumit® läutet für Actelion vermutlich einen Wachwechsel mit dem bisherigen Blockbuster des Unternehmens, Bosentan (Tracleer®) ein, dessen Patentschutz 2015 erlischt. Den Vergleich mit diesem und weiteren Wirkstoffen zur Behandlung der PAH muss Macitentan nun in klinischen Studien suchen und es bleibt abzuwarten, ob auch hier und nicht nur gegenüber Placebo Verbesserungen erzielt werden können.
Quelle
Fachinformation Opsumit®, Actelion Registration Ltd. Stand Dezember 2013.
Pulido T et al. Macitentan and Morbidity and Mortality in Pulmonary Arterial Hypertension. N Engl J Med (2013) 369: 809–818.
Seferian A, Simonneau G. Therapies for pulmonary arterial hypertension: where are we today, where do we go tomorrow? Eur Respir Rev (2013) 22: 217–226.
Correspondence to the editor. Macitentan and pulmonary arterial hypertension. N Engl J Med (2014) 370(1): 81–83.





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.