
- DAZ.online
- DAZ / AZ
- DAZ 14/2014
- Innovation nach über 40 ...
Arzneimittel und Therapie
Innovation nach über 40 Jahren
Antituberkulotikum Bedaquilin jetzt auch in Europa zugelassen
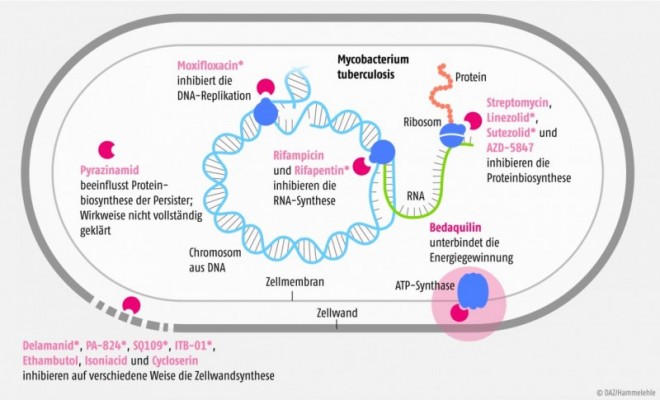
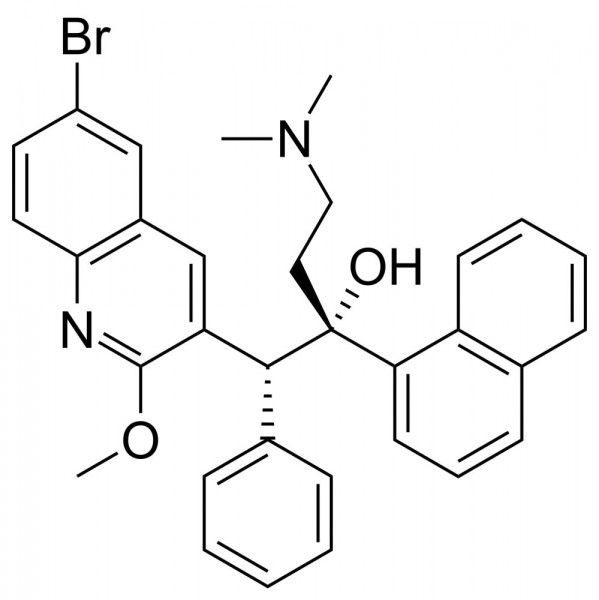
Adenosintriphosphat (ATP) ist der wichtigste Energielieferant einer jeden Zelle, so auch des Erregers der Tuberkulose Mycobacterium tuberculosis. Diese Spezies kann zwar im Ruhezustand ihren ATP-Verbrauch auf ein Minimum reduzieren, aber ganz ohne ATP ist auch sie nicht überlebensfähig. Auf dieser Tatsache beruht das Wirkprinzip von Bedaquilin. Die Substanz, die den Diarylquinolonen zuzuordnen ist und strukturelle Ähnlichkeiten sowohl zu den Fluorchinolonen als auch zu Chloroquin aufweist, blockiert die mycobakterielle ATP-Synthase in der inneren Mitochondrienmembran und unterbindet so die Energiegewinnung des Bakteriums. Die humane mitochondriale ATP-Synthase ist, obwohl sie als hochkonserviert gilt, unempfindlich gegen Bedaquilin. Der Sensitivitäts-Unterschied beläuft sich etwa auf den Faktor 20.000. Bei der Wirkstoff-Entwicklung wird ein Unterschied um den Faktor 1000 als Grenzwert angesehen, ab dem eine Substanz hinsichtlich ihrer Selektivität als vielversprechend gilt. Viele Substanzen, die DNA-Replikation oder die Zellwandsynthese inhibieren (siehe Abbildung), können ihre bakterizide Wirkung nur bei Zellen entfalten, die sich teilen. Bedaquilin hingegen wirkt auf sich teilende und auf ruhende Zellen, die sogenannten Persister.
Nicht perfekt, aber vielleicht etwas besser
Da Tuberkulostatika, unter anderem um Resistenzbildung vorzubeugen, immer kombiniert werden, sollte der ideale Wirkstoff möglichst wenig Interaktionen mit anderen Tuberkulostatika oder, da Tuberkulose häufig als opportunistische Infektion auftritt, mit HIV-Medikamenten aufweisen: Diese Erwartung konnte Bedaquilin nicht ganz erfüllen, da es als Substrat von CYP3A4 mit den Enzyminduktoren Rifampicin und Efavirenz interagiert. Daneben wurden unter Lopinavir/Ritonavir erhöhte Plasmaspiegel von Bedaquilin gemessen. Da primär Ritonavir dafür verantwortlich gemacht wird, ist diese Interaktion auch bei anderen Ritonavir-geboosterten HIV-Protease-Inhibitoren zu erwarten. Um die klinische Relevanz der beschriebenen Interaktionen beurteilen zu können, sind weitere Studien mit Tuberkulostatika und antiretroviralen Mitteln notwendig. Es besteht aber Hoffnung, dass die Wechselwirkungen von Bedaquilin von geringerer Bedeutung sind als die anderer Wirkstoffe gegen Tuberkulose.
Multi- oder extremresistent
MDR-Tb (Multidrug-resistant tuberculosis): Der Erreger ist mindestens gegen die zwei wichtigsten Erstrangmedikamente Isoniazid und Rifampicin resistent.
XDR-Tb (extensively drug resistent): Der Erreger ist gegen die wichtigsten Erstrangmedikamente, Isoniazid und Rifampicin, sowie gegen alle Fluorochinolon-Antibiotika und eines der Aminoglycosid-Antibiotika resistent.
TDR-Tb (totally-drug resistant-tuberculosis): Der Erreger ist gegen alle derzeit verfügbaren Erstrangmedikamente sowie gegen Zweitrangmedikamente resistent. Diese Definition ist jedoch von der WHO derzeit nicht anerkannt.
Als Erstrangmedikamente gelten: Isoniazid (INH), Rifampicin (RMP), Ethambutol (EMB), Pyrazinamid (PZA) und Streptomycin (SM).
Zulassung unter Auflagen
Bedaquilin wurde vergangenes Jahr von der FDA als Orphan Drug zur Behandlung der multiresistenten Tuberkulose (MDR-Tb) in Kombination mit anderen Antituberkulotika beschleunigt zugelassen. Und zwar auf der Basis von nur zwei Phase-II-Studien mit insgesamt 440 Patienten. In der EU hat Bedaquilin eine Zulassung unter Auflagen erhalten („conditional approval“), ebenfalls basierend auf Phase-II-Studien. Als Grund für diese Entscheidung wird – neben dem positiven Nutzen-Risiko-Verhältnis und der überzeugenden Wirksamkeit – angeführt, dass Wirkstoffe gegen multiresistente Tuberkulose dringend benötigt werden. Zudem handelt es sich bei Bedaquilin um ein völlig neues Wirkprinzip, bei dem bisher keine Kreuzresistenzen mit anderen Wirkstoffen aufgetreten sind. Kreuzresistenzen stellen ein großes Problem bei der Behandlung der multiresistenten Tuberkulose dar.
Der Hersteller ist angehalten, Phase-III-Studien durchzuführen, um weitere Daten zu Benefit und Sicherheit zu generieren, insbesondere Daten zur Anwendung in Kombination mit anderen Tuberkulostatika innerhalb therapeutischer Regime. Außerdem gibt es einen „Risk Management Plan“, der auf der Internetseite der EMA zur Verfügung steht. Die Zulassung wird regelmäßig überprüft.
Die Markteinführung in Deutschland ist für Mitte Mai geplant. Bis dahin ist Bedaquilin weiterhin im Rahmen eines Härtefall-Programms („Compassionate Use“) für austherapierte Patienten verfügbar.
Herz und Leber im Blick behalten
Ein weiteres Argument für die beschleunigte Zulassung war das günstige Sicherheitsprofil. In den Zulassungsstudien unterschieden sich die gemeldeten Nebenwirkungen zwischen Verum- (Standard-Regime + Bedaquilin) und Placebo-Gruppe (Standard-Regime + Placebo) kaum: Vor allem erhöhte Leberwerte und QT-Strecken-Verlängerungen waren aufgetreten. Außerdem gab es bei einer der Studien unter Verum mehr Todesfälle als unter Placebo. Der Beweis dafür, dass diese Todesfälle auf die Einnahme von Bedaquilin zurückzuführen sind, wurde jedoch nicht erbracht. Aber der Hersteller muss weitere Daten zur Sicherheit liefern. Bezüglich der kardialen und hepatischen Toxizität wurden in der Packungsbeilage entsprechende Vorsichtsmaßnahmen und Anwendungsbeschränkungen formuliert (siehe Steckbrief). Aber auch hier sind weitere Daten gefordert.
Steckbrief Bedaquilin
Handelsname: Sirturo
Hersteller: Janssen-Cilag International
Einführungsdatum: voraussichtlich Mai 2014
Zusammensetzung: eine Tablette enthält 100 mg Bedaquilin als Bedaquilinfumarat
Stoffklasse: andere Mittel zur Behandlung der Tuberkulose, ATC-Code: J04AK05
Indikation: Sirturo wird bei erwachsenen Patienten als Teil einer geeigneten Kombinationstherapie der multiresistenten pulmonalen Tuberkulose [multi-drug-resistant Mycobacterium tuberculosis (MDR-TB)] angewendet, wenn ein wirksames Behandlungsregime aufgrund von Resistenz oder Unverträglichkeit nicht anders zusammengestellt werden kann.
Dosierung: Woche 1 bis 2: 400 mg (4 Tabletten zu je 100 mg) einmal täglich; Woche 3 bis 24: 200 mg (2 Tabletten zu je 100 mg) dreimal pro Woche (mit mindestens 48 Stunden Abstand zwischen den Einnahmen der einzelnen Dosen)
Behandlungsdauer 24 Wochen, bei Bedarf auch länger.
Gegenanzeigen: Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile.
Nebenwirkungen: Die häufigsten Nebenwirkungen (bei > 10,0% der Patienten) während der Behandlung in den kontrollierten Studien waren Nausea, Arthralgien, Kopfschmerzen, Erbrechen und Schwindel. Des Weiteren wurden ein verlängertes QT-Intervall im Elektrokardiogramm, Diarrhöen, erhöhte Transaminasen sowie Myalgien beobachtet.
Wechselswirkungen: Bedaquilin wird über CYP3A4 metabolisiert. Daher kann die Bioverfügbarkeit von Bedaquilin während der gleichzeitigen Anwendung mit CYP3A4-Induktoren vermindert sein und sollte vermieden werden.
Die kurze gleichzeitige Anwendung von Bedaquilin und CYP3A4-Inhibitoren führt zu erhöhter Bedaquilin-Bioverfügbarkeit. Je länger die gleichzeitige Anwendung, desto ausgeprägter dieser Effekt. Eine gleichzeitige Anwendung von Bedaquilin und mäßigen oder starken CYP3A4-Inhibitoren (z.B. Ciprofloxacin, Erythromycin, Fluconazol, Clarithromycin, Ketoconazol, Ritonavir) über einen Zeitraum von mehr als 14 aufeinander folgenden Tagen sollte wenn möglich vermieden werden. Andernfalls wird eine häufigere EKG- und Transamin–asen-Kontrolle empfohlen.
Bei gleichzeitiger Anwendung der Tuberkulostatika Isoniazid/Pyrazinamid Ethambutol, Kanamycin, Pyrazinamid, Ofloxacin oder Cycloserin wurden keine relevanten Effekte auf die Plasmaspiegel beobachtet.
Ein additiver oder synergistischer Effekt auf die Verlängerung der QT-Strecke durch Bedaquilin bei gleichzeitiger Anwendung mit Arzneimitteln, die ebenfalls das QT-Intervall verlängern, kann nicht ausgeschlossen werden. In diesen Fällen werden regelmäßige EKG-Kontrollen empfohlen.
Warnhinweise und Vorsichtsmaßnahmen:
Kardiotoxizität: Da Bedaquilin das QT-Intervall verlängert, sollte vor Behandlungsbeginn und danach mindestens einmal monatlich ein EKG durchgeführt werden. Unter folgenden Umständen wird eine Behandlung nicht empfohlen: bei Herzinsuffizienz, bei QT-Intervall > 450 m, bei angeborener QT-Verlängerung in der Eigen- oder Familienanamnese, bei bestehender oder anamnestischer Hypothyreose, bei bestehender oder anamnestischer Bradyarrhythmie, bei Torsade-de-Pointes-Tachykardien in der Anamnese, bei gemeinsamer Anwendung mit Fluorochinolon-Antibiotika, die potenziell signifikant QT-Zeit-verlängernd wirken können, bei Hypokaliämie.
Hepatotoxizität: AST, ALT, alkalische Phosphatase und Bilirubin sollten vor der Behandlung und monatlich sowie bei Bedarf während der Behandlung kontrolliert werden und gegebenenfalls das Therapieschema überprüft werden. Andere hepatotoxische Arzneimittel und Alkohol sollten während der Behandlung vermieden werden, besonders bei Patienten mit eingeschränkter Leberfunktion.
Mit Bedacht einsetzen
Neben der Vermeidung der Selektion oder Entwicklung resistenter Keime gibt es einen weiteren Grund dafür, dass Tuberkulose immer mit einer Kombination von Medikamenten behandelt werden muss. Tuberkulose-Erreger können in biologisch sehr verschiedenen Populationen vorkommen, zu deren optimaler Bekämpfung je nach pH-Wert und Wachstumsgeschwindigkeit verschiedene Antituberkulotika jeweils am besten geeignet sind. Die Medikamente unterscheiden sich in ihren Wirkmechanismen und Wirkorten (Zytosol, Lysosom etc., siehe Abbildung), so dass die Erreger auf unterschiedlichen Stufen abgetötet oder in ihrer Vermehrung gestoppt werden. In vielen Ländern der Welt wird eine Tuberkulose-Behandlung begonnen ohne das Ergebnis eines Resistenztests zu haben, der dort teuer und zeitaufwendig ist. Daher werden MDR-Tb-Patienten nicht selten mit Wirkstoffen behandelt, gegen die ihre Erreger resistent sind. Fügt man diesem unwirksamen Regime Bedaquilin hinzu, wird de facto eine Monotherapie durchgeführt, bei der sich in kurzer Zeit Resistenzen bilden. Eine weitere Waffe im Kampf gegen MDR-Tb wäre verpulvert. Von daher sehen Experten zwar das große Potenzial der Substanz, mahnen aber auch, sie mit Bedacht einzusetzen.
Quelle
Fachinformation Sirturo®, Stand März 2014.
Cohen J. Science 2013: 339 (6116); 130. DOI: 10.1126/science.339.6116.130
Haagsma, AC. et al. Antimicrob Agents Chemother. Mar 2009; 53(3): 1290–1292.
Mageshwaran, L., Alphienes, SX. J Young Pharm. 2013 Dec;5(4):112-115. Epub 2013 Dec 30.
Neues zur Tuberkulose in Deutschland – Welttuberkulosetag 2014 im RKI; Pressemitteilung des Robert Koch-Instituts, www.rki.de.
Resistenz gegen Antibiotika. Therapie einer resistenten und multiresistenten Tuberkulose www.tuberkulose-ratgeber.de/therapie/kombinationstherapie/multiresistente-tuberkulose.
www.who.int/tb/challenges/mdr/tdrfaqs/en/
EPAR summary for the public: Sirturo. www.ema.europa.eu/
Sirturo® (Bedaquiline) Receives Conditional Approval in the European Union for the Treatment of Multi-Drug Resistant Tuberculosis. www.janssen-emea.com





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.