
- DAZ.online
- DAZ / AZ
- DAZ 13/2014
- Nanopartikel
Technologie
Nanopartikel
Innovative Anwendungsgebiete in der Diagnostik und vor allem in der Therapie
Eisenoxid-Nanopartikel
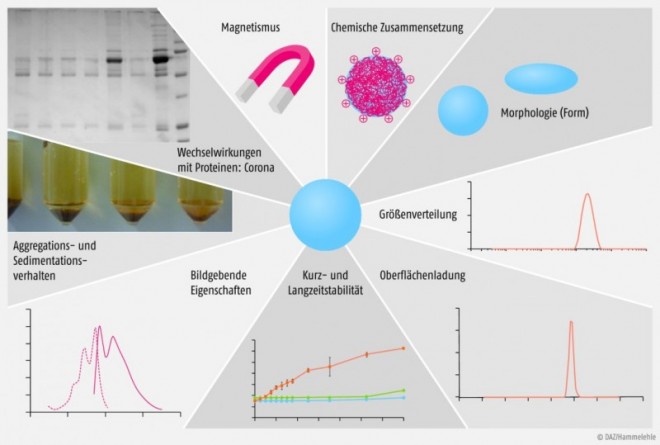
Eisenoxidhaltige Kontrastmittel wurden vor mehr als 20 Jahren in die Klinik eingeführt. Die heute in der Diagnostik eingesetzten Eisenoxid-Nanopartikel haben in der Regel einen Kern aus Magnetit (Fe3O4) oder Maghemit (Fe2O3), seltener eine Mischung mit Übergangsmetallen wie Kobalt, Mangan, Zink oder Gadolinium [1–3]. Sie können mittels alkalischer Präzipitationstechniken, Mikroemulsionsverfahren, hydrothermaler Synthese, elektrochemischer Ablagerung etc. kontrolliert mit definierter Partikelgrößenverteilung und Form hergestellt werden [1]. Abbildung 1 zeigt typische physikochemische Eigenschaften von Eisenoxid-Nanopartikeln, die bei der Entwicklung von Produkten für bestimmte Anwendungsgebiete untersucht werden.
Die Vorteile von Nanopartikeln mit Eisenoxidkern in der Medizin liegen auf der Hand: Sie werden über den körpereigenen Eisenstoffwechsel verstoffwechselt (über die Fäzes in ca. 3 Monaten), die Abbauwege sind bekannt, die für eine Diagnostik verabreichten Eisenmengen sind gering, und das Risiko einer Überdosierung ist damit minimal [2]. Eine typische MRT-Dosis für einen Erwachsenen enthält ca. 50 bis 200 mg Eisen, wenig im Vergleich zu den physiologischen Eisendepots mit zusammen ca. 3500 mg [4].
MRT und Kontrastmittel
Die MRT basiert auf der Kernspinresonanz von Wasserstoff, einem extrem häufigen Element in unserem Körper. Während der MRT werden (fast) alle Protonen im Grundzustand parallel ausgerichtet, wobei es zu einer sog. Längsmagnetisierung kommt. Um ein Signal zu messen, wird die Längsmagnetisierung in die Querrichtung ausgelenkt (Anregung). Die T1-Relaxationszeit besagt, wie schnell die Protonen aus dem angeregten Zustand in den Grundzustand zurückkehren. Auch das Dephasieren der Protonen nach der Anregung ist ein Relaxationsvorgang, seine Dauer ist die T2-Relaxationszeit. Da die T1- und T2-Relaxationszeiten der Gewebe sich unterscheiden, wird bei der MRT eine spezifische „Kontrastierung“ erreicht, die durch die selektive Anreicherung von Kontrastmitteln (idealerweise Eisenoxid-Nanopartikel) moduliert werden kann, weil diese die Relaxation der umliegenden Protonen des Gewebes verändern [5, 6].
Superparamagnetismus, Größenklassen und Formen
Bei abnehmender Größe der Eisenoxid-Nanopartikel vollzieht sich im Bereich von etwa 30 bis 40 nm der Übergang von den ferromagnetischen zu den superparamagnetischen Eigenschaften [8]. Superparamagnetismus heißt, dass die Nanopartikel beim Anlegen eines äußeren magnetischen Feldes bis zur Sättigung aufmagnetisiert werden, beim Abschalten des Feldes jedoch sofort wieder ihre magnetischen Eigenschaften verlieren (relaxieren). Dabei ist die Relaxivität durch die Größe des Eisenoxidkerns determiniert. Deshalb werden die diagnostischen Eisenoxid-Nanopartikel gemäß dem Durchmesser ihres Eisenoxidkerns in drei Größenklassen eingeteilt [1, 2, 6]:
- USPIOs (ultra-small superparamagnetic iron oxide) < 50 nm,
- SPIOs (small superparamagnetic iron oxide) 50 nm–1 µm,
- MPIOs (micron-sized particles of iron oxide) > 1 µm.
SPIOs besitzen nur eine magnetische Domäne. Da bei ihnen die thermische Energie größer als die Energiebarriere ist, kann jeder einzelne Partikel als Paramagnet bezeichnet werden, sodass alle Partikel zusammen einen Superparamagneten darstellen.
MPIOs dürfen nur oral, z.B. für Untersuchungen des Gastrointestinaltrakts, appliziert werden, um das Risiko von Thrombosen und Embolien auszuschließen. SPIOs werden deutlich rascher von Leber und Milz aufgenommen und phagozytiert als USPIOs, weshalb sie sich vor allem als Kontrastmittel für die Leber eignen. USPIOs dagegen können in Lymphknoten aufgenommen werden.
Nanopartikel < 300 nm verweilen länger in der Blutbahn und werden daher auch als intravaskuläre Kontrastmittel („blood pool agents“, BPA) zur Angiografie eingesetzt [7].
Üblicherweise bestehen die Eisenoxidkerne aus einem einzigen sphärischen Partikel, oder sie sind multipartikulär in Form von „Himbeeren“ aus mehreren Einheiten aufgebaut (sog. Multidomänen-Nanopartikel). Genauso gut können jedoch stäbchenförmige Strukturen verwendet werden, deren biologische Auswirkungen bisher allerdings nur unzureichend erfasst worden sind. Längere Zirkulationszeiten im Blut, eine verlangsamte Clearance, eine Verlagerung der Verteilung von der Leber zur Milz, eine geringere Aktivierung von Makrophagen und niedrigere Zelltoxizitäten lassen nicht-sphärische Nanoteilchen vorteilhaft erscheinen [9]. Allerdings sind sie als Träger für Wirkstoffe weniger geeignet, da diese Effekte mit einer verringerten Aufnahme in Zellen einhergehen [10].
Datenbank
Wichtige Informationen zu Eisenoxid-Nanopartikeln können in der Datenbank Nanopartikel (DaNa) abgerufen werden:
Die Hülle als Schlüssel für Anwendungsmöglichkeiten
Der Kern der Nanopartikel ist in der Regel von einer Hülle aus anorganischen oder organischen Materialien umgeben, die sowohl während der Synthese als auch nachträglich kovalent oder adsorptiv gebunden werden können. Die Hülle kann zahlreiche Vorteile bieten [1, 2, 6, 11]:
- Erhöhung der kolloidalen Stabilität durch Verminderung der Agglomerations- und Sedimentationstendenz,
- Schutz der eisenhaltigen Oberfläche vor Oxidation,
- Verbesserung der Biokompatibilität,
- Anknüpfungsstelle für Wirkstoffe und Liganden zum zell- und gewebespezifischen Targeting,
- Gezielte Steuerung der Biodistribution,
- Hemmung der Clearance durch das retikuloendotheliale System.
Zusammengefasst bedeutet dies, dass die Hüllen die physikochemischen Oberflächeneigenschaften der Nanopartikel determinieren und wesentlichen Einfluss auf ihre Toxizität und Pharmakokinetik haben.
Bei kommerziellen Systemen werden bisher nur einige wenige Hüllmaterialien wie Polysaccharide (z.B. Dextran, Carboxydextran, Carboxymethyldextran, Stärke), Polyethylenglykol oder Siloxane verwendet. Dabei ist zu beachten, dass selbst nicht-magnetische Hüllmaterialien die Magnetisierung schwächen können. Niedermolekulare Dextrane finden sich in vielen kommerziellen Produkten, da sie einfach eliminierbar sind (renal in ca. 2 Monaten), keine immunogenen Reaktionen oder Langzeiteffekte hervorrufen und intrazellulär über Dextranasen abgebaut werden können. Oftmals sind die Dextrane nur adsorptiv an die Kerne gebunden, sodass eine erleichterte Dissoziation im Organismus und damit Abbau der Nanopartikel über die Zeit möglich ist. Polyethylenglykol fungiert als Stealth-Polymer (Tarnkappen-Polymer), d.h. dass es die Nanopartikel maskiert und gegen Opsonierung und Eliminierung durch das Immunsystem schützt und somit ihre Zirkulationshalbwertszeit verlängert.
Innovative Ansätze beschäftigen sich auch mit Hüllen aus Albumin, Pullulan, Chitosan, Silica, Silanen, Polyethylenimin, Methacrylsäure- und Cellulose-Derivaten, um nur einige zu nennen. Polymere mit hohen Molekularmassen, hohen Ladungsdichten (vor allem bei kationischer Oberflächenladung) und flexibler Gestalt sind prädestiniert für hohe Toxizitäten und unspezifische Interaktionen. Andererseits können positiv geladene SPIOs hervorragend in Zellen internalisiert werden, weil die Zellmembran negativ geladen ist (elektrostatische Wechselwirkung) [12].
Durch geschickte Auswahl der Umhüllungen können die Eisenoxid-Nanopartikel im Organismus gezielt gesteuert werden. Während z.B. Nanopartikel mit Citrathüllen mittels Phagozytose von Zellen aufgenommen werden, werden Nanopartikel mit einer Carboxydextranhülle via Pinozytose internalisiert [13].
Die Proteincorona der Nanopartikel
Bei systemischer Anwendung von Nanopartikeln tritt ein Phänomen auf, welches zwar seit Langem bekannt ist, dessen Bedeutung allerdings erst in den letzten Jahren nach und nach verstanden wird: die Proteincorona. Sie entsteht, weil sich im Organismus Hunderte verschiedener Proteine innerhalb von wenigen Sekunden an die Nanopartikel anlagern können. Dabei hängen die Struktur und Zusammensetzung der Proteincorona von verschiedenen Faktoren ab wie den physikochemischen Eigenschaften der Nanopartikel (Größe, Form, Oberflächenbeschaffenheit, Ladung), der physiologischen Umgebung (Blut, interstitielle Flüssigkeit, Zellplasma etc.) und auch der Dauer der Exposition [14–16].
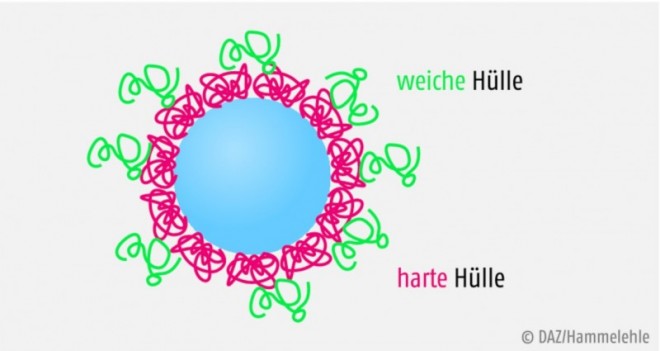
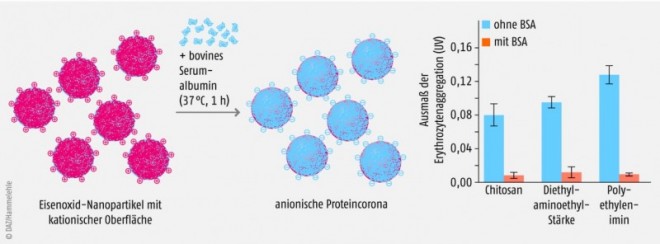
Die Zusammensetzung der Corona ist nicht konstant, sondern ändert sich allmählich. Während sich zunächst Proteine, die abundant vorkommen und eine hohe Mobilität aufweisen, an die Nanopartikel anlagern, werden diese mit der Zeit durch Proteine verdrängt, die zwar selten sind, aber eine hohe Bindungsaffinität aufweisen (Vroman-Effekt). Letztendlich entsteht eine „harte“ Hülle aus sich langsam austauschenden Proteinen, die von einer „weichen“ Hülle aus locker gebundenen und schnell wechselnden Proteinen umgeben ist (Abb. 2). An viele Nanopartikel binden vor allem Albumin und Fibrinogen, die in großen Mengen im Blut vorhanden sind. Kationische Nanopartikel interagieren bevorzugt mit den negativ geladenen Bindungsstellen des Albumins. An Dextran-Umhüllungen kann C3-Komplement binden. Transferrin, Fetuin A, Haptoglobin und Kininogen sind typische Proteine, die auf Nanopartikeln mit anorganischer Hülle zu finden sind [17].Die Proteincorona kann den Nanopartikeln eine völlig neue Identität geben, und zwar oftmals zum Nachteil durch die Veränderung toxikologischer und immunogener Eigenschaften, die Erhöhung von Phagozytose und Clearance sowie eine Behinderung der Bindung an Zielzellen [18]. Umgekehrt versuchen Nanowissenschaftler nun, sich die Proteincorona für eine gezielte Anwendung der Nanopartikel zunutze zu machen. Obwohl sie die „Sprache“ dieser Proteine bisher nur ansatzweise verstehen, versuchen sie, Gesetzmäßigkeiten der Corona-Bildung zu finden, indem sie die Eigenschaften der Nanopartikel variieren (Größe des Kern, Zusammensetzung der Hülle, Oberflächeneigenschaften) und mit ihnen experimentieren (Abb. 3). Die vielen Gestaltungsmöglichkeiten sind bisher bei Weitem nicht ausgeschöpft, geschweige denn erforscht.
Doppelter Nutzen: Theranostika
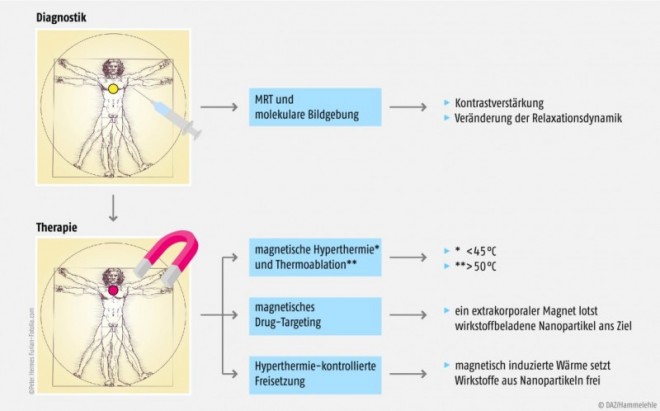
Die von den Behörden zugelassenen Eisenoxid-Nanopartikel werden vor allem in der MRT von Leber, Milz und Lymphknoten-Metastasen eingesetzt, allerdings sind sie von gadoliniumhaltigen Kontrastmitteln zurückgedrängt worden. Ihre Zukunft wird heute vor allem in speziellen diagnostischen Anwendungen und neuen Techniken in der Arzneimitteltherapie gesehen (Abb. 4). So könnten SPIOs mit einem Arzneistoff beladen werden, dessen Anreicherung und Lokalisation im Organismus man dann mithilfe der MRT verfolgen könnte (sog. „Theranostika“, aus „Therapeutika“ und „Diagnostika“).
Verbesserung der Diagnostik mit und ohne „Cell targeting“
SPIOs ohne zellspezifisches Targeting werden vornehmlich von Monozyten/Makrophagen aufgenommen. Daher eignen sie sich zur Darstellung von Organen des mononukleären Phagozytensystems, der Leber und der Milz, in denen Monozyten/Makrophagen zahlreich vorkommen. Gesundes Lebergewebe stellt sich in einer T2-gewichteten Bildgebung durch das vorhandene Eisenoxid dunkel dar, während Tumoren oder gutartige Veränderungen (Hämangiome, Zysten) hell sind, weil sie keine Nanopartikel aufgenommen haben. Beispiele für solche SPIOs sind Ferumoxid (Endorem®, Guerbet) und Ferrixan (Resovist®, Bayer). Ferumoxtran (Sinerem®, Guerbet), das aus sehr kleinen Eisenoxid-Nanopartikeln besteht, kann als Kontrastmittel für Gefäße sowie zur Identifikation von Lymphknoten-Metastasen verwendet werden.
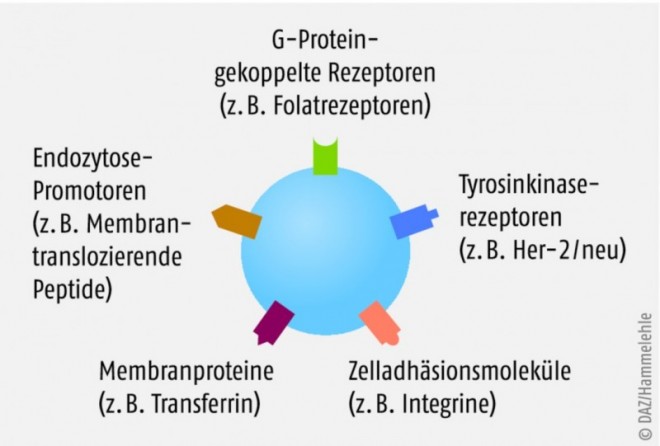
In neuen diagnostischen Ansätzen werden SPIOs mithilfe von Liganden an molekulare Strukturen adressiert, die ausschließlich und in hoher Dichte an der Oberfläche bestimmter pathologisch veränderter Zellen vorkommen, sodass sie ideale Biomarker sind. So gibt es bereits SPIOs, die gezielt an Transferrinrezeptoren, Folatrezeptoren, Integrine, Her-2/neu oder definierte Phospholipide (z.B. Phosphatidylserin auf der Oberfläche apoptotischer Zellen) binden (Abb. 5) [19–27].
„Magnetic-guided targeting“ in der Tumortherapie
Klassische Chemotherapeutika weisen ein hohes zytotoxisches Potenzial, aber nur eine geringe Selektivität für die Tumorregion auf. Dies führt zu den allgemein bekannten Nebenwirkungen im gesunden Gewebe. An diesem Punkt setzt die Idee an, durch „magnetisches Lotsen“ die Wirkstoffe in der Tumorregion anzureichern und zugleich ihre Konzentration in gesunden Geweben zu verringern. Der jeweilige Wirkstoff wird an magnetische Nanopartikel gebunden, die aufgrund der Anziehungskraft eines extrakorporalen Magneten durch die Blutgefäße zum Zielgewebe schwimmen. Diese Idee geht zwar auf die 70er Jahre zurück, gewinnt heute aber wieder zunehmend an Bedeutung, nachdem verschiedene Untersuchungen in Präklinik [28] und Klinik [29] ihre Machbarkeit gezeigt haben.
Die Nanopartikel müssen einen relativ kleinen Kern haben (Durchmesser 10–30 nm), damit sie lange genug im Blut verweilen, um ihr Ziel erreichen zu können. Auch der Magnetfeldgradient ist von großer Bedeutung, da die Kraft, welche auf den Nanopartikel einwirkt, nicht nur vom magnetischen Moment abhängt. Weitere Parameter, die den Erfolg des „Magnetic-guided targeting” beeinflussen, sind die Temperatur, die Viskosität des Umgebungsmediums, die Fließgeschwindigkeiten, die Interaktionen der Nanopartikel mit den umgebenden Komponenten sowie ihre Größe und Form.
Den Tumoren einheizen mit magnetischer Hyperthermie
Aufgrund ihres Wärmepotenzials eignen sich die Nanopartikel als Werkzeuge für die magnetische Hyperthermie, d.h. die gezielte Überwärmung einzelner Körperregionen oder Organe. Das Wärmepotenzial definiert die freigesetzte Wärmemenge pro Masse- und Zeiteinheit während der Exposition des Materials in einem magnetischen Wechselfeld. Hinsichtlich der Temperaturen unterscheidet man
- magnetische Hyperthermie, bis 46 °C [30] und
- magnetische Thermoablation, über 50 °C [31].
Ursachen der Freisetzung von Wärme sind vornehmlich die Reorientierung der remagnetisierten Nanopartikel während der Exposition in einem magnetischen Wechselfeld und die Reibungsverluste, wenn die Partikel in einem Medium rotieren können.
Zur Erwärmung von Gewebe hat man zunächst sog. Multidomänen-Nanopartikel eingesetzt [32, 33], neuerdings auch nadelförmige Nanopartikel [34]. In diesen Fällen hängt das Wärmepotenzial von Remagnetisierungsprozessen ab, welche in komplexer Art durch Größe, Form und Nanostruktur der Nanopartikel definiert sind. Die induktive Erwärmung über Wirbelströme spielt dabei eine untergeordnete Rolle. Multidomänen-Nanopartikel (ferromagnetische Materialien, MPIOs) sind durch Bereiche gleicher magnetischer Momente gekennzeichnet, die durch eine Domänenwand voneinander getrennt sind. Während der Exposition im magnetischen Wechselfeld wird Energie in das System eingebracht, damit die magnetischen Momente definierte Energiebarrieren überwinden können, was sich in Domänenwandverschiebungen äußert [35]. Dabei wurden Wärmepotenziale bis zu 1 kW/g (Amplitude: 9 kA/m, 410 kHz) erreicht. In letzter Zeit wurde jedoch die Anwendung von SPIOs favorisiert. Die wesentlichen Gründe dafür sind eine bessere Suspendierbarkeit, die Zulassung von Formulierungen durch die FDA und die Möglichkeit von gut reproduzierbaren Applikationen.
Die generierte Wärme erhöht die Bewegung einzelner Moleküle in den Zellen. Sie kann auch zu einem erhöhten Metabolismus und einer ausgeprägten strukturellen Transformation (vom geordneten zum ungeordneten Status) von Zellbestandteilen (DNA, RNA, Proteine) führen. Weitere Folgen sind: Proteinaggregation und -unlöslichkeiten, erhöhte Fluidität und veränderte Ionenpermeabilität zellulärer Membranen, Hemmung des Aminosäurentransports, morphologische Veränderungen z.B. als Folge von Schädigungen des Zytoskeletts, Hemmung der DNA-Reparatur etc. [36].
Temperaturen bis 45°C verringern die Hypoxie von Tumoren und erhöhen ihre Durchblutung durch die Erweiterung innervierter Gefäße [37]. Bei der Kombination der Hyperthermie mit der Radiotherapie ergibt sich ein synergistischer Effekt, weil hypoxisches Gewebe relativ insensitiv für die Bestrahlung ist. In ähnlicher Weise kann die Hyperthermie die zytotoxischen Effekte einiger Chemotherapeutika verstärken, insbesondere von Alkylanzien, Platinverbindungen und Anthracyclinen (z.B. Doxorubicin) [38, 39].
Temperaturen über 50°C führen zu Nekrosen im Tumorgewebe sowie zur Koagulation [31]. Die kritischen Temperaturen zur Induktion der Apoptose liegen zwischen 51 und 55°C bei einer Expositionszeit von etwa 5 min [40]. In zahlreichen präklinischen Studien konnte eindeutig gezeigt werden, dass Eisenoxid-Nanopartikel die zur Tumorzerstörung notwendigen Temperaturerhöhungen generieren können [31, 40–42].
Mittels magnetischer Hyperthermie sind bereits Tumorpatienten mit Glioblastoma multiforme [43] und Prostatakarzinom [44] behandelt worden; ihnen wurden Aminosilan-umhüllte Eisenoxid-Nanopartikel intratumoral appliziert. Der Median der erzielten Temperaturen lag bei 44,6 bzw. 41,1°C. Die Analyse von Gehirnbiopsien bestätigte die Anwesenheit von verstreuten oder aggregierten Nanopartikeln im Tumorgewebe; sie waren von Makrophagen phagozytiert worden, während die Aufnahme durch Glioblastomzellen vergleichsweise gering war [45]. Insgesamt haben die Patienten die Therapie gut toleriert. Ungeachtet dieses Erfolges ist es aber noch zu früh, die therapeutische Effizienz der Hyperthermie im Vergleich zu etablierten onkologischen Verfahren zu bewerten.
Derzeit wird die Eignung von Nanopartikeln zur Therapie von Tumoren der Brust und der Bauchspeicheldrüse untersucht. Dabei wird vor allem das „Magnetic-guided Targeting“ in Kombination mit der magnetischen Hyperthermie erprobt. Die Abgabe des Wirkstoffs im Tumor kann wärmebedingt durch Desorption oder durch physikochemische Konformationsänderungen der Nanopartikel (z.B. Schwellung der Hülle) erfolgen. Derartige temperatursensitive Materialien sind Polymere mit einem Phasenübergang zwischen 35 und 42°C wie PNIPAM [Poly(N-isopropylacrylamide)] [46] oder Alginate [47]. Zur Wirkstofffreisetzung werden im Allgemeinen wesentlich geringere Wärmemengen benötigt als zur Zerstörung von Tumoren.
Monitoring der Stammzelltherapie
Der Applikation von Stammzellen verspricht ein hohes Potenzial für die Behandlung von vielen degenerativen Erkrankungen [48, 49]. Sie könnte z.B. eine Option sein bei Patienten mit kardiovaskulären oder neurologischen Erkrankungen [52], Hirntraumata [53], multipler Sklerose [54] Melanomen [55] oder Diabetes mellitus Typ 1 [56].
Die Migration der Stammzellen vom Injektionsort in das Zielgewebe sowie ihre Verteilung und Ausbreitung im Körper können mittels MRT kontrolliert werden, wenn sie magnetische Nanopartikel aufgenommen haben. Die zelluläre Aufnahme hängt in komplexer Weise von Größe, Form, Oberflächenladung und -zusammensetzung der Nanopartikel, aber auch vom verwendeten Stammzelltyp ab. Zugleich müssen Funktionalität, Migrationspotenzial und Vitalität der Stammzellen erhalten bleiben.
Diese Aspekte wurden in umfangreichen In-vitro-Tests erforscht [50]. Die Stammzellen wurden mit zugelassenen Eisenoxid-Nanopartikeln (Resovist®, Endorem®, s.o.) oder auch mit nicht-zugelassenen Nanopartikeln (z.B. manganhaltige Nanopartikel) markiert. Um ihre Aufnahme in nicht-phagozytierenden Zellen zu steigern, wurden zusätzlich u.a. Membran-translozierende Peptide eingesetzt, die als „Schlepper“ an der Zellmembran fungieren [51, 52]. Eine von mehreren Herausforderungen beim Monitoring mittels MRT ist die asymmetrische Teilung von Nanopartikel-markierten Stammzellen [57].
Nanosensoren
Nanosensoren ändern nach der Interaktion mit bestimmten Molekülen ihren Aggregatzustand, was wiederum ihre Relaxivität ändert und zu einer spezifischen Signalgebung im MRT führt. Somit eignen sie sich zum Nachweis von krankheitsspezifischen Enzymen; beispielsweise konnte die Anwesenheit der ADP-Ribosyltransferase 2 (ein Marker auf der Oberfläche von Lymphomzellen) in einem MRT-Scanner ermittelt werden [58]. Auch Methylasen, Restriktionsendonucleasen, Trypsin, Renin, Matrixmetalloproteinasen oder Caspase 3 lassen sich durch Nanosensoren im Gewebe nachweisen [59–62].
Zusammenfassung
Verzögerungen in der klinischen Entwicklung, organisatorische Probleme beim Marktzugang, auslaufende Patente und Weiterentwicklungen der bildgebenden Techniken haben die Verwendung von Eisenoxid-Nanopartikeln als Kontrastmittel eingeschränkt. Durch innovative therapeutische und diagnostische Indikationen könnten sie wieder an Bedeutung gewinnen. Zahlreiche Initiativen auf nationaler und internationaler Ebene fördern das Grundlagenwissen (siehe http://nanopartikel.info).
Besondere Herausforderungen sind nach wie vor die Optimierung der magnetischen Eigenschaften für die jeweilige Anwendung sowie umfangreiche toxikologische Studien zur Verbesserung der Verträglichkeit. Weitere Forschungsfelder sind die Anbindung von biologischen Molekülen an die Oberfläche der Nanopartikel, die Weiterentwicklung der Nanopartikelumhüllungen und das Monitoring nach der Injektion in die Blutbahn.
Literatur
[1] Wahajuddin and S. Arora, Superparamagnetic iron oxide nanoparticles: magnetic nanoplatforms as drug carriers. Int J Nanomedicine, 2012. 7: p. 3445-71.
[2] Mandarano, G., et al., Development and use of iron oxide nanoparticles (Part 2): The application of iron oxide contrast agents in MRI. Biomedical Imaging and Intervention Journal, 2010. 6: p. 1823-5530.
[3] Reddy, L.H., et al., Magnetic Nanoparticles: Design and Characterization, Toxicity and Biocompatibility, Pharmaceutical and Biomedical Applications. Chemical Reviews, 2012. 112(11): p. 5818-5878.
[4] Rosenthal, M. and R. Glew, Medical Biochemistry - Human Metabolism in Health and Disease. 2009, New Jersey USA: Wiley.
[5] Hilger, I. and W.A. Kaiser, Iron oxide-based nanostructures for MRI and magnetic hyperthermia. Nanomedicine (Lond), 2012. 7(9): p. 1443-59.
[6] Kircher, M.F. and J.K. Willmann, Molecular Body Imaging: MR Imaging, CT, and US. Part I. Principles. Radiology, 2012. 263(3): p. 633-643.
[7] Geraldes, C.F.G.C. and S. Laurent, Classification and basic properties of contrast agents for magnetic resonance imaging. Contrast Media & Molecular Imaging, 2009. 4(1): p. 1-23.
[8] Dunlop, D.J., Superparamagnetic and Single-Domain Threshold Sizes in Magnetite. Journal of Geophysical Research, 1973.
[9] Huang, X., et al., The shape effect of mesoporous silica nanoparticles on biodistribution, clearance, and biocompatibility in vivo. ACS Nano, 2011. 5(7): p. 5390-9.
[10] Mahmoudi, M., et al., Cell toxicity of superparamagnetic iron oxide nanoparticles. J Colloid Interface Sci, 2009. 336(2): p. 510-8.
[11] Bahring, F., et al., Suitability of Viability Assays for Testing Biological Effects of Coated Superparamagnetic Nanoparticles. Magnetics, IEEE Transactions on, 2013. 49(1): p. 383-388.
[12] Mahmoudi, M., et al., Superparamagnetic iron oxide nanoparticles (SPIONs): Development, surface modification and applications in chemotherapy. Advanced Drug Delivery Reviews, 2011. 63(1–2): p. 24-46.
[13] Fleige, G., et al., In vitro characterization of two different ultrasmall iron oxide particles for magnetic resonance cell tracking. Invest Radiol, 2002. 37(9): p. 482-8.
[14] Betker, J.L., J. Gomez, and T.J. Anchordoquy, The effects of lipoplex formulation variables on the protein corona and comparisons with in vitro transfection efficiency. J Control Release, 2013. 171(3): p. 261-8.
[15] Tenzer, S., et al., Rapid formation of plasma protein corona critically affects nanoparticle pathophysiology. Nature nanotechnology, 2013. 8(10): p. 772-781.
[16] Jansch, M., et al., Adsorption kinetics of plasma proteins on ultrasmall superparamagnetic iron oxide (USPIO) nanoparticles. International Journal of Pharmaceutics, 2012. 428(1–2): p. 125-133.
[17] Rahman, M. et al., Protein-Nanoparticle Interactions. Vol. 15. 2013, Berlin Heidelberg: Springer-Verlag.
[18] Safi, M., et al., The effects of aggregation and protein corona on the cellular internalization of iron oxide nanoparticles. Biomaterials, 2011. 32(35): p. 9353-9363.
[19] Weissleder, R. and U. Mahmood, Molecular imaging. Radiology, 2001. 219(2): p. 316-33.
[20] Bohm, I., et al., [Molecular imaging of apoptosis in cardiovascular diseases]. Rofo, 2007. 179(8): p. 780-9.
[21] Bohm, I., et al., [Molecular imaging of apoptosis and necrosis -- basic principles of cell biology and use in oncology]. Rofo, 2006. 178(3): p. 263-71.
[22] Chen, T.J., et al., Targeted Herceptin-dextran iron oxide nanoparticles for noninvasive imaging of HER2/neu receptors using MRI. Journal of Biological Inorganic Chemistry, 2009. 14(2): p. 253-260.
[23] Fan, C.X., et al., Tumor selectivity of stealth multi-functionalized superparamagnetic iron oxide nanoparticles. International Journal of Pharmaceutics, 2011. 404(1-2): p. 180-190.
[24] Lee, H.Y., et al., PET/MRI dual-modality tumor imaging using arginine-glycine-aspartic (RGD) - Conjugated radiolabeled iron oxide nanoparticles. Journal of Nuclear Medicine, 2008. 49(8): p. 1371-1379.
[25] Sperling, R.A. and W.J. Parak, Surface modification, functionalization and bioconjugation of colloidal inorganic nanoparticles. Philos Trans A Math Phys Eng Sci, 2010. 368(1915): p. 1333-83.
[26] Zhang, C., et al., Specific targeting of tumor angiogenesis by RGD-conjugated ultrasmall superparamagnetic iron oxide particles using a clinical 1.5-T magnetic resonance scanner. Cancer Res, 2007. 67(4): p. 1555-62.
[27] Zhang, C.Y., J. Lu, and A. Tsourkas, Iron chelator-based amplification strategy for improved targeting of transferrin receptor with SPIO. Cancer Biology & Therapy, 2008. 7(6): p. 889-895.
[28] Alexiou, C., et al., Locoregional cancer treatment with magnetic drug targeting. Cancer Res, 2000. 60(23): p. 6641-8.
[29] Lubbe, A.S., et al., Clinical experiences with magnetic drug targeting: a phase I study with 4‘-epidoxorubicin in 14 patients with advanced solid tumors. Cancer Res, 1996. 56(20): p. 4686-93.
[30] Jordan, A., et al., Effects of magnetic fluid hyperthermia (MFH) on C3H mammary carcinoma in vivo. International Journal of Hyperthermia, 1997. 13(6): p. 587-605.
[31] Hilger, I., et al., Electromagnetic heating of breast tumors in interventional radiology: In vitro and in vivo studies in human cadavers and mice. Radiology, 2001. 218(2): p. 570-575.
[32] Gilchrist, R.K., R. Medal, and W.D. Shorey, Selective inductive heating of lymph nodes. Annals of Surgery 1957. 146: p. 596 - 606
[33] Berkov, D., Basic Physical Principles, in Magnetism in Medicine, A Handbook, W. Andra and H. Nowak, Editors. 2007, Wiley-VCH Verlag GmbH & Co. KGaA: Berlin. p. 26-64.
[34] Zablotskii, V., O. Lunov, and C. Gomez-Plo, Magnetic Heating by Tunable Arrays of Nanoparticles in Cancer Therapy. Acta Physica Polonica A, 2009. 115(1): p. 413-417.
[35] Hergt, R., et al., Physical limits of hyperthermia using magnetite fine particles. Ieee Transactions on Magnetics, 1998. 34(5): p. 3745-3754.
[36] Lepock, J.R., Cellular effects of hyperthermia: relevance to the minimum dose for thermal damage. International Journal of Hyperthermia, 2003. 19(3): p. 252-266.
[37] Multhoff, G. and U. Gaipl, Molekulare und immunologische Effekte der Hyperthermie auf Tumorprogression und Metastasierung. Onkologe, 2010. 11: p. 1043 - 1050.
[38] Hildebrandt, B., et al., The cellular and molecular basis of hyperthermia. Crit Rev Oncol Hematol, 2002. 43(1): p. 33-56.
[39] Schildkopf, P., et al., Biological Rationales and Clinical Applications of Temperature Controlled Hyperthermia - Implications for Multimodal Cancer Treatments. Current Medicinal Chemistry, 2010. 17(27): p. 3045-3057.
[40] Hilger, I., et al., Assessment of DNA damage in target tumor cells after thermoablation in mice. Radiology, 2005. 237(2): p. 500-506.
[41] Hilger, I., et al., Magnetic Heating as a Therapeutic Tool. Thermology international, 2001. 11/3: p. 130-136.
[42] Hilger, I. and W.A. Kaiser, Parameters Influencing the Efficacy of Magnetic Heating of Small Breast Tumors, in Nanomedicine - Basic and Clinical Applications in Diagnostics and Therapy, C. Alexiou, Editor. 2011.
[43] Maier-Hauff, K., et al., Intracranial thermotherapy using magnetic nanoparticles combined with external beam radiotherapy: Results of a feasibility study on patients with glioblastoma multiforme. Journal of Neuro-Oncology, 2007. 81(1): p. 53-60.
[44] Johannsen, M., et al., Thermotherapy of prostate cancer using magnetic nanoparticles: Feasibility, imaging, and three-dimensional temperature distribution. European Urology, 2007. 52(6): p. 1653-1662.
[45] Kettering, K., et al., Enhanced detection criteria in implantable cardioverter defibrillators: sensitivity and specificity of the stability algorithm at different heart rates. Pacing Clin Electrophysiol, 2001. 24(9 Pt 1): p. 1325-33.
[46] Luo, B., et al., Multi-functional thermosensitive composite microspheres with high magnetic susceptibility based on magnetite colloidal nanoparticle clusters. Langmuir, 2010. 26(3): p. 1674-9.
[47] Hawkins, A.M., N.S. Satarkar, and J.Z. Hilt, Nanocomposite degradable hydrogels: demonstration of remote controlled degradation and drug release. Pharm Res, 2009. 26(3): p. 667-73.
[48] Weissman, I.L., Translating stem and progenitor cell biology to the clinic: Barriers and opportunities. Science, 2000. 287(5457): p. 1442-1446.
[49] Morigi, M., et al., The regenerative potential of stem cells in acute renal failure. Cell Transplantation, 2006. 15: p. S111-S117.
[50] Conner, S. and S. Schmid, Regulated portals of entry into the cell. Nature, 2003. 422: p. 37 - 44.
[51] Neoh, K.G. and E.T. Kang, Surface modification of magnetic nanoparticles for stem cell labeling. The Royal Society of Chemistry, 2012. 8: p. 2057 - 2069.
[52] Berman, S.M.C., P. Walczak, and J.W.M. Bulte, Tracking stem cells using magnetic nanoparticles. Wiley Interdisciplinary Reviews-Nanomedicine and Nanobiotechnology, 2011. 3(4): p. 343-355.
[53] Zhu, J.H., L.F. Zhou, and F.G. XingWu, Tracking neural stem cells in patients with brain trauma. New England Journal of Medicine, 2006. 355(22): p. 2376-2378.
[54] Karussis, D., et al., Safety and Immunological Effects of Mesenchymal Stem Cell Transplantation in Patients With Multiple Sclerosis and Amyotrophic Lateral Sclerosis. Archives of Neurology, 2010. 67(10): p. 1187-1194.
[55] de Vries, I., et al., Magnetic resonance tracking of dendritic cells in melanoma patients for monitoring of cellular therapy. Nat Biotechnol, 2005. 23 p. 1407–1413.
[56] Toso, C., et al., Clinical magnetic resonance imaging of pancreatic islet grafts after iron nanoparticle labeling. American Journal of Transplantation, 2008. 8(3): p. 701-706.
[57] Walczak, P., et al., Applicability and limitations of MR tracking of neural stem cells with asymmetric cell division and rapid turnover: The case of the shiverer dysmyelinated mouse brain. Magnetic Resonance in Medicine, 2007. 58(2): p. 261-269.
[58] Bannas, P., et al., Quantitative Magnetic Resonance Imaging of Enzyme Activity on the Cell Surface: In Vitro and In Vivo Monitoring of ADP-Ribosyltransferase 2 on T Cells. Molecular Imaging, 2010. 9(4): p. 211-222.
[59] Perez, J.M., et al., DNA-based magnetic nanoparticle assembly acts as a magnetic relaxation nanoswitch allowing screening of DNA-cleaving agents. J Am Chem Soc, 2002. 124(12): p. 2856-7.
[60] Perez, J.M., et al., Magnetic relaxation switches capable of sensing molecular interactions. Nat Biotechnol, 2002. 20(8): p. 816-20.
[61] Josephson, L., J.M. Perez, and R. Weissleder, Magnetic nanosensors for the detection of oligonucleotide sequences. Angewandte Chemie-International Edition, 2001. 40(17): p. 3204-+.
[62] Zhao, M., et al., Magnetic sensors for protease assays. Angew Chem Int Ed Engl, 2003. 42(12): p. 1375-8.
Autorinnen
Friedrich-Schiller-Universität Jena
Institut für Pharmazie Professur für Pharmazeutische Technologie
Otto-Schott-Str. 41, 07745 Jena
Dagmar.Fischer@uni-jena.de























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.