
- DAZ.online
- DAZ / AZ
- DAZ 4/2013
- Rezepturen elektronisch ...
Praxis
Rezepturen elektronisch dokumentieren
Die elektronische Rezepturdokumentation des Laborprogramms versieht die einzelnen Schritte der notwendigen Dokumentation (Plausibilitätsprüfung, Herstellungsanweisung, Herstellungsprotokoll und Etikettendruck) mit dem Komfort einer Datenbank-Unterstützung. So braucht der Anwender des Programms die Rezepturzusammensetzung nur noch einmal einzugeben, um alle drei genannten Dokumente zu erhalten.
Automatisierung spart Zeit und Arbeit
Der Ablauf im Laborprogramm gliedert sich in vier aufeinanderfolgende Schritte:
- Rezepturdatenerfassung,
- Plausibilitätsprüfung,
- Herstellungsanweisung und
- Herstellungsprotokoll.
Wurde in der Apotheke bereits eine Rezeptur gleicher Zusammensetzung hergestellt und mit dem Laborprogramm dokumentiert, kann der Anwender auf die elektronisch gespeicherte Plausibilitätsprüfung und Herstellungsanweisung zurückgreifen. Unter Bezugnahme auf die genannten Dokumente genügt es, die erneute Anfertigung dieser Rezeptur lediglich in einem neuen Herstellungsprotokoll festzuhalten. Den Verweis auf die richtigen Referenzdokumente übernimmt das Programm automatisch. Alle Dokumente werden übersichtlich und nachvollziehbar in einem Protokollarchiv abgelegt, wo sie jederzeit einsehbar sind.
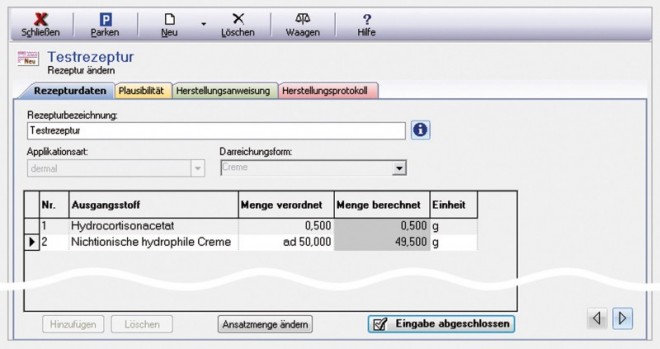
Rezepturdatenerfassung (Abb. 1)
Zu Beginn einer jeden neuen Rezeptur müssen die Rezepturdaten erfasst werden. Zur leichteren Identifikation und Wiederauffindung der Rezeptur wird die Vergabe einer eindeutigen Kurzbezeichnung (Rezepturname) nach einem festen Schema empfohlen. Ferner sind die Applikationsart und die Darreichungsform der Zubereitung anzugeben. Deren Wahl wirkt sich auf die im weiteren Verlauf angezeigten Daten und Abfragen aus. So wird beispielsweise bei Augentropfen auf Isotonie geprüft, bei dermal applizierten Zubereitungen hingegen nicht. Ferner wird für die Beurteilung des ärztlichen Therapiekonzepts die Angabe der Applikationsart benötigt. Nur so kann mithilfe der im Laborprogramm hinterlegten Datenbank überprüft werden, ob die Applikationsart für den Wirkstoff oder die Wirkstoffe bekannt bzw. plausibel ist. Außerdem muss für jeden einzelnen Wirkstoff kontrolliert werden, ob dessen Konzentration bzw. Einzeldosis innerhalb des angegebenen, üblichen Dosierungsbereiches liegt, wobei ebenfalls die Applikationsart der Zubereitung maßgeblich ist.
Nach der Eingabe der Applikationsart stellt das Programm automatisch eine Liste der infrage kommenden Darreichungsformen zusammen, aus der der Anwender auswählen kann. Im Anschluss daran gibt er nacheinander die einzelnen Rezepturbestandteile ein. Diese stehen dann für alle nachfolgenden Dokumentationsschritte zur Verfügung und müssen dort nicht erneut eingegeben werden. Nachdem die Eingabe der Rezepturzusammensetzung abgeschlossen ist, folgt die Plausibilitätsprüfung.
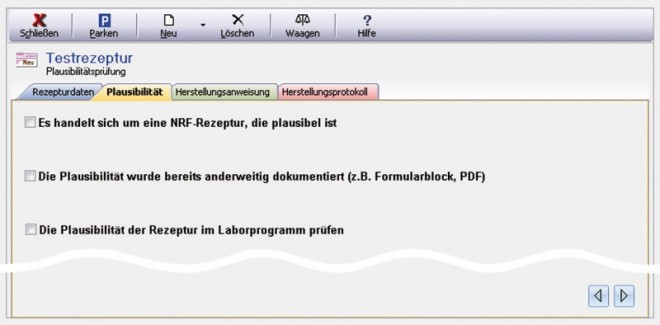
Bezugnahme auf vorhandene Dokumente möglich (Abb. 2)
Auf der Startseite der Plausibilitätsprüfung stehen drei Optionen zur Verfügung.
Die erste Option bietet die Möglichkeit, auf eine NRF-Monografie Bezug zu nehmen. Da NRF-Rezepturen im Rahmen ihrer Entwicklung ausgiebig hinterfragt und im Labor analytisch untersucht worden sind, kann eine Plausibilitätsprüfung in diesen Fällen entfallen. Konsequenterweise überspringt das Laborprogramm bei Auswahl der Option "NRF-Rezeptur" die Plausibilitätsprüfung.
Wenn auf eine bereits durchgeführte und anderweitig dokumentierte Plausibilitätsprüfung Bezug genommen wird, kann ebenfalls auf eine neuerliche Prüfung im Laborprogramm verzichtet werden (vorausgesetzt, die Bewertungsgrundlage entspricht noch dem aktuellen Stand der Wissenschaft). Es ist lediglich eine eindeutige Referenz anzugeben, die das schnelle und problemlose Auffinden des Originaldokuments der Plausibilitätsprüfung gewährleistet. Auch hierfür ist im Laborprogramm eine entsprechende Option vorgesehen.
Die dritte Option bietet die Möglichkeit, die Plausibilität einer Rezeptur mithilfe des Laborprogramms zu überprüfen. Bei Auswahl dieser Option gelangt der Anwender in einen Prüfdialog, in dem die verfügbaren Literaturdaten für die eingegebenen Ausgangsstoffe als Grundlage für eine Bewertung der Plausibilität angezeigt werden.
Bei Start der elektronischen, datenbankgestützten Plausibilitätsprüfung wird zunächst festgelegt, ob die Zubereitung wasserfrei ist oder nicht. Dies wirkt sich auf die im weiteren Verlauf zu beantwortenden Fragen aus. So wird bei wasserfreien Zubereitungen etwa auf eine Überprüfung von Konservierung und Hydrolyseempfindlichkeit verzichtet.
Der Anwender entscheidet
Allen Registerkarten des Prüfdialogs ist gemeinsam, dass im oberen Bereich Literaturdaten präsentiert werden, die als Entscheidungsgrundlage für die Beantwortung einer Frage dienen. Die Frage ist durch Klick auf die entsprechende Schaltfläche unten mit [Ja] oder [Nein] zu beantworten. Die angezeigten Literaturdaten dienen dem Anwender dabei als Hilfestellung bei der theoretischen Beurteilung einer Rezeptur. Ihm obliegt demzufolge die abschließende Entscheidung, sodass er auch nicht seiner pharmazeutischen Verantwortung entbunden wird. Bei unklarer Datenlage oder wenn mehrere Optionen bestehen (z. B. können monografierte Grundlagen sowohl unkonserviert als auch konserviert zum Einsatz kommen), legt die Anzeige des Laborprogramms aus Sicherheitsgründen eine präventiv zurückhaltende Bewertung nahe. Konsequenterweise steht es dem Anwender jederzeit frei, eigenverantwortlich und unabhängig von den angezeigten Literaturdaten aufgrund eigener und/oder rezepturspezifischer Erkenntnisse zu einer anderen Einschätzung zu gelangen, als dies die angezeigte Datenlage implizieren würde.
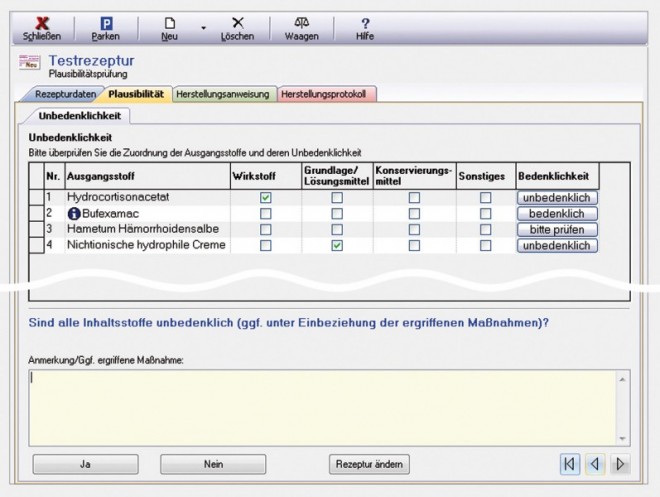
Unbedenklichkeit (Abb. 3)
Zunächst muss der Anwender die einzelnen Rezepturbestandteile auf ihre Unbedenklichkeit im Sinne des § 5 Abs. 1 des Arzneimittelgesetzes (AMG) prüfen. Um ihm dies zu erleichtern, gleicht das Laborprogramm die einzelnen Bestandteile der Rezeptur mit der jeweils aktuellen Liste der bedenklichen Rezepturgrundstoffe ab, die von der Arzneimittelkommission der Deutschen Apotheker veröffentlicht wird (AMK-Liste). Werden bedenkliche Inhaltsstoffe erkannt, so wird dies durch den Vermerk "bedenklich" in der letzten Spalte angezeigt. Ausgangsstoffe, die bekanntermaßen unbedenklich sind, werden als "unbedenklich" markiert. Ausgangsstoffe, die vom Programm nicht erkannt werden oder zu denen keine Daten vorliegen, tragen den Vermerk "bitte prüfen". Durch einen Klick auf die jeweilige Schaltfläche in der Spalte [Bedenklichkeit] kann sich der Anwender des Programms die AMK-Liste im Volltext anzeigen lassen und die vorgeschlagene Einstufung ggf. ändern.
Neben der Bedenklichkeitsprüfung ist auf dieser Registerkarte auch eine Zuordnung vorzunehmen, ob es sich bei den einzelnen Ausgangsstoffen um einen Wirkstoff, eine Grundlage bzw. ein Lösungsmittel, ein Konservierungsmittel oder sonstige Substanzen (z. B. Emulgatoren, Puffer o. ä.) handelt. Diese Einstufung ist u. a. für die nachfolgende Überprüfung der Wirkstoff- bzw. Konservierungsmittelkonzentration relevant. Auch hierfür unterbreitet das Laborprogramm – sofern für die ausgewählten Stoffe Daten in der Datenbank enthalten sind – entsprechende Vorschläge, die der Anwender ändern kann bzw., falls keine Daten hinterlegt sind, ergänzen muss. Substanzen, die vom Programm sowohl als Wirkstoff als auch als Konservierungsmittel gekennzeichnet sind, wirken in therapeutischer Konzentration konservierend. Ausgangsstoffe, die vom Programm sowohl als Grundlage/Lösungsmittel als auch als Konservierungsmittel gekennzeichnet sind, sind ausreichend konserviert, sofern kein weiteres Wasser zugefügt wird.
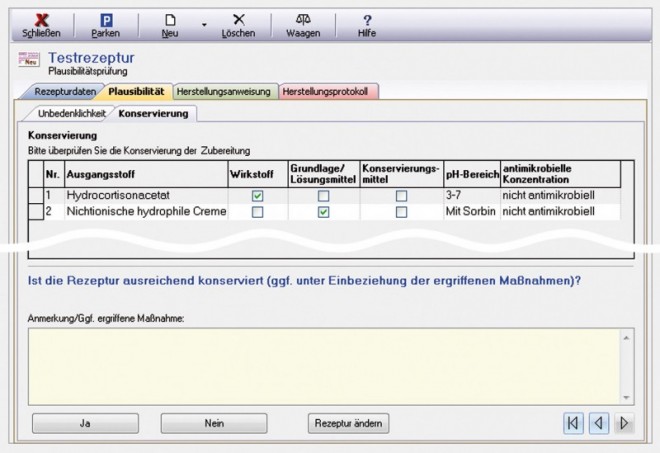
Konservierung (Abb. 4)
Diese Registerkarte wird nur bei wasserhaltigen Zubereitungen angezeigt. Das Laborprogramm zeigt für alle Wirk- und Konservierungsmittel automatisch den rezeptierbaren bzw. antimikrobiell wirksamen pH-Bereich sowie die antimikrobielle Substanzkonzentration an – sofern entsprechende Daten vorliegen. Wirkstoffe, die in therapeutischer Konzentration nicht antimikrobiell wirksam sind, werden als "nicht antimikrobiell" gekennzeichnet. Gleiches gilt für Grundlagen / Lösungsmittel, die kein Konservierungsmittel enthalten oder sowohl konserviert als auch unkonserviert vorkommen können. Falls es sich im konkreten Fall um eine konservierte Variante der Grundlage handelt, kann der Anwender das Häkchen in der Spalte Konservierungsmittel ggf. selbst ergänzen.
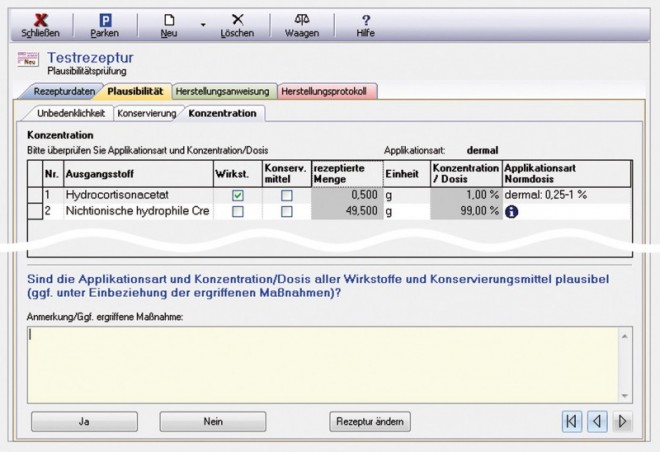
Applikationsart und Dosis (Abb. 5)
Zur Beurteilung des ärztlichen Therapiekonzepts wird mithilfe von Literaturdaten überprüft, ob die bei den Rezepturdaten ausgewählte Applikationsart für den Wirkstoff / die Wirkstoffe bekannt bzw. plausibel ist. Außerdem wird für jeden einzelnen Wirkstoff überprüft, ob die errechnete Konzentration bzw. Einzeldosis innerhalb des üblichen Dosierungsbereiches liegt. Auch hierbei wird die Applikationsart der Zubereitung berücksichtigt.
Um die Dosierung zu beurteilen, zeigt das Laborprogramm die Normdosis für die ausgewählte Applikationsart an. Ist die bei der Rezepturdatenerfassung eingestellte Applikationsart für den jeweiligen Wirkstoff unüblich oder liegen hierfür keine Normdosen vor, so bleibt die Spalte "Applikationsart/Normdosen" bis auf einen Info-Button leer. Durch einen Klick auf den Info-Button werden die für den jeweiligen Wirkstoff üblichen Applikationsarten sowie die dazugehörigen Normdosen angezeigt:
Im Einzelfall kann eine Überschreitung der genannten Konzentrationen bzw. Einzeldosen therapeutisch durchaus begründet sein. In solch einem Fall wäre die Frage nach der Plausibilität von Applikationsart und Konzentration mit [Ja] zu beantworten und im vorhandenen Freitextfeld eine entsprechende Anmerkung einzutragen. Bei Grundlagen findet sich in der Spalte "Applikationsart/Normdosen" ein Info-Button, der darauf verweist, dass eine Konzentrationsüberprüfung bei reinen Grundlagen nicht notwendig ist.
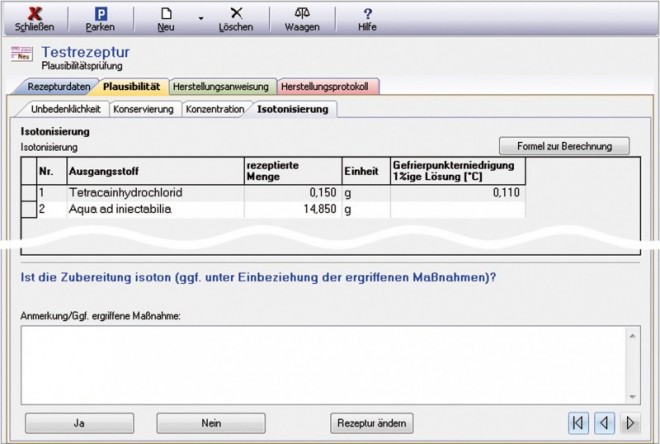
Isotonisierung (Abb. 6)
Diese Registerkarte wird nur bei denjenigen Darreichungsformen angezeigt, für die Isotonie zu gewährleisten ist. Das Laborprogramm stützt sich hierbei auf die weit verbreitete Berechnungsmethode über die Gefrierpunktserniedrigung. Dazu wird in der Tabelle die Gefrierpunktserniedrigung für eine 1%ige Lösung der entsprechenden Substanz angezeigt. Die Formel zur Berechnung der Gefrierpunktserniedrigung der Zubereitung (Sollwert: ΔTf = 0,52 °C) sowie eingehende Erläuterungen hierzu erhält der Anwender durch einen Klick auf die Schaltfläche [Formel zur Berechnung].
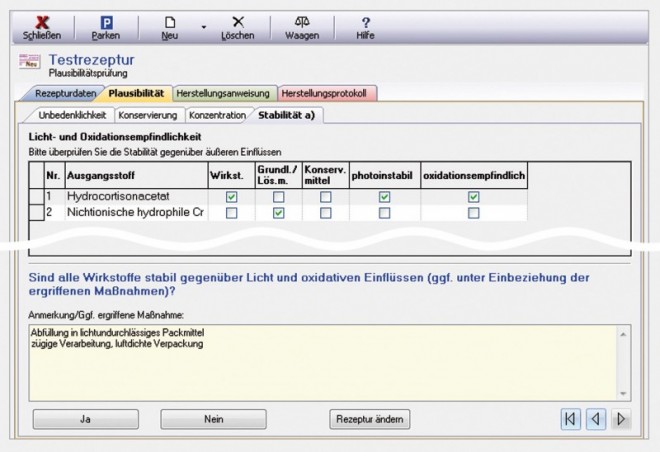
Licht- und Oxidationsempfindlichkeit (Abb. 7)
Diese Registerkarte zeigt an, ob für die einzelnen Ausgangsstoffe in der Literatur Hinweise auf Photoinstabilität oder Oxidationsempfindlichkeit zu finden sind. Die Bewertung der Relevanz etwaiger Photoinstabilitäten oder Oxidationsempfindlichkeit obliegt dem Anwender, der die Häkchen nach seinem pharmazeutischen Ermessen ergänzen oder entfernen kann. Sollte eine der Substanzen als "photoinstabil" gekennzeichnet sein, wird bei den ergriffenen Maßnahmen automatisch der Textbaustein "Abfüllung in lichtundurchlässiges Packmittel" eingefügt. Das Gleiche gilt analog für die Eigenschaft "oxidationsempfindlich" und den Textbaustein "zügige Verarbeitung, luftdichte Verpackung". Sollten diese Maßnahmen vom Anwender des Programms als unzureichend oder übertrieben erachtet werden, können diese jederzeit abgeändert werden.
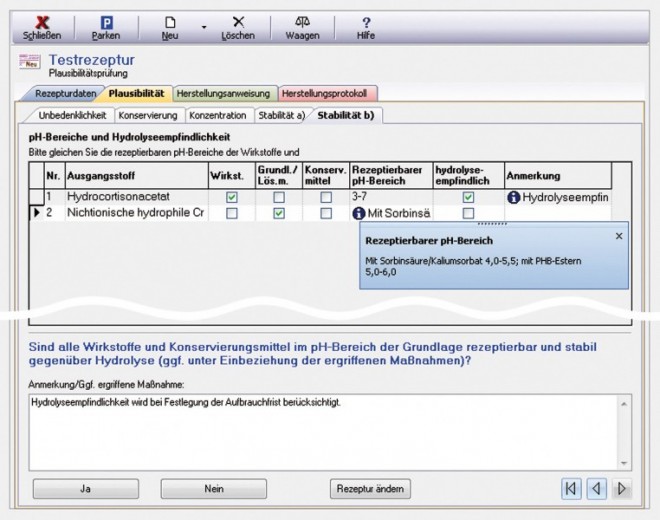
pH-Bereiche / Hydrolyseempfindlichkeit (Abb. 8)
Mithilfe dieser Registerkarte kann der Anwender die Übereinstimmung der rezeptierbaren pH-Bereiche sowie die Hydrolyseempfindlichkeit der eingesetzten Ausgangsstoffe überprüfen. Sie zeigt die rezeptierbaren pH-Bereiche der Wirkstoffe sowie die pH-Bereiche der eingesetzten Grundlagen (vor der Einarbeitung anderer Substanzen) an, damit die entsprechenden Literaturdaten möglichst einfach miteinander verglichen werden können. Die in der darauf folgenden Spalte tabellierte Angabe zur Hydrolyseempfindlichkeit ist das Resultat ganz grundsätzlicher Erwägungen, ohne den pH-Bereich im Einzelnen zu berücksichtigen. In vielen Fällen ist es möglich, die Hydrolyse auf ein tolerierbares Minimum zu reduzieren, indem man sich dem jeweiligen pH-Stabilitätsoptimum und dem pH-Wirkoptimum hydrolysegefährdeter Wirkstoffe so weit wie möglich annähert. Der Hinweis auf eine hydrolytische Gefährdung des Wirkstoffs ist daher nur als Warnsignal und nicht als Ausschlusskriterium für die Verarbeitung in wässrigen Zubereitungen zu verstehen, insbesondere wenn der angegebene rezeptierbare pH-Bereich eingehalten wird. Ein gesetzter Haken in der Spalte "hydrolyseempfindlich" löst automatisch den Eintrag "Hydrolyseempfindlichkeit wird bei der Festlegung der Aufbrauchfrist berücksichtigt" bei den ergriffenen Maßnahmen aus. Auch dieser Eintrag kann bei Bedarf nach eigenem pharmazeutischem Ermessen gelöscht oder ergänzt werden.
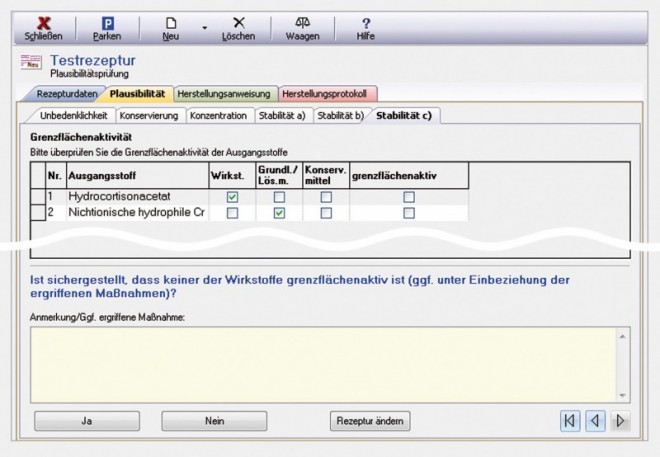
Grenzflächenaktivität (Abb. 9)
Diese Registerkarte wird nur bei Emulsionen und Cremes angezeigt. Denn in diesen Darreichungsformen können grenzflächenaktive Wirkstoffe mit an der Grenzfläche fixierten Emulgatoren in Konkurrenz treten und so eine Schwächung des Emulgatorfilms bewirken, wodurch das Emulsionssystem als Ganzes destabilisiert wird. Prinzipiell können alle tensidartigen Stoffe mit Emulgatoren Wechselwirkungen eingehen, allerdings ist das nicht immer ein Problem; der Effekt kann sogar gezielt eingesetzt werden (z. B. bei Komplexemulgatoren). Werden grenzflächenaktive Substanzen jedoch unkontrolliert kombiniert, führt das meist zu Unverträglichkeiten und in letzter Konsequenz zum Brechen der Emulsionssysteme. Grenzflächenaktive Wirkstoffe sollten daher in solchen Systemen möglichst nicht verarbeitet werden, sofern keine geprüfte Rezeptur vorliegt.
Ein Häkchen in der Spalte [grenzflächenaktiv] weist also lediglich auf eine potenzielle Instabilität hin und ist nicht zwingend gleichbedeutend mit einer Nichtanfertigbarkeit der Zubereitung. Bewertet der Anwender die Einarbeitung einer grenzflächenaktiven Substanz in ein Mehrphasensystem als unproblematisch, kann er dies ggf. im Freitextfeld als Anmerkung dokumentieren und die Frage mit der [Ja]-Schaltfläche beantworten.
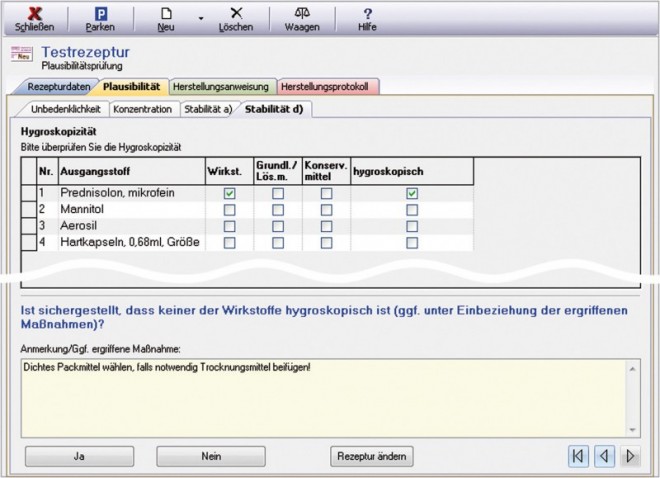
Hygroskopizität (Abb. 10)
Diese Registerkarte wird nur bei festen Zubereitungen angezeigt. Insbesondere bei der Verarbeitung von Pulvern kann sich hygroskopisches Verhalten als problematisch erweisen. Beginnen die Pulver zu kleben oder zu verklumpen, ändert sich dadurch möglicherweise sogar die systemische Bioverfügbarkeit bei oraler Verabreichung. Der Anwender soll durch einen entsprechenden Hinweis auf hygroskopische Substanzen für eventuell auftretende Probleme sensibilisiert werden. Sind laut Literaturangaben hygroskopische Bestandteile in einer festen Zubereitung (Pulver, Kapseln o. ä.) enthalten, setzt das Laborprogramm in der Spalte "hygroskopisch" automatisch ein Häkchen und fügt den Autotext "dichtes Packmittel wählen, falls notwendig Trocknungsmittel beifügen!" in das Maßnahmenfeld ein. Sowohl das Häkchen als auch den Maßnahmenvorschlag kann der Anwender bei Bedarf löschen, ändern oder ergänzen.
Kompatibilität (Abb. 11 + 12)
Für die Beurteilung der Kompatibilität stehen grundsätzlich zwei unterschiedliche Registerkarten zur Verfügung, von denen je nach Zusammensetzung der Rezeptur entweder die eine (bei nachgewiesener Kompatibilität) oder die andere (bei individuell zu prüfender Kompatibilität) angezeigt wird.
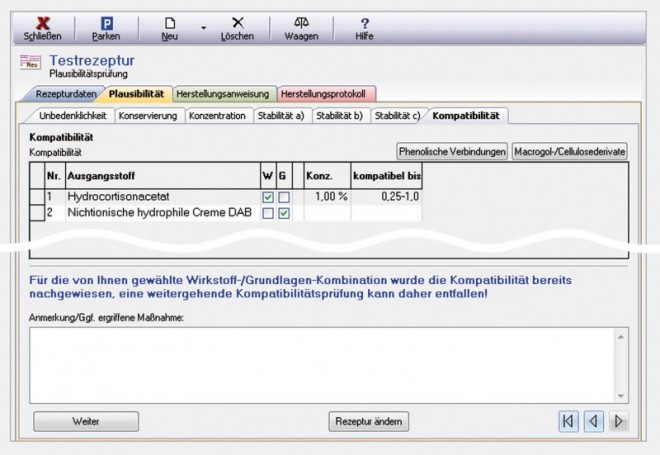
Für dermatologische Rezepturen gibt es eine Reihe von erprobten Vorschriften, die in nationalen und internationalen Vorschriftensammlungen sowie in Industrierezepturen und wissenschaftlichen Veröffentlichungen zusammengestellt sind. Wesentlicher Vorteil dieser Rezeptursammlungen ist, dass es sich um erprobte, therapeutisch sinnvolle und über den Anwendungszeitraum galenisch stabile Rezepturen handelt, bei denen die Kompatibilität ihrer Einzelbestandteile nachgewiesen ist. Liegt für eine bestimmte Rezepturzusammensetzung derlei Erkenntnismaterial vor, so wird dies vom Laborprogramm erkannt und eine Registerkarte angezeigt (siehe Abb. 11).
Die Spalten "W" und "G" geben an, ob es sich um einen Wirkstoff oder eine Grundlage handelt. In der Spalte "Konz." ist die aus den Rezepturdaten errechnete Wirkstoffkonzentration angegeben. In der Spalte "kompatibel bis" wird die höchste getestete Konzentration mit nachgewiesener Stabilität und Kompatibilität angezeigt. Da der Kompatibilitätsnachweis nur für Wirkstoffkonzentrationen bis zur tabellierten Maximalkonzentration gilt, sind Extrapolationen nicht statthaft und Aussagen nicht auf höhere Wirkstoffkonzentrationen übertragbar.
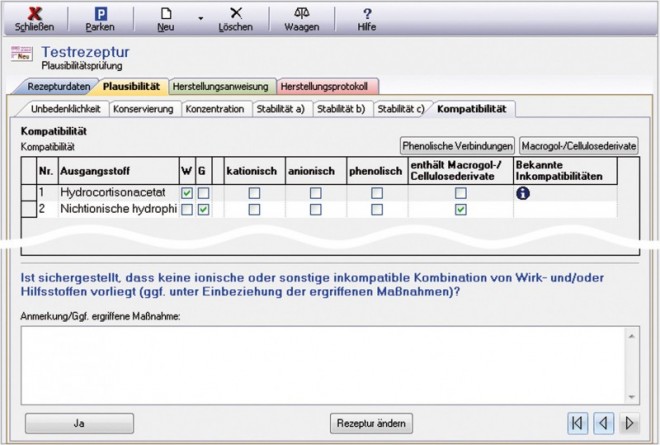
Liegt ein solcher Kompatibilitätsnachweis nicht vor, muss die Kompatibilität der einzelnen Bestandteile individuell geprüft werden. In diesem Fall wird eine andere Registerkarte angezeigt (siehe Abb. 12).
Da ionische Wechselwirkungen einerseits und Wechselwirkungen von Phenolen mit Macrogolen oder Cellulosederivaten andererseits die häufigsten Ursachen von Inkompatibilitäten darstellen, prüft das Laborprogramm anhand der angezeigten Stoffeigenschaften zunächst auf diese stoffgruppenspezifischen Inkompatibilitäten. Anschließend prüft es für jeden einzelnen Ausgangsstoff, ob bekannte substanzspezifische Inkompatibilitäten vorliegen. Wenn dies der Fall ist, wird durch einen blauen Info-Button darauf hingewiesen. Ein Klick auf den Info-Button öffnet eine entsprechende Liste, die der Anwender mit den übrigen Inhaltsstoffen der Zubereitung abgleichen kann:
Aufbrauchfrist (Abb. 13)
Rezepturen müssen bei Abgabe an den Patienten mit dem konkreten Enddatum der Aufbrauchfrist gekennzeichnet werden (§ 14 ApBetrO). Um dem Anwender die Festlegung der Aufbrauchfrist zu erleichtern, werden auf dieser Registerkarte im oberen Bereich standardisierte, arzneiformenspezifische Richtwerte angezeigt.
Die Auswahl der angezeigten Richtwerte ist abhängig von der ausgewählten Applikationsart und Darreichungsform. Die Datengrundlage, die der Anwender zur Festlegung der Aufbrauchfrist heranzieht, wird vom Laborprogramm ebenfalls dokumentiert. Die Aufbrauchfrist ist in der standardisierten, vom Programm vorgesehenen Weise einzutragen, da der Eintrag dann für die Herstellungsanweisung, das Herstellungsprotokoll und das Etikett übernommen wird. Da die Aufbrauchfrist unter anderem auch von der Wahl des jeweiligen Packmittels abhängt, ist Letzteres hier ebenfalls anzugeben.
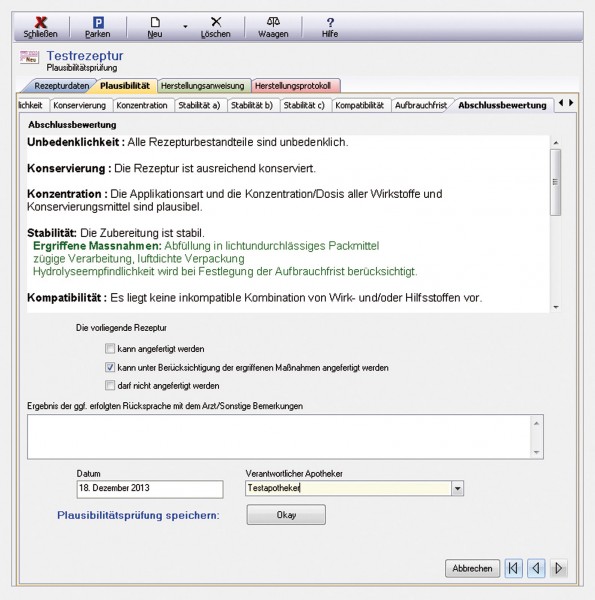
Abschlussbewertung
Nachdem alle für die Rezeptur relevanten Registerkarten der Plausibilitätsprüfung durchlaufen wurden, muss der Apotheker auf der letzten Registerkarte eine Abschlussbewertung vornehmen (Abb. 14). Hierzu werden die Ergebnisse aller vorausgegangenen Einzelprüfungen sowie ggf. ergriffenen Maßnahmen noch einmal zusammengefasst. Auf deren Grundlage kann der Apotheker beurteilen, ob die Rezeptur (ggf. unter Berücksichtigung ergriffener Maßnahmen) angefertigt werden kann oder nicht angefertigt werden darf. Ferner besteht die Möglichkeit, das Ergebnis etwaiger Rücksprachen mit dem Arzt zu dokumentieren.
Abschließend wird der für die Plausibilitätsprüfung verantwortliche Apotheker ausgewählt. Beim Speichern wird das Protokoll automatisch mit einer Dokumenten-Nummer versehen und ins Protokollarchiv verschoben, wo es als Referenzdokument für wiederkehrende Anforderungen zur Verfügung steht. Bei künftigen Rezepturherstellungen kann also einfach darauf Bezug genommen werden.
HinweisIn der nächsten DAZ lesen Sie: Rezepturen elektronisch dokumentieren – Teil 2: Mit wenigen Mausklicks zur fertigen Herstellungsanweisung |























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.