
- DAZ.online
- DAZ / AZ
- DAZ 14/2013
- Organische Polysulfide
UniDAZ
Organische Polysulfide
EditorialLiebe Leserinnen, liebe Leser! Der Siegerbeitrag des diesjährigen UniDAZ-Wissenschaftspreises ging aus einer Diplomarbeit hervor, die im Rahmen eines Kooperationsprojektes der Professur Bioorganische Chemie in der Fachrichtung Pharmazie an der Universität des Saarlandes mit dem Laboratoire de Biologie Moléculaire et Cellulaire du Cancer in Luxemburg angefertigt wurde. Damit geht der UniDAZ-Wissenschaftspreis zum zweiten Mal in Folge an ein internationales Kooperationsprojekt, das von der Universität des Saarlandes initiiert wurde. Der Preis wurde während der Interpharm in Hamburg an Anne-Kathrin Baltes verliehen (siehe DAZ Nr. 12, S. 48). Frau Baltes untersuchte in vitro die chemopräventive und ‑therapeutische Aktivität natürlicher, geruchsintensiver und synthetischer, geruchloser Schwefelverbindungen. Dabei konnte sie nachweisen, dass einige synthetische Verbindungen nicht minder wirksam sind als die im Knoblauch vorkommenden Verbindungen, da sie nicht nur deren zytotoxisches Potenzial besitzen, sondern darüber hinaus auch eine erheblich höhere Stabilität aufweisen. Lesen Sie Frau Baltes‘ spannende Abhandlung, und überzeugen Sie sich von der wissenschaftlichen Leistungsfähigkeit des pharmazeutischen Nachwuchses! Ihre UniDAZ-Redaktion |
Das antikanzerogene Potenzial von Knoblauch
Bereits vor 2500 Jahren erkannte Hippokrates den Zusammenhang zwischen der Ernährung und der körperlichen Verfassung des Menschen [3, 4]. Auch in der Pharmazeutischen Biologie wird gelehrt und erforscht, inwiefern Nahrungsbestandteile unser gesundheitliches Wohlbefinden sowohl negativ als auch positiv beeinflussen können.
Knoblauch (Allium sativum) und verwandte Arten werden seit Jahrtausenden wegen ihrer kulinarischen Vorzüge und aufgrund ihrer antiviralen, antibakteriellen, antimykotischen und weiteren Eigenschaften sowohl in der Küche als auch zur Therapie eingesetzt [2, 5 – 7]. Durch wissenschaftliche Studien hat zuerst Louis Pasteur im Jahre 1858 die antibakterielle Wirkung dieser Pflanzen nachgewiesen [5].
Neueste epidemiologische Studien belegen, dass ein direkter Zusammenhang zwischen Knoblauchkonsum und einem geringen Krebsrisiko besteht, wobei sich dieser präventive Effekt nicht auf eine bestimmte Krebsart beschränkt, sondern eine Bandbreite von Dickdarmkrebs, Hautkrebs, Lungenkrebs, Rachenkrebs bis Prostatakrebs umfasst [3, 5, 6, 8 – 12].
Organische Schwefelverbindungen
In der medizinischen und pharmazeutischen Chemie werden pflanzliche Sekundärstoffe als "privilegierte Strukturen" bezeichnet, weil sie oft einem natürlichen Target zugeordnet werden können, an das sie mit hoher Spezifität binden. Insofern besteht auch ein großes Interesse an der Erforschung von "Nutrizeutika", von Nahrungsmitteln mit gesundheitsfördernden Wirkungen [5].
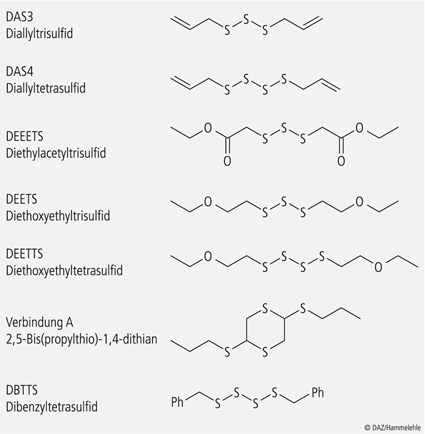
Mehr als 30 organische Schwefelverbindungen sind nicht allein für das charakteristische Aroma der Allium-Spezies verantwortlich, sondern auch für ihr chemopräventives und -therapeutisches Potenzial [3, 5, 6]. Bezüglich des antikanzerogenen Potenzials spielen die Diallylpolysulfide, insbesondere Diallyltetrasulfid (DAS4; Abb. 1), eine zentrale Rolle, wie bereits durch Cerella [3, 14], Jacob [10, 13, 15], Viry [16] und Kelkel [Publikation in Vorbereitung] in vitro an verschiedenen Zelllinien nachgewiesen wurde. Diese Studien ergaben eine Korrelation zwischen der Anzahl der in der jeweiligen Verbindung enthaltenen Schwefelatome und ihrem antikanzerogenen Potenzial. Zudem zeigten In-vitro-Studien, dass Knoblauchextrakte die Viabilität und Proliferation von Krebszellen vermindern [17]. In den zitierten Arbeiten wurden auch synthetische Polysulfide getestet, und zwar hinsichtlich ihres zytotoxischen und antiproliferativen Potenzials auf U937-Zellen.
Versuche an Ratten und Mäusen bestätigten die antikanzerogene Aktivität der Diallylpolysulfide [8]. Außerdem wurde in vitro festgestellt, dass gesunde Zellen keinen Veränderungen nach einer Inkubation mit Diallylpolysulfiden unterliegen [18].
Die genaue Wirkweise der organischen Schwefelverbindungen ist bis dato noch nicht geklärt; es kann allerdings festgehalten werden, dass sie bei Krebszellen einen Zellzyklus-Arrest in der G2/M-Phase sowie – nach einer längeren Inkubation – schließlich eine Apoptose (programmierter Zelltod) bewirken [14]. Neben der Anzahl der Schwefelatome scheint die Struktur der Seitenketten einen Einfluss auf die biologischen Eigenschaften der Verbindungen zu nehmen [3].
Da der intensive Geruch der Diallylpolysulfide die Compliance der damit behandelten Patienten verschlechtern könnte, sind geruchlose synthetische Polysulfide eine interessante Alternative, sofern sie die gleichen erwünschten Eigenschaften aufweisen.
Zellviabilitätstests
Um das antiproliferative Potenzial von natürlichen und synthetischen Polysulfiden (Abb. 1) zu untersuchen, wurden die Zellviabilitätstests XTT, CellTiter Glo® und Trypanblau-Assay an den Krebszelllinien U937, K562, Jurkat, Raji und der "gesunden" Zelllinie PBM durchgeführt. Während die Tests XTT und CellTiter Glo® eine metabolische Aktivität der Zellen voraussetzen, muss die Zelle beim Trypanblau-Assay bereits abgestorben sein, damit die Zellmembran für den hydrophilen Farbstoff durchlässig ist.
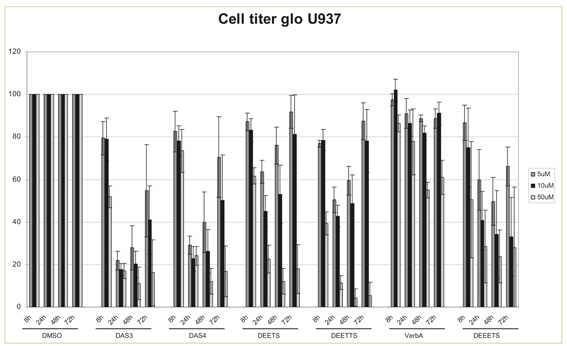
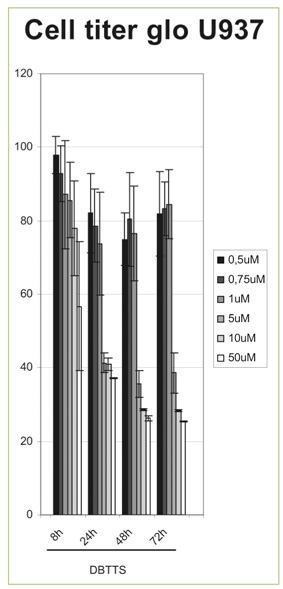
Im CellTiter Glo®-Test an U937-Zellen zeigen die synthetischen Polysulfide ein mit den natürlichen Verbindungen DAS3 und DAS4 vergleichbares antiproliferatives Potenzial (Abb. 2 und 3). Allerdings besitzt die aromatische Verbindung DBTTS nach einer 48-stündigen Inkubation eine Stabilität, die bei allen übrigen Testsubstanzen vermisst wird. Das bedeutet, dass die aromatischen Seitenketten stabilisierend wirken (Mesomeriestabilisierung).
Bei den übrigen Krebszelllinien wirken die synthetischen Polysulfide ebenfalls antiproliferativ, jedoch weniger ausgeprägt. Auch hier wird eine Instabilität vermutet, da die Zellzahl nach 48 Stunden wieder ansteigt. Die Tests an "gesunden" PBM-Zellen zeigen, dass die Polysulfide deren Proliferation nicht beeinträchtigen. Somit scheinen sie gezielt entartete Zellen anzugreifen.
Die Ergebnisse der XTT-Tests stimmen mit den Ergebnissen der CellTiter Glo®-Tests überein. Beim Trypanblau-Assay hingegen erfolgt die Reduktion der Zellzahl später und ist erst nach 72 Stunden deutlich ausgeprägt. Dies ist darauf zurückzuführen, dass der Farbstoff die Zellmembran erst nach dem Tod der Zelle passieren kann, sodass lediglich die bereits abgestorbenen Zellen erfasst werden.
Zellkernmorphologie
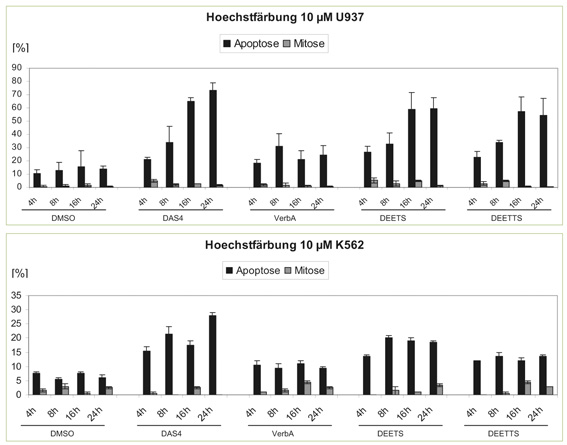
Mithilfe des Fluoreszenzfarbstoffs Hoechst 33342 lassen sich apoptotische bzw. mitotische Zellen aufgrund der morphologischen Unterschiede ihres Zellkerns identifizieren. So zeigt sich, in welchem Maße die einzelnen Testsubstanzen, mit denen die Zellen inkubiert worden sind, eine Apoptose induzieren. Im Laufe von 24 Stunden nach der Inkubation steigt die Anzahl der apoptotischen Zellen stetig an, während die mitotischen Zellen in vergleichsweise geringer Zahl auftreten (Abb. 4 und 5). Dabei fällt die aromatische Verbindung DBTTS auf, denn nach 24 Stunden weist sie eine Apoptoserate von rund 80% auf, die mit derjenigen von Diallyltetrasulfid (DAS4) vergleichbar ist.
Durchflusszytometrie zur Analyse des Zellzyklus
Um die Auswirkungen der Polysulfide auf den Zellzyklus zu testen, wurden U937-Zellen mit ihnen inkubiert und anschließend eine Durchflusszytometrie der mit Propidiumiodid markierten Zellen durchgeführt. Die prozentuale Verteilung der Zellen in den verschiedenen Zellzyklusphasen lässt erkennen, ob und wie sehr die Testsubstanzen den Zellzyklus in der G2/M-Phase unterbrechen (Zellzyklus-Arrest) [10, 11, 14]. Durch die Bindung eines Schwefelatoms der Polysulfide an einen Cysteinrest der Mikrotubuli wird der Spindelapparat funktionsunfähig gemacht und die Zellteilung blockiert [15]. Darauf folgt die Apoptose der Zelle [10]. (Gesunde Zellen verharren in der G2/M-Phase, wenn beispielsweise der Spindelapparat nicht korrekt gebildet wurde oder die identischen Schwesterchromatide ungleichmäßig verteilt wurden.)
Bereits vier Stunden nach der Inkubation mit DBTTS verharren deutlich mehr U937-Zellen in der G2/M-Phase, und nach acht Stunden sind es schon ca. 25%; dann sinkt ihr Anteil wieder, während die Zellen in der sub-G1-Phase einen Anteil bis über 60% erreichen. Diallyltetrasulfid (DAS4) wirkt etwa gleich stark wie DBTTS, denn nach vier Stunden sind etwa 20% der Zellen in der G2/M-Phase. Bei den übrigen Zelllinien waren diese Resultate ähnlich, aber etwas schwächer ausgeprägt.
Modulation der Mitosestadien
Die mit DBTTS inkubierten U937-Zellen zeigen keinen langfristigen Arrest in der G2/M-Phase, sondern eine sofortige Häufung in der sub-G1-Phase. Es wird deshalb davon ausgegangen, dass bereits vier Stunden nach der Inkubation der Großteil der Zellen einen fragmentierten DNA-Gehalt besitzt und demnach apoptotisch vorliegt.
Da man aufgrund der langen Zellzyklusdauer der U937-Zellen keinen früheren Zeitpunkt wählen kann, um die Induktion der Apoptose festzustellen, wird zu dieser Analyse die Giemsafärbung gewählt.
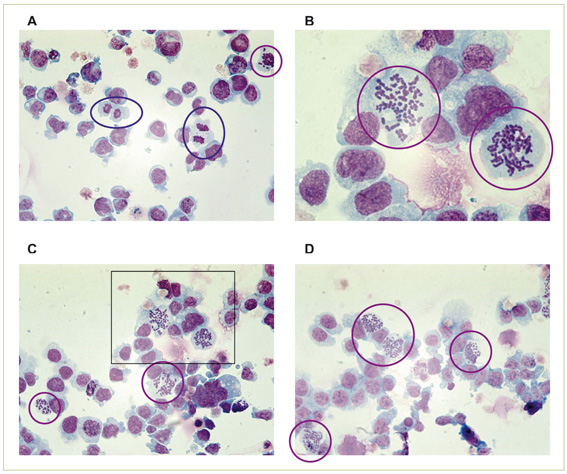
Bereits nach einer zweistündigen Inkubation mit DBTTS fällt auf, dass sich die mitotischen Zellen lediglich in der Prophase befinden. Keine einzige mitotische Zelle wurde in einer anderen Mitosephase entdeckt. In der mit DMSO inkubierten Kontrollprobe hingegen können mitotische Zellen der Ana-, Telo- und Prophase entdeckt werden (Abb. 6). Eine Inkubation mit DBTTS scheint demnach eine Blockade des Zellzyklus in der Prophase zu bewirken, sodass eine Zellteilung nicht mehr möglich ist. Wegen dieser Blockade, die zur Apoptose führt, tritt der Arrest in der G2/M-Phase nicht im erwarteten Ausmaß auf.
Western Blot-Analyse
Nachdem nachgewiesen war, dass die Polysulfide bei Krebszellen eine Apoptose einleiten, sollte eine Western Blot-Analyse zeigen, welche Caspasen an der Apoptose beteiligt sind.
Nach der Inkubation mit den verschiedenen synthetischen und natürlichen Diallylpolysulfiden werden sowohl die beiden Initiatorcaspasen 8 und 9 als auch die Effektorcaspasen 3 und 7 relativ zeitgleich aktiviert. Somit kann dieses Experiment nicht klären, ob der intrinsische oder der extrinsische Apoptoseweg eingeleitet wird.
Immunfluoreszenzmikroskopie
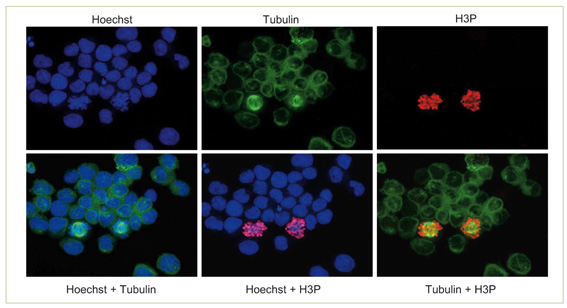
Mithilfe der Immunfluoreszenzmikroskopie wurde untersucht, wie die Polysulfide während der Mitosephase in das Tubulinnetzwerk des Spindelapparates von U937-Zellen eingreifen. Dabei wird der Zellkern mittels Fluoreszenzfarbstoff Hoechst 33342 visualisiert. Tubulin und das Histon H3 im phosphorylierten Zustand, wie er nur während der mitotischen Phase vorkommt, werden mittels Immunfärbung durch spezielle Antikörper sichtbar (Abb. 7).
In diesem Experiment wird bereits nach einer vierstündigen Inkubation mit DAS4 kein ausgeprägter Spindelapparat mehr gebildet. Das Tubulin kann nicht mehr polymerisieren, wie es bei einem intakten Spindelapparat der Fall wäre, sondern verteilt sich monomer und oligomer in der gesamten Zelle. Dieses Resultat bestätigt die Ergebnisse der Zellviabilitätstests (s. o.).
Bedeutung der Seitenketten für die Wirkung
Insgesamt kann festgehalten werden, dass die synthetischen Polysulfide (Abb. 1) nicht minder wirksam sind als die natürlichen Verbindungen, denn sie besitzen nicht nur deren zytotoxisches Potenzial, sondern sie sind aufgrund ihrer molekularen Struktur auch stabiler. Mit der Stabilität einer Verbindung steht und fällt ihr zytotoxisches Potenzial. So übertrifft DBTTS durch die Mesomeriestabilisierung der aromatischen Seitenketten die Wirksamkeit der natürlichen Polysulfide. Auch die Etherfunktion von DEETS und DEETTS scheint eine Stabilität in die Verbindung zu bringen. Die zyklische Verbindung A scheint dagegen aufgrund der fehlenden freien Drehbarkeit so inflexibel zu sein, dass sie kein maßgebliches, zytotoxisches Potenzial besitzt.
Literatur[1] Delhalle S, et al. An introduction to the molecular mechanisms of apoptosis. Ann N Y Acad Sci 2003; 1010:1.[2] Chung LY. The antioxidant properties of garlic compounds: allyl cysteine, alliin, allicin, and allyl disulfide. J Med Food 2006;9:205.[3] Aggarwal BB, Shishodia S. Molecular targets of dietary agents for prevention and therapy of cancer. Biochem Pharmacol 2006;71:1397.[4] Kelekar A, Thompson CB. Bcl-2-family proteins: the role of the BH3 domain in apoptosis. Trends Cell Biol 1998;8:324.[5] Lanzotti V. The analysis of onion and garlic. J Chromatogr A 2006; 1112:3.[6] Vazquez-Prieto MA, Miatello RM. Organosulfur compounds and cardiovascular disease. Mol Aspects Med 2010;31:540.[7] Powolny AA, Singh SV. Multitargeted prevention and therapy of cancer by diallyltrisulfide and related Allium vegetable-derived organosulfur compounds. Cancer Lett 2008;269:305.[8] Shukla Y, Kalra N. Cancer chemoprevention with garlic and its constituents. Cancer Lett 2007;247:167.[9] Wargovich MJ. Colon cancer chemoprevention with ginseng and other botanicals. J Korean Med Sci 2001;16 Suppl:S81.[10] Busch C, et al. Diallylpolysulfides induce growth arrest and apoptosis. Int J Oncol 2010;36:743.[11] Herman-Antosiewicz A, et al. Molecular targets of cancer chemoprevention by garlic-derived organosulfides. Acta Pharmacol Sin 2007; 28:1355.[12] Reddy L, et al. Natural products for cancer prevention: a global perspective. Pharmacol Ther 2003;99:1.[13] Scherer C, et al. Potential role of organic sulfur compounds from Allium species in cancer prevention and therapy. Phytochem Rev 2009; 8:349.[14] Cerella C, et al. Cell cycle arrest in early mitosis and induction of caspase-dependent apoptosis in U937 cells by diallyltetrasulfide (Al2S4). Apoptosis 2009;14:641.[15] Munchberg U, et al. Polysulfides as biologically active ingredients of garlic. Org Biomol Chem 2007; 5:13.[16] Viry E, et al. Antiproliferative effect of natural tetrasulfides in human breast cancer cells is mediated through the inhibition of the cell division cycle 25 phosphatases. Int J Oncol 2011;38:1103.[17] Herman-Antosiewicz A, Singh SV. Signal transduction pathways leading to cell cycle arrest and apoptosis induction in cancer cells by Allium vegetable-derived organosulfur compounds: a review. Mutat Res 2004;555:121.[18] Kim YA, et al. Mitochondriamediated apoptosis by diallyl trisulfide in human prostate cancer cells is associated with generation of reactive oxygen species and regulated by Bax/Bak. Mol Cancer Ther 2007;6:1599.
Autorin
























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.