
- DAZ.online
- DAZ / AZ
- DAZ 34/2012
- Botulinumtoxine
Toxikologie
Botulinumtoxine

Kaum ein anderes mikrobiologisches bzw. toxikologisches Thema hat so viele Facetten wie die Exposition gegenüber Clostridium botulinum bzw. den Exotoxinen, die dieses grampositive, anaerobe Bakterium produziert. Der Erreger ist ubiquitär verbreitet und kann zum Beispiel in Bodenproben nachgewiesen werden. Charakteristisch ist die Bildung von hitzeresistenten Sporen.
Botulismus – immer noch relevant und aktuell
Obwohl die Intoxikation als „Botulismus“ seit Langem bekannt ist und auch der verantwortliche Erreger als Ursache von Lebensmittelvergiftungen bereits Ende des neunzehnten Jahrhunderts beschrieben wurde, gibt es auch in der heutigen Zeit immer wieder Fälle von Botulismus. Die oft tödlich verlaufende Intoxikation stellt weltweit ein Problem dar.
Auslöser kontaminierte Kartoffelsuppe
Die verschiedenen klinischen Formen des Botulismus werden aus folgenden Fallberichten deutlich. Im Januar 2011 wurde ein 29-jähriger Mann aus Ohio, USA, in ein Krankenhaus zur stationären Behandlung aufgenommen. Seit einigen Tagen hatten sich folgende Symptome entwickelt: zunehmender Schwindel, verschwommenes Sehen, sowie Probleme beim Schlucken. Auch seine Atmung war zunehmend beeinträchtigt. Zehn Tage zuvor hatte er eine abgepackte Kartoffelsuppe gegessen. Vor dem Öffnen bemerkte er, dass die Kunststoffverpackung aufgebläht war, die Suppe schmeckte schlecht und er aß daher nicht die ganze Portion. Trotz Hinweisen auf der Verpackung, dass die Fertigzubereitung gekühlt aufzubewahren sei, hatte er das Lebensmittel wochenlang ungekühlt gelassen. Er verbrachte 57 Tage im Krankenhaus, überlebte aber die Intoxikation. Ähnlich ging es einer 41-jährigen Frau aus Georgia, USA, auch sie hatte eine abgepackte Kartoffelsuppe ungekühlt aufbewahrt und war an Botulismus erkrankt. Für die US-amerikanischen Centers for Disease Control waren diese Fälle Anlass, darauf hinzuweisen, dass Lebensmittel mit Sporen von Clostridium botulinum kontaminiert sein können. Kühlvorschriften müssen beachtet werden und ein Erhitzen der Lebensmittel auf Temperaturen über 85 °C kann lebensrettend sein weil so die Toxine inaktiviert werden [NN, 2011].
Wundbotulismus durch kontaminiertes Heroin
Über einen anderen Fall berichteten Ärzte aus London. Ein 42-jähriger Mann mit beidseitiger Ptosis sowie zahlreichen Abszessen an Armen und Beinen wurde in eine Klinik aufgenommen. Er fiel durch eine verwaschene Sprache auf. Sein Sehvermögen war durch Doppelbilder beeinträchtigt, er klagte über Schluckstörungen. Durch Nachweis des Toxins im Serum und Kultur des Erregers aus den Abszessproben konnte die Diagnose Wundbotulismus gesichert werden. Ursächlich waren subkutane Injektionen von Heroin, das mit Sporen von C. botulinum kontaminiert war. Wegen der fortschreitenden Symptomatik musste der Patient intubiert und zwei Wochen lang beatmet werden. Die vollständige neurologische Besserung war erst nach mehreren Monaten zu verzeichnen [Sam und Beynon, 2010]. Im Gegensatz zu der Lebensmittelvergiftung mit Botulinumtoxinen werden beim Wundbotulismus Toxine in situ weiter gebildet bis die Wunden saniert und der Erreger durch geeignete Antibiotika beseitigt ist [Sobel, 2005)].
Säuglingsbotulismus durch Besiedelung des Magen-Darm-Traktes
Ähnlich ist die Situation beim Botulismus von Säuglingen, deren Magen-Darm-Trakt mit den toxinbildenden Bakterien besiedelt ist. Die Erkrankung äußert sich zunächst in gastrointestinalen Symptomen, sowie Seh- und Akkommodationsstörungen. Später kommen Saug- und Schluckstörungen dazu, die Atemmuskulatur kann gelähmt sein. Eine mangelnde Ausbildung der physiologischen Darmflora wird als Ursache angenommen. Bei Erwachsenen mit chronischen Darmerkrankungen, wie zum Beispiel Morbus Crohn, kann eine ähnliche Situation entstehen.
Wie Botulinumtoxine angreifen ...
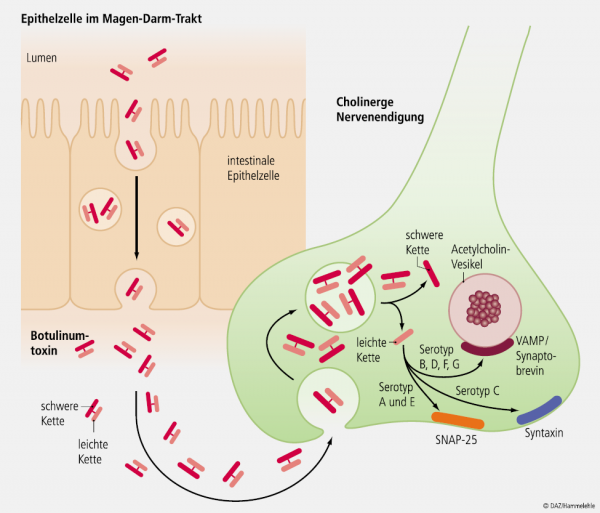
Botulinumtoxin gilt als das stärkste bekannte Gift. Mengen im Bereich eines Nanogramm – also eines milliardstel Gramm – pro Kilogramm Körpergewicht sind tödlich für Säugetiere. Die tödliche Dosis für einen 70 kg schweren Menschen wird auf 90 bis 150 ng bei parenteraler Zufuhr und etwa 700 ng bei inhalativer bzw. 70 µg bei oraler Aufnahme geschätzt [Arnon et al., 2001]. Verschiedene Subtypen des Botulinumtoxins sind bekannt, sie werden mit den Zusatzbezeichnungen A, B, C, D, E, F und G gekennzeichnet. Alle hemmen die Freisetzung der wichtigen Transmittersubstanz Acetylcholin aus den präsynaptischen Speichervesikeln cholinerger Nervenendigungen. Da sie verschiedene Proteine verändern, die an der Acetylcholinfreisetzung beteiligt sind, unterscheiden sie sich zum Beispiel in ihrer Wirkungsdauer und toxischen Potenz. Für die Botulismuserkrankungen sind hauptsächlich die Toxine A, B und E, in seltenen Fällen auch F verantwortlich. Die Proteine sind aus einer schweren und leichten Kette zusammengesetzt, die durch eine Disulfidbrücke verbunden sind. Ohne intakte Disulfidbrücke können die Proteine nicht in die Zellen aufgenommen werden und verlieren ihre Toxizität. Da cholinerge Neurone sowohl an den motorischen Endplatten als auch im vegetativen Nervensystem vorkommen, können die Toxine den Muskeltonus reduzieren, eine schlaffe Lähmung verursachen oder die Hyperaktivität verschiedener Drüsen reduzieren.
Der detaillierte Angriffsort der Toxine ist der Exocytoseapparat – er gewährleistet die blitzschnelle Freisetzung der Transmitter, wenn es bei Eintreffen eines Aktionspotenzials zum Einstrom von Natrium und Calcium kommt. Sowohl Tetanus- als auch Botulinumtoxine wirken auf diese Strukturen. Der Exocytoseapparat besteht aus verschiedenen Proteinen: die vesikulären Proteine Synaptotagmin und Synaptobrevin und die in der Zellmembran verankerten Proteine Syntaxin und SNAP-25, die auch als SNARE-Komplex bezeichnet werden (Abb.). Die schwere Kette der Toxine vermittelt die Anlagerung an die präsynaptische Membran und die anschließende Endozytose in Vesikel. Hier wird die Disulfidbrücke gespalten, und die leichte Kette, die als Zink-Endopeptidase wirkt, gelangt in das Zytoplasma. Sie spaltet dort die Proteine des Exocytoseapparats. Dabei bestehen Unterschiede zwischen den einzelnen Toxinen. Das Botulinumtoxin A spaltet SNAP-25, die Toxine B, D, F und G Synaptobrevin und das Toxin C vor allem Syntaxin [Simpson, 2004].
... und wie sie sich verteilen
Von Interesse ist die Verteilung der Toxine im menschlichen Körper. Zunächst ist es bemerkenswert, dass ein Protein nach oraler Exposition intakt bleibt und im Magen-Darm-Trakt nicht gespalten wird. Das Toxinmolekül ist von Hämagglutininen und weiteren Makromolekülen umgeben, die es offenbar vor einer Proteolyse im sauren Milieu des Magens schützen. Das Toxin muss mehrere Barrieren überwinden, um an den Wirkort, die Nervenendigungen, zu gelangen. Nach Anlagerung und aktivem Transport durch die Epithelzellen des Magen-Darm-Trakts gelangt es in die systemische Zirkulation. Wie es die Blutgefäße wieder verlässt, ist nicht bekannt. Es überwindet nicht die Blut-Hirn-Schranke. Dies ist ein Unterschied zum Tetanustoxin, welches Krampfanfälle hervorrufen kann. Schließlich muss das Toxin in die cholinergen Nervenendigungen gelangen, ein Prozess der über die schwere Kette vermittelt wird, wie zuvor beschrieben.
Vielfältige therapeutische Nutzung
Die mögliche Anwendung der Botulinumtoxine als Arzneimittel geht auf Untersuchungen des Ophthalmologen Scott zurück. Nachdem er zunächst Versuche an Rhesusaffen durchgeführt hatte, behandelte er erstmals vor 30 Jahren eine kleine Gruppe von Patienten mit Strabismus (Schielen).
In den folgenden Jahren wurde das Neurotoxin bei weiteren augenärztlichen Indikationen, wie Blepharospasmus (Lidkrampf), eingesetzt. Im Jahr 1989 erfolgte die erste Zulassung durch die US-amerikanische Zulassungsbehörde FDA für die Indikationen Blepharospasmus und Nystagmus. Heute sind vier verschiedene Zubereitungen von verschiedenen Herstellern im Handel, die zum Teil auch für diverse weitere Indikationen, wie Zerebralparesen oder spastische Lähmungen nach Schlaganfall zugelassen sind (Tab. 1).
Tabelle: Botulinumtoxin-haltige Arzneimittel [mod. nach Albanese, 2011] | ||||
Handelsname |
Botox |
Dysport |
Xeomin |
Neurobloc |
Freiname (FDA) |
Onabotulinumtoxin A |
Abobotulinumtoxin A |
Incobotulinumtoxin A |
Rimabotulinumtoxin B |
Hersteller |
Allergan Inc. |
Ipsen Pharma |
Merz Pharma |
Eisai Ltd, UK |
Serotyp |
A |
A |
A |
B |
Spezifische Aktivität [U/ng] |
20 |
40 |
167 |
75 – 125 |
Dosis/Flasche oder/ml |
50, 100 oder 200 Allergan-Einheiten/Flasche |
500 Einheiten |
50 Xeomin-Einheiten/Flasche |
5000 Einheiten/ml |
Sonstige Bestandteile, Zusatzstoffe |
Hämagglutinin,
Humanalbumin,
Saccharose,
Natriumchlorid
|
Hämagglutinin,
Humanalbumin,
Lactose
|
Humanalbumin,
Saccharose
|
Hämagglutinin,
Humanalbumin,
Natriumchlorid,
Natriumsuccinat
|
Komplexgröße [kDa] |
900 |
900 |
150 (ohne Komplexproteine) |
700 |
Indikationen |
Zervikale Dystonie,
(Torticollis) Blepharospasmus,
Fokale Spastizität
(Zerebralparese, Schlaganfall)
Hyperhidrosis axillaris
Harninkontinenz
(Detrusorhyperaktivität) Migräne
|
Zervikale Dystonie,
(Torticollis) Blepharospasmus,
Armspastik nach Schlaganfall
|
Zervikale Dystonie,
(Torticollis) Blepharospasmus,
Armspastik nach Schlaganfall
|
Zervikale Dystonie, (Torticollis) |
Die verabreichten Dosierungen sind extrem niedrig und liegen im Picogrammbereich. Anders ausgedrückt: eine handelsübliche Flasche mit Botulinumtoxin zur Herstellung einer Injektionslösung enthält nur 0,005% der Menge, die bei oraler Gabe für einen Menschen wahrscheinlich tödlich wäre [Arnon et al., 2001].
In den vergangenen Jahren sind auch mehrere Studien zum Einsatz des Neurotoxins A bei Patienten mit chronischer Migräne veröffentlicht worden. Insgesamt werden bis zu 39 Injektionen in verschiedene Muskeln im Kopf- und Nackenbereich gegeben. Der Wirkmechanismus bei dieser Indikation ist nicht bekannt, das Toxin blockiert jedoch die Freisetzung von Neurotransmittern, die mit der Schmerzentstehung im Zusammenhang stehen. Es wird vermutet, dass die Toxine die periphere und zentrale Sensibilisierung hemmen. Ein wichtiger Endpunkt in den Studien war die Reduktion der Tage mit Kopfschmerzen innerhalb eines Zeitraums von vier Wochen im Vergleich zu der Ausgangssituation. In der Gruppe mit Botox-Behandlung waren es 9 Tage, in der Placebogruppe nur 6,7 Tage [Diener et al., 2010; Frampton, 2012].
Standardisierung mit Mäusen
Ein Problem bei der Verwendung von Botox® und ähnlichen Präparaten entsteht dadurch, dass die Zubereitungen biologisch standardisiert werden müssen. Eine "Einheit" entspricht dabei der Menge an Botulinumtoxin, die nach intraperitonealer Gabe bei Mäusen tödlich wirkt und zum Tod von 50% der behandelten Tiere führt (LD50). Hier wird also ein Test angewandt, der in anderen Bereichen der Toxikologie weitgehend abgeschafft wurde. Im Sinne des Tierschutzes sind dringend Alternativen notwendig und scheinen auch möglich zu sein, wie die Entwicklung eines zellbasierten Testverfahrens zeigt, das zwar seit einigen Monaten zunehmend behördliche Akzeptanz findet, allerdings zur Zeit noch nicht zu einem generellen Ersatz der Tierversuche geführt hat.
Einheiten nicht übertragbar
Die Einheiten der einzelnen Präparate sind nicht identisch. Daher kann die Dosierung nicht von einem Präparat auf das andere übertragen werden. Um die Unterschiede deutlich herauszustellen, hat die US-amerikanische FDA verschiedene generische Bezeichnungen für die einzelnen Zubereitungen festgesetzt, die sich aber international noch nicht allgemein durchgesetzt haben. Die neuen Namen, wie Onabotulinumtoxin A (900 kDa), Abobotulinumtoxin A (900 kDa) oder Incobotulinumtoxin A (150 kDa) sollen deutlich machen, dass die Produkte von verschiedenen Clostridium -Stämmen gebildet werden, unterschiedlich produziert und isoliert werden, und sich auch hinsichtlich ihrer Molekülgröße unterscheiden können. Das Incobotulinumtoxin A ist frei von Komplexmolekülen und hat daher ein deutlich geringeres Molekulargewicht [Albanese, 2011].
In einigen Publikationen wird darauf hingewiesen, dass selbst bei identischem Molekulargewicht Unterschiede hinsichtlich Wirkung und Verträglichkeit feststellbar seien [Bentivoglio et al., 2009]. Direkte klinische Vergleichsstudien der Präparate untereinander sind allerdings kaum verfügbar.
Unerwünschte Wirkungen
Die bei der Anwendung von Botulinumtoxin-Präparaten beobachteten möglichen unerwünsch-ten Wirkungen sind vielfältig. Sie treten in Abhängigkeit von der Indikation, der Dosierung, dem Ort der Injektion und nicht zuletzt der Injektionstechnik auf. Die Präparate dürfen daher nur von Ärzten mit geeigneter Qualifikation und Fachkenntnis angewandt werden. Bei der Behandlung eines Blepharospasmus kommt es sehr häufig zu einer Ptosis des Oberlids, bei der Therapie einer zervikalen Dystonie tritt eine Ptosis seltener auf, allerdings sind Schluckbeschwerden, trockener Mund und Übelkeit häufig bis sehr häufig. Die Anwendung bei Hyperhidrosis axillaris ist sehr häufig mit Schmerzen an der Injektionsstelle und lokalen Reaktionen verbunden. Bei klinischen Studien zur Anwendung der Toxine bei chronischer Migräne lag die Häufigkeit von behandlungsbedingten unerwünschten Erscheinungen (adverse events) bei 33,4% der Patienten in der Verum- und 13,7% in der Placebogruppe. Die Abbruchrate bei den Botox-Behandelten betrug 3,5% im Vergleich zu 1,4% in der Placebogruppe [Diener et al., 2010].
Seit dem Jahr 2009 verlangt die US-amerikanische FDA eine Black Box Warning für alle Präparate, die Botulinumtoxin enthalten: „The effects of BOTOX and all botulinum toxin products may spread from the area of injection to produce symptoms consistent with botulinum toxin effects.“ Hintergrund waren Meldungen an die Zulassungsbehörde über unerwünschte Wirkungen im Zusammenhang mit der Injektion von Botulinumtoxin-haltigen Präparaten. Die Wirkstoffe hatten in Körperbereichen, die von der Injektionsstelle entfernt lagen, botulismusähnliche Nebenwirkungen verursacht (Atem- und Schluckbeschwerden, Blasenkontrollverlust, Sehstörungen, hängende Augenlider etc.). Mehrere Berichte betrafen Kinder, die hochdosierte oder Off-label-Injektionen erhalten hatten, um spastische Lähmungen als Folge von Zerebralparesen zu behandeln. In seltenen Fällen kam es zu Todesfällen. Die Risiken nehmen zu mit steigenden Dosierungen und Injektionen an mehreren Stellen [Kuehn, 2009].
Tödliches Risiko
Bei grob fehlerhafter Anwendung stellen Injektionen von Botulinumtoxin ein tödliches Risiko dar. In einer Klinik wurde eine Flasche mit 0,1 mg Botulinumtoxin A, das nicht für die Humananwendung hergestellt oder zugelassen war, in 10 ml aufgelöst. Ein Arzt injizierte sich selbst und drei weiteren Patienten einen Teil dieser viel zu konzentrierten Lösung aus kosmetischen Gründen im Gesichtsbereich. Alle Patienten mussten bereits zwei bis drei Tage später wegen des „iatrogenen Botulismus“ stationär behandelt werden, sie wurden mehr als einen Monat beatmet. Alle überlebten die schwere Intoxikation, der Arzt wurde zu drei Jahren Gefängnis verurteilt [Chertow et al., 2006].
Ästhetische Medizin
Bereits Ende der 1980er Jahre bemerkte eine Patientin, die wegen eines Lidkrampfes mit Botulinumtoxin behandelt worden war, eine Glättung ihrer Stirnfalten. Die erste klinische Studie mit Botulinumtoxin bei Patienten mit Glabellafalten markiert den Beginn der Anwendung dieser Stoffe in der ästhetischen Medizin. In den vergangenen Jahren ist die Injektion der Toxine in den USA zur häufigsten medizinisch-kosmetischen Maßnahme geworden. Seit 2002 sollen 11 Millionen Injektionen durchgeführt worden sein [Cartee und Monheit, 2011].
Von drei Herstellern werden in Deutschland Präparate angeboten, die zur Faltenbeseitigung entwickelt wurden. Sie sind unter den Namen Bocouture®, Vistabel® und Azzalure® im Handel. Die offizielle Formulierung der Zulassung lautet zum Beispiel: „Bocouture wird angewendet zur vorübergehenden Verbesserung des Aussehens bei mittelstarken bis starken vertikalen Falten zwischen den Augenbrauen beim Stirnrunzeln (Glabellafalten) bei Erwachsenen im Alter unter 65 Jahren, wenn das Ausmaß dieser Falten eine erhebliche psychologische Belastung für den Patienten darstellt.“ Die Präparate unterscheiden sich in der Konzentration des Wirkstoffes bzw. der Menge pro Injektionsflasche von den in der Tabelle aufgeführten Präparaten.
Da die Toxinmengen, die für kosmetische Zwecke injiziert werden, relativ gering sind, gibt es bei sachgerechter Anwendung vergleichsweise wenig unerwünschte Wirkungen. Völlig risikofrei ist die Injektion auch bei diesen Indikationen nicht. Ödeme der Augenlider oder eine Ptosis sind häufiger als nach Placeboinjektionen. Darüber hinaus ist die Injektion mit leichten Schmerzen und möglichen Druckstellen bzw. leichten lokalen Blutungen verbunden. Unter diesen Aspekten ist die Entwicklung einer neuen Gel-Zubereitung zur lokalen Applikation von Interesse. Das Präparat mit der Bezeichnung RT001 ist derzeit in der klinischen Prüfung. Im direkten Vergleich beseitigte es leichte laterale Falten am Auge („Krähenfüße“) besser als Placebo [Brandt et al., 2010].
Botulinumtoxine werden in Zukunft zunehmend wichtige Arzneistoffe sein. Wie bei anderen pharmazeutisch verwendeten Substanzen muss bei jeder Anwendung eine sorgfältige Nutzen-Risikoabwägung vorgenommen werden. Der Abstand zwischen den therapeutisch verwendeten und den toxikologisch relevanten Dosen ist größer als bei manch anderen Arzneistoffen, allerdings liegen die Dosen im Pico- und Nanogrammbereich anstatt im Milligrammbereich und damit in einem ungewohnten Bereich auf der Größenordnungsskala. Der Abstand ist jedoch hinreichend groß, um eine sichere Therapie zu gewährleisten – wenn die Anwendung mit ausreichender Qualifikation und Fachkenntnis erfolgt.
Literatur:
Albanese, A. Terminology for preparations of botulinum neurotoxins. What a difference a name makes. JAMA 2011; 305:89 – 90
Arnon SS, Schechter R, Inglesby TV, Henderson DA, Bartlett JG, Ascher MS, Eitzen E, Fine AD, Hauer J, Layton M, Lillibridge S, Osterholm MT, O‘Toole T, Parker G, Perl TM, Russell PK, Swerdlow DL, Tonat K; Working Group on Civilian Biodefense. Botulinum toxin as a biological weapon: medical and public health management. JAMA 2001;285:1059 –1070 Bentivoglio AR, Fasano A, Ialongo T, Soleti F, Lo Fermo S, Albanese A. Fifteen-year experience in treating blepharospasm with Botox or Dysport: same toxin, two drugs. Neurotox Res 2009;15:224 – 231 Brandt F, O‘Connell C, Cazzaniga A, Waugh JM. Efficacy and safety evaluation of a novel botulinum toxin topical gel for the treatment of moderate to severe lateral canthal lines. Dermatol Surg 2010;36 (Suppl 4):2111 – 2118 Cartee, T.V., Monheit, G.D. An overview of botulinum toxins: past, present, and future. Clin Plast Surg 2011; 38:409-426 Chertow DS, Tan ET, Maslanka SE, Schulte J, Bresnitz EA, Weisman RS, Bernstein J, Marcus SM, Kumar S, Malecki J, Sobel J, Braden CR. Botulism in 4 adults following cosmetic injections with an unlicensed, highly concentrated botulinum preparation. JAMA 2006; 296:2476 – 2479 Diener HC, Dodick DW, Aurora SK, Turkel CC, DeGryse RE, Lipton RB, Silberstein SD, Brin MF; PREEMPT 2 Chronic Migraine Study Group. OnabotulinumtoxinA for treatment of chronic migraine: results from the double-blind, randomized, placebo-controlled phase of the PREEMPT 2 trial. Cephalalgia. 2010;30:804 – 814 Frampton, J.E. Onabotulinumtoxin A (Botox®): a review of its use in the prophylaxis of headaches in adults with chronic migraine. Drugs 2012; 72:825 – 845 Kuehn, B. M. FDA requires black box warnings on labeling for botulinum toxin products. JAMA 2009; 301:2316 NN, Botulism caused by consumption of commercially produced potato soups stored improperly – Ohio and Georgia, 2011. MMWR 2011; 60:890 Sam, A.H., Beynon,. H.L.C. Wound Botulism. N Engl J Med 2010; 363: 2444 Simpson, L.L. Identification of the major steps in botulinum toxin action. Annu Rev Pharmacol Toxicol 2004; 44:176-193 Sobel, J. Botulism. Clin Infect Dis 2005;41:1167 –1173Autor
Prof. Dr. Ralf Stahlmann
Leiter des Masterstudiengangs Toxikologie
Institut für Klinische Pharmakologie und Toxikologie
Charité – Universitätsmedizin Berlin
Luisenstr. 7, 10117 Berlin




















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.