
- DAZ.online
- DAZ / AZ
- DAZ 28/2012
- Dabrafenib verlängert ...
Arzneimittel und Therapie
Dabrafenib verlängert progressionsfreies Überleben
Fortschritt bei metastasierten Melanomen
Wie Vemurafenib ist Dabrafenib ein selektiver BRAF-Inhibitor und konnte bereits in Phase-I/II-Studien bei Patienten mit BRAFV600E-mutierten metastasierten Melanomen seine Effektivität bei angemessener Toxizität zeigen. Das war die Rationale für die sogenannte BREAK-3-Studie, einer Phase-III-Studie, deren Ergebnisse während der ASCO-Tagung von Dr. Axel Hauschild, Kiel, vorgestellt wurden [1].
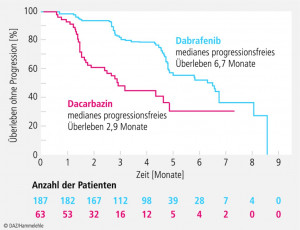
In 93 Zentren waren 250 bisher unbehandelte Patienten mit nicht resezierbaren BRAFV600E-mutierten metastasierten Melanomen rekrutiert worden. Sie wurden 3:1 randomisiert und entweder mit Dabrafenib (2 x täglich 150 mg p.o., 187 Patienten) oder Dacarbazin (1000 mg/m2, i.v., alle drei Wochen, 63 Patienten) behandelt. 50% der Patienten der Dabrafenib-Gruppe sprachen auf die Therapie an, im Dacarbazin-Arm nur 6%. Das mediane progressionsfreie Überleben, der primäre Studienendpunkt war im Dabrafenib-Arm signifikant länger und betrug 6,7 Monate vs. 2,9 Monate unter Dacarbazin (siehe Abbildung). Daten zum Gesamtüberleben waren noch nicht analysiert worden, werden aber insofern wenig Aussagekraft haben, als Patienten, die unter Dacarbazin progredient geworden waren, der cross-over in den Dabrafenib-Arm erlaubt war. Beide Therapien wurden gut vertragen. Im Dacarbazin-Arm kam es häufiger zu hämatologischen Toxizitäten, im Dabrafenib-Arm öfter zu milden bis moderaten Hautreaktionen, Gelenkschmerzen und Fieber. Im Vergleich zum Vorgänger Vemurafenib, der ersten verfügbaren Therapie bei BRAFV600E-mutierten metastasierten Melanomen, führt Dabrafenib aber zu weniger schweren Hauttoxizitäten.
Wirksam bei Hirnmetastasen
Hirnmetastasen als Folge von Melanomen haben eine sehr schlechte Prognose mit einem medianen Überleben von weniger als vier Monaten und effektive Therapien wären wünschenswert. In einer Phase-I-Dosis-Eskalationsstudie mit Dabrafenib, die im Mai 2012 im Lancet veröffentlicht wurde, zeigte sich bei neun von zehn Patienten mit Hirnmetastasen unter Dabrafenib eine Verkleinerung der Läsionen [3]. Das war insofern völlig unerwartet, weil Dabrafenib speziell so synthetisiert worden war, dass eine Penetration der Blut-Hirn-Schranke nicht erfolgen sollte, um potenziellen neurotoxischen Effekten auf im Hirn reichlich vorhandenen Zellen mit BRAF-Wildtyp vorzubeugen. Präklinische unpublizierte Studien haben auch nach einer Einmaldosis von Dabrafenib nur eine minimale Penetration von Dabrafenib durch die intakte Blut-Hirn-Schranke vermuten lassen. Die Erklärung der guten Wirksamkeit von Dabrafenib auf Hirntumoren könnten Läsionen der Blut-Hirn-Schranke durch Makrometastasen sein, die eine Penetration des Wirkstoffs ermöglichen. Außerdem fiel in dieser Studie auf, dass nicht nur Patienten mit BRAFV600E-mutierten metastasierten Melanomen auf die Therapie angesprochen hatten, sondern auch solche mit anders mutierten Melanomen und Nicht-Melanom-Patienten mit soliden Tumoren und BRAF-Mutationen. Die Ergebnisse dieser Phase-I-Studie waren die Rationale für eine Phase-II-Studie [2]: In der BREAK-MB-Studie wurden Melanom-Patienten im Stadium IV mit mehr als einer intrakranialen Metastase (0,5 cm bis 4 cm) aufgenommen, die noch keine Therapie der Hirnmetastasen erhalten hatten (Gruppe A) oder die nach einer Therapie der Hirnmetastasen progredient geworden waren (Gruppe B). Von 325 gescreenten Patienten wurden 172 in die Studie aufgenommen und mit 2 x täglich Dabrafenib 150 mg behandelt. 46% hatten zwei bis vier Hirnmetastasen, 38% hatten vorher schon eine Chemotherapie erhalten, 30% eine Immuntherapie. Der Erstautor Dr. John Kirkwood, Pittsburgh, bezeichnete die Ergebnisse, die er während der ASCO-Tagung präsentierte, als beispiellos: In der Gruppe A ergab sich bei V600E-Mutationen eine Krankheitskontrollrate von 81%, in der Gruppe B sogar von 89% mit einer Dauer des intrakraniellen Ansprechens von 20,1 bzw. 28,1 Wochen. In beiden Kohorten betrug die Gesamtüberlebensrate über 30%. Die Ansprechraten bei Patienten mit BRAFV600K Mutationen waren nicht ganz so gut (7% bzw. 22%), aber die intrakraniellen Kontrollraten betrugen auch hier 33% für die Gruppe A bzw. 50% für die Gruppe B. Schwere unerwünschte Wirkungen traten in beiden Gruppen bei 30% der Patienten auf, 17% davon ließen sich auf die Studienmedikation zurückführen. Die Therapie wurde deswegen aber nur bei 2% der Patienten abgebrochen.
Dabrafenib und das maligne MelanomDas BRAF-Protein ist ein wichtiger Bestandteil des RAS-MAP-Kinase-Signaltransduktionswegs, der am normalen Wachstum und Überleben der Zellen beteiligt ist und unter anderem Zellproliferation und Apoptose steuert. Bei 40 bis 50% der Patienten mit metastasiertem Melanom sind Mutationen im BRAF-Onkogen nachweisbar, bei etwa 95% als sogenannte Mutation BRAF V600E oder V600K. Diese Mutationen führen zur Aktivierung der MEK-Proteine (MEK1 und 2) und konsekutiv der MAP-Kinasen. Die aktivierenden Mutationen dieses Proteins führen zu einer verstärkten Signalweiterleitung und letztlich zu einer unregulierten Zellproliferation. Dabrafenib hemmt selektiv die mutierte BRAF-V600-Kinase und zeigte hohe Aktivität in Phase-I/II-Studien. |
Fazit
Dabrafenib ist sicher und hat eine außergewöhnliche Wirkung bei metastasierten Melanomen. Außerdem ist es der erste Wirkstoff dieser Klasse, der eine sehr gute Wirksamkeit bei Hirnmetastasen zeigt. Das könnte zu einem Paradigmenwechsel hin zu der systemischen Therapie von Hirnmetastasen führen. Weitere Studien, in die auch Patienten mit anderen Mutationen und anderen soliden Tumoren aufgenommen werden und/oder in denen Kombinationstherapien überprüft werden, sollten folgen.
Apothekerin Dr. Annette Junker





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.