
- DAZ.online
- DAZ / AZ
- DAZ 49/2011
- Das Influenza-Supervirus...
Forschung
Das Influenza-Supervirus - Wird "Contagion" Wirklichkeit?
Brisanter hätte dieser Nachrichtencocktail nicht ausfallen können. Was Epidemiologen im Vorfeld der letzten offiziell ausgerufenen Pandemie befürchtet hatten, war keine Fiktion oder Panikmache. Es war eine realistische Option, die aber in dieser Form durch das natürliche Mutations- und Kombinationspotenzial dieser gemeinen Viren Gott sei Dank (noch) nicht realisiert wurde.
Wie jetzt bekannt wurde, fehlten nur wenige Schritte zur Realisierung eines "Super-Bacs". Zwar waren dabei Kopf und Hände von Wissenschaftlern mit im Spiel. Aber alles wäre auch ohne menschliches Zutun möglich gewesen. Und – auch das sollte nicht unerwähnt bleiben – ist nach wie vor möglich!
Dürfen Forscher "biologisch zündeln"?
Aber dürfen Forscher so mit dem "Feuer spielen"? Ist es nicht viel zu gefährlich, derart biologisch zu "zündeln"? Schließlich könnte so ein Virus leicht mal aus dem Labor entfleuchen, oder Bioterroristen könnten das Virus als Waffe gegen die Menschheit einsetzen. Und dann wäre "Contagion" eben keine schaurig-schöne Hollywood-Geschichte, sondern blanke Realität.
Was war gemacht worden?
Die niederländische Forschergruppe um Ron Fouchier am Erasmus Medical Centre in Rotterdam hatte offensichtlich im Auftrag der US-amerikanischen National Institutes of Health (NIH) die Pathogenität und Infektiosität des Vogelgrippevirus H5N1 genauer untersucht. Die Frage, die dahinter stand, war herauszufinden, welche Veränderungen im Bauplan dieser Viren erforderlich sind, um von einem relativ harmlosen Virus zu einem "Killerkeim" zu werden. Denn nur, wenn man den biologischen Feind genau kennt, kann man ihn vielleicht auch wirkungsvoll bekämpfen. Und: Wenn man weiß, auf welche Mutationen es ankommt, kann man frühzeitig die zirkulierenden Viren daraufhin untersuchen, um das Gefahrenpotenzial besser abschätzen und rechtzeitig geeignete, aber nicht überschießende Gegenmaßnahmen ergreifen zu können.
Zunächst wurden nur drei Mutationen gezielt in das H5N1-Influenzavirus eingebracht, um es optimal an Säugetierzellen anzupassen. Und tatsächlich: Die resultierenden Viren infizierten Frettchen und töteten sie recht effizient. Allerdings war die Übertragbarkeit zwischen den Tieren noch sehr ineffizient. Dieses "Manko" wurde durch ein, wie die Forscher meinen, "dummes Experiment" behoben: Sie infizierten gesunde Frettchen mit virushaltigem Sekret von kranken Tieren, und nach 10 derartiger Infektionsrunden hatten sich die Viren soweit angepasst, dass sie per Tröpfcheninfektion und ohne Hilfe der Wattestäbchen der Wissenschaftler die Ansteckung neuer Tiere schafften. Letztendlich waren diese 10 Passagen also nur die forcierte Variante dessen, was während einer Grippesaison mehr oder weniger effizient zwischen eng zusammenlebenden Menschen passiert.
Und was war das Ergebnis?
Nach diesen 10 Passagen wurden die neuen Viren sequenziert und auf Mutationen hin untersucht. Wie es sich für Influenzaviren "gehört", die durch ihre fehlerhaft arbeitende RNA-Polymerase einem "antigenen Drift" unterliegen und daher bei jedem Replikationszyklus Mutationen ansammeln (siehe Infokasten), waren auch in diesem Fall zahlreiche Veränderungen aufgetreten. Unter diesen fanden sich zwei Mutationen in allen untersuchten, hochpathogenen Viren. Die Vermutung lag also nahe, dass diese beiden Mutationen zusammen mit den drei vorher eingeführten genetischen Veränderungen ausreichen, ein "Supervirus" zu erzeugen. Allerdings muss diese Vermutung noch durch gezielte Veränderung von H5N1 an den gefundenen fünf Positionen verifiziert werden.
Bekannt waren diese Mutationen auch schon vorher, waren sie – jede für sich – doch bereits in H5N1-Isolaten aus Vögeln nachgewiesen worden. Glücklicherweise sind sie aber bisher in der freien Wildbahn noch nicht zusammengekommen, was aber durchaus passieren kann.
Vermehrungszyklus von Influenza-A-Viren
Influenzaviren gehören zur Familie der Orthomyxoviren. Von den drei bekannten Typen A, B und C sind jedoch nur die Typen A und B als Grippe-Erreger von Bedeutung; die größten Probleme verursachen Typ-A-Viren.
Klassifiziert werden die Influenza-A-Viren anhand der beiden Oberflächenproteine Hämagglutinin (H) und Neuraminidase (N). Hämagglutinin ist für die Bindung des Virus an die Wirtszelle verantwortlich, die Neuraminidase sorgt dafür, dass sich die Nachkommen-Viren von der Wirtszelle ablösen können. Bisher sind 16 verschiedene Hämagglutinin- und 9 Neuraminidase-Subtypen bekannt.
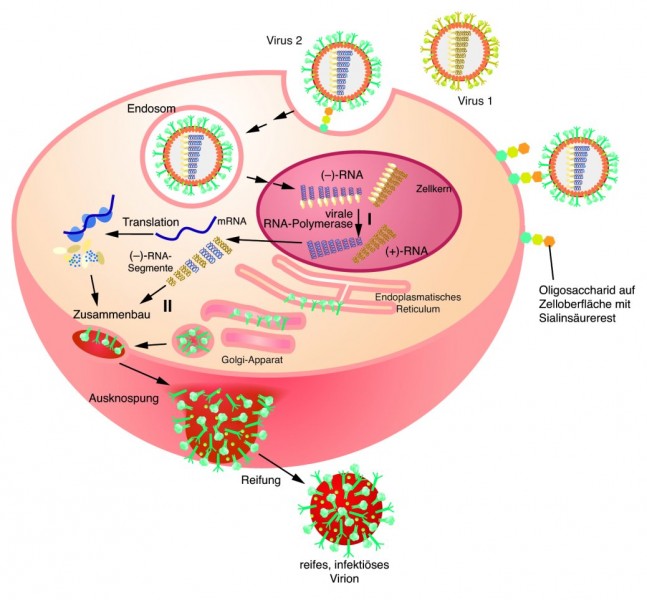
Nach der Bindung des Hämagglutinins an Sialinsäuremoleküle auf der Oberfläche einer Wirtszelle wird das Viruspartikel endosomal aufgenommen. Das Ionenkanalprotein M2, das ebenfalls in der Oberflächen-Membran eingelagert ist, sorgt für ein Verschmelzen der Endosomen-Membran mit der Virus-Membran. Dadurch wird das Virusgenom freigesetzt, das dann im Zellkern der Wirtszelle transkribiert werden kann. Influenza-A-Viren besitzen ein RNA-Genom aus 8 Segmenten mit negativ-strängiger Polarität. Dieses Genom muss zunächst von einer viralen RNA-Polymerase in (+)-RNA umgeschrieben werden, die dann einerseits als mRNA für die Translation der Virusproteine verwendet wird, andererseits als Matrize für die Bildung neuer Virusgenome ((-)-RNA) dient. Die virale RNA-Polymerase arbeitet allerdings um den Faktor 1000 ungenauer als DNA-Polymerasen der Wirtszelle, so dass aus jeder Transkriptionsrunde eine schrittweise Variation des RNA-Genoms resultiert, ein Vorgang, der als antigenic drift bezeichnet wird (Schritt I in der Abbildung). Wegen der Variation der Viren durch den antigenic drift muss auch alljährlich die Zusammensetzung des Impfstoffes angepasst werden.
Wesentlich dramatischer sind die Veränderungen des Virus bei einem antigenic shift. Dazu kommt es, wenn eine Zelle gleichzeitig von zwei Viren mit unterschiedlichen Genomen infiziert wird. Bei der Herstellung neuer Viruspartikel können dann die 8 Segmente willkürlich aus beiden Genomen kombiniert werden, wodurch Reassortanten entstehen, die völlig neue pathogene und immunologische Eigenschaften aufweisen können (Schritt II in der Abbildung). Reassortanten sind als Auslöser für Influenza-Pandemien gefürchtet.
Darf man diese Ergebnisse veröffentlichen?
Ähnliche Resultate lieferten Experimente von Yoshihiro Kawaoka und seinem Team an der University of Wisconsin und in Tokio. Beide Arbeitsgruppen haben wohl bereits entsprechende Veröffentlichungen vorbereitet und beim Fachjournal Science eingereicht. Aber die Publikationen werden noch vom US-amerikanischen National Science Advisory Board for Biosecurity (NSABB) zurückgehalten. Zu groß sei die Gefahr, dass die Informationen von den falschen Leuten gelesen, nachgebaut und für Terroranschläge verwendet werden.
Eine ganz ähnliche Diskussion entbrannte bereits 2005, als das Virus der Spanischen Grippe genauer untersucht und die Virulenzmechanismen aufgeklärt wurden. Die Arbeit wurde damals ebenfalls in Science publiziert [1]. Allerdings wurde das rekonstruierte Virus sowie alle Gensegmente aufgrund der Brisanz der Daten sofort zu "select agents" erklärt, also zu Agenzien, deren Besitz, Verwendung und Weitergabe sehr streng von den Centers for Disease Control and Prevention (CDC) reguliert werden. Und offensichtlich hat das bisher ganz gut funktioniert, schließlich haben wir auch sechs Jahre nach dieser Veröffentlichung noch keine neue Spanische Grippe. Eine Maßnahme, die sicherlich jetzt auch bei dem H5N1-Supervirus greifen wird.
Es spricht also eigentlich nichts gegen eine Veröffentlichung dieser neuen Daten, allerdings ohne die genetischen Details des Supervirus preiszugeben. So könnte auch noch einmal verdeutlicht werden, wie leicht ein derartiges "Supervirus" prinzipiell entstehen kann.
Das Bewusstsein in der Gesellschaft schärfen!
Es sind eben nur fünf Mutationen nötig, um aus einem Vogelgrippevirus ein für Frettchen tödliches Influenzavirus zu machen. Fünf Mutationen, die jede für sich bereits in freier Wildbahn existieren und die nur noch zusammentreffen müssen. Ob diese fünf Mutationen auch dazu führen würden, dass ein für Menschen hochgefährliches Virus entsteht, ist jedoch nicht absolut gesichert.
Mutationen sind eine integrale Konsequenz der Replikation von RNA-Viren. Eine hoch effiziente Maßnahme, um die virale Replikation in einem Wirt zu unterbinden, ist die effiziente Konditionierung des Immunsystems, ein eindringendes Pathogen zu eliminieren – also zu impfen. Gerade bei der Impfung gegen die Influenza geht es bei einer breit angelegten Kampagne nicht nur darum, Krankheits- und eventuelle Todesfälle zu vermeiden, sondern auch darum, durch die Unterbrechung von Infektionszyklen die Mutationsmöglichkeiten zirkulierender Viren – sei es durch antigenen Drift oder durch antigenen Shift – zu minimieren.
Ausrotten, wie es mit den Pocken gelungen ist, wie es schon fast mit der Poliomyelitis erreicht ist und wie es auch theoretisch mit den Masern möglich wäre, lässt sich die Influenza nicht. Dafür gibt es zu viele unterschiedliche Wirte. Aber vielleicht gelingt es ja, die Gesellschaft für die Relevanz der Impfung gerade gegen diese Viren zu sensibilisieren, damit sich im Pandemiefall eben nicht nur gut 10% der Bevölkerung, sondern ausreichend viele impfen lassen, um die weitere Ausbreitung zu stoppen. Oder auch für die Impfung gegen Masern zu sensibilisieren, die sich tatsächlich nur über eine flächendeckende Impfung, aber sicherlich nicht mit Masernparties ausrotten lassen.
Hier sind sowohl Politiker als auch Wissenschaftler und Journalisten in der Pflicht, gut und umfassend zu informieren. Viren mit RNA-Genomen, die – wie im Falle der Influenzaviren – ihr genetisches Repertoire zudem auch noch in voneinander getrennten Funktionspaketen mit sich tragen, sind kleine "Ungeheuer", auch wenn sie noch so unscheinbar daherkommen. Es ist ein gesellschaftliches Gebot, diesen Viren möglichst keine Chance zu bieten, ihr zerstörerisches Potenzial auszureizen. Impfen ist hier die effektivste Möglichkeit. Es reicht aber nicht, einen Impfstoff herstellen zu lassen und ihn kostenfrei der Bevölkerung zur Verfügung zu stellen. Man muss auch dafür sorgen, dass dieses "Geschenk" angenommen wird. Dazu ist es wichtig, ruhig und allgemein verständlich zu informieren. Panikmache oder Verharmlosung sind gleichermaßen fehl am Platz. Um es ganz deutlich zu sagen: Das, was anlässlich der Schweinegrippe durch die Medien und auch durch die Fachpresse ging, war zum Teil katastrophal!
[1] Tumpey, T.M., Basler, C.F., Aguilar, P.V., et al.: Characterization of the Reconstructed 1918 Spanish Influenza Pandemic Virus. Science 370 (2005), 77 – 80.
AutorenDr. Ilse Zündorf, Prof. Dr. Theodor Dingermann, Institut für Pharmazeutische BiologieUniversität Frankfurt, Max-von-Laue-Str. 9, 60438 Frankfurt/M.





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.