
- DAZ.online
- DAZ / AZ
- DAZ 48/2011
- Klinische Studie mit ...
Arzneimittel und Therapie
Klinische Studie mit neuem TGF-beta-Blocker
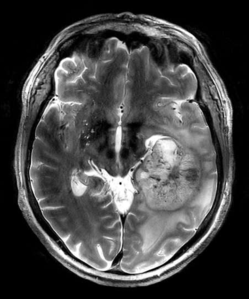
Glioblastome gelten als die bösartigsten unter den Hirntumoren. Oft gelingt es den Neurochirurgen nicht, den Tumor vollständig zu entfernen, weil die Gefahr besteht, zu viel Gehirngewebe zu zerstören. Zudem ist es häufig unmöglich, während der Operation alle feinen Ausläufer zu erkennen, mit denen der Tumor in umgebendes gesundes Gewebe einwächst. Um das Wachstum der im Kopf verbliebenen Tumorzellen zumindest zu verlangsamen, werden daher so gut wie alle Glioblastom-Patienten nach ihrer Operation bestrahlt. Damit wird aber nur ein Wachstumsaufschub und keine wirkliche Heilung erreicht, denn die Tumorzellen, insbesondere die Krebsstammzellen, sind sehr strahlenresistent. Untersuchungen hatten gezeigt, dass Strahlentherapien bei verschiedenen Krebserkrankungen besser wirken, wenn gleichzeitig bestimmte zelluläre Wachstumsfaktoren blockiert werden.
Hemmung von TGF-beta
Zellen des Glioblastoms produzieren häufig große Mengen des Wachstumsfaktors TGF-beta (transforming growth factor beta). Bei TGF-beta handelt es sich um ein Zytokin, das je nach Zelltyp, Entwicklungsstadium, Differenzierung und Zellzyklus-Position der Zielzelle unterschiedliche Reaktionen auslöst. In Abhängigkeit von diesen Parametern moduliert TGF-beta Proliferation, Apoptose, Aktivierung und Differenzierung der Zellen. Ein hoher TGF-beta-Spiegel in Glioblastomen geht mit besonders aggressivem Wachstum und schlechter Prognose einher. Außerdem scheint der Faktor die Selbsterneuerungsfähigkeit der Glioblastom-Stammzellen aufrechtzuerhalten. "Wir vermuteten daher, dass eine Blockade der TGF-beta-Signalwege die Selbsterneuerungsfähigkeit der Krebsstammzellen bremst und damit den Erfolg einer Strahlentherapie verbessern kann. Die Forscher untersuchten den Effekt einer Kombination aus Bestrahlung und dem neu entwickelten Wirkstoff LY2109761. Die Substanz blockiert die Signale, die der Rezeptor des Wachstumsfaktors TGF-beta in die Zellen weiterleitet. Untersucht wurden zunächst Glioblastomzellen aus Gewebeproben, die bei der chirurgischen Entfernung der Tumoren entnommen worden waren. Bestrahlung bei gleichzeitiger Zugabe des Wirkstoffes reduzierte die Selbsterneuerungsfähigkeit der Tumorstammzellen und verzögerte ihr Wachstum deutlich stärker als Strahlenbehandlung allein.
Wirksame Kombinationstherapie
Mäuse, denen menschliche Glio blastomzellen ins Gehirn transplantiert worden waren, überlebten nach der Kombinationstherapie länger als Tiere, die nur die Bestrahlung erhielten. Die Gewebeuntersuchung zeigte, dass unter der Kombinationstherapie Tumoren langsamer und weniger invasiv wuchsen und eine geringere Dichte an neugebildeten Blutgefäßen aufwiesen. Paradoxerweise kann die Strahlentherapie in überlebenden Tumorzellen ein bösartigeres Wachstumsverhalten provozieren. LY2109761 scheint diesen fatalen Effekt zu verhindern.
Die Blockade der TGF-beta-Signale war so vielversprechend, dass nun in einer multizentrischen klinischen Studie untersucht wird, ob dieses Wirkprinzip auch bei Patienten das Wachstum von Glioblastomen wirkungsvoller verlangsamt als die derzeitige Standardtherapie. Jetzt wird die Kombinationsbehandlung in Heidelberg, in Spanien und in den USA geprüft.
Quelle
hel





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.