
- DAZ.online
- DAZ / AZ
- DAZ 20/2011
- Über farbige ...
Feuilleton
Über farbige Arzneistoffe und den Zusammenhang von Farbigkeit und Wirkung*
Stoffe (Moleküle) erhalten bekanntlich ihre Farbe dadurch, dass sie einen Teil des auf sie fallenden Lichtes absorbieren. Der nicht absorbierte Anteil des Lichtes wird reflektiert und erscheint als Farbe.
Organische Arzneistoffe sind für das menschliche Auge dann farbig, wenn ihre Moleküle eine entsprechend ausgedehnte chromophore Gruppe enthalten, die eine Lichtabsorption ermöglicht, oder wenn das ganze Molekül ein Chromophor darstellt. Ein Chromophor ist planar und besitzt konjugierte ungesättigte Funktionen (C=C, N=N, C=N, C=O, C6H6, NO2).
Robert Koch stellte schon als Landarzt fest, dass bestimmte Farbstoffe eine große Affinität zu lebenden Zellen besitzen. Er konnte Tuberkelbazillen mit Methylenblau anfärben. Sein Schüler Paul Ehrlich erkannte (1885), dass sich bestimmte Gewebearten mit Methylenblau selektiv anfärben lassen – Voraussetzung für die verschiedenen Färbemethoden der Pathologie und Histologie.
Sulfonamide
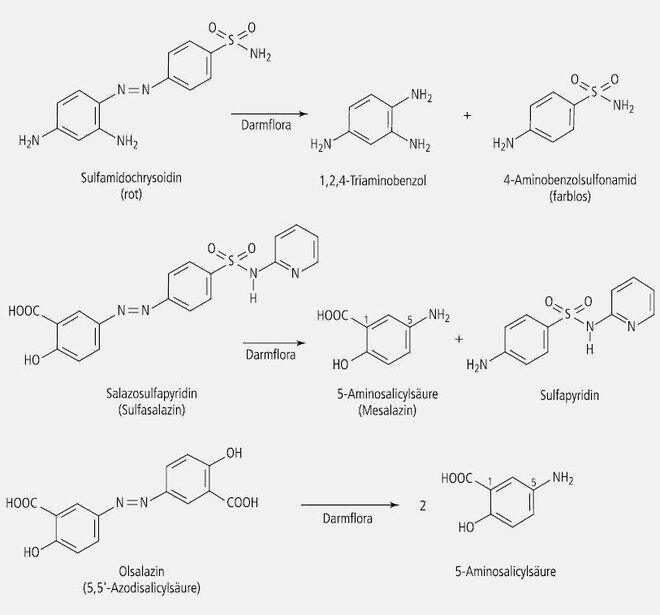
Die Überlegung, mit Farbstoffen Bakterien nicht nur anzufärben, sondern auch so zu schädigen, dass ihre Vitalität eingeschränkt wird (Bakteriostase) oder dass sie absterben (bakterizide Wirkung), war begründet und veranlasste Georg Domagk, Azofarbstoffe, die zur Färbung von Textilien Anwendung fanden, auf ihre antibakterielle Wirkung zu untersuchen. Schließlich fand das Domagksche Team nach unzähligen Molekülprofilierungen und Tierversuchen im roten Sulfamidochrysoidin einen Farbstoff, der Streptokokken absterben ließ und sich gleichzeitig für den Menschen als ausreichend verträglich erwies. Der Wirkstoff kam 1935 als Prontosil® auf den Markt (Bayer-Werke). Später stellte sich heraus, dass das farbige Prontosil ein Prodrug war, das im Organismus zum farblosen Wirkstoff Sulfanilamid (Prontalbin®) und dem unwirksamen 1,2,4-Triaminobenzol abgebaut wird (Abb. 1).
Wenn damit auch ein Zusammenhang zwischen Farbigkeit und Wirksamkeit ausgeschlossen werden musste, so führten doch die ursprünglichen Überlegungen zur Entwicklung einer hochwirksamen Gruppe von Chemotherapeutika, den Sulfonamiden. Deren therapeutische Bedeutung ging erst durch die Entdeckung des Penicillins und die Entwicklung von Penicillinen mit geeigneten pharmakokinetischen Eigenschaften zurück.
Chromophor gleich Pharmakophor
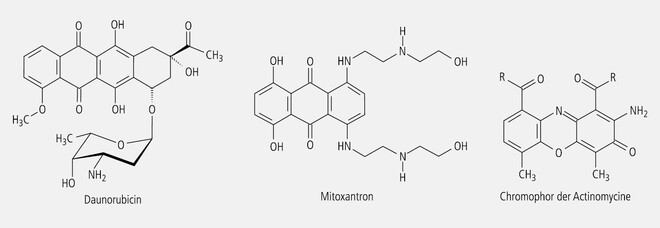
Bei anderen farbigen Arzneistoffen ist das enthaltene Chromophor (Farbträger) identisch mit dem Pharmakophor (Wirkungsträger) oder ein wesentlicher Teil desselben. Denken wir beispielsweise an die verschiedenen DNA-interkalierenden Wirkstoffe wie die nativen Anthracycline (orangerot) und Actinomycine (orangerot) oder das synthetische Mitoxantron (tiefblau), die als Zytostatika Verwendung finden (s. u., Abb. 4).
Nach Art des Chromophors können farbige Arzneistoffe in verschiedene Gruppen unterteilt werden.
Chinone, Hydrochinone und chinoide Verbindungen
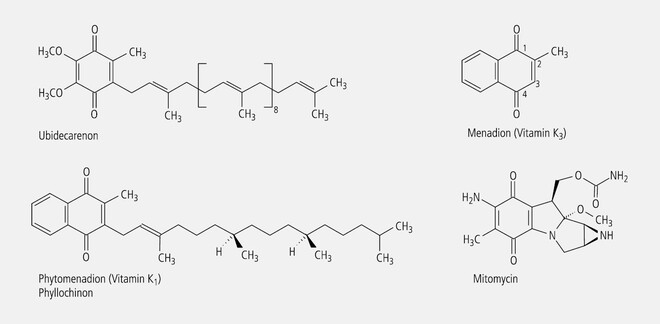
Wird das einfache 1,4-Benzochinon als Chromophor prenyliert, d. h. mit kettenförmig verknüpften Isoprenresten substituiert, so resultieren die Ubichinone, die als Coenzyme Q in fast allen Lebewesen anzutreffen sind und als Elektronenüberträger in der Atmungskette dienen. Im Europäischen Arzneibuch (Ph. Eur.) ist das Ubidecarenon (Ubichinon-10, Coenzym Q10; Abb. 2) als Arzneistoff beschrieben. Da alle Ubichinone gleichartig wirken, muss postuliert werden, dass die Wirkung an das Chromophor gebunden ist.
Das denkbar einfachste Naphthochinon-Derivat ist Menadion (2-Methyl-1,4-Naphthochinon, Vitamin K3; Abb. 2). Auch in diesem Fall ist das Chromophor Träger der Eigenschaft, die durch Hydroxycumarine verursachte Blutgerinnungshemmung wieder rückgängig machen zu können. Daran ändert sich auch nichts, wenn das Wirkstoffmolekül, wie es im nativen Phytomenadion (Vitamin K1; Abb. 2) der Fall ist, durch eine längere Kette prenyliert wird.
Im Mitomycin C (Abb. 2) ist die Partialstruktur des Benzochinon-Chromophors zwar am DNA-alkylierenden Wirkmechanismus beteiligt, aber nicht alleiniges Pharmakophor.
Chinone, Hydrochinone und chinoide Verbindungen | |
Ubidecarenon (Q 10) |
gelb bis orangefarben |
Menadion (Vit. K3) Phytomenadion |
blassgelb
intensiv gelb
|
|
Anthrachinone
Emodin Aloeemodin
Sennoside
|
orange bis gelbbraun gelb gelb |
Hypericin |
blauschwarze Nadeln* |
Anthracycline** |
orangerot |
Mitoxantron |
dunkelblau |
Mitomycin |
blauviolett |
Rifabutin |
rötlich-violett |
Rifampicin |
rötlich-braun |
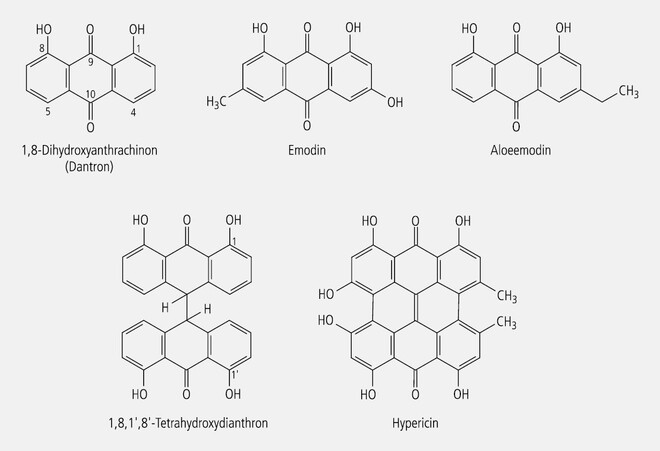
Beim Begriff "Chinone" denkt jeder Pharmazeut sofort an Anthrachinone, dann an methylierte Di- und Trihydroxychinone und gelangt so zu den Anthraglykosiden, die als Laxanzien in Aloe, Faulbaumrinde, Rhabarberwurzeln oder Sennesblättern enthalten sind. Ihre Aglyka, die zugleich Chromo- und Pharmakophore sind, werden als Emodine bezeichnet, abgeleitet vom sekundären Naturstoff Emodin (Abb. 3). Die Tetrahydroxydianthrone, die ebenfalls in den genannten Abführdrogen zu finden sind, stellen Dimerisate dar (Abb. 3).
Worauf beruht die laxierende Wirkung der Anthraglykoside? Im Darm werden sie hydrolysiert, worauf die Emodine durch die Aktivität der Colibakterien zu Anthronen oder Anthranolen reduziert werden; diese wirken antiresorptiv (indem sie die Na+/K+-abhängige ATPase hemmen) und hydragog.
Ein anderes natürliches Dimer des Emodins ist das Hypericin (Abb. 3), das als antidepressiver Wirkstoff von Johanniskrautpräparaten Bedeutung erlangt hat. Das Wirkstoffmolekül ist ein durch zwei Methylgruppen substituiertes Chromophor.
Bei den DNA-interkalierenden Wirkstoffen mit Anthrachinon-Partialstruktur (Abb. 4) ist die Identität von Chromophor und Pharmakophor über jeden Zweifel erhaben. Die planare Struktur schiebt sich zwischen die Basen der DNA und hemmt dadurch die Nucleinsäuresynthese.
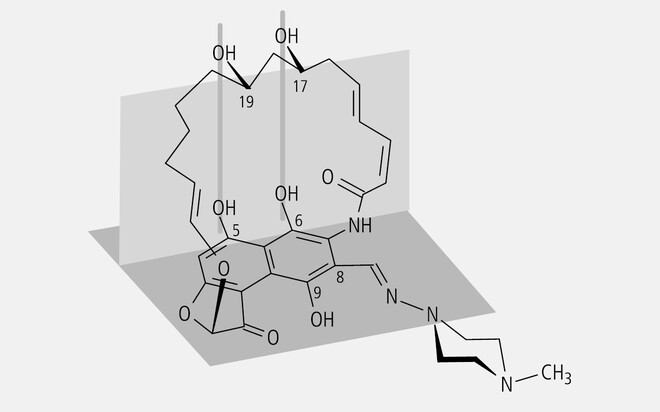
Die Ansamycine Rifampicin, Rifabutin und Analoga bestehen aus einem Naphthohydrochinon-Chromophor, das von einer langen, ringförmigen aliphatischen Kette überspannt ist (Abb. 5). Strukturelle Voraussetzung für die antimykobakterielle Wirkung ist neben der Präsenz von zwei freien OH-Gruppen an der Kette auch das Vorhandensein von zwei Sauerstoff-Funktionen, die Bestandteile des Chromophors darstellen.
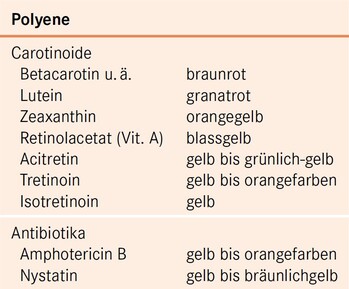
Polyene
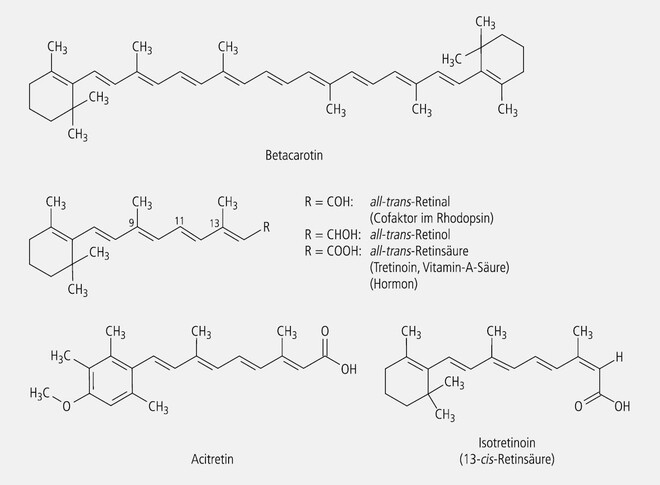
Zu den ernährungsphysiologisch "gesündesten" Polyenen gehören die Carotinoide. Als Prototypen werden hier das Betacarotin, das Lutein (Abb. 6) und das Zeaxanthin genannt – das erstere, weil es das wichtigste, bekannteste und am häufigsten (bewusst oder unbewusst) konsumierte Carotin ist, die beiden anderen, weil sie zusammen das makuläre Pigment ausmachen.
Da bei ihnen die ganzen Moleküle Chromophore darstellen, sind Chromophor und Pharmakophor identisch.
Carotinoide senken das Risiko für degenerative Erkrankungen, indem sie Zellen vor der schädigenden Einwirkung reaktiver Sauerstoffspezies schützen; dabei bilden sie resonanzstabilisierte Carotin-Radikale, die mithilfe von Ubichinonen oder Ascorbinsäure regeneriert werden.
Lutein und Zeaxanthin schützen das Auge vor einer meist altersbedingten Makuladegeneration, weshalb sie als Arzneistoffe zur Substitutionstherapie geeignet sind.
Viele Carotinoide, an der Spitze das Betacarotin, sind physiologisch als Provitamine A von Bedeutung. Vitamin A (Retinal, Abb. 6) ist Bestandteil des Sehpurpurs und als ganzes Chromophor direkt am Sehprozess beteiligt.
Tretinoin (Vitamin-A-Säure, Retinsäure, Abb. 6) wird als lokales Therapeutikum bei verschiedenen Akneformen eingesetzt und entfaltet seine Wirkung als unverändertes Chromophor. Isotretinoin (Abb. 6) wird als orales Reservetherapeutikum zur Behandlung der Akne verwendet. Wirksam ist ein oxidativer Metabolit, der selbst auch ein Chromophor darstellt.
Acitretin (Abb. 6) ist ein selektiver Retinsäurerezeptor-Agonist und bei schweren Verhornungsstörungen der Haut wie Psoriasis vulgaris indiziert. Die Wirkung seines aktiven Metaboliten ist an das Chromophor gebunden.
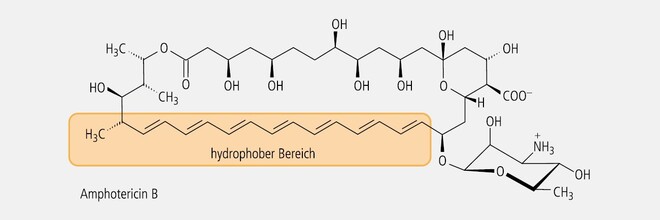
Antimykotische Polyen-Antibiotika wie Amphotericin B (Abb. 7), Nystatin oder Natamycin sind amphiphil; sie besitzen einen hydrophilen und einen lipophilen Bereich, der im Wesentlichen aus einer Polyenkette besteht. Indem diese mit dem Ergosterol in der Zellwand von Pilzen lipophile Komplexe bildet, entstehen feinste Poren, durch welche Ionen austreten können. Man kann also folgern, dass das lipophile Chromophor wesentlich an der antibiotischen Wirkung der Polyen-Antibiotika beteiligt ist.
Substituierte, farbige Heterocyclen
Monoheterocyclen
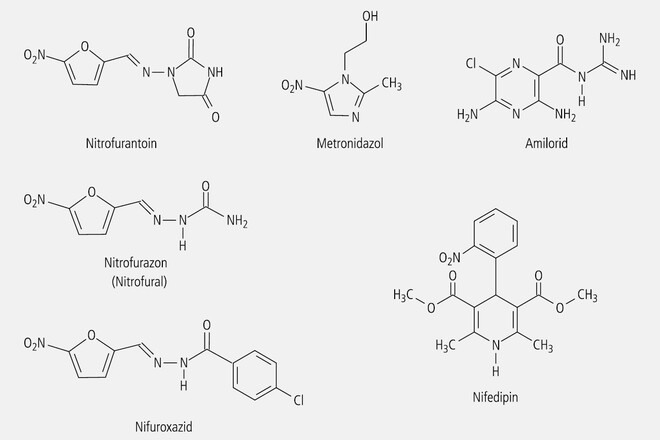
Zu den monocyclischen Verbindungen gehören Dihydropyridin-, Furan-, Imidazol-und Pyrazin-Derivate. Nifedipin, Nimodipin, Nitrendipin und viele weitere Dihydropyridin-Derivate (Abb. 8) entfalten ihre antihypertensive Wirkung, indem sie an bestimmte Calciumkanäle binden. Daran sind die freie NH-Gruppe und eine Carboxylgruppe des Chromophors beteiligt.
Die 5-Nitrofuran-Derivate Nitrofural, Nitrofurantoin und Nifuroxazid sowie das 5-Nitroimidazol-Derivat Metronidazol (Abb. 8) interferieren mit der DNA-Funktion von anaeroben Bakterien und Protozoen. Obwohl der Wirkmechanismus dieser Stoffe noch nicht völlig geklärt ist, weiß man, dass die Nitroverbindungen in der Zelle zu wirksamen Metaboliten reduziert werden; die Chromophore besitzen somit Prodrug-Charakter.
Das kaliumsparende Diuretikum Amilorid ist ein chloriertes, basisch substituiertes Pyrazin-Derivat und stellt als Ganzes ein Chromophor dar.
Substituierte, farbige Heterocyclen | |
monocyclisch | |
|
Dihydropyridine
Nifedipin
Nimodipin
Nitrendipin
|
gelb
hellgelb
gelb
|
|
Furane
Nifuroxazid
Nitrofural (Nitrofurazon)
Nitrofurantoin
|
leuchtend gelb
gelb
gelb
|
Imidazol: Metronidazol |
weiß bis schwach gelblich |
Pyrazin: Amilorid |
blassgelb bis grünlich |
bicyclisch | |
Indol: Indometacin |
weiß bis gelb |
|
Chinolone
Ciprofloxacin
Ofloxacin Pipemidsäure |
blassgelb
hellgelb
gelb
|
|
Pteridine
Folsäure u. Methotrexat
Triamteren
|
gelb bis orange
gelb
|
|
Benzodiazepine
Nitrazepam
Chlordiazepoxid
Midazolam (tricyclisch!)
|
gelb
weiß bis hellgelb
weiß bis gelblich
|
|
Thiazine
Benzothiazin: Piroxicam
Thienothiazin: Tenoxicam
|
weiß bis schwach gelb
gelb
|
tricyclisch | |
Acridin: Ethacridinlactat |
gelb |
Isoalloxazin: Riboflavin |
gelb bis orange |
Phenoxazone: Actinomycine, Dactinomycin |
orangerot
|
tetracyclisch | |
(Dihydro-) Porphyrine* |
rot |
Corrin: Cyanocobalamine (Vitamine B12) |
dunkelrot |
| * Hämatoporphyrin, Verteporfin, Temoporfin | |
Heterobicyclen
Zu den bicyclischen Verbindungen gehören Indol-, Chinolon-, Benzodiazepin- und Pteridin-Derivate.
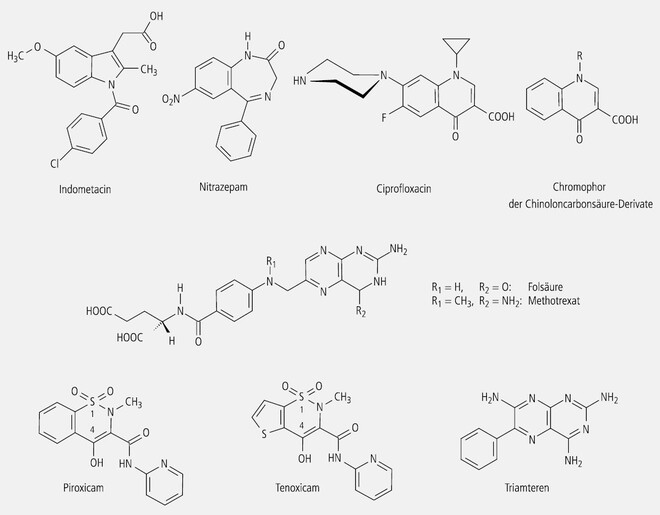
Da die Metaboliten des Indolderivats Indometacin (Abb. 9) unwirksam sind, darf man davon ausgehen, dass es in toto als COX-Hemmer agiert.
Die Gyrasehemmer Ciprofloxacin (Abb. 9), Ofloxacin, Pipemidsäure – und wie sie alle noch heißen – bilden einen ternären Komplex mit DNA und dem Enzym Gyrase, der durch Magnesium-Ionen stabilisiert wird. Da dabei das intakte Molekül gebunden wird, ist sein Chromophor auch Träger der Wirkung.
Benzodiazepin-Derivate, die als Tranquillanzien, Anxiolytika, Hypnotika, Antiepileptika und Muskelrelaxanzien eingesetzt werden, können dem menschlichen Auge gelb (Nitrazepam, Abb. 9), weiß bis gelblich (Chlordiazepoxid) oder weiß (Lorazepam, Oxazepam, Tenazepam) erscheinen. Das gilt auch für die tricyclischen Vertreter dieser Arzneistoffgruppe (z. B. Alprazolam weiß, Midazolam weiß bis gelblich). Benzodiazepine binden als unveränderte Moleküle an Untereinheiten von GABA-Rezeptoren und werden dadurch wirksam. Die anhaftenden Substituenten verändern die pharmakokinetischen Eigenschaften. Ihre Wirkung ist also an das Chromophor gebunden, das auch dann als Chromophor anzusehen ist, wenn die Substanz unserem Auge weiß erscheint (viele Insekten z. B. sehen Verbindungen farbig, die uns farblos erscheinen).
Das B-Vitamin Folsäure und ihr Antagonist Methotrexat (Abb. 9) sind Pteridin-Derivate. Zur Entfaltung ihrer Wirkung muss ihre chromophore Partialstruktur über die Dihydro- zur Tetrahydro-Form reduziert werden. Das Chromophor stellt demnach ein partielles Prodrug dar.
Ein synthetisches Pteridin ist ferner das Diuretikum Triamteren, das insgesamt ein Chromophor repräsentiert (Abb. 9).
Oxicame vom Typ des Piroxicams oder Tenoxicams (Abb. 9) stellen substituierte Benzothiazine bzw. Thienothiazine dar, die als COX-Hemmer entzündungshemmende und analgetische Wirkungen zeigen. Strukturelle Wirkungsvoraussetzungen sind eine chromophore Teilstruktur und eine vinyloge Säurefunktion.
Heterotricyclen
Farbige Acridin-, Isoalloxazin- und Phenoxazin-Derivate gehören zu den tricyclischen Verbindungen.
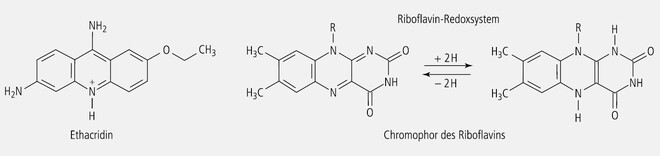
Beim Ethacridin (Abb. 10), dessen Anwendung als Antidiarrhoikum allerdings problematisch ist, sind Chromophor und Pharmakophor wiederum identisch.
Die Bezeichnungen Riboflavin oder Lactoflavin für Vitamin B2 weisen schon darauf hin, dass es ein gelbes Chromophor enthält. Es ist das 7,8-Dimethyl-isoalloxazin, das ein Redoxsystem darstellt (Abb. 10), auf dem die Funktionen der Flavin-Enzyme beruhen. Der chromophore Teil des Vitamins ist also eindeutig der Wirkungsträger.
Die tricyclischen Actinomycine als DNA-interkalierende Wirkstoffe wurden eingangs schon erwähnt; ihre chromophore Partialstruktur ist ein carboxyliertes Phenoxazin (Abb. 4).
Heterotetracyclen
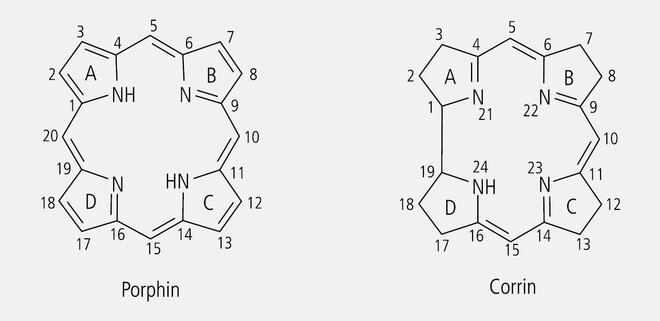
Farbige tetracyclische Verbindungen sind einige Porphyrinabkömmlinge (Abb. 11), die zur photodynamischen Therapie eingesetzt werden, wie Hämatoporphyrin, Verteporfin oder Temoporfin. In diesen Fällen ist das Chromophor die Conditio sine qua non, da es nach Applikation des Wirkstoffs und geeigneter Bestrahlung den tumorschädigenden Effekt auslöst.
Zu nennen sind hier auch die Cobalamine (Vitamin-B12-Gruppe), welchen als Gerüst das Corrin (Abb. 11) mit dreiwertigem Kobalt als Zentralatom zugrunde liegt. Corrin unterscheidet sich vom Porphyrin durch einen – aus Sicht der Biosynthese – nachträglich eingebauten "Webfehler". Im zentrosymmetrischen Porphyrin sind vier Pyrrol-Einheiten durch je eine Methingruppe ringförmig miteinander verbunden. Das Corrin unterscheidet sich davon durch das Fehlen einer Methingruppe zwischen Ring A und Ring D und eine geringere Anzahl von Doppelbindungen, was seiner Farbkraft aber keinen Abbruch tut. Das Cobalamin mit der höchsten praktischen Bedeutung ist das dunkelrote Cyanocobalamin. Es wird zur Substitutionstherapie bei perniziöser Anämie eingesetzt. Die Funktion der Cobalamine als Coenzyme verschiedener Stoffwechselprozesse ist an das intakte Molekül mit zentralem Chromophor gebunden.
Azofarbstoffe, die heute noch als Arzneimittel verordnet werden, sind Olsalazin und Sulfasalazin (Abb. 1). Die beiden intestinalen Antiphlogistika stellen Prodrugs dar, die zu 5-Aminosalicylsäure, dem eigentlichen Wirkstoff, metabolisiert werden.
"Weiß bis gelb oder schwach gelblich"
Wenn ein Arzneistoff im Europäischen Arzneibuch im Abschnitt "Eigenschaften" als weiß bis gelblich (wie Indometacin) oder als weiß bis schwach gelblich (wie Diclofenac-Kalium/Natrium) bezeichnet wird, so handelt es sich dabei nicht um einen weißen Stoff, der durch einen gelben Stoff verunreinigt ist. Denn die Farbe (Farbigkeit) einer Verbindung wird nicht nur durch das darin enthaltene Chromophor bestimmt, sondern auch von Kristallfeld-, Beugungs- und Interferenzprozessen beeinflusst.
Dagegen können Angaben "weiß bis fast weiß" oder "weiß bis schwach grauweiß" u. U. auch auf grenzwertigen Verunreinigungen beruhen.
Weitere farbige Arzneistoffe
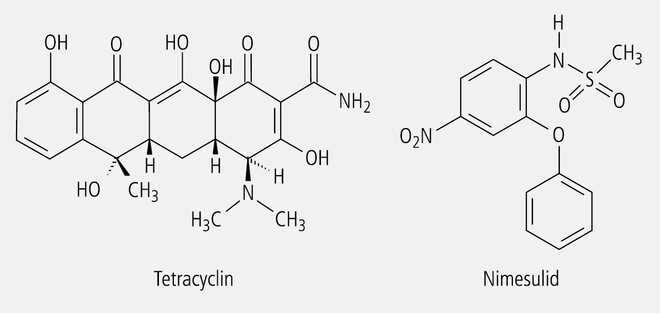
Die gelben Tetracycline (Abb. 12) besitzen chromophore Teilstrukturen, die wesentlich zu ihrer antibiotischen Wirkung beitragen.
Der präferenzielle COX-2-Hemmer Nimesulid (in Deutschland nicht als Humanarzneimittel zugelassen) ist ein Sulfonamid mit einer Nitrobenzolgruppe (Abb. 12). Im Gegensatz zu den eingangs erläuterten Sulfonamiden mit einer Azogruppe ist Nimesulid kein Prodrug, sondern in unveränderter Form wirksam.
Die Farbigkeit anorganischer Salze und Verbindungen beruht in der Regel auf der Farbe des darin enthaltenen Metallatoms oder Metallkations, z. B.:
Bismut gelb,
Eisen(II) grün,
Eisen(III) bräunlich,
Kupfer(II) grün bis blau,
Mangan rosa,
Natrium gelb.
Farbige Elemente, die als Arzneistoffe benutzt wurden (heute obsolet), sind Schwefel und Iod.
Schlussbemerkung. Wenn Sie einen Chemiker, einen Apotheker oder einen Arzt fragen, ob es viele farbige Arzneistoffe gibt (ich habe es getan), so lautet die Antwort meistens "nein, höchstens einige wenige".
Würde man nach der Beteiligung der farbgebenden Strukturen an der pharmakologischen Wirkung von Arzneistoffen fragen, so wäre die Antwort vermutlich "selten".
Der aufmerksame Leser des vorliegenden Essays wird diese Meinungen revidieren müssen.
Autor
Prof. Dr. rer. nat. Dr. h. c. Hermann J. Roth, Friedrich-Naumann-Str. 33, 76187 Karlsruhe, www.h-roth-kunst.com, info@h-roth-kunst.com




















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.