
- DAZ.online
- DAZ / AZ
- DAZ 12/2011
- Sind das leuchtende Rot ...
Feuilleton
Sind das leuchtende Rot des Fliegenpilzes und das satte Pigment der Roten Bete molekulare Geschwister oder molekulare Kontrahenten?*
Zwar ist der Pilz nicht gar so giftig, wie man oft meint, und die Rübe nicht ganz so gesund (Nitrate, Oxalsäure), wie es bestimmte Bioapostel predigen, aber beide hat die Natur rot "angestrichen". Ein Erwachsener kann schon einige rote Fliegenpilze essen, ohne Schaden zu nehmen. In Hamburg und Umgebung stand der Fliegenpilz früher auf der Speisekarte. In bestimmten japanischen Gegenden gilt er heute noch als Delikatesse. Die leberschädigenden Phallotoxine der Knollenblätterpilze, die durch Kochen oder Trocknen nicht eliminiert werden, sind im Fliegenpilz nicht anzutreffen. Giftig sind die mehr oder minder halluzinogenen Inhaltsstoffe wie Ibotensäure, Muscimol, Muscazon und Muscarin [1]. Bei sibirischen Völkern werden der Fliegenpilz oder seine wässrigen Extrakte immer noch als kultische, psychedelische Rauschmittel eingesetzt. In der Szene wird er heute sogar geraucht. Dazu zieht man die Huthaut des frischen Pilzes ab, trocknet sie und benutzt sie zum Rauchen.
So weit zum Stand der Dinge um den schönen Pilz, der jedem Kind bekannt ist. Kommen wir jetzt zur Sache, nämlich zur Farbe.
Die rote Farbe des Fliegenpilzes (Amanita muscaria) und die der herkömmlichen Roten Rübe (Beta vulgaris ssp. vulgaris var. conditiva) werden durch Vertreter derselben Pigmentfamilie, der Betalaine, verursacht. Daraus kann geschlossen werden, dass die Pigmente des Fliegenpilzes nicht giftig sind. Man könnte sie nach ihrer Isolierung genauso zum Färben von Lebensmitteln verwenden wie den Saft oder das getrocknete Pulver der Roten Bete.
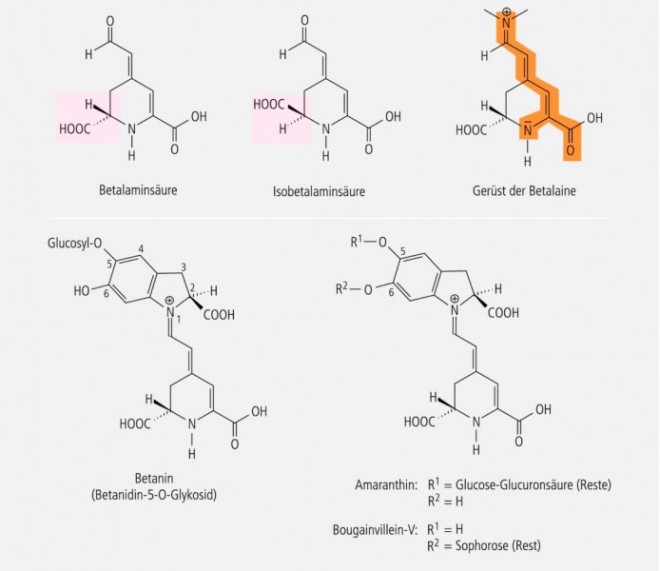
Im Gegensatz zu den Anthocyanen enthalten die Betalaine Stickstoff und stellen Derivate der Betalaminsäure (Abb. 1) dar, die man als Chromo-Alkaloide bezeichnen kann. In Übereinstimmung mit den Anthocyanen sind es wasserlösliche Vakuolen-Farbstoffe. Man unterscheidet zwei Gruppen: rotviolette Betacyane und gelbe Betaxanthine, zu welchen auch die gelben bis purpurfarbenen Muscaaurine gehören [2].
• Ein typischer Vertreter der Betacyane ist das Betanin (Betanidin-5-O-Glykosid, Abb. 1), der Farbträger der Roten Bete.
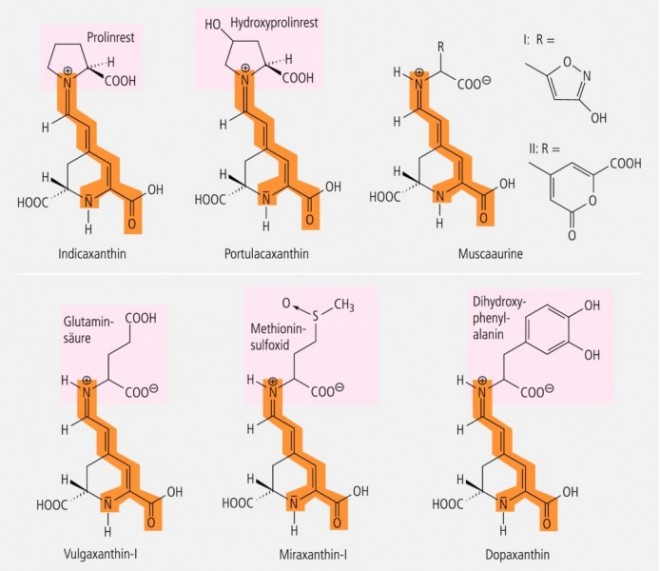
• Ein Pigment vom Typ der Betaxanthine ist das Indicaxanthin (Abb. 2), das die Kaktusfeigen (Opuntia ficus-indica) gelb färbt.
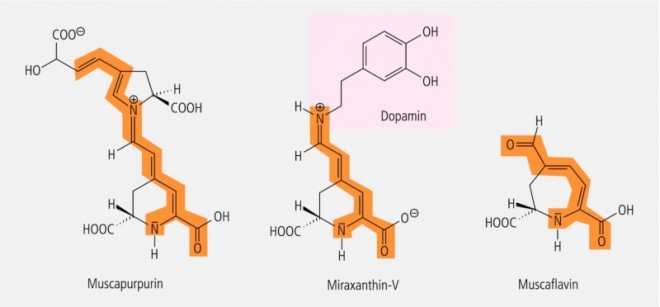
• Zur Gruppe der Muscaaurine zählen die Muscaaurine I, II, III etc. (Abb. 2) sowie das um zwei Doppelbindungen reichere Muscapurpurin (Abb. 3), die zusammen mit dem gelben Dihydroazepin-Farbstoff Muscaflavin (Abb. 3) das leuchtende Rot der Huthaut der Fliegenpilze ausmachen.
Betalainsäure und Muscaflavin sind strukturisomere Verbindungen (C9H9O5N) und entstehen biochemisch aus demselben Edukt DOPA (C9H11O4N).
Zur Erklärung der Farbigkeit der Betalaine, die zu den Polymethinen zu rechnen sind, vergleiche man die Angaben in der "Arzneistoffanalyse" [3] über Cyanine und Merocyanine.
Betanin (Betenrot), der Naturfarbstoff aus der Wurzelknolle der Roten Rübe, ist unter den Kürzeln E 162 und L-Rot 10 als Lebensmittelfarbstoff zugelassen [4]. Es handelt sich dabei um ein Gemisch von Betacyaninen und Betaxanthinen.
Im Handel befinden sich Konzentrate aus Rote-Bete-Saft und Betenrotpulver, das durch Trocknen des Saftes gewonnen wird. Obwohl Fleischwaren in Deutschland nicht zu den Lebensmitteln gehören, die gefärbt werden dürfen (außer: indirekt durch Pökeln), kommt es vor, dass Rote-Bete-Saft zum Färben von Brüh- und Rohwürsten eingesetzt wird [4].
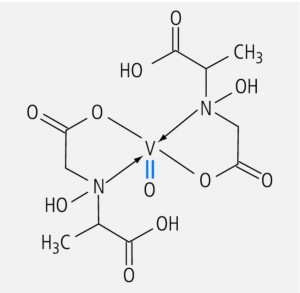
Fliegenpilze enthalten aber noch einen anderen Farbstoff, nämlich das Amavadin, einen blauen 1:2-Vanadium(IV)-Komplex (Abb. 4).
In welchen Pflanzen kommen außerdem noch Betalaine vor?
Betacyane finden wir in Kakteen (Cactaceae), in Bougainvillea-Arten (Nyctaginaceae), in der Kermesbeere (Phytolaccaceae), in Fuchsschwanz-Arten (Amaranthaceae) und in Gänsefußgewächsen (Chenopodiaceae) wie der Roten Bete, die nach neuester Taxonomie ebenfalls zu den Amaranthaceae gehören [5].
Die meisten Betacyane sind 5‑O-Glykoside des Betanidins (z. B. Betanin oder Amaranthin), einige aber auch 6-O-Glykoside (z. B. Bougainvillein-V; Abb. 1).
A propos: wenn wir die ursprünglich lilafarbenen und heute durch Züchtung gelben, orangefarbenen, rosaroten, roten bis violetten Blüten der Bougainvillea-Arten bewundern, so sollten wir wissen, dass es die Hochblätter des Blütenstandes sind. Dieser besteht jeweils aus drei kleinen bis unscheinbaren Blüten, die von drei auffallend farbigen Hochblättern umgeben sind. Den Namen gab ihnen der Botaniker und Schiffsarzt Philibert Commerçon, der den großen Seefahrer und Entdecker Louis-Antoine de Bougainville (1729 – 1811) auf seiner Weltumseglung begleitete.
Neben den Betanidin-Derivaten kommen als pflanzliche Pigmente auch Abkömmlinge des Isobetanidins vor, die sich von der Isobetalaminsäure ableiten (Abb. 1).
Betaxanthine findet man in den Rüben (Beta vulgaris ssp.), in den Mittagsblumengewächsen (Aizoaceae), z. B. Glottiphyllum longum, im Portulakröschen (Portulaca grandiflora, Portulacaceae), oder in der Wunderblume (Mirabilis jalapa, Nyctaginaceae) [5]. Als Beispiele seien genannt: Vulgaxanthin-I, Miraxanthin-I, Miraxanthin-V und Portulacaxanthin (Abb. 2 und 3).
Betaxanthine sind in der Regel Kondensationsprodukte der Betalaminsäure mit α‑Aminosäuren (Abb. 2). So ist im Indicaxanthin der Prolin-Rest, im Portulacaxanthin der Hydroxyprolin-Rest, im Vulgaxanthin-I der Glutaminsäure-Rest und im Dopaxanthin der Rest des Dihydroxyphenylalanins (DOPA) enthalten. Miraxanthin-I ist aus Betalaminsäure und dem Methioninsulfoxid aufgebaut. Im Miraxanthin-V (Abb. 3) ist keine Aminosäure enthalten, sondern das biogene Dopamin.
Übrigens: Alle bisher genannten Pflanzenfamilien zählen zur Ordnung Caryophyllales; die Betalaine sind ein taxonomisches Merkmal, allerdings sind sie nicht für das Rot der Gartennelke (Dianthus caryophyllus) verantwortlich, die den Caryophyllales ihren Namen gegeben hat.
Welche pharmakokinetischen und pharmakodynamischen Effekte haben die Betalaine?
Aus vergleichenden Untersuchungen nach oraler Applikation von Betanin und Indicaxanthin kann geschlossen werden, dass Betacyane schlecht, Betaxanthine hingegen gut resorbiert werden [6]. Die renale Elimination von Betanin lag unter 5%, die von Indicaxanthin bei 75%. Maximale Konzentrationen im Blutserum werden nach drei Stunden erreicht und betragen bei Betanin 0,2 nmol/ml, bei Indicaxanthin
6,9 nmol/ml.
Betalaine sind effektive Antioxidanzien mit Radikalfängereigenschaften, was in vitro und in vivo nachgewiesen wurde. Im Blutserum führen sie zu einer deutlichen Abnahme der Biomarker für den oxidativen Stress.
Literatur
Autor
Prof. Dr. rer. nat. Dr. h. c. Hermann J. Roth
Friedrich-Naumann-Str. 33,
76187 Karlsruhe
www.h-roth-kunst.com























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.