
- DAZ.online
- DAZ / AZ
- DAZ 1/2011
- Sind Viren Lebewesen
DAZ wissenswert
Sind Viren Lebewesen?
Widersprüchliche Theorien
Viren sind keine Lebewesen. Sie atmen nicht, können sich nicht selbstständig vermehren und betreiben keinerlei Stoffwechsel. Diese Definition wird angezweifelt. Die Entdeckung von immer mehr Riesenviren zwingt dazu, deren Rolle und Aufgabe in der Evolution und in der Biosphäre ebenso zu überdenken wie ihre definitorische Beschreibung. Dabei liegt ihre Herkunft immer noch im Dunkeln. Hierzu existieren insbesondere drei Theorien.
Nach dem Prophagen- und dem Protoonkogenkonzept haben sich die Viren aus Genen von Prokaryonten oder Eukaryonten entwickelt ("Escape-Modell"). Durch die Kombination mit Nucleocapsidgenen entstanden infektiöse Körper, die Virionen, die außerhalb des Wirtes überdauern und sich innerhalb des Wirtes vermehren können.
Nach einer ähnlichen Theorie könnten Viren aus parasitischen Zellen entstanden sein, deren Genom reduziert wurde (z. B. Amöbentheorie, s. u.).
Diesen entgegen steht das "Virus-first-Modell". Es besagt, Viren seien bereits vor den ersten biologischen Strukturen in einer präzellulären RNA-Welt (selbstreplizierende Moleküle) entstanden.
Riesenviren und ihre genetische Analyse sorgen nun für Diskussionen. Die Frage, ob die Viren vor oder nach LUCA (Last Universal Cellular Ancestor) entstanden sind, wird neu gestellt. Der französische Forscher Patrick Forterre vom Pasteur-Institut in Paris stellt ein Virozell-Konzept vor, das auf der Grundlage der Riesenviren versucht, Viren generell als lebende Organismen in die Evolutionsgeschichte einzuordnen – zumal Viren ein weit größeres Reservoir an Genen aufweisen als die zellulären Organismen.
|
"Dieses Mimivirus sieht mir aus wie eine neue parasitische Lebensform." Jean-Michel Claverie |
Die ersten Riesenviren
Das erste Riesenvirus war bereits 1975 beschrieben worden: der Phage G, der den Bacillus megaterium infiziert. Seine DNA-Sequenz war größer als die kleiner Bakterien. Lange blieb er ein unerklärlicher Einzelfall. Man fand keine weiteren Riesenviren, weder in Filtraten noch in Plaques. Für die 0,2-μm-Filter sind sie schlicht zu groß. Und in Petrischalen scheinen sie sich offenbar nur sehr langsam zu vermehren. Ihr Nachweis gelingt erst mit den modernen molekularen Analysenmethoden.
So kam die nächste Entdeckung erst 2003. Forscher um Jean-Michel Claverie und Didier Raoult von der Universität Aix-Marseille II hatten 1992 in Bradford in England Kühlkreisläufe von Klimaanlagen auf Legionellen (Legionella pneumophila) untersucht und in der Amöbe Acanthamoeba polyphaga einen grampositiven Kokken identifiziert, den sie Bradfordcoccus nannten. Erst elf Jahre später erkannten sie, dass das vermeintliche Bakterium ein ikosaedrisches Capsid ist. Die Virushülle ist mit Fibrillen besetzt wie bei einem Bakterium und hat einen Durchmesser von 400 nm; somit handelt es sich um das größte bisher bekannte Virus. Seine doppelsträngige (ds) DNA ist 1,2 Mio. Kilobasenpaare (kb) lang und zählt 981 codierende Sequenzen, darunter auch Gene, die man bis dahin nur aus Lebewesen kannte. Die Forscher nannten ihr Fundstück "Mimicking Virus" oder kurz "Mimivirus", da es das Mimikry eines Bakteriums hat.
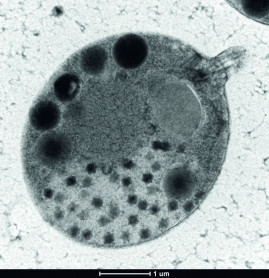
Im Jahr 2010 wurde vor der Küste von Texas im Golf von Mexiko das Cafeteria roenbergensis Virus, kurz CroV, entdeckt (Abb. 1). Seine dsDNA ist 618 kb lang und trägt 544 Gene; davon werden 274 Gene während der Infektion des Flagellaten Cafeteria roenbergensis zur Proteinsynthese exprimiert. Zum Vergleich: Ein "normales" Virus besitzt nur etwa zehn Gene, ein Bakterium hingegen mindestens 470 (Mycoplasma genitalium). Als Bakterium mit dem kleinsten Genom (145 kb) gilt derzeit Hodgkinia cicadicola , die endosymbiontisch in der Zikade Diciceroprocta semicincta lebt.
Während Acanthamoeba nur im Süßwasser lebt, ist der heterotrophe Flagellat Cafeteria (er gehört zu den Bicosoecida innerhalb der Stramenopilen oder Heterokonta) in marinen Oberflächenwassern, in Tiefseesedimenten und sogar in hydrothermalen Schloten sehr weit verbreitet und kann bis zu 20% des Nanoplanktons ausmachen, das am Beginn der Nahrungskette des Meeres steht. Er ist (ohne Geißeln) 4 bis 6 μm lang und ernährt sich phagozytotisch von Bakterien und Viren.
Wird ein solch wichtiger Organismus von Viren befallen, ist das Anlass genug, deren Rolle und Einfluss genauer zu betrachten. Das außerordentlich komplexe CroV besitzt viele Gene, die an der DNA-Replikation, ‑Transkription und -Translation und sogar an der Proteinmodifikation und dem Kohlenhydratmetabolismus seines Wirtes beteiligt sind. Das lässt vermuten, dass CroV eine autonome Strategie bei der Vermehrung in Cafeteria verfolgt (s. u. "Killing the winner").
| In der Cafeteria Cafeteria soll seinen Namen von seinem Entdecker Curtis Suttle, University of British Columbia, erhalten haben, nachdem dieser in einer Cafeteria stundenlang mit seinen Studenten über diesen Flagellaten diskutiert hatte. |
Viele Giren – viele Theorien
Immer mehr Riesenviren (giant viruses) werden entdeckt. Man nennt sie mittlerweile Giren, um sie von den "normalen" Viren abzugrenzen. Giren besitzen nicht nur ungewöhnlich viele Gene, sie produzieren auch viel tRNA, die für die Proteinsynthese notwendig ist. Da erstaunt es kaum, dass sie auch atypische Sequenzen wie Introns und Inteine besitzen. Dadurch sind sie in der Lage, die Sequenzen ihrer DNA und der von ihnen synthetisierten Proteine zu modifizieren.
Da es kein Gen gibt, das allen Viren gemeinsam ist, ist ihr monophyletischer Ursprung unwahrscheinlich. Einige Forscher vermuten, dass alle Giren aus demselben Genpool stammen wie die Pro- und Eukaryonten. Andere sehen lediglich einen regen horizontalen Gentransfer zwischen diesen Gruppen.
Die Amöbentheorie ist besonders originell. Da Amöben gewöhnlich besonders viele verschiedene Mikroorganismen in ihr Cytoplasma aufnehmen, sind sie als eine Art "Marktplatz" der Mikroorganismen zu betrachten, die dort ihre Gene austauschen können. Hier könnten durch Rekombinationen und Reduktionen von DNA die Giren entstanden sein. Giren, die auf ihr Capsid eine Schicht von Fibrillen aufbauen, ähneln grampositiven Bakterien und sind groß genug, um bei Amöben den phagozytotischen Reflex auszulösen.
Die meisten Giren werden zu den NCLDV (Nucleocytoplasmic Large DNA Viruses) zusammengefasst. Diese sind zwar sehr variabel in ihrer Morphologie, haben aber 47 Gene gemeinsam. Derzeit werden die VCLDV in fünf bis sechs Untergruppen gegliedert (Tab. 1).
Tab. 1: Giren (VCLDV) und ihre Eigenschaften; kleine Auswahl [7]. | ||||
Gruppe |
Girus |
DNA (Länge), davon codierend |
Capsid Ø (nm) |
Wirte |
Mimiviridae |
Acanthamoeba polyphaga Mimivirus (APMV) |
1181 kb, 86% |
400 |
Protozoen |
Myoviridae |
Pseudomonas chlororaphis Phage |
317 kb, 93% |
120 |
Proteobacteria |
Bacillus megaterium Phage G |
670 kb, ? |
? |
Firmicutes* |
|
Nimaviridae |
Shrimp WSSV (White spot syndrome Virus) |
305 kb, 92% |
? |
Tiere |
Phycodnaviridae |
Chlorovirus PBCV-1 (Paramecium bursaria chlorella Virus 1) |
331 kb, 90% |
190 |
Pflanzen |
Cafeteria roenbergensis Virus (CroV)** |
618 kb, 90% |
280 |
Stramenopile |
|
Heterocapsa circularisquama Virus |
356 kb, ? |
200 |
Protozoen |
|
Poxviridae |
Canarypox Virus (CNPV) |
360 kb, 90% |
160 – 190 |
Tiere |
? |
Marseillevirus |
368 kb, 89% |
250 |
Protozoen |
| * grampositive Bakterien; ** andere Forscher zählen CroV zu den Mimiviridae | ||||
Konzept der Virozelle
Nach klassischer Definition ist ein Virion, also ein komplettes Virus mit Genom und Hülle außerhalb einer Zelle, kein Lebewesen, da es sich nicht vermehren kann. Patrick Forterre (s. o.) und Claudiu Bandea (Centers for Disease Control and Prevention, USA) hingegen sehen nicht im Virion das entscheidende Stadium des viralen Lebenszyklus, sondern in der intrazellulären Form des Virus.
Die Replikation des Mimivirus in Acanthamoeba lässt sich im Lichtmikroskop beobachten: Auf klar abgegrenzten sphärischen Strukturen entstehen die Virionen. Durch die virale Infektion der Amöbe wird deren Stoffwechsel vollständig neu organisiert; es entsteht eine "Virozelle" mit einer "viralen Fabrik" (Forterre), einem intrazellulären parasitischen Organismus mit metabolischer Aktivität.
Das Mamavirus, ein naher Verwandter des Mimivirus, kann seinerseits von winzigen Sputnik-Viren infiziert werden, was die Reproduktionsrate verringert. Die virale Fabrik hat somit alle Eigenschaften einer lebenden Zelle: Reproduktion und Stoffwechselaktivität und sogar Anfälligkeit für "Krankheiten".
Analog zur These von Jacques Monod (1910 – 1976; Nobelpreis 1965), es sei der Traum jeder Zelle, zwei Zellen zu werden, sagt Forterre, es sei der Traum einer Virozelle, Hunderte neuer Virozellen durch das Freisetzen der Virionen zu erzeugen. Er stellt die Virozelle den Ribozellen der Pro- und Eukaryonten gegenüber; dabei entspricht die virale Fabrik der Virozelle dem Zellkern der Ribozelle.
Viren im NetzViren-Datenbank: www.ictvdb.org Mimiviren: www.nationmaster.com/ encyclopedia/mimivirus Datenbank der Giren mit Bildern: www.giantvirus.org |
Koevolution
Virale Fabriken und Zellkerne liegen beide im Zytoplasma, und beider Membranen werden aus dem Endoplasmatischen Retikulum aufgebaut. Da sie in der infizierten Zelle nebeneinander existieren, ergeben sich viele Möglichkeiten des Genaustausches und der Koevolution. Neue genetische Analysen lassen vermuten, dass 13% der Gene von Archaea und Bakterien von Viren und ähnlichen mobilen Elementen eingeführt worden sind. Das menschliche Genom soll sogar bis zu 40% aus Retroviren stammen. Telomere und Zentromere stammen in jedem Fall von Retroviren. Das Maisgenom soll zu 85% aus Transposons, die wiederum Viren entstammen, aufgebaut sein.
Aus all diesen Gründen sollten Viren älter sein als die Ribozellen der Nachfahren von LUCA.
Viren spielten (und spielen) eine entscheidende Rolle in der Evolution des Lebens, indem sie ihre Wirte zwangen, Abwehrstrategien zu entwickeln. So wird vermutet, dass pathogene Bakterien ihre Virulenzgene aus Viren bezogen haben, was ihnen nützte, weil sie sich damit gegen ihre einzelligen Fressfeinde wehren konnten. Im Laufe der Evolution gingen sie zum Angriff über und nutzten die Virulenzgene zur Infektion eukaryontischer Zellen.
Die Koevolution spielt auch bei Giren eine Rolle. Hier schließt sich der Kreis zu Cafeteria.
Killing the winner
Die Populationsgröße eines Organismus in seiner Umwelt wird bestimmt von seinem Wachstum und seiner Mortalität. Da Bakterien und Archaea im Pelagial (uferfernes Wasser oberhalb der Bodenzone) eine Nahrungsknappheit (Bottom-Up-Control) lange überstehen können, wird ihre Mortalitätsrate wesentlich von der viralen Lysis und dem Hunger von Fressfeinden (Top-Down-Control) bestimmt. Die marinen Viren infizieren dabei sowohl die Bakterien als auch deren Feinde, allerdings infizieren bestimmte Viren immer nur bestimmte Spezies.
Dieses Zusammenspiel ist sehr komplex und noch kaum aufgeklärt. Generell kann man aber sagen, dass Viren vornehmlich die stark wachsenden Populationen befallen. Das nennt man das Phänomen "killing the winner". Dieser Mechanismus kann erklären, weshalb so viele verschiedene Bakterien- und Phytoplanktonarten nebeneinander existieren können. Die Viren begrenzen diejenigen, die sich stärker vermehren. Seltene Arten werden hingegen weniger zahlreich infiziert.
Der Anteil der Viren an der gesamten Mortalität wird auf etwa 20% geschätzt. Bei der Kalkalge Emiliania huxleyi, der Alge des Jahres 2009, kann dieser Anteil aber auch 100% betragen, wenn sie sich massenhaft vermehrt hat und mit ihrer "Algenblüte" Flächen von über 100.000 km2 bedeckt.
|
"Der Milliarden Jahre währende Kampf zwischen Zellen und Viren ist der wichtigste Motor der Evolution." Patrick Forterre |
Rolle im Nährstoffkreislauf
In den letzten Jahren hat sich immer deutlicher gezeigt, dass Viren eine wichtige Rolle in den marinen Ökosystemen spielen. Als Virionen sind sie ubiquitär und können vor allem in küstennahen Gewässern eine Konzentration bis zu 108 Partikeln je Milliliter Wasser erreichen. Ihre Anzahl korreliert mit der der Bakterien und ist typischerweise fünf- bis zehnmal so hoch. Ihre im Seewasser gelöste DNA ist ein wichtiger Bestandteil des Phosphorzyklus innerhalb der Nahrungsnetze und Nahrungsketten. Die Lysis ihrer Wirte beeinflusst die Zusammensetzung und die Menge gelöster organischer Materie (DOM = dissolved organic matter); während tote Organismen zu Boden sinken, bleibt die DOM in der oberen, euphotischen (lichtreichen) Zone der Wassersäule und steht hier den Mikroben als Nährstoff zur Verfügung. Ein Viertel der Primärproduktion soll durch diesen viralen Degenerationsprozess fließen.
Potenzial ohne Ende
Das nutzbare Potenzial der Viren wächst mittlerweile in große Höhen. Ihre Gene stellen einen Pool vieler noch unbekannter Genprodukte dar. Interessant ist dabei, dass viele virale Proteine besonders klein sind. Auch die Gentechnologie möchte diesen Pool nutzen. Beispielsweise sind neue Restriktionsendonukleasen gefunden worden und neue Promotor- und Enhancer-Sequenzen, die sowohl in Mono- als auch Dikotyledonen funktionieren. Die Nanotechnologie entwickelt ebenfalls neue Produkte mittels Viren.
Viren könnten die neue Schnittstelle zwischen Biologie, Chemie und Materialwissenschaften werden. Biosensoren, katalytische oder enzymatische Nanofabriken, Nanoelektronik – der Fantasie scheinen derzeit keine Grenzen gesetzt. Zudem sind in den Weiten und Tiefen der Meere noch viele Giren zu entdecken.
Vielleicht kommt auch die Phagentherapie wieder zu Ehren. Sie war von dem Frankokanadier Felix d‘Herelle (1873 – 1949) bereits 1920 begründet worden. 1935 forschte er am Institut seines Freundes George Eliava in Tiflis (Georgien, damals Sowjetunion), um mit Phagen Wundinfektionen und Diarrhö zu therapieren. Trotz Penicillin und anderen Antibiotika gibt es noch heute rezeptfreie Phagenpräparate in russischen Apotheken.
Literatur
[1] Patrick Forterre. Manipulation of cellular syntheses and the nature of viruses: The virocell concept. Comptes Rendus Chimie 2010, im Druck; doi:10.1016/j.crci.2010.06.007.
[2] Matthias Fischer et al. Giant virus with a remarkable complement of genes infects marine zooplankton. Proc Natl Acad Sci USA 2010; 107(45):19508 – 19513.
[3] Patrick Forterre. Defining Life: The Virus Viewpoint. Orig Life Evol Biosph 2010;40:151 – 160.
[4] Eugene V Koonin et al. The ancient virus world and evolution of cells. Biol Direct 2006;1:29.
[5] Mimivirus: discovery of a giant virus. Presseveröffentlichung des CNRS (Centre national de la recherche scientifique) in Paris am 28. März 2003; www.cnrs.fr/cw/en/pres/compress/mimivirus.htm.
[6] Jakob Pernthaler. Predation on prokaryotes in the water column and its ecological implications. Nat Rev Microbiol 2005;3:537 – 546; doi:10.1038/nrmicro1180.
[7] James L van Etten et al. DNA Viruses: The really big ones (Giruses). Annu Rev Microbiol 2010;64:83-99; doi: 10.1146/annurev.micro.112408.134338.
Autor
Dr. Uwe Schulte, Osterholzallee 82, 71636 Ludwigsburg, schulte.uwe@t-online.de
DAZ 2011, Nr. 1, S. 84





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.