
- DAZ.online
- DAZ / AZ
- DAZ 18/2010
- Symmetrische Alkaloide
Feuilleton
Symmetrische Alkaloide*
Als Hans Möhrle (Jahrgang 1930) in Freiburg und ich (Jahrgang 1929) in Mainz mit dem Studium der Pharmazie begannen (1951/52), war das Fach Pharmazeutische Chemie noch weitgehend identisch mit der Alkaloidchemie. Die Liste bedeutender Professoren, die sich in Forschung und Lehre überwiegend oder auch mit Alkaloiden befassten, können Sie hier ansehen.
Interessant erscheint, dass sich drei der Genannten gleichzeitig (Awe) oder später (Graf und List) der Pharmazeutischen Technologie zuwandten, die damals noch als Galenik bezeichnet wurde.
Der Begriff Alkaloide wurde im Jahr 1819 von einem Hallenser Apotheker namens Carl F. W. Meissner geprägt. Er wollte damit das "alkaliähnliche" Verhalten bestimmter Pflanzeninhaltsstoffe charakterisieren. 1806 entdeckte und isolierte Friedrich Wilhelm Sertürner das Morphin, 1819 gewann Friedlieb Ferdinand Runge das Coffein aus Kaffee. Die erste Synthese eines Alkaloids gelang 1886 Albert Ladenburg mit der Darstellung des Coniins.
Alkaloide sind sekundäre, basische Naturstoffe, die vorwiegend von Pflanzen gebildet werden und ein oder mehrere Stickstoffatome enthalten, meist in Form eines Heterozyklus. Bis heute wissen wir nicht, wozu sie eigentlich produziert werden. Die Argumente Fraßgifte oder Abwehrstoffe treffen nur gelegentlich zu. Alkaloide sind Nebenprodukte des Aminosäuren-Stoffwechsels. Sie bilden die Naturstoffklasse mit der höchsten Toxizität für Warmblütler.
Nach der Definition von Kurt Mothes besitzen sie "eine starke, meist sehr spezifische Wirkung auf verschiedene Bezirke des Nervensystems". Das dürfte auch der Grund sein, warum nur wenige Alkaloide aus dem Tierreich stammen. Alkaloide finden seit alters her therapeutische Verwendung und sind auch im aktuellen Arzneischatz präsent. Erinnert sei in diesem Zusammenhang an Morphin, Chinin, Cocain, Mutterkorn-Alkaloide, Curare-Alkaloide, Rauvolfia -Alkaloide, Vinca -Alkaloide.
Die meisten Alkaloide sind optisch aktiv, und ihre Stereochemie ist oft sehr kompliziert. Davon abgesehen kann ihre Struktur sehr komplex und schwer einzuordnen sein. Man denke beispielsweise an die Taxus -Alkaloide. Einfacher, besser zu überschauen und von ästhetisch reizvoller Struktur sind symmetrisch gebaute Alkaloide. Sie besitzen durchweg bestimmte pharmakologische und antibiotische Wirkungen, deren therapeutische Verwendung noch nicht ausgereizt ist.
Symmetrische Alkaloide mit einem N-Atom
Enthält ein Alkaloid nur ein Stickstoffatom, so muss dieses eine zentrale Position im Molekül einnehmen, damit es symmetrisch sein kann. Belege für diese Binsenweisheit sind als Prototypen: Lobelanin und Lobelanidin, Pseudopelletierin, Coccinellin und Pavin.
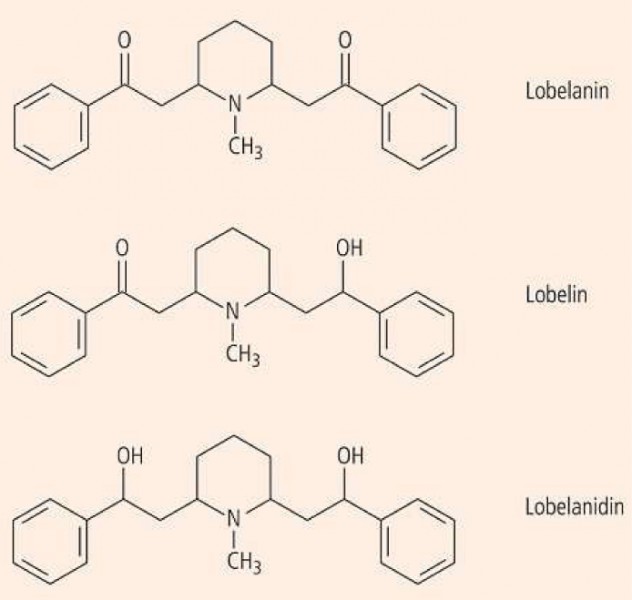
Lobelia-Alkaloide. Der "Indianer-Tabak", das "Asthmagras" oder das "Brechkraut", wie die Lobelia inflata , die früher als atemstimulierendes Analeptikum bei Asthma verabreicht wurde, im Volksmund genannt wird, enthält etwa zwanzig 2,6-disubstituierte Piperidin-Derivate als Alkaloide. Hauptalkaloid ist das nicht symmetrische Lobelin, das strukturell zwischen die beiden symmetrischen Nebenalkaloide Lobelanin und Lobelanidin einzuordnen ist (Abb. 1).
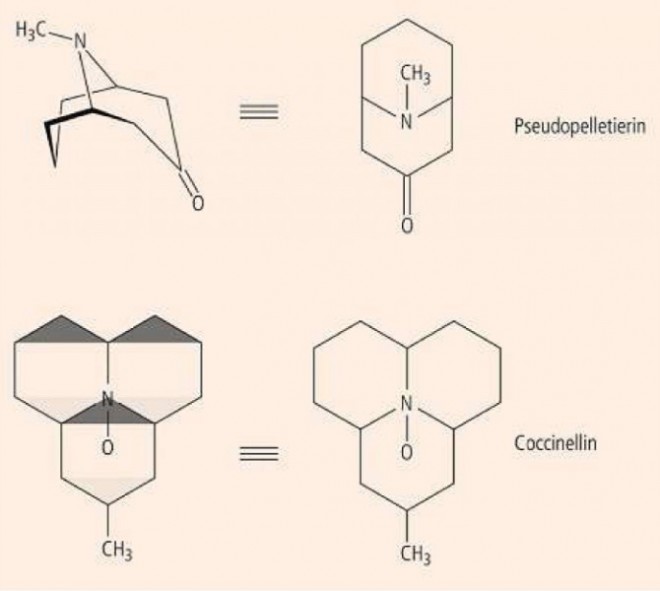
Bei Pseudopelletierin , dem Hauptalkaloid aus der Wurzelrinde des Granatapfelbaumes (Punica granatum), ist ein tertiärer Stickstoff symmetrisch von zwei chiralen CH-Funktionen flankiert, wovon die eine R -, die andere S -konfiguriert ist. Der starr fixierte Stickstoff wird dadurch pseudoasymmetrisch. Untersucht und bekannt ist die Biosynthese, die von der Aminosäure Lysin ausgeht, sowie die Totalsynthese, die auf einer klassischen Mannich-Kondensation beruht (Robinson-Synthese).
Coccinellin (Abb. 2). Die Marienkäfer (Coccinellidae) scheiden zu ihrer Verteidigung eine Reihe strukturell verwandter Alkaloide (Allomone) aus, die das gleiche trizyklische Grundgerüst aufweisen. Davon sind Coccinellin, Precoccinellin und Myrrhin bilateral-symmetrisch. Coccinellin ist das N-Oxid von Precoccinellin, in dem die Ringe A/B trans - und die Ringe A/C und B/C cis -verknüpft vorliegen. Dadurch ist das Molekül (bezogen auf die Grundflächen der Sesselformen) stark gewinkelt.
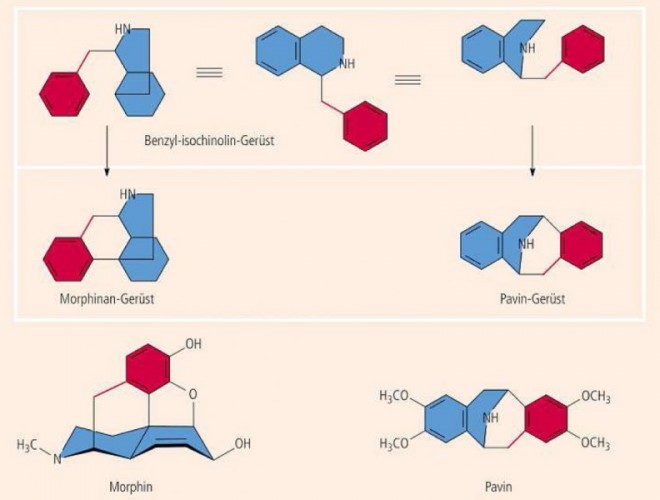
Pavin (Abb. 3). Die Alkaloide teilt man zweckmäßigerweise nach ihren Grundgerüsten ein. Eine der wichtigsten Gruppen ist die der Benzyl-isochinolin-Alkaloide. Zu ihr gehören die Opiumalkaloide wie Morphin, Codein, Thebain und Narcotin. Wer denkt dabei an molekulare Symmetrie? Niemand! Und doch scheint es für die Natur ein Kinderspiel zu sein, das benzylierte und teilhydrierte Isochinolin ebenso leicht zum hochsymmetrischen Pavin-Gerüst wie zum dreifach asymmetrischen Morphinan-Gerüst zu verknüpfen (Abb. 3).
Der überbrückte Heterozyklus steckt in den Alkaloiden Pavin, Argemonin und Eschscholtzin (= Californin) und Californidin. Sie bestechen graphisch durch ihre Drehachsen-Symmetrie, und das dürfte auch der Grund sein, dass man auf den ersten Blick nicht erkennt, welcher Alkaloid-Familie sie zuzuordnen sind.
Symmetrische Alkaloide mit zwei N-Atomen
Bei zwei N-Atomen im symmetrischen Alkaloid muss sich zwischen beiden eine spiegelsymmetrische Kette oder Brücke (Abb. 4) oder eine zentrosymmetrische Partialstruktur (Abb. 5) befinden.
Oft kann man den symmetrischen Alkaloiden ansehen, dass sie durch Dimerisierung oder Verknüpfung zweier identischer Partialstrukturen über ein symmetrisches Bindeglied entstanden sind.
In der ersten, bilateral-symmetrischen Gruppe sind die N-Atome in einen symmetrischen Ring oder in zwei gleichwertige Ringe eingebunden.
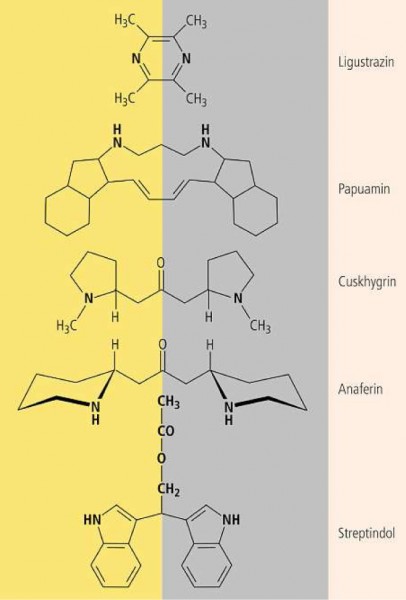
Prototypen sind Ligustrazin, Papuamin, Cuskhygrin, Anaferin und Streptindol
Ligustrazin (Abb. 4) ist nichts anderes als ein vierfach methyliertes Pyrazin, dem jeder chirale Schnörkel fehlt. Der antihypertensive und antithrombotische Inhaltsstoff von Ligusticum chuanxiong , einer chinesischen Heilpflanze aus der Familie der Apiaceae, inhibiert die Thrombozytenaggregation durch Verdrängung der Calcium-Ionen aus den Membranen.
Im Papuamin (Abb. 4) sind die beiden N-Atome im Abstand von drei C-Atomen in einen 13‑gliedrigen Ring eingebaut. Das antifungale Alkaloid aus dem Meeresschwamm Haliclona besitzt trotz seiner acht Asymmetriezentren eine Symmetrieachse. Es ist jedoch keine meso -Verbindung, sondern zeigt eine spezifische Drehung.
Bei Cuskhygrin (Cuscohygrin) und Anaferin (Abb. 4) bildet eine Carbonylgruppe die Molekülmitte, symmetrisch flankiert von zwei Aminogruppen, deren CH-Substituenten jeweils chiral sind. Cuskhygrin kommt in vielen Pflanzen vor, u. a. in Atropa bella-donna (Tollkirsche) und in Erythroxylum coca ( Coca-strauch). Anaferin ist Inhaltsstoff der Schlafbeere (oder Winterkirsche) Withania somnifera , Solanaceae.
Das genotoxische Streptindol (Abb. 4) wird von bestimmten Darmbakterien (Streptococcus faecium) produziert. Der Verdacht, dass hier ein Zusammenhang mit der Entstehung von Dickdarmkrebs besteht, konnte bisher nicht bestätigt werden. Wie Ligustrazin weist Streptindol keine Asymmetriezentren auf.
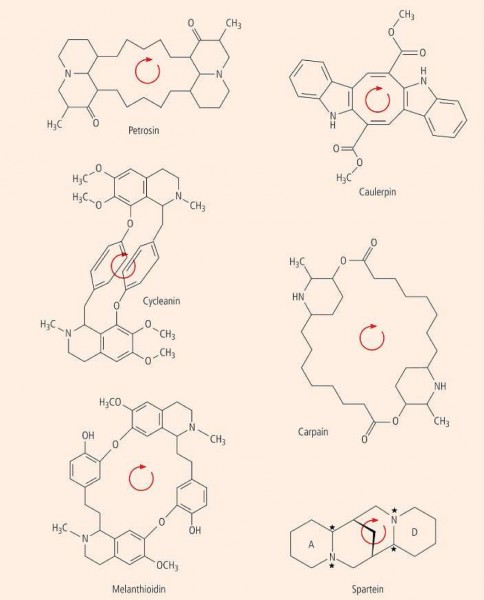
In der zweiten Gruppe der symmetrischen Alkaloide mit zwei N-Atomen sind diese in einen zentrosymmetrischen Ring integriert. Prototypen sind Petrosin, Caulerpin, Cycleanin, Carpain, Melanthioidin und Spartein.
Das für Fische giftige Petrosin (Abb. 5) ist ein dimeres Chinolizidin-Alkaloid und wird vom Schwamm Petrosia seriata produziert.
Im Caulerpin (Abb. 5) sind zwei Indole in ein Cyclo-octatetraen-System integriert. Auch hier fehlt jede molekulare Asymmetrie oder Chiralität. Die beiden Indolsysteme sind zwar eben, doch der Cyclo-octatetraen-Ring ist gewinkelt. Nach der Röntgenstrukturanalyse liegt im Caulerpin eine Wannenform vor.
Obwohl sich in diesem Ringsystem Einfach- und Doppelbindungen abwechseln, also ein in sich geschlossener, konjugierter Ring vorliegt, haben wir es nicht mit einem ebenen, aromatischen System zu tun.
Caulerpin wurde aus der Grünalge Caulerpa racemosa isoliert. Algen der Gattung Caulerpa sind aus zwei weiteren Gründen bemerkenswert. Im pazifischen Raum sind sie als salatartiges Nahrungsmittel sehr beliebt, im Mittelmeer überwuchern sie allmählich die einheimische Algenflora, nachdem der Fremdling aus einem Aquarium in Monaco entsprungen ist.
Cycleanin (Abb. 5) gehört zur Familie der Bis-coclaurin-Alkaloide. Diese enthalten zwei Benzyl-isochinolin-Kerne, die durch eine, zwei oder drei Etherbrücken bzw. C– C-Brücken miteinander verknüpft sind, und kommen in verschiedenen Pflanzenfamilien vor, u. a. in Berberidaceen, Magnoliaceen, Lauraceen, Menispermaceen, Nymphaeaceen und Ranunculaceen.
Betrachtet man die Dimerisierung rein statistisch, so darf man unter den zahlreichen möglichen Bis-coclaurin-Alkaloiden auch einen symmetrisch gebauten Typ erwarten. Diesen gibt es in der Tat, es ist der Iso-chondodendrin-Typ. Einer seiner Vertreter ist das Cycleanin.
Carpain (Abb. 5), ein Alkaloid aus den Blättern des Papayabaumes (Carica papaya), ist ein aus zwei gleichartigen und gleichartig konfigurierten Einheiten (Hydroxyaminosäuren) gebildetes, zyklisches Dilacton. Es verursacht Bradykardie und stellt ein wirksames Amoebizid dar. In den Papayafrüchten ist es nicht enthalten.
Melanthioidin (Abb. 5) ist ein mit dem Cycleanin vergleichbares zentrosymmetrisches Bisphenyl-ethyl-tetrahydro-isochinolin-Alkaloid. Es wurde aus Androcymbium melanthioides (Colchicaceae, früher Liliaceae) isoliert.
Spartein • Stereochemisch komplizierter ist das überbrückte Ringsystem des Sparteins und seiner Isomeren. Im Spartein befindet sich an zentraler Stelle eine CH2 -Gruppe, die einen symmetrischen Heterozyklus überbrückt, der vier chirale C-Atome enthält. Das native linksdrehende L-Spartein ist insgesamt nicht zentrosymmetrisch gebaut. Dieses Chinolizidin-Alkaloid, das in Lupinen, Besenginster (Cytisus scoparius) und anderen Schmetterlingsblütlern vorkommt, wurde als Antiarrhythmikum therapeutisch eingesetzt. Das Enantiomer von Spartein wird als Pachycarpin bezeichnet, ist hochtoxisch und kommt ebenfalls in verschiedenen Leguminosen vor. Symmetrische Epimere von Spartein sind Genistein, (α-Isospartein) und β‑Isospartein. Die Verknüpfung mit den äußeren Ringen A und D ist im Genistein cis-cis , im β‑Isospartein trans-trans und im Spartein cis-trans .
Symmetrische Alkaloide mit drei N-Atomen
Ein theoretisch leicht vorstellbares symmetrisches Alkaloid mit drei N-Atomen, von denen eines an zentraler Stelle und die zwei anderen in gleichem und gleichartigem Abstand angeordnet sein müssten, ist mir leider bis heute nicht begegnet.
Symmetrische Alkaloide mit vier N-Atomen
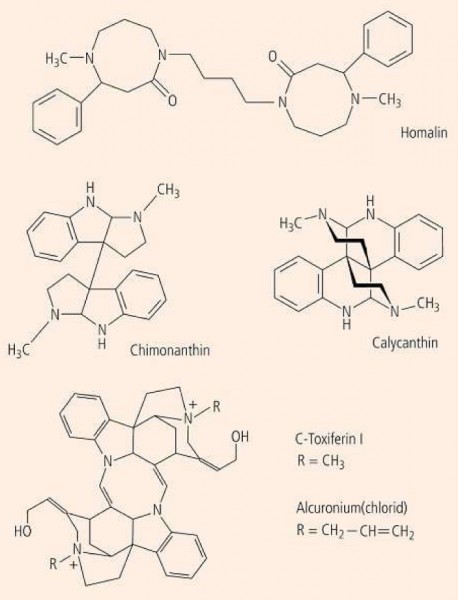
Enthält ein symmetrische Alkaloid vier N-Atome, so handelt es sich in der Regel um die Verknüpfung zweier gleichartiger Partialstrukturen mit jeweils zwei Stickstoff-Atomen. Prototypen sind Homalin, Chimonanthin, Calycanthin und C-Toxiferin I.
Homalin (Abb. 6), das zu den Polyamin-Alkaloiden zählt, enthält zwar vier N-Atome, aber pro Modul nur ein Asymmetriezentrum, das jeweils gleichartig konfiguriert ist. Als biogenetisches Edukt ist im Homalin und verwandten Alkaloiden das Spermin zu erkennen (H2 N-(CH2)3 -NH-(CH2)4 -NH-(CH2)3 -NH2). Das strukturell einfache Alkaloid wurde aus den Blättern einiger Homalium -Arten isoliert, die zur Familie der Flacourtiaceae gehören.
Chimonanthin ist ein zentrosymmetrisches Alkaloid, in welchem zweimal das Skelett des Physostigmins steckt. Es wurde aus den Blättern von Chimonanthus fragans, Ch. praecox und aus Calycanthus floridus isoliert.
Neben dem dimeren Pyrroloindol-Alkaloid Chimonanthin existieren auch trimere bis octamere Formen, darunter solche, die für Leukämiezellen toxisch sind, und andere, die spezifisch an Somatostatin-Rezeptoren binden und die Freisetzung von Hypophysenhormonen beeinflussen.
Calycanthin wurde aus Calycanthus floridus (Weinröschen, ein wohlriechender, nach Erdbeeren duftender Gewürzstrauch) isoliert und kommt auch im Hautsekret südamerikanischer Pfeilgift-Frösche vor. Die Rinde des Gewürzstrauchs wird von den Chirokee-Indianern bei Nierenerkrankungen verwendet. Chimonanthin und Calycanthin sind isomer.
C-Toxiferin I ist das Hauptalkaloid des Kalebassen-Curare, das zwei Gruppen von Alkaloiden enthält, nämlich
- mit zwei N-Atomen und etwa 20 C-Atomen und
- mit vier N-Atomen und etwa 40 C-Atomen.
Daraus kann man ableiten, dass die zweite Gruppe Dimere der ersten Gruppe darstellt. C-Toxiferin I und Verwandte (Abb. 6) sind Kondensationsprodukte des Wieland-Gumlich-Aldehyds, der durch partiellen oxidativen Abbau von Strychnin entsteht und auch als Naturstoff vorkommt. Sie weisen Spielkarten-Symmetrie auf. Cum grano salis kann man im C-Toxiferin I ein doppeltes Strychnin erkennen.
Therapeutische Verwendung als Muskelrelaxans bei großen Operationen findet heute das halbsynthetische Alcuroniumchlorid.
Zum Schluss sei bemerkt, dass dieses Essay keinen Anspruch auf Vollständigkeit erhebt und dass es auch verschiedene Alkaloide gibt (Hyoscyamin, Scopolamin, Chinin, Chinidin, Ajmalin, Ibogamin, α-Truxillin, Santiaguin u. a.), die symmetrische Teilstrukturen enthalten.
Weiterführende Literatur Anaferin: Flora of China, Band 17, 1994, S. 313. Calycanthin: Phytochemistry 31, 317 (1992); Tetrahedron 23, 4131 (1967). Carpain: Tetrahedron Lett 1965, 1907; J Chem Soc (B) 1966, 539. Caulerpin: Phytochemistry 26, 619 (1987), 30, 304 (1991). Chimonanthin: Proc Chem Soc1961, 465; Tetrahedron 18, 1495 (1963); J Am Chem Soc 116, 9480 (1994). Coccinellin: Tetrahedron 49, 9333 (1993). C-Toxiferin I: E. Teuscher und U. Lindequist, Biogene Gifte, Gustav Fischer Verlag, Stuttgart 1993, S. 418 f.; J Org Chem 48, 1869 (1983). Cuskhygrin: J Am Chem Soc 104, 1403 (1982). Cycleanin: H. Boit, Ergebnisse der Alkaloid-Chemie bis 1960, Akademie-Verlag, Berlin 1961, S. 232 ff. Homalin: Tetrahedron Lett 27, 5147 (1986). Ligustrazin: Acta Pharm Sin 20, 334, 689 (1985); Med Chem Res 2, 434 (1992). Lobelia-Alkaloide: Sci Pharm 48, 365 (1980); Merck-Index 12, Nr 5577–5580. Melanthioidin: E. Breitmaier, Alkaloide, Vieweg und Teubner, 2008, S. 66; J Chem Soc Chem Commun 1992, 974. Papuamin: J Am Chem Soc 110, 965 (1988); 116, 9789 (1994). Pavin-Alkaloide: J Chem Soc 97, 1324 (1910) 1955, 2888. Petrosin: Tetrahedron Lett 23, 4277 (1982); 30, 4149 (1989). Pseudopelletierin: J Org Chem 42, 629 (977); Tetrahedron 38, 1959 (1982). Spartein: Pharm Unserer Zeit 15, 172 (1986). Streptindol: Tetrahedron 44, 5897 (1988).
AutorProf. Dr. rer. nat. Dr. h. c. Hermann J. Roth Friedrich-NaumannStr. 33, 76187 Karlsruhe |





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.