
- DAZ.online
- DAZ / AZ
- DAZ 26/2009
- Wege aus der Depression
Pharmakogenetik in der Praxis
Wege aus der Depression
Für den Phase-I-Metabolismus von Arzneistoffen stehen der Leber hauptsächlich die Cytochrom-P450-Enzyme zur Verfügung. Den Hauptteil der Arbeit übernimmt hierbei das Isoenzym 3A4 (CYP3A4). Ungefähr 25% der Abbauleistung werden durch das Isoenzym 2D6 (CYP2D6) bewerkstelligt, obwohl es mengenmäßig mit ungefähr 2% nur einen sehr geringen Anteil am Gesamtgehalt der Leber hat [1]. Wie in DAZ 18/2009 beschrieben, sind die über dieses Isoenzym verstoffwechselten Arzneistoffe äußerst vielfältig und reichen von Betablockern über Östrogen-Rezeptorantagonisten bis hin zu den im Folgenden näher beleuchteten Antidepressiva.
In DAZ 18/2009 wurden die Folgen eines Gendefektes, der zur Funktionslosigkeit der gebildeten CYP2D6-Enzyme führte, thematisiert. Die betroffenen Patientinnen – sogenannte langsame Metabolisierer (PM, Poor Metabolizer) – konnten verabreichte Schmerzmittel, die als Prodrugs vorlagen, nicht in den wirksamen Metaboliten überführen und somit nicht von einer analgetischen Wirkung des Arzneistoffs profitieren.
In diesem Artikel soll nun die übermäßig starke CYP2D6-Enzymaktivität von Personen, die nicht nur zwei sondern mehrere funktionelle Gene besitzen, sogenannte ultraschnelle Metabolisierer (URM, Ultra Rapid Metabolizer), an einem Fallbeispiel dargestellt werden. Ultraschnelle Metabolisierer verstoffwechseln Enzymsubstrate überdurchschnittlich schnell und haben dadurch genau die umgekehrten Probleme eines langsamen Metabolisierers. Der aktive Wirkstoff wird von ihnen so schnell abgebaut, dass meist keine ausreichenden Wirkspiegel resultieren.
Der authentische Patientenfall ist zum besseren Verständnis in eine mögliche Arzt-Apotheker-Patienten-Situation gebracht worden [2].
Die verzweifelte Frau FischerFrau Fischer betritt die Apotheke und überreicht dem Apotheker ein Rezept über das trizyklische Antidepressivum Mianserin. Der Apotheker schließt aus der Packungsgröße, dass das Medikament zur Dauertherapie der Kundin gehört. Im Gespräch mit Frau Fischer erfährt er, dass sie das Präparat schon seit einiger Zeit gegen ihre Depression bekomme, ohne dass es ihr helfen würde. Der Arzt wolle noch einmal die nächsten zwei Wochen abwarten und dann eventuell die Therapie ändern. Der Apotheker bestärkt die Kundin durchzuhalten und erklärt ihr, dass das Medikament über längere Zeit kontinuierlich eingenommen werden muss, um seine Wirkung zu entfalten. Nach ungefähr zehn Tagen kommt Frau Fischer erneut in die Apotheke. Diesmal legt sie eine Verordnung über Paroxetin-Tabletten vor. Sie erklärt, dass sie den Arzt gewechselt habe, weil keinerlei Therapiefortschritte zu sehen waren. Der neue Arzt habe nun dieses Medikament gegen ihre Depression verschrieben und sie hoffe, dass es jetzt endlich wieder bergauf mit ihr gehe. Der Apotheker spricht der Frau Mut zu und weist sie noch einmal auf die Wichtigkeit der regelmäßigen Einnahme hin. Nach einiger Zeit kommt Frau Fischer wieder in die Apotheke. Sie macht immer noch keinen besseren Eindruck und auch die Antworten, die sie auf die Frage des Therapiefortschrittes gibt, lassen auf einen weiterhin ausbleibenden antidepressiven Effekt schließen. Sie legt ein Rezept vor, auf dem wider Erwarten Mianserin verordnet ist, diesmal wieder von Frau Fischers ursprünglichem Arzt. Auf die Frage, ob Frau Fischer zu ihrem ursprünglichen Arzt zurückgekehrt sei, gibt sie an, bei zwei Ärzten in Behandlung zu sein, weil sie so hoffe, schneller wieder gesund zu werden. Da die Kundin einen sehr angespannten Eindruck macht, bittet der Apotheker Frau Fischer in das Beratungszimmer, um in Ruhe mit ihr reden zu können. Er erklärt ihr, dass es für ihre Therapie und vor allem für ihre Gesundheit nicht von Vorteil ist, wenn sie unterschiedliche Medikamente von verschiedenen Ärzten erhält, die nichts voneinander wissen. So könne ihre Therapie nicht richtig eingestellt werden, da Medikamente sich auch untereinander beeinflussen können. Schlimmstenfalls wären sogar schwere Nebenwirkungen möglich. Frau Fischer beginnt zu weinen und sagt, sie wisse einfach nicht mehr, was sie jetzt tun solle. Der Apotheker beruhigt sie und verspricht, mit den beiden Ärzten zu telefonieren und mit ihnen über die weitere Therapie zu sprechen. Das Telefonat mit den Ärzten verläuft erfolgreich. Die Ärzte sind froh, dass in der Apotheke das Problem erkannt wurde, dennoch wundern sich alle ob des weiterhin ausbleibenden Effekts der Therapie, denn die Medikamente hätten sich in ihrer Wirkung eigentlich sogar verstärken müssen. Da allerdings weder erwünschte noch unerwünschte Wirkungen aufgetreten waren, verständigt man sich darauf, die Therapie mit Paroxetin und Mianserin unter engmaschiger Überwachung und Bestimmung der Plasmaspiegel weiterzuführen. Der Apotheker telefoniert im Anschluss mit Frau Fischer und setzt sie über das Ergebnis des Gesprächs in Kenntnis. Sie ist froh, dass das Problem aus der Welt geschafft wurde und teilt dem Apotheker mit, dass sie von nun an nur noch ihren langjährigen Arzt aufsuchen wird. Für einige Zeit hört der Apotheker nichts von Frau Fischer, bis sie eines Tages wieder in der Apotheke steht. Sie macht einen sehr abgeschlagenen und zerfahrenen Eindruck. Sie ist verzweifelt. Es hätte alles keinen Sinn. Auch die neue Therapie mit beiden Arzneistoffen habe noch zu keinem Erfolg geführt. Trotz Erhöhung der Dosis von 20 mg auf 30 mg Paroxetin pro Tag sei der Serumspiegel des Arzneistoffs viel zu gering. Auch die Serumspiegel von Mianserin seien viel zu niedrig gewesen. Sie beteuert aber, dass sie wirklich regelmäßig ihre Arzneimittel nach der Anweisung des Arztes einnehmen würde. Der Apotheker verspricht Frau Fischer nachzuforschen und sich noch einmal mit ihrem Arzt in Verbindung zu setzen, um mögliche Alternativen zur Therapie zu besprechen. Dem Apotheker ist bekannt, dass fehlendes Therapieansprechen oder verstärktes Auftreten von Nebenwirkungen bei Patienten mit genetischen Besonderheiten in der Arzneistoffmetabolisierung auftreten kann und vermutet daher ein derartiges Problem. Diese Hypothese bespricht er mit Frau Fischers Arzt. Der Arzt hat davon zwar schon gehört, dass pharmakogenetische Besonderheiten auch zu Therapieversagen führen können, kann sich aber nicht wirklich vorstellen, dass dieses Phänomen so häufig ist und in diesem Fall eine Bedeutung hat. Er entschließt sich aber trotzdem, eine genetische Untersuchung von Frau Fischer zu veranlassen. Der Apotheker informiert Frau Fischer über das Gespräch und Frau Fischer lässt bei ihrem Arzt die genetische Untersuchung durchführen. Das Ergebnis überrascht den Arzt und bestätigt die Vermutung des Apothekers. Der Arzt bittet den Apotheker, ihm die Unterlagen, die er bei seiner Literaturrecherche zusammengetragen hat, zukommen zu lassen. Der Apotheker verspricht, ihm einen ausführlichen Bericht zuzusenden. Auf die Frage des Arztes, ob der Apotheker bei der Recherche auch Informationen über mögliche Alternativen für eine medikamentöse Therapie von Frau Fischer gefunden hätte, nennt ihm der Apotheker mögliche Arzneistoffe. Der Arzt notiert sich die Medikamente und verspricht, sich nach dem Studium der Unterlagen umgehend mit Frau Fischer in Verbindung zu setzen. Zwei Tage später erscheint Frau Fischer mit einem neuen Rezept in der Apotheke. Der Arzt hat ihr den Serotonin-Wiederaufnahmehemmer Sertralin verschrieben. Sie ist nun wieder zuversichtlich und bedankt sich vielmals, da ihr Arzt über die guten und hilfreichen Informationen des Apothekers gesprochen hatte. Einige Wochen später legt Frau Fischer in der Apotheke ein Sertralin-Folgerezept vor. Sie spricht sehr gut auf die Behandlung an und kann auch wieder ihrem ganz normalen Tagesablauf nachgehen. |
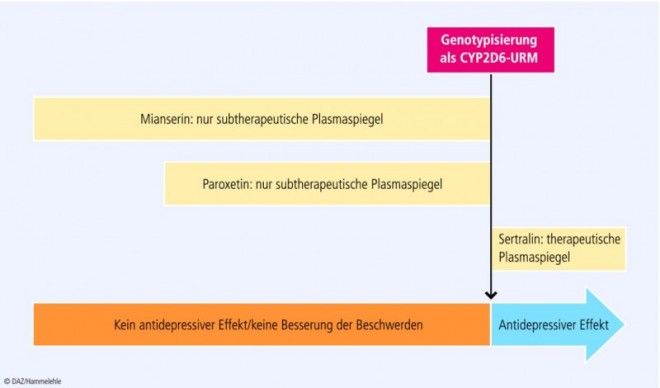
Im Folgenden soll im Rahmen eines Fragenkatalogs auf die verschiedenen Aspekte des Patientenfalls eingegangen werden. Der Therapieverlauf ist in Abbildung 1 noch einmal schematisch dargestellt.
Zu welchem Schluss kam der Apotheker nach seiner Literatur-Recherche?
Da Frau Fischer sowohl auf die Therapie mit dem trizyklischen Antidepressivum Mianserin als auch auf den selektiven Serotonin-Wiederaufnahmehemmer Paroxetin nicht ansprach, hat der Apotheker nach Gemeinsamkeiten der beiden Substanzen bezüglich pharmakokinetischer oder pharmakodynamischer Eigenschaften gesucht. Darüber hinaus hat er überprüft, ob bereits ähnliche Patientenfälle publiziert worden sind. Die Recherche in der frei zugänglichen Online-Datenbank Pubmed (www.pubmed.gov) sowie den Fachinformationen zu den Präparaten (www.fachinfo.de) und die Inanspruchnahme des medizinischen Informationsdienstes der Hersteller ergab, dass beide Arzneimittel über das Cytochrom-P450-Isoenzym 2D6 verstoffwechselt werden. Aus Fortbildungen wusste der Apotheker, dass dieses Enzym polymorph exprimiert wird und es langsame, normale und sehr schnelle Verstoffwechsler gibt. Insbesondere die sehr schnelle Metabolisierung kann zu einer erfolglosen Therapie führen.
Was zeigte der Genotypisierungsbefund von Frau Fischer?
Die Genotypisierung von Frau Fischer wurde mithilfe einer Blutprobe durchgeführt. Für die Bestimmung wird meist weniger als 1 ml Blut benötigt. Das Ergebnis zeigte, dass Frau Fischer Trägerin eines CYP2D6*2Xn-Allels war. Dadurch ist sie in die Gruppe der CYP2D6-URM (Ultra Rapid Metaboliser), der sehr schnellen Metabolisierer für Substrate des Enzyms, einzuordnen. Sie besitzt mehrere funktionsfähige Kopien des CYP2D6*2-Gens, welches eine normale Enzymfunktion aufweist. Ihre Zellen sind deshalb in der Lage, überproportional viele CYP2D6-Enzyme zu bilden, die für den unerwartet schnellen Abbau der Substrate verantwortlich sind [3]. In Europa sind etwa 2% der Bevölkerung Träger von Genduplikationen und Genmultiplikationen, die dem CYP2D6-URM-Typ zugeordnet werden [4].
Wieso waren die bisherigen Arzneimitteltherapien von Frau Fischer erfolglos?
Mianserin und Paroxetin werden über das CYP2D6-Enzym verstoffwechselt. Paroxetin besitzt außerdem eine inhibitorische Wirkung auf CYP2D6 [5, 6]. Das bedeutet, dass es als Hemmer der Metabolisierung von anderen Arzneistoffen wirkt, die ebenfalls über das CYP2D6-Enzym metabolisiert werden. Da Frau Fischer aufgrund ihres URM-Status Substrate für diese Enzyme aber sehr schnell abbaut, konnten weder Mianserin noch Paroxetin therapeutische Wirkspiegel aufbauen und Paroxetin auch keine Hemmwirkung auf den Mianserin-Abbau entfalten. Auch die Dosiserhöhung von 20 mg auf 30 mg Paroxetin konnte hier nicht zu einer Spiegelerhöhung beitragen.
Hätte eine weitere Dosiserhöhung von Mianserin und Paroxetin zum Erfolg führen können?
Weder Mianserin noch Paroxetin wurden hinsichtlich der Dosis bis zum Ende ausgereizt. Mit einer Dosierung von 10 mg Mianserin war der Arzneistoff sogar unterdosiert, da die Erhaltungsdosis bei 30 mg bis sogar 90 mg pro Tag liegt. Die Dosierung von Paroxetin wurde zwar von 20 mg auf 30 mg erhöht, sie hätte aber auch bis zu maximal 50 mg am Tag gesteigert werden können. Diese Angaben beziehen sich allerdings auf die Monotherapie mit nur einem der beiden Arzneistoffe [5, 7]. Ein schrittweises Steigern der Dosis bis zum Maximum hätte aufgrund der gesteigerten Abbauleistung des URM-Genotyps vermutlich trotzdem nicht oder erst zu einem sehr späten Zeitpunkt zum Erfolg geführt. Empfehlungen für eine Genotyp-basierte Dosierungsanpassung bei Antidepressiva sehen vor, bei CYP2D6-URM für Paroxetin und Mianserin ca. 140% der durchschnittlich verabreichten Arzneistoffmenge zu applizieren [8].
Welches Medikament hat der Arzt Frau Fischer am Ende verschrieben und warum?
Es gibt eine Vielzahl von Möglichkeiten zur medikamentösen Therapie von Frau Fischers Depression. Der limitierende Faktor ist allerdings das Ergebnis ihrer CYP2D6-Genotypisierung. Die Arzneistoffe, die sich der Apotheker während seiner Recherche notierte und die er dem Arzt als Therapiealternativen weitergab, hatten als Gemeinsamkeit den fehlenden bzw. geringen Einfluss von CYP2D6 auf den Abbau des Arzneistoffs. In Tabelle 1 sind die zehn meistverordneten Antidepressiva gemessen an den täglichen Tagesdosen des Jahres 2007 aufgelistet. Wie man der Tabelle entnehmen kann, ist CYP2D6 das Hauptmetabolisierungsenzym der angegebenen Antidepressiva. Die Bedeutung des CYP2D6-Polymorphismus für das Auftreten von unerwünschten Wirkungen bei Antidepressiva insbesondere bei den Langsammetabolisierern ist belegt [10, 11, 12]. Die abschließende Empfehlung des Apothekers beinhaltete neben den SSRI Sertralin und Citalopram auch den Noradrenalin-Wiederaufnahmehemmer Reboxetin. Da der Arzt die Therapie mit einem SSRI fortsetzen wollte, entschied er sich aufgrund seiner besseren Erfahrung mit Sertralin für diesen Arzneistoff. Sertralin wird hauptsächlich über CYP3A4 und nur in geringem Umfang über CYP2D6 metabolisiert [6, 9, 10]. Die Therapie führte mit einer Dosierung von 150 mg letztlich bei Frau Fischer zum gewünschten Therapieerfolg.
Steckbrief des CYP2D6 PolymorphismusDer Polymorphismus des Cytochrom-P-450 Isoenzyms 2D6 (CYP2D6) ist einer der am besten untersuchten genetischen Unterschiede der Arzneimittel metabolisierenden Enzyme. Das Enzym CYP2D6 ist das einzige funktionale Enzym aus der 2D-Familie. Es wird hauptsächlich in der Leber exprimiert, aber auch in anderen Geweben wie dem Magen-Darm-Trakt, den Nieren oder dem Gehirn. Obwohl es am Cytochrom-P-450 Gesamtgehalt der Leber nur einen Anteil von ungefähr 2% besitzt, werden etwa 25% aller Arzneistoffe von CYP2D6 im Rahmen des Phase-I-Metabolismus verstoffwechselt. Neben dem Wildtyp-Allel *1 sind mittlerweile mehr als 80 Allelvarianten bekannt, was den polymorphen Charakter dieses Enzyms unterstreicht [3, 18, 19]. Man kann CYP2D6-Träger hinsichtlich ihrer Enzymaktivität in vier verschiedene Klassen unterteilen. Diese unterscheiden sich aufgrund der Anzahl von funktionsfähigen Enzymen, die gebildet werden können, und der hiermit zusammenhängenden Stoffwechselleistung. Die Punktmutationen wie *3, *4, *6, *7, *8, *11 in der DNA-Sequenz führen zu einer Veränderung der Aminosäureabfolge des entstehenden CYP2D6-Enzyms und hierdurch zu einer Funktionslosigkeit. Der *5-Polymorphismus resultiert in einer Deletion, also einem Fehlen des kompletten Gens. Darüber hinaus gibt es auch Polymorphismen, die zu einer eingeschränkten Metabolisierungsfähigkeit des Enzyms führen (*9, *10, *17). Daneben gibt es genetische Veränderungen, die sich allerdings nicht auf die Enzymfunktion auszuwirken scheinen (*2, *33, *35) [3]. In Abhängigkeit der Kombination von Allelen mit diesen möglichen Mutationen teilt man die verschiedenen Genotypen ein.
Der CYP2D6-Status (PM, IM, EM, URM) hat also einen maßgeblichen Einfluss auf die Arzneistoffexposition und somit auch auf die Wirkung von Arzneistoffen. Mit zunehmender Enzymleistung nimmt die Arzneistoff-Exposition durch die Abbauvorgänge in der Leber ab. Im Falle eines Prodrugs ist die Situation umgekehrt: Hier können nur Personen mit funktionierenden Enzymen einen Wirkspiegel aufbauen, wie am klinischen Beispiel einiger Opiate in den Patientenfällen gezeigt, da hier der Metabolit und nicht die Muttersubstanz für die klinische Wirkung verantwortlich ist. Die Bestimmung des CYP2D6-Phänotyps kann über die Messung der Verstoffwechselung von sogenannten Testsubstanzen bestimmt werden. Dextromethorphan, Debrisoquin und Spartein sind solche Testsubstanzen. Hierzu wird der Urin nach Einnahme einer definierten Menge des Arzneistoffs gesammelt und dort das Verhältnis von Muttersubstanz zu Metabolit, der über CYP2D6 gebildet wird, gemessen. Das Verhältnis der beiden Werte spiegelt die Stoffwechselleistung des Enzyms wieder und korreliert mit den jeweiligen Genotypen [6, 17, 26]. |
Hätte vor Beginn der antidepressiven Therapie von Frau Fischer eine Genotypisierung durchgeführt werden müssen?
Eine prädiktive Genotypisierung vor Beginn einer antidepressiven Therapie wird in Deutschland bisher nicht routinemäßig durchgeführt und auch nicht von der gesetzlichen Krankenkasse erstattet. Eine CYP2D6-Genotypisierung könnte die Kosten einer Arzneimitteltherapie von Psychopharmaka allerdings senken. In einer Studie wurden 100 Patienten einer psychiatrischen Klinik für CYP2D6-Allele genotypisiert und ein Jahr lang begleitet. Dabei wurden die Medikation, die Anzahl an unerwünschten Arzneimittelwirkungen, die Anzahl der Krankenhaustage und die Gesamtkosten erfasst und in Verbindung zum jeweiligen Genotyp gebracht. Die Ergebnisse zeigten, dass die Therapiekosten für Patienten mit genetischen Besonderheiten (PM, URM) im Durchschnitt 4000 bis 6000 $ über den Kosten für EM (Extensive Metabolizer), also für normale Metabolisierer, lagen. Verantwortlich waren vermehrt unerwünschte Wirkungen und längere Krankenhausaufenthalte [13].
Eine prädiktive Genotypisierung von Frau Fischer hätte einer erfolglosen Therapie vorbeugen können und hätte vielleicht auch noch Kosten eingespart. Ein Problem stellt zurzeit allerdings noch die korrekte Detektion der ultraschnellen Metabolisierer durch den Genotyp dar. Nur ca. 30% von ihnen können durch eine Genotypbestimmung aufgespürt werden. Eine höhere Detektionsquote könnte durch eine Phänotypisierung mit einer geeigneten Testsubstanz erzielt werden [4, 14]. Im Gegensatz dazu können bei den langsamen Metabolisierern (PM) vom Typ CYP2D6 nahezu alle Patienten auch bei einer alleinigen Genotypisierung zweifelsfrei identifiziert werden [15, 16]. Als Ursache dieser Diskrepanz bei den sehr schnellen Metabolisierern werden u. a. noch nicht identifizierte Mutationen, die auch zu einer verstärkten Enzymaktivität führen, vermutet [17].
Wäre eine solche prädiktive Genotypbestimmung negativ, würde allerdings eine Bestimmung der Blutplasmaspiegel bei therapieauffälligen Patienten einen weiteren sicheren Anhaltspunkt dafür liefern, dass evtl. doch ein ultraschneller Metabolisierungstyp vorliegt. Dieses Ergebnis könnte dann durch eine Phänotypisierung gefestigt werden.
Welche Bedeutung hat dieser Fall für den Apothekenalltag?
Der vorgestellte Fall zeigt, wie wichtig es ist, dass sich der Apotheker für seine Patienten interessiert und auch das Gespräch mit seinen Patienten sucht. Darüber hinaus darf er sich nicht scheuen, mit dem Arzt Kontakt aufzunehmen. Wenn er merkt, dass ein Patient Arzneimittel-bezogene Probleme hat und Rat sowie Tat der ärztlichen Kollegen zu keiner befriedigenden Lösung führen, sollte er mit seinem Fachwissen zur Seite stehen. Denn seine Aufgabe besteht auch darin, die Kommunikation über Arzneimittel zwischen Patient und Arzt zu verbessern und so zu einer effektiven und sicheren Arzneimitteltherapie beizutragen.
Voraussetzung ist natürlich, dass der Apotheker kontinuierlich mit seinem Wissen auf dem Laufenden bleibt und dass er in der Praxis die Anwendung seines Wissens trainiert. Jeder Apotheker kann sich dabei gewiss sein: Sein Patient vertraut ihm als Arzneimittelfachmann! Ein Vertrauen, dass nicht enttäuscht werden sollte.
Literatur
[1] Bertz RJ et al.: Use of in vitro and in vivo data to estimate the likelihood of metabolic pharmacokinetic interactions. Clin Pharmacokinet 1997; 32:210 – 58
[2] Güzey C, Spigset O: Low serum concentrations of paroxetine in CYP2D6 ultrarapid metabolizers. J Clin Psychopharmacol 2006; 26:211–2
[3] Human Cytochrome P450 (CYP) Allele Nomenclature Committee http://www.cypalleles.ki.se/ 09/06/2009
[4] Johansson I et al.: Inherited amplification of an active gene in the cytochrome P450 CYP2D locus as a cause of ultrarapid metabolism of debrisoquine. Proc Natl Acad Sci U S A 1993; 90: 11825 – 9
[5] Fachinformation Seroxat® 20 mg Filmtabletten. Stand November 2008
[6] Kirchheiner J et al.: CYP2D6 and CYP2C19 genotype-based dose recommendations for antidepressants: a first step towards subpopulation-specific dosages. Acta psychiatrica Scandinavica 2001; 104:173
[7] Fachinformation Tolvin® Filmtabletten. Stand Juni 2008
[8] Kirchheiner J, Seeringer A: Clinical implications of pharmacogenetics of cytochrome P450 drug metabolizing enzymes. Biochim Biophys Acta 2007; 1170:489 – 94
[9] Rocchetti M et al.: Genetic polymorphism and reboxetine metabolism. Therapie 1995; 50:80
[10] Hamelin BA et al.: The disposition of fluoxetine but not sertraline is altered in poor metabolizers of debrisoquin. Clin Pharmacol Ther 1996; 60:512 – 21
[11] de Leon J et al.: The CYP2D6 poor metabolizer phenotype may be associated with risperidone adverse drug reactions and discontinuation. J Clin Psychiatry 2005; 66:15 – 27
[12] Rau T: Cyp2d6 Genotype: Impact on Adverse Effects and Nonresponse During Treatment with Antidepressants – a Pilot Study&ast. Clinical pharmacology and therapeutics 2004; 75:386
[13] Chou W et al.: Extension of a Pilot Study: Impact From the Cytochrome P450 2D6 Polymorphism on Outcome and Costs Associated With Severe Mental Illness. Journal of clinical psychopharmacology 2000; 20:246
[14] Panserat S. DNA haplotype-dependent differences in the amino acid sequence of debrisoquine 4-hydroxylase (CYP2D6): evidence for two major allozymes in extensive metabolisers. Human Genetics 1994; 94:401
[15] Sachse C et al.: Cytochrome P450 2D6 variants in a Caucasian population: allele frequencies and phenotypic consequences. American Journal of Human Genetics 1997; 60:284
[16] de Leon J: AmpliChip CYP450 test: personalized medicine has arrived in psychiatry. Expert Rev Mol Diagn 2006; 6:277 – 86
[17] Bertilsson L: Molecular genetics of CYP2D6: clinical relevance with focus on psychotropic drugs. Br J Clin Pharmacol. 2002;53:111 – 22
[18] Evans WE, Relling MV. Pharmacogenomics: translating functional genomics into rational therapeutics. Science 1999;286:487 – 91
[19] DeVane CL, Markowitz JS. Psychoactive drug interactions with pharmacotherapy for diabetes. Psychopharmacol Bull 2002;36: 40 – 52.
[20] Meyer UA et al.: Pharmacogenetics and adverse drug reactions. Lancet 2000;356:1667 – 71.
[21] Broly F et al: Debrisoquine/sparteine hydroxylation genotype and phenotype: analysis of common mutations and alleles of CYP2D6 in a European population. DNA Cell Biol 1991;10:545 – 58
[22] Gaedigk A et al.: Deletion of the entire cytochrome P450 CYP2D6 gene as a cause of impaired drug metabolism in poor metabolizers of the debrisoquine/sparteine polymorphism. Am J Hum Genet 1991;48:943 – 50
[23] Dickinson GL et al.: Incorporating in vitro information on drug metabolism into clinical trial simulations to assess the effect of CYP2D6 polymorphism on pharmacokinetics and pharmacodynamics: dextromethorphan as a model application. J Clin Pharmacol 2007;47:175 – 86
[24] Løvlie R et al.: Polymorphisms in CYP2D6 duplication-negative individuals with the ultrarapid metabolizer phenotype: a role for the CYP2D6*35 allele in ultrarapid metabolism? Pharmacogenetics 2001;11:45 – 55
[25] de Leon J: The crucial role of the therapeutic window in understanding the clinical relevance of the poor versus the ultrarapid metabolizer phenotypes in subjects taking drugs metabolized by CYP2D6 or CYP2C19. Clin Psychopharmacol 2007;27:241 – 5
[26] McElroy S et al.: CYP2D6 genotyping as an alternative to phenotyping for determination of metabolic status in a clinical trial setting. AAPS PharmSci 2000;2:E33
[27] Kirchheiner J et al.: Pharmacogenetics of antidepressants and antipsychotics: the contribution of allelic variations to the phenotype of drug response. Mol Psychiatry. 2004; 9:442 – 73
[28] Zanger UM et al.: Cytochrome P450 2D6: overview and update on pharmacology, genetics, biochemistry. Naunyn Schmiedebergs Arch Pharmacol 2004; 369:23 – 37
Autoren
Daniel Schmidt, Prof. Dr. Stephanie Läer
Korrespondenz
Prof. Dr. Stephanie Läer
Institut für Klinische Pharmazie und Pharmakotherapie
Heinrich-Heine-Universität Düsseldorf
Universitätsstraße 1
40225 Düsseldorf
GlossarAllel Allele sind die unterschiedlichen Varianten eines Gens an einer bestimmten Stelle (Genort). Jeder Mensch hat immer zwei Allele, nämlich eines von der Mutter und eines vom Vater. AUC Area Under the Curve. Fläche unter der Konzentrations-Zeitkurve als Maß für die Arzneistoffexposition. Deletion Deletion beschreibt den Verlust von genetischem Material. Hierbei können beliebig viele DNA-Bausteine fehlen, von einer einzelnen Base (Punktmutation) bis hin zum gesamten Chromosom. Genotyp Er stellt das Erbbild eines Organismus dar, also seine exakte genetische Ausstattung, die jeder Zellkern in sich trägt. Heterozygot Bedeutet generell mischerbig. Hier: Die beiden vorhandenen Allele unterscheiden sich. Homozygot Bedeutet reinerbig. Hier: Sowohl das mütterliche wie auch das väterliche Allel sind identisch. Mutation Veränderung des Erbgutes eines Organismus durch Veränderung der Abfolge der DNA-Basen. Phänotyp Wird auch als Erscheinungsbild bezeichnet und stellt die Summe aller Merkmale eines Individuums dar. Zwar sind die äußeren Merkmale eines Organismus durch seine genetischen Informationen festgelegt (Genotyp), der Phänotyp ist jedoch davon abhängig, welche Gene tatsächlich ausgeprägt werden. So liegen z. B. beim Menschen viele Gene in zwei Varianten vor, eine vom Vater, die andere von der Mutter (Allele). Nur das dominante Gen wird umgesetzt. Polymorphismus Variation in der DNA-Sequenz mit einer Häufigkeit in der Bevölkerung von über 1%. Punktmutation Veränderung in der DNA-Sequenz, von der nur eine Base betroffen ist. Einzelne Mutationen werden mit einem (*) markiert und durchnummeriert. Wildtyp Erscheinungsform (hier die eines Gens), die in der freien Natur am häufigsten anzutreffen ist. Abweichungen hiervon werden als Mutation bezeichnet. |
| Tab. 1: Abbauweg der Antidepressiva mit den meisten verschriebenen täglichen Tagesdosen (DDD) [8, 27, 28; DDD-Angaben: Arzneiverordnungsreport 2008] | |||||
| Wirkstoff | DDD*1 | Wirkstoffklasse*2 | Abbauweg | Prodrug | Folgen für URM |
| Citalopram | 169,5 | SSRI | CYP2C19; Beteiligung von CYP3A4,CYP2D6 möglich | Nein | Der CYP2D6-Genotyp hat nur einen sehr geringen Einfluss auf die Verstoffwechselung des Arzneistoffs |
| Mirtazapin | 91,5 | tetrazyklisches Antidepressivum | CYP2D6 | Nein | Verstärkter Abbau des Arzneistoffs, sehr geringe Plasmaspiegel, verminderte Wirkung |
| Amitriptylin | 91,2 | trizyklisches Antidepressivum | CYP2D6 | Nein | Verstärkter Abbau des Arzneistoffs, sehr geringe Plasmaspiegel, verminderte Wirkung |
| Opipramol | 62,8 | trizyklisches Antidepressivum | CYP2D6 | Nein | Verstärkter Abbau des Arzneistoffs, sehr geringe Plasmaspiegel, verminderte Wirkung |
| Venlafaxin | 61,6 | SNRI | CYP2D6 | Nein | Verstärkter Abbau des Arzneistoffs, sehr geringe Plasmaspiegel, verminderte Wirkung |
| Doxepin | 55,4 | trizyklisches Antidepressivum | CYP2D6 | Nein | Verstärkter Abbau des Arzneistoffs, sehr geringe Plasmaspiegel, verminderte Wirkung |
| Fluoxetin | 41,2 | SSRI | CYP2D6 | Nein | Verstärkter Abbau des Arzneistoffs, sehr geringe Plasmaspiegel, verminderte Wirkung |
| Sertralin | 39,2 | SSRI | CYP3A4; geringe Beteiligung CYP2D6 | Nein | Der CYP2D6-Genotyp hat nur einen sehr geringen Einfluss auf die Verstoffwechselung des Arzneistoffs |
| Paroxetin | 32,3 | SSRI | CYP2D6 | Nein | Verstärkter Abbau des Arzneistoffs, sehr geringe Plasmaspiegel, verminderte Wirkung |
| Trimipramin | 30,3 | trizyklisches Antidepressivum | CYP2D6 | Nein | Verstärkter Abbau des Arzneistoffs, sehr geringe Plasmaspiegel, verminderte Wirkung |
*1 DDD = Defined Daily Dose = Menge an verordneten Tagesdosen des Arzneistoffs in Millionen *2 SSRI = Selektiver Serotonin-Reuptake-Inhibitor; SNRI = Serotonin- und Noradrenalin-Reuptake-Inhibitor | |||||





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.