
- DAZ.online
- DAZ / AZ
- DAZ 25/2009
- Mit Vitamin D3 ...
Prävention
Mit Vitamin D3 chronischen Erkrankungen vorbeugen
Mikronährstoffversorgung im grünen Bereich?
Zwischen ausgewogener, vitaminreicher Ernährung in der Theorie und dem tatsächlichen Ernährungsverhalten klafft offensichtlich eine große Lücke. Aktuelle Informationen hierzu liefern die 2008 publizierten Ergebnisse der Nationalen Verzehrsstudie II (NVS II), einer bundesweiten Befragung zur Ernährung von Jugendlichen und Erwachsenen, die im Auftrag des Bundesministeriums für Ernährung, Landwirtschaft und Verbraucherschutz durchgeführt wurde [1]. Dabei wurde die Vitamin- und Mineralstoffversorgung anhand eines Vergleichs der von der Deutschen Gesellschaft für Ernährung (DGE) empfohlenen Zufuhr mit der tatsächlichen Aufnahme beurteilt. Der aktuelle Lebensmittelverzehr wurde mit Fragebögen erfasst und dann der Gehalt an Vitaminen und Mineralstoffen mithilfe des Bundeslebensmittelschlüssels berechnet. Die Ergebnisse sind alarmierend:
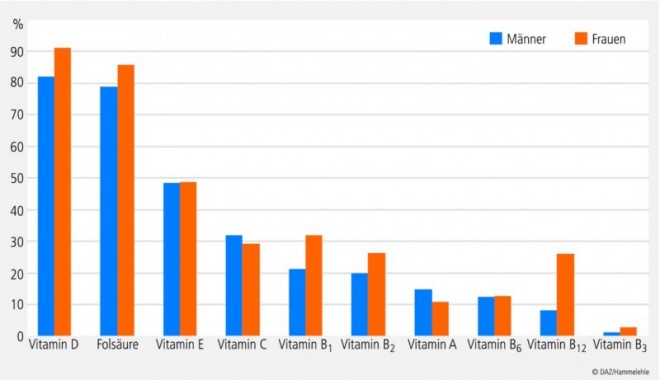
- 86% der befragten Frauen und 79% der befragten Männer sind in Deutschland nicht ausreichend mit Folsäure versorgt (DGE-Zufuhrempfehlung für gesunde Erwachsene: 0,4 mg Folsäure pro Tag).
- 91% der Frauen und 82% der Männer sind nicht ausreichend mit Vitamin D versorgt (DGE-Zufuhrempfehlung für gesunde Erwachsene: 200 I.E. Vitamin D pro Tag).
- 20 bis 50% der deutschen Bevölkerung zwischen 14 und 80 Jahren sind zudem unzureichend versorgt mit Vitamin B1 , Vitamin B2 , Vitamin B12 , Vitamin C und Vitamin E (Abb. 1 ).
Labormedizinische MessungenUm den Versorgungsstatus der verschiedenen Mikronährstoffe zu messen, gibt es verschiedene Ansätze:
Hinweis: Die derzeit übliche Messung von Mikronährstoffen wie Calcium, Magnesium und Eisen im Plasma ist obsolet, weil sie nicht den tatsächlichen Mikronährstoffstatus erfasst. | |||
Labordiagnostik versus Soll-Ist-Vergleiche
Derartige Soll-Ist-Vergleiche anhand von Schätzungen erlauben keine aussagekräftigen Rückschlüsse über den tatsächlichen Mikronährstoffstatus, den man nur mittels einer labormedizinischen Analyse und geeigneter klinisch-biochemischer Parameter ermitteln kann. Im Gegensatz zu der nur schätzbaren Mikronährstoffzufuhr über Ernährungsprotokolle in der NVS II liefern labormedizinische Messungen (s. Kasten) konkrete Werte zum tatsächlichen Versorgungsstatus eines Menschen [2].
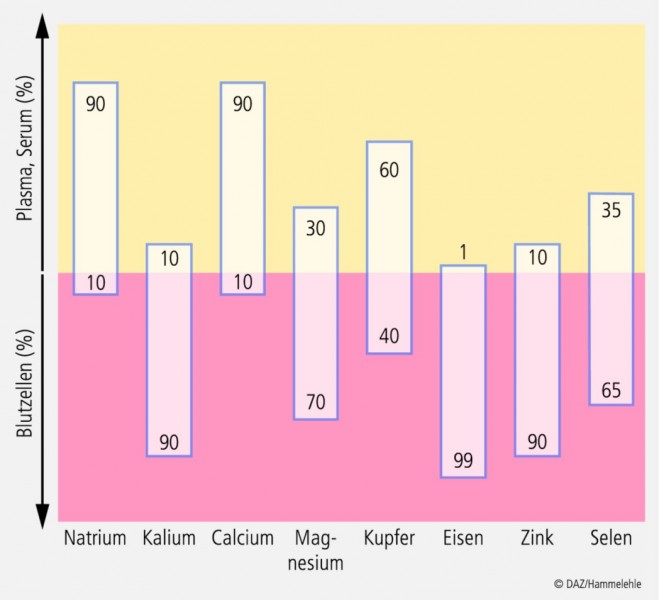
Dabei ist Folgendes zu berücksichtigen: Im Gegensatz zur Serumdiagnostik werden bei der Analyse des Vollbluts auch die Erythrozyten mit einbezogen. Das Magnesium im Blut ist beispielsweise zu ca. 70% an Erythrozyten gebunden, nur 30% liegen im Serum vor [3]. Im Rahmen der Homöostase werden auf Kosten der intrazellulären Versorgung die extrazellulären Spiegel möglichst lange konstant gehalten. Ein beginnender Magnesiummangel kann somit über einen längeren Zeitraum unentdeckt bleiben, wenn der Magnesiumspiegel nur im Serum bestimmt wird. Ähnliche Verhältnisse zeigen sich bei den Mikronährstoffen Eisen, Kalium, Kupfer, Selen und Zink (Abb. 2).
DGE-Empfehlungen gelten nicht für Risikogruppen
Die Empfehlungen der DGE zur Mikronährstoffzufuhr beziehen sich auf gesunde Personen. Dagegen haben bestimmte Bevölkerungsgruppen einen erhöhten Bedarf an Mikronährstoffen. Zu den potenziellen Risikogruppen zählen vor allem
- Kinder und Jugendliche (z. B. erhöhter Bedarf durch Wachstum),
- viele Berufstätige (z. B. erhöhter Bedarf durch einseitige Ernährungsgewohnheiten, Stress, Genussmittelkonsum),
- Schwangere und Stillende,
- ältere Menschen (z. B. erhöhter Bedarf durch altersphysiologische und medikationsbedingte Störungen der Mikronährstoffutilisation, altersbedingte Beeinträchtigung verschiedener Organe, z. B. Haut, Niere, Leber),
- Personen mit Magen-Darm-Störungen (z. B. atrophische Gastritis),
- viele Kranke, insbesondere Patienten mit Chrono- und/oder Polypharmakotherapie [4].
Multimorbidität bedingt vor allem im Alter einen erhöhten Medikamentenkonsum, der die Resorption und Utilisation von Mikronährstoffen erheblich beeinträchtigen kann (Tab. 1).
| Tab. 1: Im Alter häufig eingesetzte Arzneimittel, die einen Mangel bzw. erhöhten Bedarf an bestimmten Mikronährstoffen verursachen (Auswahl) | ||
| Indikationsgruppe | Arzneistoff(-gruppe) | Mikronährstoffe |
| Magen-Darm-Mittel | Protonenpumpenhemmer (z. B. Omeprazol, Pantoprazol) | Vitamin B12 , Folsäure, Vitamin D3 |
| Antidiabetika, orale | Metformin | Folsäure, Vitamin B12 |
| Antiepileptika | Carbamazepin, Phenytoin, Phenobarbital | Vitamin D3 , Vitamin K, Folsäure |
| Antirheumatika | Methotrexat | Folsäure |
| Corticosteroide | Prednisolon, Dexamethason etc. | Vitamin D3 , Calcium, Vitamin C |
| Diuretika | Thiazide (z. B. Hydrochlorothiazid), Schleifendiuretika (z. B. Furosemid) | Magnesium, Kalium, Folsäure, Zink |
| Lipidsenker | Statine (z. B. Lovastatin, Atorvastatin) | Coenzym Q10 (Ubichinon/-ol) |
| Psychopharmaka | Amitriptylin, Imipramin | Vitamin B2 |
Latenter Mikronährstoffmangel
Ein suboptimaler Mikronähstoffstatus kann komplexe metabolische Störungen auslösen, die sich über Jahre zu handfesten Zivilisationserkrankungen entwickeln. Mikronährstoffmängel durchlaufen verschiedene Stadien, bevor sie klinisch eindeutig in Erscheinung treten. Bereits im Stadium der "suboptimalen Bedarfsdeckung" werden Enzymleistungen sowie immunologische Funktionen gehemmt. Dadurch wird einerseits der Immunstatus geschwächt, was zu einem vermehrten Auftreten von Infektionskrankheiten führt. Andererseits steigt die Anfälligkeit für chronisch degenerative Krankheiten (z. B. Demenz), da die körperliche und geistige Entwicklung sowie die allgemeine Leistungsfähigkeit deutlich vermindert werden.
Merke: Ein Mikronährstoffmangel macht sich nicht zwangsläufig mit einem klinisch eindeutigen Symptom bemerkbar; um ihn zu erkennen, bedarf es einer validen Labordiagnostik.
Im Alltag muss von einer breiten Grauzone undiagnostizierter Mikronährstoffmängel ausgegangen werden, die sich nicht immer durch spezifische Mangelsymptome zu erkennen geben. Vielmehr imponieren sie in der Regel durch unspezifische Befindlichkeitsstörungen (Tab. 2).
| Tab. 2: Symptome von latentem Mikronährstoffmangel (Auswahl) | |
| Mikronährstoff | Unspezifische Symptome |
| Vitamin B1 | Antriebslosigkeit, Lern- und Konzentrationsstörungen |
| Vitamin B3 | Müdigkeit, Nervosität, Mundwinkelrhagaden, Stimmungsschwankungen |
| Vitamin B6 | Kopfschmerzen, Nervosität, Reizbarkeit, Stimmungsschwankungen, Infektanfälligkeit |
| Vitamin B12 | Antriebslosigkeit, kognitive Leistungseinbußen, depressive Verstimmung |
| Folsäure | Antriebslosigkeit, mentale Defizite, depressive Verstimmung |
| Vitamin C | Infektanfälligkeit, physische und psychische Leistungseinbußen, depressive Verstimmung, Reizbarkeit |
| Vitamin D | Infektanfälligkeit, Muskelschwäche, Müdigkeit, depressive Verstimmung (vor allem im Winter) |
| Magnesium | Nervosität, Reizbarkeit, Spannungskopfschmerzen, Stressanfälligkeit |
| Eisen | Blässe, Infektanfälligkeit, Müdigkeit, Mundwinkelrhagaden, Muskelschwäche |
| Zink | Infektanfälligkeit, Konzentrationsstörungen, Reizbarkeit, gestörte Wundheilung |
In der medizinischen Praxis wird diesen Symptomen in der Regel nur wenig Aufmerksamkeit geschenkt, oder sie werden als alters-, umwelt- oder genetisch bedingte Stoffwechselschwächen hingenommen, obwohl sie die Gesundheit und das Wohlbefinden der Betroffenen erheblich einschränken. Dies ist bedenklich, da latente Mangelzustände rasch in einen klinisch manifesten Mangel übergehen können, wenn der Organismus größeren Belastungen ausgesetzt ist (z. B. grippaler Infekt, Stress, Medikation).
Mikronährstoffmangel: Unterschätzt, unterdiagnostiziert und untertherapiert
Obwohl es in der wissenschaftlichen Literatur eine Vielzahl von Hinweisen dafür gibt, dass eine unzureichende Versorgung mit Mikronährstoffen wie Folsäure, Vitamin B12 (→ Schlaganfall, Demenz), Vitamin D3 (→ Osteoporose, plötzlicher Herztod) oder den langkettigen Omega-3-Fettsäuren EPA und DHA (→ plötzlicher Herztod) einen bedeutsamen Risikofaktor bei der Entstehung von chronischen Erkrankungen darstellt, wird in Deutschland das darin schlummernde präventive Potenzial bislang nicht ausreichend ausgeschöpft. Die Anreicherung von Bonbons mit Vitamin C oder von Fruchtzwergen mit Vitamin D3 stellt mit Sicherheit keine geeignete Maßnahme dar, die Mikronährstoffversorgung in der Bevölkerung zu verbessern. Man stellt sich zudem die Frage, warum die seit Jahren vorliegenden Studienergebnisse und der damit verbundene hohe finanzielle Aufwand zu keinem größeren Ergebnis geführt hat als zu dem Ratschlag, fünfmal am Tag Obst und Gemüse zu essen. Die starke Zunahme ernährungsbedingter Erkrankungen in den letzten zehn Jahren zeigt doch, dass der Anteil derjenigen, die solche Ratschläge konsequent befolgen, relativ gering ist.
Die vielen Erkenntnisse aus Labor- und Tierversuchen sowie zahlreichen klinischen Studien weisen so deutlich auf präventive Wirkungen von Mikronährstoffen hin, dass man unter Berücksichtigung der stetig steigenden Kosten im Gesundheitswesen nicht länger warten sollte, bis weitere Studien, die erst in Jahrzehnten abgeschlossen sind, diese Erkenntnisse untermauern. Unter der Prämisse, dass die gezielte Supplementierung von Mikronährstoffen zur Prävention chronischer Erkrankungen auch nur mit einer gewissen Wahrscheinlichkeit effektiv ist, wäre es falsch, dieses Potenzial nicht zu nutzen und stattdessen auf Gewissheiten zu warten.
Aktuelle Ergebnisse aus Kohorten- und Interventionsstudien belegen, dass eine suboptimale Versorgung mit Vitamin D3 , Omega-3-Fettsäuren (EPA/DHA), Vitamin B12 und Folsäure bereits vor dem Auftreten spezifischer Mangelerkrankungen das Risiko für verschiedene chronische Erkrankungen erhöht (s. Kasten).
Prävention mit Mikronährstoffen – aktuelle Studien (Auswahl
In einer aktuellen randomisierten und placebokontrollierten Doppelblindstudie (n = 818 Männer und Frauen, 50 – 70 Jahre alt) verbesserte die Supplementierung von täglich 800 µg Folsäure über einen Zeitraum von 3 Jahren signifikant die geistige Leistungsfähigkeit: Gedächtnisleistung, Denkgeschwindigkeit und sensomotorische Geschwindigkeit. Der Homocystein-Plasmaspiegel sank um 26% [1].
In einer prospektiven Kohortenstudie mit 3258 Patienten (Durchschnittsalter: 62 Jahre) konnte gezeigt werden, dass eine unzureichende Versorgung mit Vitamin D3 einen unabhängigen Risikofaktor für die allgemeine und kardiovaskuläre Mortalität darstellt [2]. Dieses Ergebnis wird durch eine weitere Studie mit 3299 Patienten unterstrichen, die zusätzlich darauf hinweist, dass ein Vitamin-D3 -Mangel (25(OH)-Vitamin D3 < 25 nmol/l) gegenüber einer guten Versorgung (25(OH)-Vitamin D3 ≥ 75 nmol/l) das Risiko für den plötzlichen Herztod signifikant steigert [3].
Die am 1. Januar 1998 in den USA und Kanada gesetzlich vorgeschriebene Anreicherung von Grundnahrungsmitteln mit Folsäure (150 µg Folsäure auf 100 g Mehl) zeigt nach ersten Auswertungen nicht nur eine drastische Reduktion der Inzidenz von Neuralrohrdefekten, sondern auch von Schlaganfällen. Dabei wurde die Schlaganfallhäufigkeit über einen mehrjährigen Zeitraum vor Inkrafttreten der Anreicherung (1990 – 1997) und nach entsprechender Fortifikation über den Zeitraum von 1998 bis 2002 erfasst (Teilnehmerzahl: ca. 200 Mio. Personen in den USA und Kanada). Die Ergebnisse sind beeindruckend:
Omega-3-Fettsäuren: Prävention beginnt im Mutterleib Prävention beginnt im Mutterleib. Seefisch ist die wichtigste Quelle für die langkettigen Omega-3-Fettsäuren EPA und DHA, die vor allem für eine gesunde Gehirnentwicklung wichtig sind. Die Ergebnisse der ALSPAC-Studie an 11.875 Schwangeren zeigen, dass eine Omega-3-Fettsäuren-reiche Ernährung in der Schwangerschaft die gesunde geistige Entwicklung des Kindes fördert (z. B. bessere sprachliche, feinmotorische und soziale Entwicklung) [5]. |
Vitamin D3 -Mangel kann krank machen
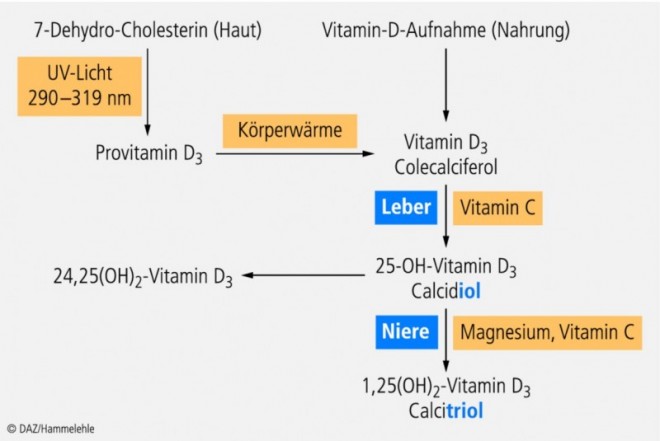
Seit der Entdeckung seiner antirachitischen Wirkung in den 1920er Jahren hat man Vitamin D lange Zeit nur im Hinblick auf seine Funktion im Calcium- und Knochenstoffwechsel betrachtet (Abb. 3). Eine Vielzahl von Forschungsergebnissen der vergangenen Jahre hat allerdings gezeigt, dass es nicht nur ein Regulator der Calcium- und Phosphathomöostase ist, sondern zahlreiche extraskelettäre Wirkungen aufweist. Darunter sind von besonderer Bedeutung sein Einfluss auf das Immunsystem sowie auf die Zelldifferenzierung und das Zellwachstum (Tab. 3).
| Tab. 3: Vitamin D3: Physiologische und biochemische Eigenschaften im Überblick | |
| Zielgewebe/-organ | Physiologische und biochemische Eigenschaften |
| Immunsystem | Wirkt antiinflammatorisch und immunstabilisierend: Vitamin-D-Rezeptoren befinden sich auf Monozyten und Leukozyten mit der höchsten Phagozytoserate Differenzierung von Monozyten zu Makrophagen↑ Infektanfälligkeit (z. B. Atemwegsinfekte)↓ Aktivität lysosomaler Enzyme in Makrophagen↑ Risiko für Kolon-, Mamma- und Prostatakarzinom↓ Phagozytoseaktivität und -rate↑ Th1-/Th-2-Regulation: Zytokine des Th1-Weges (z. B. IL -2, IFN-γ)↓, Endogene antimikrobielle Cathelicidin-Synthese↑ (potenzielle Indikationen: Allergien, Asthma bronchiale, chronisch entzündliche Darmerkrankungen, HIV-Infektion, Multiple Sklerose, rheumatoide Arthritis, Tuberkulose) |
| Tumoren | Tumorzellproliferation↓ Differenzierung und Apoptose von malignen Zellen↑ (potenzielle Indikationen: Kolon-, Mamma- und Prostatakarzinom, |
| Pankreas | Reguliert die Insulinsekretion Schützt Betazellen vor Zytokin-induzierter Apoptose Im Maus-Modell: Verhinderung der Entwicklung eines Typ-1-Diabetes Supplemente (2000 I.E./Tag) in der frühen Kindheit verringern das Risiko für (potenzielle Indikationen: Insulinresistenz, Metabolisches Syndrom, Typ-2-Diabetes) |
| Herz-Kreislauf-System | Wirkt über Vitamin-D-Rezeptoren auf Kardiozyten Kofaktor der Adenylatcyclase Systolischer Blutdruck↓ Aktivität des Renin-Angiotensin-Systems↓ Risiko einer Herzhypertrophie↓ (potenzielle Indikationen: Herzinsuffizienz, Hypertonie) |
| Haut | Differenzierung und Reifung der Keratinozyten↑ Wirkt antiproliferativ und immunregulativ (Th-1-, Th-2-Zellen) (potenzielle Indikationen: Psoriasis, Neurodermitis, Lupus erythematodes) |
| Knochen | Reguliert die Calcium- und Phosphathomöostase Calciumabsorption in Duodenum und Jejunum↑ Einbau von Calcium in den Knochen↑ Calcium-Exkretion über die Niere↑ → Nebenschilddrüsenfunktion↓ Aktivität der Osteoklasten↑ Synthese von Osteocalcin, Osteopontin↑ (Indikationen: Rachitis, Osteomalazie, Osteoporose) |
| Muskel-/Nervenzellen | Muskelmasse↑ Muskuläre Koordination↑(Sturzprophylaxe) (Indikationen: Muskelschwäche, Myopathien, Osteoporose) |
Die stoffwechselaktive Verbindung 1,25(OH)2 -Vitamin D3 (Calcitriol) ist ein Steroidhormon, das seine physiologischen Effekte überwiegend durch die Bindung an Vitamin-D-Rezeptoren (VDR) ausübt. VDR wurden in über 30 Geweben gefunden, die mit dem Calcium- und Phosphatstoffwechsel (Knochenstoffwechsel) nichts zu tun haben (z. B. Endothelzellen, Inselzellen des Pankreas, Herz-, Skelettmuskelzellen, Monozyten, T-Lymphozyten) [5].
Nach aktuellen Studien dürfte ein unzureichender Vitamin-D-Status (25-OH-Vitamin D3 im Serum ≤ 75 nmol/l) ein wichtiger ätiologischer Faktor bei der Pathogenese zahlreicher chronischer Erkrankungen sein:
- Autoimmunerkrankungen (z. B. Multiple Sklerose, Typ-1-Diabetes),
- entzündlichen Darmerkrankungen (z. B. Morbus Crohn),
- Infektionen, Immunschwäche,
- kardiovaskulärer Erkrankungen (z. B. Bluthochdruck, Herzinsuffizienz, plötzlicher Herztod),
- Krebserkrankungen (z. B. Kolon-, Mamma-, Ovarial-, Prostatakarzinom, Non-Hodgkin-Lymphom).
Definiert man unter präventiven Aspekten einen guten Vitamin-D-Status als 25-OH-Vitamin-D3 -Serumspiegel > 80 nmol/l, so dürften in Deutschland bis zu 90% der Bevölkerung unterversorgt sein. Besonders kritisch ist, dass die DGE Jugendlichen und Erwachsenen im Alter zwischen 15 bis 65 Jahren die Aufnahme von nur 200 I.E. Vitamin D3 (= 5 µg) pro Tag empfiehlt. Man könnte durchaus behaupten, dass die behördlichen Zufuhrempfehlungen dazu führen, dass gesunde Menschen in Deutschland krank werden. Um 25-OH-Vitamin-D3 -Serumspiegel von > 80 nmol/l zu erreichen, müssen 1000 bis 2000 I.E. Vitamin D3 (Colecalciferol) pro Tag supplementiert werden, da unsere Lebensmittel nur sehr niedrige Konzentrationen an diesem Vitamin enthalten. Im jüngeren Lebensalter reicht in den Sommermonaten zwar ein gelegentliches Sonnenbad aus, um bis 100% des Vitamin-D3 -Bedarfs zu decken. Dagegen ist in Deutschland von Oktober bis April die für die Vitamin-D3 -Synthese notwendige UV-B-Strahlung (280 – 315 nm) sehr gering. Auch hier gilt der altbewährte Spruch "Vertrauen ist gut, labordiagnostische Kontrolle ist besser!"
Vitamin D3 und die Telomerlänge der Leukozyten-DNA
Vitamin D3 ist ein potenter Inhibitor der proinflammatorischen Immunantwort und vermindert den Leukozyten-Turnover. Die Länge der Telomere in der DNA der Leukozyten ist ein prognostischer Faktor für altersbedingte Erkrankungen. Telomere fungieren im Zellkern sozusagen als eingebaute "Lebenszeituhr", die jede Zellerneuerung mitzählt.
Ein guter Vitamin-D3 -Status scheint altersassoziierten Erkrankungen und Störungen des Immunsystems vorzubeugen, wie eine Studie aus England zeigt [6]. Bei 2160 Frauen zwischen 18 und 79 Jahren wurden die 25-OH-Vitamin-D3 -Werte im Serum gemessen und anschließend mit der Länge der Telomere ihrer Leukozyten-DNA verglichen. Nach der Anpassung der Ergebnisse an das jeweilige Alter der Frauen und Korrektur störender Faktoren zeigte sich, dass Frauen mit mehr Vitamin D3 im Blut längere Telomere haben und umgekehrt. Bei der Gliederung der Frauen aufgrund ihres Vitamin-D-Status in drei gleich große Gruppen, betrug der Unterschied der Telomerlängen in der ersten und der dritten Gruppe 107 Basenpaare. Das entspricht einer Alterung von fünf Jahren. Der Unterschied wuchs mit steigenden Werten für das C-reaktive Protein (CRP), einen Parameter für die systemische Entzündung.
Vitamin D bei Krebserkrankungen
Epidemiologische Studien zeigen, dass eine vermehrte Sonnenlichtexposition mit einer verminderten Häufigkeit und Mortalität vieler Krebserkrankungen wie Brust-, Darm-, Ovarial-, Prostatakarzinom und Non-Hodgkin-Lymphom assoziiert ist [7]. Calcitriol wirkt über die Wechselwirkung mit Vitamin-D-Rezeptoren (VDR) antiproliferativ, stimuliert die Apoptose und kann die Synthese der Telomerase sowie die Invasion von Tumorzellen hemmen.
Niedrige Calcidiol- und Calcitriolspiegel sind mit einem 5- bis 7-fach erhöhten Risiko für Brustkrebs assoziiert. Bei niedrigen Calcitriolspiegel verläuft zudem die Progression von Brustkrebsmetastasen schneller [8]. In einer Studie an 777 prämenopausalen und 783 postmenopausalen Frauen konnte gezeigt werden, dass die tägliche Calcium- und Vitamin-D3 -Aufnahme aus der Nahrung und Supplementen invers mit der Brustdichte korreliert. Die tägliche Zufuhr von 1000 mg Calcium und 400 I.E. Vitamin D3 war mit einer 8,5% niedrigeren Brustdichte assoziiert. Die Autoren der Studie schlussfolgern, dass eine bessere Versorgung mit Vitamin D3 und Calcium einen sicheren und kostengünstigen Beitrag zur Prävention von Brustkrebs leisten könnte [9].
In einer kanadischen Studie wurde zwischen 1989 und 1995 in Blutproben von 512 neu auf Brustkrebs diagnostizierten Frauen mithilfe eines Radioimmunoassays der Vitamin-D-Status anhand der 25-OH-Vitamin-D-Spiegel erfasst. Die Frauen wurden bis 2006 nachbeobachtet (medianes Follow-up 11,6 Jahre). Zum Zeitpunkt der Diagnose hatten nur 24% der untersuchten Frauen einen normalen Vitamin-D-Status. Frauen mit niedrigem Vitamin-D-Status (Calcidiol < 50 nmol/l) wiesen häufiger aggressivere und höhergradige Formen von Brustkrebs auf (p = 0,03). Nach zehn Jahren lebten noch 85% der Frauen mit adäquatem Vitamin-D-Status (Calcidiol > 72 nmol/l), und 83% von ihnen waren frei von Metastasen. Im Vergleich dazu lebten in der Gruppe mit schlechtem Vitamin-D-Status nur noch 74%, und nur 69% waren frei von Metastasen [10].
Die adjuvante Therapie mit Bisphosphonaten (z. B. Ibandronsäure) und/oder Aromatasehemmern (z. B. Anastrozol, Letrozol) kann durch eine adäquate Supplementierung von Vitamin D (z. B. 1000 – 2000 I.E.) und Calcium im Hinblick auf den Knochenstoffwechsel (Vorbeugung von Osteoporose) und die Nebenwirkungsrate optimiert werden [11, 12].
Vitamin D bei Multipler Sklerose (MS)
Eine inverse Korrelation zwischen UV-B-Lichtexposition und der MS-Inzidenz ist seit Jahren bekannt. In epidemiologischen Studien wird eine erhöhte MS-Prävalenz bei schlechtem Vitamin-D3 -Status und niedriger Knochendichte beschrieben [13]. Studien haben gezeigt, dass über 48% der MS-Patienten einen subklinischen Vitamin-D3 -Mangel (< 50 nmol/l = 20 ng/ml) aufweisen.
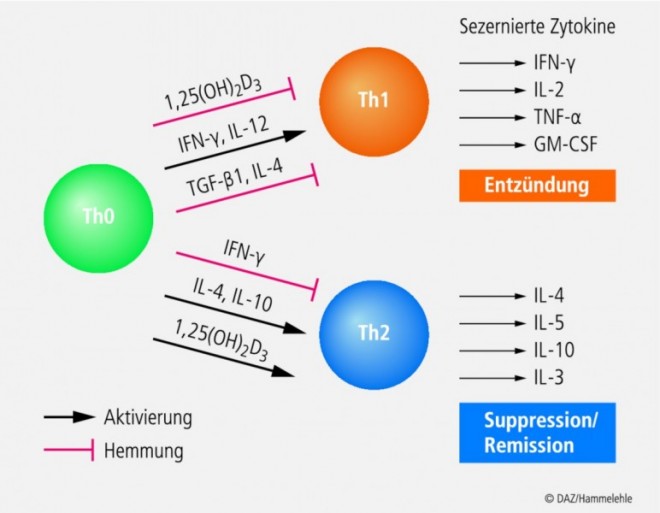
Im Mausmodell der Multiplen Sklerose verhindert die orale oder parenterale Applikation von Calcitriol sowohl den Ausbruch als auch die Progression der Erkrankung. Die positiven Effekte des Vitamin-D-Hormons bei MS stehen vor allem mit seinem regulierenden Einfluss auf die Immunantwort der T-Helferzellen in Verbindung. Bei Autoimmunerkrankungen dominiert häufig die Th1-Reaktion. Th1-Zellen bilden bevorzugt proinflammatorische Zytokine (z. B. TNF-α, IL -2) [14]. Th2-Zellen bilden präferenziell antiinflammatorische Zytokine wie IL -4 (Abb. 4). Vitamin-D-Hormon hemmt Th1-Zellen und vermindert die Belastung mit TNF-α und IL -2. Vitamin-D3 -Supplemente erhöhen bei MS-Patienten die Serumspiegel des antiinflammatorischen Zytokins TGF-β1 signifikant.
In einer Untersuchung an 7 Mio. Angehörigen des US-Militärs von 1992 bis 2004 wurde der Zusammenhang des Vitamin-D-Status (25-OH-Vitamin-D3 -Spiegel) mit dem Risiko für Multiple Sklerose erfasst [13]. Dabei zeigte sich für die höchste Quintile (99,1 bis 152 nmol/l) gegenüber der niedrigsten Quintile (15,2 bis 63,2 nmol) ein um 62% verringertes Risiko, an MS zu erkranken. Vitamin D3 kann Studien zufolge die Schubhäufigkeit bei MS-Patienten verringern und die Muskelfunktion sowie die Lebensqualität deutlich verbessern.
Vitamin D bei Diabetes mellitus
Studien geben Hinweise darauf, dass ein Vitamin-D3 -Mangel ein pathogenetischer Faktor für Typ-1-Diabetes und das metabolische Syndrom ist, da er die Insulinresistenz erhöht und die Insulinsekretion der Betazellen im Pankreas verringert [15]. Zwischen dem Vitamin-D3 -Status einerseits und der Diabetes-Prävalenz, der Glucosekonzentration und der Insulinresistenz andererseits besteht eine inverse Relation [16].
In einer prospektiven Kohortenstudie mit 12.058 Kindern (Jahrgang 1966) in Finnland wurde der Einfluss einer Supplementierung von Vitamin-D3 im ersten Lebensjahr auf die Diabetes-Inzidenz über einen Zeitraum von 30 Jahren verfolgt. Dabei zeigte sich, dass Kinder, die im ersten Lebensjahr täglich 2000 I.E. (= 50 µg) Vitamin D3 pro Tag zur Rachitis-Prophylaxe erhalten hatten, im Vergleich zu den Kindern mit geringer dosierten Supplementen ein um etwa 80% niedrigeres Risiko für Typ-1-Diabetes aufwiesen. Darüber hinaus hatten Kinder, bei denen im ersten Lebensjahr Rachitis auftrat, im Vergleich zu unauffälligen Kindern ein 3-fach höheres Diabetesrisiko.
Die präventiven Effekte des Vitamin-D3 -Hormons bei Typ-1-Diabetes werden wie bei der Multiplen Sklerose mit seinem regulierenden Einfluss auf die Immunantwort der T-Helferzellen in Verbindung gebracht (Abb. 4). Der Calcidiol- und Calcitriol-Spiegel korreliert invers mit proinflammatorischen Zytokinen wie TNF-α, der die Insulinresistenz fördert und die Insulinsekretion beeinträchtigt. Calcitriol scheint die Th2-Immunantwort zu begünstigen und somit einer Zytokin-induzierten Zerstörung von Betazellen entgegenzuwirken [17]. Eine Normalisierung des Vitamin-D3 -Status könnte bei Diagnose eines Typ-1-Diabetes dazu beitragen, die noch vorhandenen Betazellen vor der weiteren Zerstörung zu schützen. Bei Typ-2-Diabetikern zeigen einige Studien, dass die Supplementierung von Vitamin D3 die Glucosetoleranz verbessert und die Insulinresistenz verringert.
Vitamin D bei Herz-Kreislauf-Erkrankungen
Vitamin D3 hat einen regulierenden Einfluss auf die Herzmuskelleistung, die myokardiale Calciumhomöostase und den Blutdruck. Es wirkt einer Hypertrophie des Herzmuskels entgegen und bremst die Aktivität des Renin-Angiotensin-Systems. Studien und Metaanalysen zeigen, dass Vitamin D3 die allgemeine und die kardiovaskuläre Mortalität senkt [18, 19]. In einer Studie des Herzzentrums Ludwigshafen an 3299 Patienten mit KHK (1997 –2000, Koronarangiographie) wurde der Einfluss des Vitamin-D-Status auf die kardiovaskuläre Mortalität über einen Zeitraum von 7,7 Jahren verfolgt. Dabei zeigte sich, dass der Vitamin-D-Status invers mit dem Schweregrad der Herzinsuffizienz (NYHA-Klassifikation) und mit einer schlechten linksventrikulären Auswurffraktion (LVEF) korreliert. Ein Vitamin-D-Mangel (Calcidiol < 25 nmol/l = 10 ng/ml) war im Vergleich zu einem guten Vitamin-D-Status (Calcidiol ≥ 75 nmol/l = 30 ng/ml) mit einem 2,8-fach erhöhten Risiko für Tod durch Herzversagen und einem 5-fach erhöhten Risiko für plötzlichen Herztod assoziiert.
Fazit: Präventives Potenzial von Mikronährstoffen nutzen
Eine routinemäßige labordiagnostische Kontrolle des Vitamin-D3 -Status müsste nach den vorliegenden Daten unter präventivmedizinischen Aspekten genauso durchgeführt werden wie eine Messung des Cholesterinspiegels oder eine Blutdruckkontrolle. Das präventive Potenzial von Mikronährstoffen wie Vitamin D, Folsäure und Vitamin B12 wird in Deutschland bei Weitem nicht ausgeschöpft, obwohl die Anzahl der chronischen Erkrankungen und die damit anfallenden Kosten im Gesundheitssystem infolge der steigenden Lebenserwartung drastisch zunehmen (Aktuelles zu Folsäure und Vitamin B12 lesen Sie in der DAZ Nr. 18, S. 92).
Das System der reparativ orientierten Schulmedizin ist heute in vielen Bereichen ausgereizt und stößt immer stärker an seine therapeutischen und ökonomischen Grenzen. Andererseits ist der Begriff "Prävention" in der Gesundheitspolitik zu einem Modewort mit leerem Inhalt mutiert. Einfache und kostengünstige Präventionsmaßnahmen werden von der Leitlinien-orientierten Schulmedizin aufgrund mangelnder Kenntnis oder Ignoranz häufig nicht in die Praxis umgesetzt.
Literatur
[1] Max Rubner-Institut (Hrsg). Nationale Verzehrsstudie II Ergebnisbericht, Teil 2. Bundesforschungsinstitut für Ernährung und Lebensmittel, 2008.
[2] Thomas L. Labor und Diagnose. 5. Auflage, TH Books Verlagsgesellschaft, Frankfurt am Main 2000.
[3] Gröber U. Metabolic Tuning statt Doping. Mikronährstoffe im Sport. Hirzel Verlag, Stuttgart 2008.
[4] Gröber U. Arzneimittel und Mikronährstoffe. Medikationsorientierte Supplementierung. Wissenschaftliche Verlagsgesellschaft, Stuttgart 2007.
[5] Pietrzik K, Golly I, Loew D. Handbuch Vitamine. Elsevier, München 2008.
[6] Richards JB, et al. Higher serum vitamin D concentrations are associated with longer leukocyte telomere length in women. Am J Clin Nutr 2007;86(5):1420 –1425.
[7] Guyton KZ, et al. Cancer chemoprevention using natural vitamin D and synthetic analogs. Ann Rev Pharmacol Toxicol 2001;41:421– 442
[8] Lowe LC, et al. Plasma 25-hydroxy vitamin D concentrations, vitamin D receptor genotype and breast cancer risk in a UK Caucasian population. Eur J Cancer 2005;41:1164 –1169.
[9] Berube S, et al. Vitamin D and calcium intakes from food or supplements and mammographic breast density. Cancer Epidemiol Biomarkers Prev 2005;17(7), 1653 –1659.
[10] Goodwin J, et al. Frequency of vitamin D deficiency at breast cancer diagnosis and association with risk of distant recurrence and death in a prospective cohort study of T1-3, N0-1, M0 BC. Proc Am Soc Clin Oncol 2008;26 (Suppl):Abstr 511.
[11] Wang-Gillam A, et al. Evaluation of vitamin D deficiency in breast cancer patients on bisphosphonates. Oncologist 2008;13(7):821– 827.
[12] Lester JE, et al. Prevention of anastrozole-induced bone loss with monthly oral ibandronate during adjuvant aromatase inhibitor therapy for breast cancer. Clin Cancer Res 2008;14(19):6336 – 6342.
[13] Munger KL, et al. Vitamin D intake and incidence of multiple sclerosis. Neurology 2004;62(12):60 – 65.
[14] Cantorna MT. Vitamin D and autoimmunity: Is vitamin D status an environmental factor affecting autoimmune disease prevalence? Proc Soc Exp Biol Med 2000;223:230 –233.
[15] Boucher RJ. Inadequate vitamin D status: Does it contribute to the disorders comprising syndrome X? Br J Nutr 1998;79:315– 327.
[16] Chiu KC, et al. Hypovitaminosis D is associated with insulin resistance and beta cell dysfunction. Am J Clin Nutr 2004;79:820 – 825.
[17] Pozzilli P, et al. IMDIAB group: Low levels of 25-hydroxyvitamin D3 and 1,25-dihydroxyvitamin D3 in patients with newly diagnosed type 1 diabetes. Horm Metab Res 2005; 37:680 – 683.
[18] Pilz S, et al. Association of vitamin D deficiency with heart failure and sudden cardiac death in a large cross-sectional study of patients referred for coronary angiography. J Clin Endocrin Metab 2008;93:3927– 3935.
[19] Dobnig H, et al. Independent association of low serum 25-hydroxyvitamin D and 1,25-dihydroxyvitamin D levels with all-cause and cardiovascular mortality. Arch Intern Med 2008;168(12):1340 –1349.
Autor
Uwe Gröber,
Akademie & Zentrum für Mikronährstoffmedizin,
Zweigertstraße 55,
45130 Essen





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.