
- DAZ.online
- DAZ / AZ
- DAZ 5/2005
- Sekundäre Pflanzenstoffe...
Ernährung heute
Sekundäre Pflanzenstoffe – die neuen „Vitamine“?
Einteilung und Vorkommen
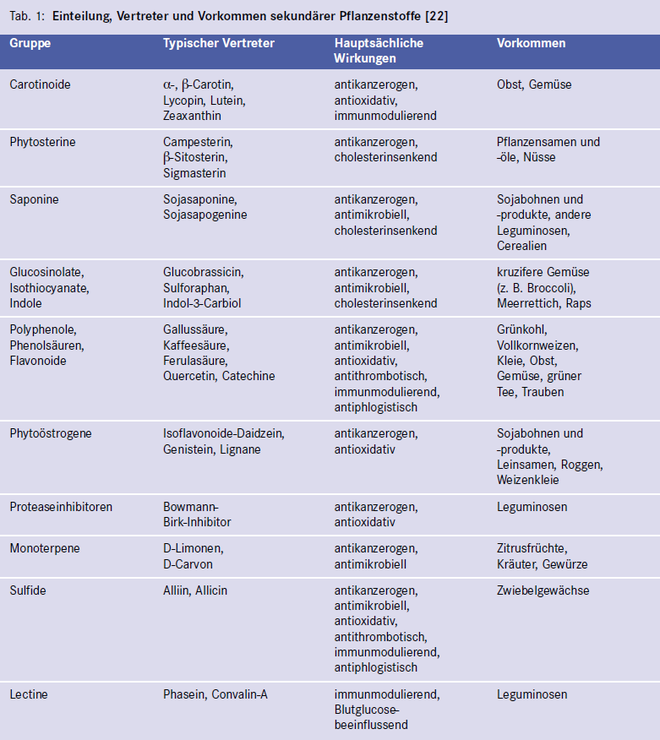
Sekundäre Pflanzenstoffe dienen der Pflanze als Farb-, Abwehr- und Schutzstoffe sowie als Wachstumsregulatoren. Chemisch handelt es sich um höchst heterogene Substanzen. Inzwischen findet eine Einteilung der Sekundären Pflanzenstoffe Verwendung, die im Wesentlichen aufgrund ihrer chemischen Struktur erfolgt, aber auch auf ihren funktionellen Eigenschaften beruht. Entsprechend ist die Klassifikation in chemischer Hinsicht nicht stringent (Tab. 1). Je nach Pflanzenfamilie finden sich typische Verbindungen, wie z.B. schwefelhaltige Stoffe in Knoblauch und Zwiebelgewächsen. Viele dieser Substanzen sind für den spezifischen Geruch, Geschmack oder die Farbe der jeweiligen Pflanze verantwortlich. Sekundäre Pflanzenstoffe kommen in den Pflanzen nur in sehr geringen Mengen vor, sodass die Gesamtaufnahme mit der Nahrung nur bei etwa 1,5 g/d liegt. Von den bislang rund 30.000 bekannten sekundären Pflanzenstoffen sind nach Schätzungen etwa 5000 bis 10.000 natürlicherweise in der menschlichen Ernährung enthalten [75].
Sekundäre Pflanzenstoffe können auf den Menschen sowohl gesundheitsfördernde als auch gesundheitsschädliche Wirkungen ausüben. Bis vor einigen Jahren stand hauptsächlich die Toxizität dieser Verbindungen im Mittelpunkt des wissenschaftlichen Interesses. Da einige sekundäre Pflanzenstoffe die Verfügbarkeit von Nährstoffen einschränken, wurden sie über lange Zeit als "antinutritive Pflanzeninhaltsstoffe" bezeichnet. Hierbei muss jedoch berücksichtigt werden, dass derartige Auswirkungen in den meisten Fällen nach sehr einseitigen Fütterungsversuchen an Tieren auftraten, die in dieser Form nicht auf die Ernährungsgewohnheiten des Menschen übertragbar sind. In den letzten Jahren ist bei der gesundheitlichen Bewertung sekundärer Pflanzenstoffe ein vollständiger Wandel zu beobachten. Es wird davon ausgegangen, dass die meisten Stoffe (mit Ausnahme von z. B. Solanin) bei üblichen Verzehrsmengen gesundheitsfördernde Eigenschaften besitzen.
Gesundheitsfördernde Wirkunge sekundärer Pflanzenstoffe
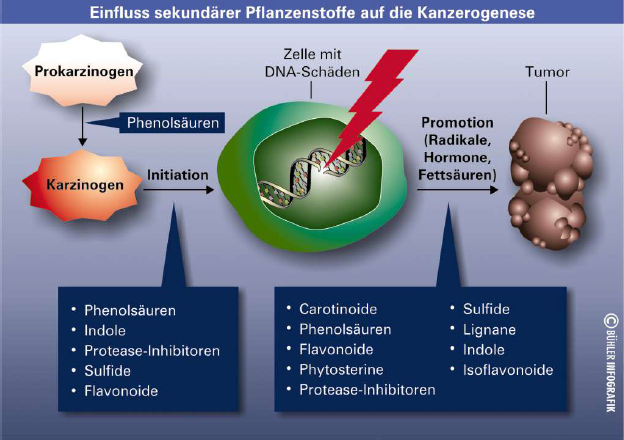
Eine Fülle von experimentellen und epidemiologischen Befunden macht deutlich, dass ein erhöhter Verzehr pflanzlicher Lebensmittel gesundheitliche Vorteile mit sich bringt. Die positiven Auswirkungen einer obst- und gemüsereichen Kost auf die Erkrankungshäufigkeit zeigt sich besonders deutlich bei epithelialen Tumoren sowie bei hormonabhängigen Krebserkrankungen [68]. Diese protektiven Effekte werden vermutlich zu einem Großteil durch sekundäre Pflanzenstoffe vermittelt. Sekundäre Pflanzenstoffe können das Krebsgeschehen auf verschiedenen Ebenen beeinflussen (s. Tab. 2 und Abb. 1). Die Erkenntnisse über die gesundheitsfördernden Wirkungen der sekundären Pflanzenstoffe basieren überwiegend auf Beobachtungsstudien. Für einige Substanzgruppen wurde inzwischen sogar ein kausaler Zusammenhang nachgewiesen.
Carotinoide – antioxidative Schutzfaktoren
Carotinoide bilden eine große Klasse verschiedenartiger Farbstoffe, die im Pflanzenreich weit verbreitet ist. Bisher wurden rund 700 Vertreter dieser Substanzklasse ermittelt, wovon bislang nur 14 im menschlichen Blut nachgewiesen werden konnten. Bei Carotinoiden wird zwischen sauerstoffhaltigen und sauerstofffreien Verbindungen unterschieden. Zur ersten Gruppe, die auch unter der Bezeichnung "Xanthophylle" bekannt ist, zählen Lutein, Zeaxanthin sowie Beta-Cryptoxanthin. Grüne Gemüse wie Spinat, Grünkohl und Broccoli sind reichhaltige Lieferanten. Sauerstofffreie Carotinoide wie Alpha-Carotin, Beta-Carotin sowie Lycopin finden sich hingegen auch in gelben und roten Obst- und Gemüsesorten in hoher Konzentration. Generell wird die Bioverfügbarkeit von Carotinoiden als schlecht eingestuft. Vor allem aus rohen Gemüsen ist die Absorptionsrate gering [73].
Die hervorstechende Eigenschaft der Carotinoide ist ihre antioxidative Wirkung. Daneben stellen Carotinoide potente Stimulatoren der zellvermittelten Immunabwehr dar [16] und verbessern die interzelluläre Kommunikation über gap junctions. Außerdem dienen Carotinoide wie das Beta-Carotin als Vitamin-A-Vorstufe. Die antioxidative Wirkung von Carotinoiden ist insbesondere im Zusammenhang mit radikal-assoziierten Erkrankungen wie seniler Makuladegeneration [10] atherosklerotischen Erkrankungen [20] und verschiedenen epithelialen Tumoren [7] von Interesse.
Während Beobachtungsstudien auf vielfältige Schutzeffekte von Beta-Carotin gegenüber Krebserkrankungen und Herz-Kreislauf-Erkrankungen hinweisen [7, 29, 56, 69], ergaben große Interventionsstudien allerdings keinen Effekt einer ergänzenden Supplementierung mit Beta-Carotin auf das Erkrankungsrisiko. So führte die Gabe von 50 mg Beta-Carotin jeden zweiten Tag in einer Interventionsstudie mit 22.000 Teilnehmern über 12 Jahre weder zu einem verminderten Auftreten koronarer Herzerkrankungen noch zu einer verminderten Mortalität durch kardiovaskuläre Erkrankungen.
Zwischen Verum- und Placebogruppe waren außerdem keine Unterschiede im Auftreten von Myokardinfarkten oder Schlaganfällen sowie im Hinblick auf das Krebsrisiko festzustellen [27]. Auch hatte eine Kombination aus 20 mg Beta-Carotin, 600 mg Vitamin E und 250 mg Vitamin C in einem Kollektiv aus 20.536 Personen keine Auswirkung auf das Auftreten von Herzinfarkt, Schlaganfall oder auf die Mortalität über einen Beobachtungszeitraum von fünf Jahren [Heart Protection Study Collaborative Group 2002].
Im Rahmen der ATBC-Studie fanden Rapola et al. [62] sogar ein signifikant höheres Risiko tödlicher Herzinfarkte bei den Probanden, die 20 mg/Tag Beta-Carotin erhalten hatten. Das Kollektiv dieser Untersuchung bestand im Unterschied zu anderen Studien allerdings aus Männern, die bereits einen Myokardinfarkt überlebt hatten. Zudem zeigen die Ergebnisse der ATBC- und CARET-Studie negative Auswirkungen hochdosierter Beta-Carotin-Supplemente im Hinblick auf das Lungenkrebsrisiko. In diesen Studien erhielten langjährige, starke Raucher entweder nur Beta-Carotin (20 mg bzw. 30 mg) oder eine Kombination aus Beta-Carotin und Vitamin A mit der Folge, dass die Lungenkrebshäufigkeit in den Verumgruppen im Vergleich zu den Placebogruppen zunahm [4, 55].
Anders stellt sich die Situation hingegen bei Personen mit schlechtem Versorgungsstatus an Antioxidanzien dar. Die Ergebnisse der französischen SU.VI.MAX Studie mit über 13.000 Erwachsenen deuten darauf hin, dass in diesem Fall eine physiologisch dosierte (!) Antioxidanziengaben günstige Effekte ausübt. So zeigte sich nach 7,5 Jahren eine verminderte Krebsinzidenz sowie eine allgemein verminderte Mortalität bei Männern, jedoch nicht bei Frauen. Die Autoren gelangen zu der Schlussfolgerung, dass eine Supplementierung bei Männern aufgrund deren niedrigeren Ausgangskonzentrationen bestimmter Antioxidanzien, insbesondere Beta-Carotin, von Nutzen sein könnte [28].
Besser sehen mit Lutein?
Bedingt durch eine zunehmende Zahl von Personen mit degenerativen Augenerkrankungen gelangten in den letzten Jahren Lutein und Zeaxanthin in den Mittelpunkt des Interesses, da beide Xanthophylle in hoher Konzentration in der Netzhaut des Auges selektiv angereichert werden [43]. Gemeinsam scheinen sie oxidative Schäden im gelben Fleck der Macula, die insbesondere durch kurzwelliges Licht induziert werden, zu vermindern [33]. Epidemiologische Daten deuten darauf hin, dass eine hohe Nahrungszufuhr bzw. hohe Serumkonzentrationen an Lutein und Zeaxanthin das Risiko für die altersbedingte Makuladegeneration (AMD) sowie für die Katarakt reduziert, wenngleich dieser Zusammenhang nicht in allen Studien nachgewiesen wurde [43].
In zahlreichen Untersuchungen erhöhte eine vermehrte Luteinzufuhr durch Ernährungsmaßnahmen oder Supplementierung die Makulapigmentdichte [8, 9, 24, 38]. Eine Erhöhung der Makulapigmentdichte kann vermutlich zu einer Senkung des AMD-Risikos beitragen, wenngleich dieser Zusammenhang bisher nicht kausal belegt ist [18]. In einer randomisierten, plazebokontrollierten Doppelblindstudie mit 90 Patienten, die an atrophischer AMD litten, erhielten die Probanden entweder täglich 10 mg Lutein, 10 mg Lutein kombiniert mit einer Antioxidanzien-/Vitamin-Mischung oder ein Plazebo.
Nach einem Jahr hatten sich die Dichte der Makulapigmente, die Sehschärfe und die Kontrastempfindlichkeit in den beiden Luteingruppen im Vergleich zur Basisuntersuchung erhöht, während in der Placebogruppe keine signifikanten Änderungen auftraten [64]. Patienten, bei denen bereits eine Katarakt diagnostiziert worden war, zeigten eine verbesserte Sehschärfe nach Luteingabe [54].
Die bisherige Datenlage spricht dafür, dass Lutein und Zeaxanthin den Verlauf der AMD und der Katarakt positiv beeinflussen, sodass sie in der Prävention und Therapie dieser Augenerkrankungen von Nutzen sein können. Um die potenziellen Wirkungen dieser Carotinoide nachzuweisen, wären langfristig angelegte, prospektive Interventionsstudien wünschenswert [47]. Bei Personen, die unter AMD oder Katarakt leiden oder ein erhöhtes Risiko für diese Erkrankungen aufweisen, ist ein regelmäßiger Verzehr lutein- und zeaxanthinreicher Gemüsesorten wie z.B. Spinat, Grünkohl, grüne Salate sowie Mais und gegebenenfalls eine Supplementierung dieser beiden Carotinoide wünschenswert.
Sauerstofffreie Carotinoide
wie Alpha-, Beta-Carotin
sowie Lycopin finden sich in
gelben und roten Gemüsesorten
in hoher Konzentration.
Phytosterole – Cholesterolsenkung ohne Nebenwirkungen?
Eine außerordentlich hohe Evidenz basierend auf zahlreichen randomisierten, plazebokontrollierten Studien besteht für die Wirksamkeit der Phytosterole bei der Senkung der Serum-Cholesterolkonzentration. Gemeinsames Merkmal der Phytosterole ist ihr Sterol-Grundgerüst, wodurch sich ihre Ähnlichkeit zum Cholesterol erklärt. Von den ca. 40 bekannten Phytosterolen ist Beta-Sitosterol der quantitativ bedeutsamste Vertreter. Phytosterole finden sich vorwiegend in fettreichen Pflanzenteilen wie Samen und Nüssen.
Nach wie vor nicht vollständig geklärt ist der Mechanismus des cholesterolsenkenden Effektes. Vermutlich basiert die hypocholesterämische Wirkung neben möglicher systemischer Effekte auf die hepatische Cholesterolsynthese vor allem auf einer Hemmung der Cholesterolabsorption: Phytosterole verringern die Löslichkeit von Cholesterol in der Fett- und mizellären Phase und hemmen so kompetitiv die Aufnahme von Cholesterol in Mizellen [52, 60].
Da Phytosterole hydrophober sind als das Cholesterolmolekül, weisen sie eine höhere Affinität zu den Mizellen auf [40]. In mehreren klinischen Studien wurde nachgewiesen, dass die Aufnahme von 2 bis 3 g Phytosterol- oder Phytostanolestern in Form von angereicherter Margarine das Gesamt-Serumcholesterol sowie das LDL-Cholesterol nach 3 bis 4 Wochen verglichen mit nicht-angereicherter Margarine um bis zu 15% senkt [57]. Wie verschiedene Untersuchungen übereinstimmend belegen, werden die HDL- und Triglyzeridkonzentrationen hingegen nicht beeinflusst [23, 77].
Obgleich die toxikologische Sicherheit von Phytosterolen in Untersuchungen nachgewiesen wurde [26, 39], kann insbesondere die beobachtete Verminderung der Absorption von Vitamin E und Beta-Carotin bei langfristiger Zufuhr von Nachteil sein. So zeigte sich in einer neueren Untersuchung, dass es bei Verabreichung von 2,2 g Phytosterolen täglich zu einer Verminderung der Absorption von Beta-Carotin um 50% und von Vitamin E um 20% kommt [63].
Die Verwendung von phytosterolangereicherten Lebensmitteln zur Senkung der Cholesterolkonzentration ist insbesondere dann eine Option, wenn andere diätetische Maßnahmen wie die Modifikation des Fettverzehrs und ein erhöhter Konsum ballaststoffreicher Lebensmittel nicht zum Erfolg führten. Dabei sollte jedoch nicht die ganze Palette an Lebensmitteln, die inzwischen mit Phytosterolen angeboten wird, gleichzeitig konsumiert werden, sondern gezielt einzelne Produkte wie Margarine oder Joghurt ausgewählt und regelmäßig verzehrt werden. Gleichzeitig ist auf eine vollwertige Ernährung mit einem hohen Anteil an Gemüse, Vollkornprodukten und Nüssen zu achten.
Phytoöstrogene – Einteilung und Stoffwechsel
Unter dem Begriff Phytoöstrogene werden mehrere, chemisch den Polyphenolen zuzurechnende Stoffklassen mit östrogener Aktivität zusammengefasst. Allen Substanzen gemeinsam ist ihre strukturelle Ähnlichkeit zu 17-beta-Östradiol und eine hierauf zurückzuführende Interaktion mit Östrogenrezeptoren. Sie ist Grundlage für die ernährungsphysiologischen Wirkungen der verschiedenen Phytoöstrogene. Neben den nachfolgend dargestellten Isoflavonen gehören hierzu die weit verbreiteten und besonders reich in Vollkornprodukten und Ölsaaten zu findenden Lignane sowie die Coumestane, die beispielsweise in Sojasprossen vorkommen und in der Ernährung nur eine geringe Rolle spielen.
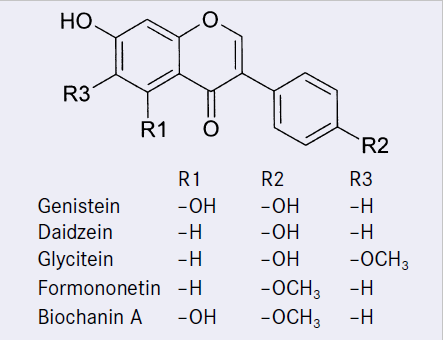
Isoflavone finden sich überwiegend in Fabacae-Arten und Leguminosen. Quantitativ bedeutendste Nahrungsquelle ist die Sojabohne; sie enthält je nach Sorte und Anbaubedingungen Isoflavongehalte von 120 bis 300 mg/100 g [81]. Dabei treten die Isoflavone Genistein, Daidzein und Glycitein etwa im Verhältnis 10 : 8 : 1 auf (Abb. 2).
Ein wesentliches Kriterium für die ernährungsphysiologischen Effekte der Isoflavone ist neben ihrem Gehalt in Lebensmitteln auch ihre Bioverfügbarkeit. Bislang galten die Isoflavon-Glycoside als nicht im Dünndarm hydrolisierbar. Entsprechend wurde postuliert, dass sie erst durch mikrobielle Enzyme im Dickdarm gespalten und daher nur in geringem Umfang absorbiert würden. Neuere Untersuchungen zeigen allerdings, dass die intakten Isoflavon-Glykoside bereits im Dünndarm über den für den Glucosetransport verantwortlichen natriumabhängigen Carrier (SGLT-1) absorbiert werden [74].
Ob die Bioverfügbarkeit von Isoflavon-Glykosiden und -Aglykonen wesentlich differiert, ist nicht abschließend geklärt [36]. Untersuchungen zur Biokinetik der Aglykone und der natürlich vorkommenden Glykosidderivate konnten zeigen, dass die Aglykone zwar schneller absorbiert werden als die Glykoside, inwieweit die Gesamtverfügbarkeit unterschiedlich ist, bleibt aber unklar.
Nach ihrer Absorption gelangen die Isoflavone und ihre Metaboliten über die Pfortader zur Leber und werden dort in Phase-II-Reaktionen überwiegend mit Glucuronsäure, Sulfat und Glycin konjugiert. Diese Konjugate werden im Blut transportiert und zum überwiegenden Teil renal, zu einem kleineren Teil biliär ausgeschieden. Darüber hinaus erfolgt bei Isoflavonen auch eine Hydroxylierung durch Cytochrom-P450-abhängige Monooxygenasen, sodass entsprechende Derivate im Harn nachweisbar sind [15, 36].
Analog zu den Steroidhormonen unterliegen die biliär ausgeschiedenen Isoflavone einem enterohepatischen Kreislauf. Im Dickdarm können nicht absorbierte oder über die Galle sezernierte Isoflavone durch die Darmflora metabolisiert werden. Dabei entsteht aus Daidzein O-Desmethylangolensin oder das Isoflavon Equol, dessen Bildung in Abhängigkeit von der Zusammensetzung der Kolonflora starken interindividuellen Schwankungen unterliegt.
So ist etwa ein Drittel der Erwachsenen nicht zur Equolbildung befähigt, was insofern bedeutsam ist, da dieser Metabolit eine besonders hohe Östrogenaktivität aufweist. Untersuchungen haben ergeben, dass die mittlere Isoflavon-Plasmakonzentration bei Asiaten mit traditioneller Ernährung bei etwa 870 nM liegt, bei Europäern hingegen nur ca. 50 nM beträgt. Im Tiermodell zeigte sich, dass Isoflavone bevorzugt in Brustgewebe, Eierstöcken und Uterus bzw. bei männlichen Tieren in der Prostata eingelagert werden [36].
Wirkmechanismen
Wie bereits erwähnt, üben Phytoöstrogene typische endokrine Effekte aus, die qualitativ denen der körpereigenen Östrogene vergleichbar sind. Dabei ist die östrogene Wirkung um den Faktor 100 bis 10.000 geringer als die des 17-beta-Östradiols [36]. Allerdings kann auch die Konzentration der Phytoöstrogene im Organismus um bis zu 10.000fach über der von körpereigenen Steroiden liegen.
Inzwischen konnten zahlreiche Wirkprinzipien von Phytoöstrogenen identifiziert werden (s. Kasten). So sind die Substanzen in der Lage, sowohl östrogene als auch antiöstrogene Wirkungen zu entfalten, wobei der vorherrschende Effekt von der individuellen Menge zirkulierender endogener Östrogene sowie Anzahl und Typ der Östrogenrezeptoren abhängt [21]. In-Vitro-Untersuchungen mit Sojabohnenextrakten zeigen deutliche Östrogenaktivität über die Östrogenrezeptoren alpha (ER-alpha) und beta (ER-beta) sowie eine Affinität zum Progesteronrezeptor und Androgenrezeptor [6, 5]. Die ausgeprägteste Fähigkeit, die Transkription zu induzieren, besitzt der aus Daidzein gebildete Metabolit Equol, dem deshalb ein besonderer Stellenwert zugemessen wird. Immerhin entspricht dessen Aktivität etwa 50% derer von 17-beta-Östradiol [46].
Ob Isoflavone östrogene oder antiöstrogene Wirkung entfalten, hängt von der Verteilung von ER-alpha und ER-beta in den verschiedenen Geweben sowie von der Konzentration endogener Östrogene ab. So findet sich ER-alpha vor allem in den Zellen von Brustdrüse, Uterus und Leber, wohingegen ER-beta in Knochen, Gehirn, Blutgefäßen, Ovarien, Lunge und Urogenitaltrakt vorherrscht. Hierdurch erklärt sich, dass Phytoöstrogene gewebespezifisch unterschiedlich wirken [21, 35, 66].
In-Vitro-Untersuchungen zeigen, dass Phytoöstrogene als ER-Agonisten und ER-Antagonisten fungieren können und dementsprechend in vivo gewebetypische ER-agonistische oder -antagonistische Aktivität ausüben. Welche Eigenschaften die Phytoöstrogene im jeweiligen Gewebe entfalten, hängt auch von liganden-induzierten Konformationsänderungen am Rezeptor ab, die gewebespezifisch die Genexpression und die physiologische Antwort modulieren können [65]. Jüngst publizierte In-Vitro-Untersuchungen mit humanen Endometrium-Zellen bestätigen das östrogene und antiöstrogene Potenzial von Phytoöstrogenen an beiden Rezeptortypen [48].
Offenbar wirken Isoflavone bei postmenopausalen Frauen mit niedrigen endogenen Östrogenspiegeln eher als Östrogenagonisten, während sie bei prämenopausalen Frauen mit hohen E2-Konzentrationen östrogen-antagonistische Eigenschaften ausüben, indem sie mit E2 um die Bindungsstelle am Rezeptor konkurrieren und diesen kompetitiv hemmen [81]. Aufgrund dieser Wechselwirkungen ergeben sich verschiedene gesundheitliche Wirkungen von Phytoöstrogenen (s. Kasten). Ein für die Apothekenpraxis besonders bedeutsamer Aspekt betrifft die Beeinflussung menopausaler Beschwerden.
Wirkungen von Phytoöstrogenen [79]
- Bindung an Östrogenrezeptoren vom Typ alpha und beta, bevorzugte Bindung an beta-Rezeptoren
- Induktion der Transkription nach Bindung an Östrogenrezeptoren
- Stimulation der Synthese von sexualhormonbindendem Globulin (SHBG) in der Leber
- Modulation von Enzymaktivitäten (Hemmung der Aktivität der 5alpha-Reduktase und der 17-beta-Hydroxysteroiddehydrogenase, die beide an der Androgensynthese beteiligt sind)
- Modulation von Cytochrom-P450-Enzymen und damit u. a. Beeinflussung der Kanzerogenaktivierung [67] und des Vitamin-D-Metabolismus
- Antioxidative Wirkung, Hemmung der LDL-Oxidation
- Antiandrogene Wirkungen
- Beeinflussung der Zellproliferation
- Modulation der Signaltransduktion, insbesondere Hemmung der Tyrosinkinase als vermuteter antikarzinogener Wirkmechanismus
- Hemmung der Synthese von TNF-alpha
- Antithyreoidale Eigenschaften (Hemmung der TSH-Sekretion; Verminderung der Peroxidaseaktivität in der Schilddrüse)
Östrogenmangel und klimakterische Beschwerden
Untersuchungen belegen die Wirkung von Phytoöstrogenen bei Beschwerden, wie sie typischerweise Frauen in den Wechseljahren betreffen. Mit der menopausalen Reduktion der Östrogenspiegel ergeben sich eine Reihe physiologischer Veränderungen, die sich in Form von Hitzewallungen, Schweißausbrüchen, atrophischer Vaginitis und vaginaler Trockenheit manifestieren [37]. Zudem entfällt der Einfluss der Östrogene auf die Osteoblasten, sodass sich das Osteoporoserisiko erhöht bzw. vorhandene Symptome der Osteoporose verstärken.
Als besonders unangenehm empfunden werden die in Form von "hot flashes" auftretenden vasomotorischen Symptome, hervorgerufen durch eine Überaktivität des hypothalamischen GnRH-Pulsgenerators. Da aufgrund des Östrogenmangels die negative Rückkopplung dieses Hormons zum Hypothalamus fehlt, werden Neurotransmitter freigesetzt, die GnRH-Neurone stimulieren. Dabei kommt es synchron auch zur Aktivierung benachbarter hypothalamischer Neurone, die das Temperatur- und das Herz-Kreislauf-Zentrum regulieren. Als Konsequenz treten Tachykardien sowie Hitzewallungen und Schweißausbrüche auf. Dementsprechend erfolgt die pulsatile LH-Ausschüttung synchron mit den "hot flashes" und eine Reduktion der Höhe der LH-Pulse deutet auf eine Anti-hot-flash-Wirksamkeit von östrogenwirksamen Substanzen hin [80].
Einfluss von Phytoöstrogenen
Das Auftreten klimakterischer Beschwerden scheint interkulturell zu variieren. So berichten japanische Frauen seltener über menopausale Symptome wie Hitzewallungen als kanadische Frauen. Gleichzeitig gaben nur 4% der japanischen Frauen an, Östrogene als Hormonersatztherapie zu verwenden, während 30% der US-amerikanischen Frauen sich einer Hormonersatztherapie mit Östrogenen unterzogen. Obwohl für diese Unterschiede vielfältige Ursachen in Frage kommen, spricht die Datenlage dafür, dass die geringere Häufigkeit menopausaler Beschwerden bei Japanerinnen auf die schwach östrogene Wirkung einer phytoöstrogenreichen Kost zurückzuführen ist [11, 32, 37].
So zeigte sich bei japanischen Frauen nach der Korrektur um Störvariablen, dass die Aufnahme von Sojaprodukten oder Isoflavonen negativ mit dem Auftreten von "hot flashes" korreliert [51]. Das relative Risiko für "hot flashes" lag im Tertil mit der höchsten Isoflavonaufnahme (51 mg/d) bei 0,42 verglichen mit dem Tertil mit der niedrigsten Zufuhr (20 mg/d).
Interventionsstudien mit Phytoöstrogenen
Um die Wirksamkeit von Isoflavonen zur Linderung klimakterischer Beschwerden zu untersuchen, wurden zahlreiche Interventionsstudien mit Frauen in der Peri- und Postmenopause durchgeführt [78]. Dabei zeigt sich in den meisten Untersuchungen eine signifikante Verminderung klimakterischer Beschwerden, insbesondere der Hitzewallungen, wenn die Symptome vor und nach der Interventionsphase verglichen wurden. Interessanterweise ergab sich in vielen Studien auch in der Plazebogruppe eine Reduktion menopausaler Symptome [17, 34, 71].
Ein Beispiel hierfür liefert die Untersuchung von Murkies et al. [50], in der sich in der Sojagruppe eine Verminderung der "hot flashes" um 40% gegenüber einer Reduktion um 25% in der Plazebogruppe ergab. Hierdurch waren die Unterschiede zwischen Verum- und Placebogruppe häufig nicht signifikant. Die unterschiedlichen Studienergebnisse sind wesentlich methodisch begründet, sodass die Studien vielfach nicht vergleichbar sind. Dies dokumentiert sich z. B. darin, dass unterschiedliche Inhaltsstoffe zum Einsatz kamen.
So fanden in den Studien unterschiedliche Inhaltsstoffe wie verschiedene Sojazubereitungen oder auch weitgehend isolierte Isoflavone in variierenden Dosierungen Verwendung. Zudem ist insbesondere bei Verwendung von Sojaextrakten zu berücksichtigen, dass diese je nach eingesetztem Rohmaterial und technologischem Verfahren unterschiedliche Gehalte und Relationen an Isoflavonen aufweisen. So kann insbesondere das Verhältnis von Daidzein, Genistein und Glycitein zueinander wie auch der Gesamtisoflavongehalt in den verschiedenen Extrakten stark variieren [72].
Insbesondere aber differierten die einzelnen Studienkollektive in qualitativer und quantitativer Hinsicht. Besonders im Hinblick auf den menopausalen Status der Probandinnen ergeben sich Unterschiede, da in einigen Studien nur perimenopausale in anderen nur postmenopausale Frauen und in wiederum anderen peri- und postmenopausale Frauen jeweils mit unterschiedlich schweren Symptomen eingeschlossen waren.
Mögliche Nebenwirkungen von Isoflavonen
Phytoöstrogene sind ein typisches Beispiel dafür, dass die Wirkung von Lebensmittelinhaltsstoffen differenziert zu betrachten ist. So wurden Bedenken geäußert, dass insbesondere bei Frauen mit erhöhtem Brustkrebsrisiko oder vorhandenem Mammakarzinom prokarzinogene Effekte von Phytoöstrogenen überwiegen könnten [1]. Zwar konnte das Tumorzellwachstum nach Implantation von MCF-7-Brustkrebszellen in ovarektomierten Mäusen durch Gabe von Genistein induziert werden [30].
Allerdings zeigten Versuche mit Nagern, dass Soja bzw. isolierte Isoflavone bei Tieren mit chemisch induziertem Mammakarzinom überwiegend protektive Wirkung entfalteten oder keinen negativen Effekt besaßen [42]. Aufgrund der kompetitiven Wirkung der Isoflavone am Östrogenrezeptor wurden insbesondere bei prämenopausalen Frauen antikanzerogene Effekte der Substanzgruppe im Hinblick auf das Mammakarzinom postuliert [14, 41]. Dies gilt aber offenbar lediglich bei Frauen, die bereits in der Jugend Phytoöstrogene verzehrten oder sehr hohe Dosierungen aufnahmen [59].
Humanstudien deuten darauf hin, dass Soja schwach östrogene Effekte auf die Brust ausübt [25, 44, 61]. Inzwischen wurde in einer tierexperimentellen Arbeit gezeigt, dass verarbeitete Sojaprodukte und isolierte Isoflavone die Zellproliferation von MCF-7-Brustkrebszellen stärker induzieren als unverarbeitete Sojaprodukte, sodass der Verzehr von Sojaprodukten aus toxikologischer Sicht sicherer zu sein scheint als die Supplementierung isolierter Isoflavone [2].
Zusammenfassend lässt sich bei Sojaisoflavonen bislang nicht abschließend beurteilen, ob und in welcher Dosierung diese zu einer Erhöhung bzw. Senkung des Brustkrebsrisikos bei postmenopausalen Frauen führen [45, 59]. Deutliche Bedenken bestehen bei der Gabe hochdosierter Isoflavone. Diese betreffen auch die Proliferation des Endometriums. Eine jüngst publizierte randomisierte, plazebokontrollierte Studie mit 298 postmenopausalen Frauen zeigte nach fünfjähriger Behandlungsdauer mit 150 mg Isoflavonen pro Tag ein signifikant höheres Auftreten einer endometrialen Hyperplasie in der Isoflavongruppe im Vergleich zur Plazebogruppe [70].
Demgegenüber gilt die langfristige Verwendung von Dosierungen in einer Größenordnung von 50 mg/d in toxikologischer Hinsicht als unproblematisch [5]. Sie entsprechen auch der erfahrungsgemäß unbedenklichen Isoflavonzufuhr (ca. 47 ± 23 mg/d, [3]), wie sie bei einer üblichen asiatischen Ernährung erreicht wird. Ältere Angaben zu einer deutlich höheren durchschnittlichen Isoflavonaufnahme gelten inzwischen als widerlegt [67]. Anders gestaltet sich die Sicherheitsbewertung von Isoflavonen nach dem derzeitigen Kenntnisstand bei Frauen mit östrogenrezeptorpositivem Mammakarzinom oder Endometriumkarzinom. Diesen Personengruppen ist aus Sicherheitsgründen schon mit Blick auf das im Lebensmittelrecht geltende Vorsorgeprinzip von einer Verwendung Isoflavon-haltiger Präparate abzuraten.
Phytoöstrogene – Empfehlungen für die Praxis
Für die Beratung in der Apotheke stellt sich vor dem Hintergrund der wissenschaftlichen Datenlage die Frage, ob Soja-Isoflavon-haltige Präparate zur diätetischen Beeinflussung von Wechseljahresbeschwerden empfohlen werden können. In einigen klinischen Studien hat sich gezeigt, dass derartige Produkte in der Lage sind, das Beschwerdebild positiv zu beeinflussen. Da mit der Verwendung von Soja-Isoflavonen in ernährungsüblichen Dosierungen bei gesunden Personen keine unerwünschten Nebenwirkungen verbunden sind, ist ihr Einsatz insbesondere bei stärkeren menopausalen Beschwerden eine diätetische Behandlungsoption.
Aus ernährungsphysiologischer Sicht nützlich sind dabei insbesondere Präparate, die neben physiologischen Dosierungen von Soja-Isoflavonen auch kritische Nährstoffe wie z. B. Vitamin D (vgl. DAZ Nr. 2f/2005, S. 49 f) und Calcium enthalten, die im Hinblick auf die Prävention und Therapie der menopausalen Osteoporose bedeutsam sind. Demgegenüber ist die langfristige Einnahme höher dosierter Präparate im Bereich von 100 mg/d und mehr beim derzeitigen wissenschaftlichen Kenntnisstand wegen der nicht abschließend geklärten Risiken nicht empfehlenswert.
Wie bereits oben dargestellt, sollten Frauen mit Mamma- und Endometriumkarzinom oder einem erhöhten Risiko für diese Erkrankungen aufgrund neuerer Studien generell von der Verwendung entsprechender Präparate absehen bzw. diese nur nach Anweisung ihres Arztes einnehmen.
Korrespondenzautor:
Prof. Dr. Andreas Hahn
Universität Hannover, Institut für Lebensmittelwissenschaft
Abteilung für Ernährungsphysiologie und Humanernährung
Wunstorfer Str. 14, 30453 Hannover
Tel: (05 11) 7 62-50 93, Fax: (05 11) 7 62-57 29
E-Mail: andreas.hahn@lw.uni-hannover.de
Literatur
[10] Blodi, B.A.: Nutritional supplements in the prevention of agerelated
macular degeneration. Insight. 29, 15 – 16 (2004).
[18] Davies, N.P., Morland, A.B.: Macular pigments: their characteristics
and putative role. Prog. Retin. Eye. Res. 23, 533 – 59 (2004).
[21] Glazier, M.G., Bowman, M.A.: A review of the evidence
for the use of phytoestrogens as a replacement for traditional
estrogen replacement therapy. Arch. Intern. Med. 161, 1161 –
1172 (2001).
[36] Kulling, S.E., Watzl, B.: Phytoöstrogene. Ernährungs-Umschau.
50: 234 – 239 (2003).
[43] Mares-Perlman, J.A., Millen, A.E., Ficek, T.L., Hankinson,
S.E.: The body of evidence to support a protective role for lutein
and zeaxanthin in delaying chronic disease. Overview. J.
Nutr. 132, 518 – 524 (2002).
[53] N.N.:Treatment of menopause-associated vasomotor symptoms:
position statement of The North American Menopause
Society. Menopause. 11, 11 – 33 (2004).
[59] Peeters, P.H., Keinan-Boker, L., van der Schouw, Y.T., Grobbee,
D.E.: Phytoestrogens and breast cancer risk. Review of
the epidemiological evidence. Breast. Cancer. Res. Treat. 77,
171 – 183 (2003).
[61] Petrakis, N.L., Barnes, S., King, E.B., Lowenstein, J., Wiencke,
J., Lee, M.M., Miike, R., Kirk, M., Coward, L.: Stimulatory
influence of soy protein isolate on breast secretion in preand
postmenopausal women. Cancer. Epidemiol. Biomarkers.
Prev. 5, 785 – 794 (1996).
[78] Wolters, M., Hahn, A.: Sojaisoflavone in der Therapie menopausaler
Beschwerden. Ernährungs-Umschau. 51, 440 – 445
(2004).
[81] Zittermann, A.: Phytoöstrogene. Zentralbl. Gynäkol. 125,
195 – 201 (2003).
Das vollständige Literaturverzeichnis finden Sie in der Online-Ausgabe
der DAZ unter www.deutsche-apotheker-zeitung.de ;
Benutzername: apotheke






















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.