
- DAZ.online
- DAZ / AZ
- DAZ 17/2005
- Viergliedrige Ringe
Chemie
Viergliedrige Ringe
Ringspannung, Reaktivität
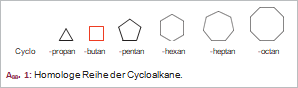
Cyclobutan, der Prototyp molekularer viergliedriger Ringe ist die Nummer zwei einer homologen Reihe gesättigter cyclischer Kohlenwasserstoffe (Abb. 1). Diese weisen in Abhängigkeit von der Ringgliederzahl Unterschiede in Ringstabilität, Reaktivität und Bildungstendenz auf. Die Bindungswinkel an den C-Atomen des Cyclobutans weichen vom normalen Tetraederwinkel, der bekanntlich 109° 28' beträgt, mit einer Deformation von 9° 44' deutlich ab. Nach der Baeyerschen Spannungstheorie bedingt das Zusammendrücken des Bindungswinkels eine erhebliche positive Spannung, die sich in der Ausbildung eines energiereichen Bindungssystems äußert. Das heißt: Cyclobutan-Derivate sind sehr reaktionsfähig, instabil und schwer zu synthetisieren.
Dagegen ist die Ringspannung im Cyclopentan und Cyclohexan vernachlässigbar gering. Bei höhergliedrigen Ringen mit entsprechend größer werdenden Bindungswinkeln steigt sie allmählich als negative Spannung wieder an. Aufgrund der leichten Bildungstendenz fünf- und sechsgliedriger Ringe sind solche bei Naturstoffen sehr häufig anzutreffen, während Cyclopropan- und Cyclobutan-Derivate relativ selten sind.
Sekundäre Naturstoffe Terpene
Alicyclische Verbindungen sind besonders unter den Terpenen zu finden. Ein monocyclisches Monoterpen mit Cyclobutanring ist Grandisol (Abb. 2), das Sexualpheromon der Männchen des Baumwollkapselkäfers (Anthonomus grandis). Sein C-1-Epimer, das Fragranol (Abb. 2), von dem bisher keine vergleichbare biologische Aktivität bekannt ist, wurde aus den Wurzeln der Beifuß-Art Artemisia fragrans isoliert.
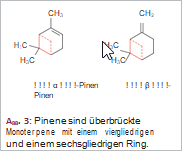
Bicyclische Monoterpene mit Cyclobutan-Struktur sind die verschiedenen Derivate des α-Pinens und β-Pinens (Abb. 3), die in den ätherischen Ölen der meisten Koniferen vorkommen, und die davon abgeleiteten Pinenole (z.B. Chrysanthenol, Verbenol, Myrtenol) und Pinenone.
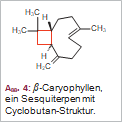
Ein Sesquiterpen mit Cyclobutan-Struktur ist das β-Caryophyllen (Abb. 4), das im Gewürznelkenöl und im Wacholderbeerenöl vorkommt. An der erfolgreichen Selbstmedikation akuter Zahnschmerzen mit Nelkenöl dürfte es kaum beteiligt sein. Vielmehr kommt es durch die lokalanästhesierende Wirkung des Hauptinhaltsstoffs Eugenol zu vorübergehender Schmerzlinderung.
Anemone pulsatilla und andere Ranunculaceen produzieren als Sekundärstoff das Anemonin (Abb. 5). Betrachtet man die in die Papierebene projizierte Formel, so entsteht der Eindruck einer spiegelsymmetrischen Verbindung. Dreidimensional gesehen ist das nicht so, was in der Stereoformel zum Ausdruck kommt. Schuld daran sind zwei stereogene Zentren in Form zweier asymmetrisch substituierter C-Atome. Das Geheimnis, das im Bereich der molekularen Chiralität anzusiedeln ist, beruht auf der Bildung aus zwei Molekülen Protoanemonin, das primär biosynthetisiert wird und das als reaktionsfähiges Di-en-on zum symmetrischen Anemonin nach Art einer Cycloaddition dimerisiert, wobei es zwei stereochemisch verschiedene Möglichkeiten der Cyclisierung gibt (Abb. 5).
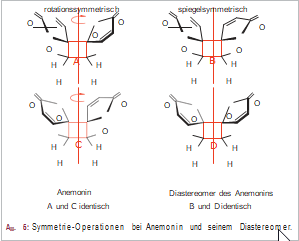
Die Formel des Anemonins enthält zwei asymmetrisch substituierte C-Atome. Also müssten formal vier Stereoisomere möglich sein. Wie jedoch aus Abbildung 6 hervorgeht, sind die dreidimensionalen Formen A und C identisch. Beide können durch Rotation in der Vertikalen um 180° ineinander überführt werden. Ebenso sind B und D identisch, was sich aus horizontalem Umklappen ergibt.
Fazit: Die symmetrische Anordnung zweier Asymmetriezentren in einem (symmetrischen) Molekül vermindert die zu erwartende Zahl der Stereoisomeren auf die Hälfte.
Oxetan und Derivate
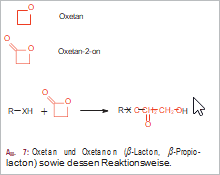
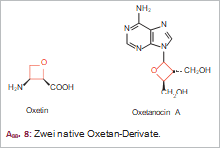
Ersetzt man im Cyclobutan eine CH2-Gruppe durch ein O-Atom, resultiert das Oxetan. Davon abgeleitet ist das Oxetan-2-on oder β-Propiolacton (Abb. 7). Unter den wenigen als sekundäre Naturstoffe bekannt gewordenen Oxetan-Derivaten sind zwei erwähnenswert, das Oxetin und das Oxetanocin A. Oxetin (Abb. 8) ist eine nichtproteinogene Aminosäure, die von einer Streptomyces-Art produziert wird, antibakterielle und herbizide Eigenschaften besitzt und einen nichtkompetitiven Inhibitor der Glutamin-Synthase darstellt. Oxetanocin A (Abb. 8), ein Oxetanyl-Adenin-Derivat, ist ein Nucleosid-Antibiotikum aus Bacillus megaterium mit antibakteriellen und beachtlichen antiviralen Eigenschaften.
Oxetanocine und synthetische Analoga hemmen die reverse Transkriptase von Retroviren und werden derzeit gegen HIV, Zytomegalievirus (CMV) und Herpes-simplex-Virus (HSV) getestet. β-Propiolacton (Abb. 7) wird ähnlich wie Ethylenoxid zur "chemischen Sterilisation" eingesetzt. Es inaktiviert Bakterien, Pilze, Phagen und Viren und kann zu den Desinfektionsmitteln gezählt werden. Es wurde zur Sterilisierung von Blutkonserven verwendet und dient heute zur Kaltentkeimung von Drogen. Infolge der Baeyer-Spannung ist β-Propiolacton ein sehr aktives Acylierungsmittel, das mit allen nucleophilen Gruppen zu 3-Hydroxypropionyl-Derivaten reagiert (Abb. 7). Im Tierversuch erwies es sich als potentes Carcinogen.
Lipase-Hemmstoffe
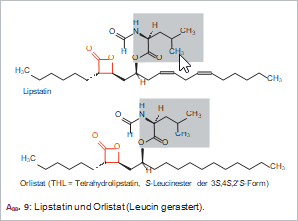
Seit kurzem steht zur Behandlung adipöser Patienten der synthetische Lipasehemmer Orlistat zur Verfügung (Abb. 9). Durch Hemmung der fettverdauenden Triacylglycerin-Lipasen, speziell der Pankreas-Lipase, kommt es zu einer um etwa 30% verminderten Absorption der Nahrungsfette bzw. deren Spaltprodukte (Mono- und Diglyceride). Die Aufnahme freier Fettsäuren wird nicht beeinflusst.
Orlistat (THL) ist das synthetisch leichter zugängliche Tetrahydro-Derivat des nativen Oxetans Lipstatin (Abb. 9), eines von Streptomyces toxytricini produzierten lipophilen, langkettigen Esters mit einem mittelständigen β-Lactonring und N-Formyl-l-Leucin als Seitenkette, der selbst schon einen spezifischen Lipase-Hemmstoff darstellt. Die relative Stabilität dieses β-Lactonrings steht im Zusammenhang mit der ausgeprägten Lipophilie der aliphatische Kette, in die er integriert ist.
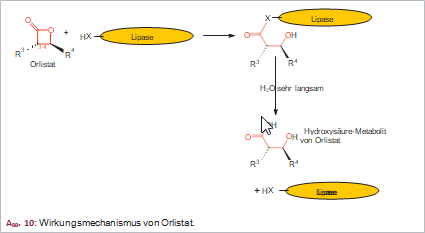
Wirkungsmechanismus. Die Enzymhemmung kommt durch Öffnung des β-Lactonrings und Veresterung eines Serinrestes im aktiven Zentrum der Lipasen zustande (Abb. 10). Danach ist das Enzym inaktiviert und nicht mehr in der Lage, die als Triglyceride vorliegenden Nahrungsfette in resorbierbare Fettsäuren und Monoglyceride zu hydrolysieren.
Orlistat wird bevorzugt in der Darmwand metabolisiert. Etwa 80% der verabreichten Gabe werden unverändert und etwa 15% als Metaboliten mit dem Stuhl ausgeschieden. Wird Orlistat, das die Resorption von Vitamin K beeinflusst, gleichzeitig mit Antikoagulanzien vom Hydroxycumarin-Typ verabreicht, so sind die Quick-Werte des Patienten zu überwachen.
Azetidin und Derivate
Ersetzt man im Cyclobutan eine CH2-Gruppe durch eine NH-Gruppe, so resultiert das Azetidin. Davon abgeleitet ist das Azetidin-2-on oder β-Lactam (Abb. 11).
Direkte Thrombin-Hemmstoffe
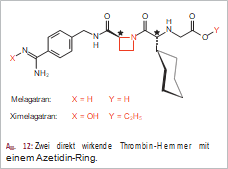
Die direkte Hemmung des Schlüsselenzyms der Blutgerinnung, des Thrombins, ist seit kurzem durch die neuen Wirkstoffe Melagatran und Ximelagatran möglich, die N-acylierte Azetidin-Derivate darstellen (Abb. 12). Die zur Therapie thromboembolischer Erkrankungen und insbesondere zur Vermeidung einer Zerebralthrombose (Schlaganfallprophylaxe) empfohlenen Wirkstoffe sind synthetische Dipeptide, von denen das eine, nämlich Ximelagatran, peroral anwendbar ist. Im Gegensatz zu den mit vielen Nachteilen behafteten Vitamin-K-Antagonisten (4-Hydroxycumarine) können die neuen Thrombin-Antagonisten in festgelegten Dosierungen verabreicht werden. Die Gerinnungswerte brauchen nicht überwacht zu werden und Interaktionen mit anderen Arzneistoffen sind nicht zu befürchten.
Melagatran und Ximelagatran sind reversible Thrombin-Inhibitoren, die mit hoher Selektivität am aktiven Zentrum des Thrombins binden. Melagatran wird vorzugsweise renal eliminiert und weist nach i.v. Gabe eine Halbwertszeit von etwa 1,7 Stunden auf. Ximelagatran ist ein Prodrug, das bei neutralem pH-Wert ungeladen vorliegt. Die intestinale Resorption ist im Vergleich mit Melagatran etwa 100-mal besser.
Cholesterol-Resorptionshemmer
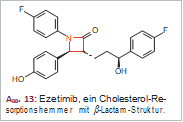
Mit Ezetimib (Abb. 13), einem dreifach substituierten β-Lactam, steht der erste Vertreter der neuen Wirkstoffklasse der Cholesterol-Resorptionshemmer zur therapeutischen Verfügung.
Ezetimib verhindert sowohl die Resorption des mit der Nahrung aufgenommenen Cholesterols als auch die Wiederaufnahme des endogenen Cholesterols aus dem enterohepatischen Kreislauf. Der Wirkstoff wurde ursprünglich als ACAT-Inhibitor (Acyl-CoA-Cholesterol-O-Acyltransferase) entwickelt. Die Hemmung der Cholesterol-Resorption in vivo beruht jedoch nicht auf der ACAT-Hemmung. Das Target des Wirkstoffs ist noch nicht genau bekannt. Es wird vermutet, dass Ezetimib Cholesterol-Transporter blockiert.
Die Anwendung des Wirkstoffs führt v. a. zur Reduktion des LDL-Cholesterolspiegels. Ferner steigert Ezetimib die HDL-Cholesterolkonzentration und senkt den Triglyceridspiegel. Nach oraler Gabe wird der Wirkstoff rasch resorbiert und in einer Phase-II-Reaktion zu einem ebenfalls aktiven 4-Hydroxyphenyl-Glucuronid metabolisiert. Die Halbwertszeit beträgt ca. 22 h.
β-Lactam-Antibiotika
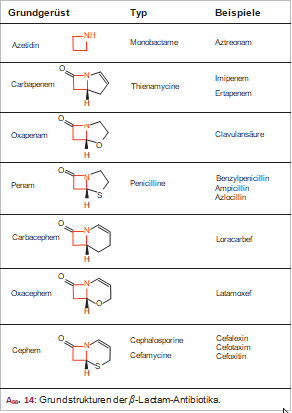
Die bekannteste Naturstoffgruppe mit viergliedrigen Ringen als essenzieller Partialstruktur sind die β-Lactam-Antibiotika. Durch das Hinzukommen einer hydrolysierbaren Funktion im β-Lactam-Ring erhöht sich im Vergleich mit dem Cyclobutanring die Reaktivität bzw. Labilität. Bekannt sind monocyclische und bicyclische β-Lactam-Antibiotika. Die Grundgerüste sind in Abbildung 14 mit Nennung bekannter Beispiele zusammengefasst. Diese tabellarische Synopse mag hier als Erinnerung an eine seit langem therapeutisch genutzte Arzneistoffgruppe genügen.
Um den intensiv untersuchten und zu Tausenden synthetisierten β-Lactam-Antibiotika einen kaum bekannten molekularen Exoten gegenüberzustellen, sei es erlaubt, das Charamin zu erwähnen (Abb. 15). Es ist ein sekundärer Naturstoff, eine antibiotisch wirksame quartäre N-Spiroverbindung, die den Azetidinring gleich zwei Mal enthält und von der im Süßwasser lebenden Armleuchteralge Chara globularis produziert wird.
Symmetrische Dimere mit Cyclobutanstruktur durch Photoaddition
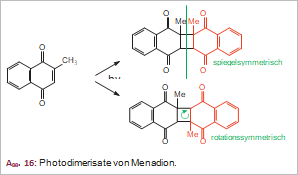
Verbindungen mit (photo)reaktiven Doppelbindungen neigen beim Bestrahlen mit Sonnenlicht oder UV-Licht zur Bildung dimerer Cyclobutan-Derivate. Die Photodimerisierung von Menadion (Vitamin K3) führt zu zwei unterschiedlichen, symmetrischen Produkten, von denen das eine spiegelsymmetrisch, das andere rotationssymmetrisch aufgebaut ist (Abb. 16).
Sonnenbaden und ein bisschen Photochemie
Dank der Fülle an Informationen aus dem überreichlichen Angebot an Printmedien spricht jeder Laie heute von "gutem und schlechtem Cholesterin". Ebenso könnte er von "guter und schlechter Sonne" reden. Ich meine nun nicht die Differenzierung des UV-Anteils in Strahlung der Wellenlänge zwischen 400 und 320 nm (UV-A), durch die eine Pigmentierung der Hautoberfläche angeregt wird, und Strahlung zwischen 320 und 280 nm (UV-B), die in tiefere Hautschichten dringt, dort die Bildung von Pigmenten verursacht, aber auch den Sonnenbrand auslöst und bei übertriebenem Sonnenbaden zu Hautkrebs führen kann.
Ich denke vielmehr an die willkommene Photolyse des körpereigenen Dehydrocholesterols zu Vitamin D3 (Colecalciferol), einem Produkt der "guten Sonne", und andererseits an eine photochemische Dimerisation, die an der DNA abläuft und dadurch zu Schäden führen kann ("schlechte Sonne"). Sonnenbräune ist "in", doch wegen des damit verbundenen Risikos, an Hautkrebs zu erkranken, warnen alle Hautärzte vor zu viel Sonne. Höchstwahrscheinlich ist die UV-geschädigte DNA daran beteiligt.
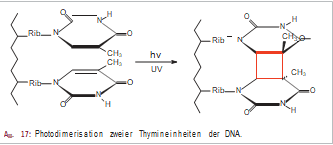
Die Dimerisierung zweier benachbarter Thyminreste bei UV-Bestrahlung der DNA ist häufig zu beobachten. Auch hier reagieren zwei Doppelbindungen unter Cycloaddition zu Cyclobutan-Derivaten (Abb. 17). Dabei wird die regelmäßige DNA-Helix-Geometrie partiell aufgehoben. Die typische Watson-Crick-Basenpaarung geht teilweise verloren. Die Konsequenz ist eine Störung der Replikation. Doch existieren zwei Arten von Reparatur-Mechanismen. Lichtabhängige Enzyme sind in der Lage, die entstandenen Photodimere wieder zu spalten. Lichtunabhängige Enzyme schneiden Fehlstellen aus der DNA heraus und bauen das fehlende Stück unter Nutzung des Basenmusters des unveränderten Gegenstrangs wieder ein.
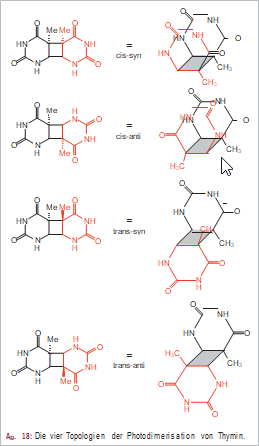
Bei Thymin (und Uracil, das dem gleichen photochemischen Schicksal ausgeliefert ist) sind prinzipiell vier Topologien der Dimerisierung zu unterscheiden, die zu verschiedenen und aus sterischen Gründen gefalteten Photoprodukten führen. Da die Photochemie aus den angeregten LUMOs (niedrigste nichtbesetzte Molekülorbitale) immer radikalisch verläuft, erscheint die maximale Anzahl von vier gepuckerten (d. h. gefalteten) Dimeren plausibel (Abb. 18).
Was von Fall zu Fall tatsächlich abläuft, d. h. welche der beiden wannenförmigen oder der beiden sesselartigen Dimeren entsteht, hängt von der gerade herrschenden Topologie der DNA während der UV-Bestrahlung ab. Vorsicht also bei intensivem Sonnenbaden, auch in unseren gemäßigten Breiten, besonders an der Küste und im Hochgebirge!
Die Sonne tut aber nicht nur dem Menschen gut und schlecht, sondern auch den Pflanzen. Für die Photosynthese ist ihre Strahlung essenziell, bei ausgeprägtem Wassermangel ist sie tödlich. Dazwischen liegen Reaktionen, bei welchen die eingestrahlte Sonnenenergie durch photochemische Umsetzungen genutzt oder unschädlich gemacht wird.
Klettern wir zur Illustration in die Anden Perus. Dort wächst der zur Ordnung Linales (Leinartige) zählende Coca-Strauch (Erythroxylum coca*), der in seinen Blättern das Sucht erzeugende Cocain produziert und akkumuliert. Dieses Alkaloid ist bekanntlich ein zweifacher Ester aus Ecgonin, Methanol und Benzoesäure. Der Strauch enthält aber auch reichlich Zimtsäure, die bei starker Sonneneinstrahlung photochemisch reagiert.
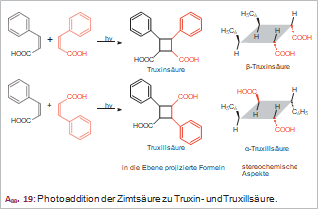
Die Zimtsäure ist ein Muster des unterschiedlich trans-disubstituierten Ethylens (Ethens) und weist keine Symmetrie auf. Doch sie neigt zur Photodimerisierung, wobei symmetrische Dicarbonsäuren entstehen, die je nach Substitutionsmuster als Truxinsäure oder Truxillsäure bezeichnet werden (Abb. 19). Verestert mit dem Methylester des Ecgonins, ergeben sie die Cocain-analogen Truxilline.
Eine Photodimerisierung nicht symmetrischer Ethylen-Derivate zu symmetrischen Cyclobutan-Derivaten kann prinzipiell bei allen entsprechend substituierten Ethylenen erfolgen, auch wenn sie in Isocyclen oder Heterocyclen eingebaut sind. Als Beleg für Isocyclen mit einer photoreaktiven Doppelbindung wurde Vitamin K3 (Menadion, Abb. 16), als Beispiel für Heterocyclen das Thymin (Abb. 17), das als Base in der DNA enthalten ist, herangezogen.
Die Truxinsäure erlaubt als Symmetrieoperation eine einfache Spiegelung, dagegen muss die Truxillsäure gedreht und gespiegelt werden, um wieder in sich selbst überzugehen. Räumlich sieht das so aus, dass in der Truxillsäure die Carboxylgruppen und die Phenylgruppen jeweils trans-ständig angeordnet sind, während in der Truxinsäure die beiden Phenylgruppen nach oben, die beiden Carboxylgruppen nach unten gerichtet sind.
Fußnote:
* Herrn Prof. Dr. Hans Möhrle, Düsseldorf, in freundlicher Verbundenheit zu seinem 75. Geburtstag gewidmet.
Literatur
Zu den neuen Arzneistoffen Lipstatin, Orlis- tat, Melagatran, Ximelagatran, Ezetimib und zu ß-Lactam-Antibiotika siehe:
D. Steinhilber, M. Schubert-Zsilavecz, H. J. Roth: Medizinische Chemie. Wissenschaftliche Verlagsgesellschaft, Stuttgart 2005. Oxetin: J. Antibiotics 37, 1324 – 1332 (1984); Chem. Pharm. Bull. 34, 3102 – 3110 (1986).
Oxetanocin: J. Antibiotics 42, 644 ff., 1308 – 1311, 1854 – 1859
(1989).
Charamin: J. Org. Chem. 52, 694 (1987); Experientia 40, 186
(1984).
Weitere Literatur beim Verfasser.
Anschrift des Verfassers:
Prof. Dr. rer. nat. Dr. h.c. H. J. Roth,
Friedrich-Naumann-Str. 33,
76187 Karlsruhe,
webmaster@h-roth-kunst.com,
www.h-roth-kunst.com
Originell, vielseitig, informativ
Die erste in der Deutschen Apotheker-Zeitung 1961 erschienene Publikation des damaligen Privatdozenten H. J. Roth am Institut für Pharmazeutische Chemie und Lebensmittelchemie der Technischen Hochschule Braunschweig trug den Titel: "Dreigliedrige Ringe mit pharmazeutisch-chemischer Bedeutung". Sie enthielt einige nicht alltägliche Aspekte. Mit dem heutigen Aufsatz erscheint die 50. Publikation von H. J. Roth in der DAZ, die zugleich gedankliche Brücken zu früheren Abhandlungen schlägt, Assoziationen weckt und den Leser zu mentalem Training herausfordert.
Alle Veröffentlichungen von H. J. Roth in der DAZ zeichneten sich durch hohe Informationsdichte, Originalität in der Themenwahl, Aktualität und lesenswerte bis humorvolle Formulierungen aus. Erwähnt seien an dieser Stelle
- der Aufsatz "Natürliche Wirkstoffe mit unwahrscheinlicher bis extravaganter Konstitution", in dem erstmals die Wortschöpfung "Spielkartensymmetrie" auftaucht (1972),
- die Abhandlung über Vitamin C "Olle Kamelle oder immergrüner Wirkstoff mit Zukunft" (1991),
- die Reflexionen über molekulare Symmetrie und Chiralität mit dem Titel "Johann Sebastian Bach – Louis Pasteur" (1996) sowie
- die Wortschöpfung "Glossay" (Essay à la Glosse oder Glosse à l'Essay), die bisher mit sieben Publikationen belegt ist und zuletzt die Frage beantwortete, ob Friedrich von Schiller ein Schnüffler war. Ein Glossay ist eine Publikation, die weit gehend im Stil einer Glosse formuliert ist, sich aber in der Sache an wissenschaftlich dokumentierte Fakten hält.
Denksportaufgabe (Zur Alzheimer-Prophylaxe geeignet)
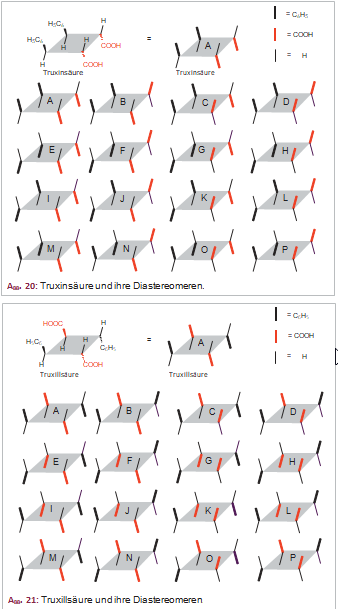
Da in Truxinsäure und Truxillsäure jeweils vier asymmetrisch substituierte C-Atome enthalten sind, sollten neben den symmetrischen Molekülen auch eine Reihe nicht symmetrischer Moleküle existieren.
Formal müssten 24 = 16 Stereoisomere zu erwarten sein. Wegen der symmetrischen Grundstruktur sind nach dem Prinzip Symmetrie versus Chiralität jedoch weitaus weniger realisierbar.
Wie viele sind es?
Um die Antwort zu finden, schauen Sie sich die Abbildungen 20 und 21 genau an.
Wer hier die Strukturen nicht nachvollziehen kann, möge das molekulare Spiel mithilfe von 16 quadratischen Bierdeckeln und einer ausreichenden Zahl an Halma-Spielkegelchen zweier verschiedener Farben aus der weniger anschaulichen zweidimensionalen Papierebene in den leichter zu beurteilenden dreidimensionalen Raum transponieren. Es geht auch mit kleinen quadratischen Kartonstückchen, die man mit roten und schwarzen Punkten auf der Ober- und Unterseite markiert. Auflösung auf Seite 72.
























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.