
- DAZ.online
- DAZ / AZ
- DAZ 48/2004
- Das Mammakarzinom, 2. ...
Onkologie
Das Mammakarzinom, 2. Teil: Medikamentöse Therapie
Leitlinien zur Primärtherapie
Eine wichtige Leitlinie zur Primärtherapie des Mammakarzinoms hat die St. Galler Konsensuskonferenz erstellt. Alle zwei Jahre findet diese Konferenz statt, um die Ergebnisse evidenzbasierter klinischer Studien mit großem Patientenkollektiv und langjährigem Follow-up zu analysieren, zu werten und hinsichtlich ihrer biologischen, klinischen, sozialen und persönlichen Relevanz für Brustkrebspatientinnen zu erörtern; daraufhin überarbeitet und aktualisiert eine Expertenkommission die Leitlinie – 2003 zum achten Mal [10].
Die im Juni 2004 aktualisierte interdisziplinäre Leitlinie der Deutschen Krebsgesellschaft und der beteiligten medizinisch-wissenschaftlichen Fachgesellschaften "Diagnostik, Therapie und Nachsorge des Mammakarzinoms der Frau" (S3-Leitlinie, d.h. vorläufige Endversion) basiert teilweise auf den Ergebnissen der St. Galler Konsensuskonferenz, befasst sich aber darüber hinaus mit der palliativen Behandlung und Nachsorge [15].
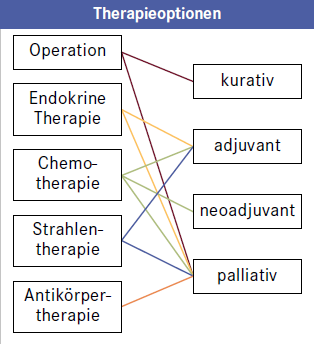
Tab. 1: Behandlungsziele und -maßnahmen in der Onkologie.
| Therapie | Ziel, Maßnahmen |
|---|---|
| palliativ | das Leiden der Patientin lindern, wenn eine Heilung nicht möglich ist |
| kurativ | die Patientin heilen |
| – adjuvant | medikamentöse Behandlung nach der chirurgischen Entfernung des Tumors |
| – neoadjuvant | medikamentöse oder radiologische Behandlung vor der Chemotherapie oder dem chirurgischen Eingriff |
| – Salvage | Maßnahmen nach einem Rezidiv |
Therapieempfehlung nach Risikogruppe
Die Therapieempfehlungen orientieren sich an prognostischen und prädiktiven Parametern (s. 1. Teil). Bei ER-negativen, nodalpositiven Patientinnen (hohes Risiko) sollte – deren Einverständnis vorausgesetzt – in jedem Fall eine Chemotherapie durchgeführt werden, bei ER-positiven Patientinnen je nach Menopausenstatus und individuellem Risiko eine endokrine Therapie oder deren Kombination mit einer Chemotherapie. Bei ER-positiven, nodalnegativen Patientinnen über 35 Jahren mit einem kleinen Tumor (minimales Risiko) ist eine Chemotherapie nicht indiziert, doch kann im Einzelfall eine endokrine Therapie sinnvoll sein (Tab. 2).
Tab. 2: Empfehlungen der St. Galler Konsensuskonferenz von 2003 für die medikamentöse Behandlung von Brustkrebspatientinnen in Abhängigkeit von Hormonrezeptorstatus, Menopausenstatus, Befall der Lymphknoten und sonstigen Risikofaktoren. Die in eckigen Klammern stehenden Empfehlungen werden noch im Rahmen von Studien untersucht [10].
| ER-positiv, prämenopausal | ER-positiv, postmenopausal | ER-negativ | |
| Nodalnegativ, minimales Risiko | Tamoxifen* oder nichts | Tamoxifen* oder nichts | nichts |
| Nodalnegativ, mittleres Risiko | GnRH-Analoga + Tamoxifen* [+/– Chemotherapie] oder Chemotherapie → Tamoxifen* [+/– GnRH-Analoga] oder Tamoxifen* oder GnRH-Analoga | Tamoxifen* oder Chemotherapie → Tamoxifen* | Chemotherapie |
| Nodalpositiv | Chemotherapie → Tamoxifen* [+/– GnRH-Analoga] oder GnRH-Analoga + Tamoxifen* [+/– Chemotherapie] | Chemotherapie → Tamoxifen* oder Tamoxifen* | Chemotherapie |
| * Gabe längstens fünf Jahre; in der Postmenopause Anastrozol bei Tamoxifen-Unverträglichkeit | |||
Endokrine Therapie
Das Wachstum des Mammakarzinoms ist bei Patientinnen mit positivem Rezeptorstatus – rund zwei Drittel aller Patientinnen – östrogenabhängig. Östrogene regen die Zellen des gesunden sowie des krebskranken Brustdrüsengewebes zur Teilung an, indem sie an deren Östrogenrezeptor (ER) binden und eine Signalkaskade auslösen. Ziel der endokrinen Therapie ist es, diese Wachstumsstimulation zu verhindern, und zwar durch
- eine Hemmung der Östrogensynthese, die prämenopausal durch GnRH-Analoga und postmenopausal durch Aromatasehemmer erfolgt,
- die Rezeptorblockade mit selektiven ER-Modulatoren (SERMs) und
- die Rezeptorreduktion mit selektiven ER-Downregulatoren (SERDs).
Eine endokrine Therapie ist weniger toxisch als eine Chemotherapie und dieser – sofern möglich – vorzuziehen; sie wird kurativ wie auch palliativ durchgeführt, am häufigsten bei postmenopausalen Patientinnen. Wie dabei vorzugehen ist, hängt unter anderem vom Menopausenstatus sowie von prognostischen und prädiktiven Faktoren ab. Bei negativem Rezeptorstatus ist eine endokrine Therapie nicht angezeigt (Tab. 2).
GnRH-Analoga: weniger Östrogene
GnRH- (Gonadorelin-)Analoga können die Funktion der Geschlechtsdrüsen völlig unterbinden; ihr Effekt entspricht dem einer Kastration. Sie sind bei ER-positiven prämenopausalen Patientinnen indiziert.
Aromatasehemmer: weniger Östrogene
Aromatasehemmer wie Exemestan (Aromasin®), Letrozol (Femara®) und Anastrozol (Arimidex®) blockieren die Aromatase, ein Enzym, welches die Umwandlung von Androgenen in Östrogene katalysiert. Vor der Menopause findet die Östrogensynthese hauptsächlich in den Eierstöcken statt (Abb. 2). In der Menopause stellen die Ovarien die Östrogenproduktion weitgehend ein. Postmenopausale Frauen decken ihren Östrogenbedarf durch Umwandlung zirkulierender Androgene in Leber, Muskulatur und peripherem Fettgewebe. Nach der Einnahme von Aromatasehemmern sinkt der Estradiol-Serumspiegel unter 10% des Ausgangswertes.
SERDs: weniger Rezeptoren
Selektive ER-Downregulatoren wie Fulvestrant (Faslodex®) sind reine ER-Antagonisten; sie blockieren die Rezeptoren vollständig, verhindern ihre Aktivierung durch andere Liganden und beschleunigen ihren Abbau (Downregulation).
SERMs: weniger Liganden
Selektive ER-Modulatoren binden selektiv an ER-α oder ER-β und verhalten sich dabei als Agonisten oder als Antagonisten. Sie wirken gewebespezifisch, da die ER-Subtypen in verschiedenen Geweben unterschiedlich häufig vorkommen. Der bekannteste SERM ist Tamoxifen, das teils östrogene, teils antiöstrogene Wirkungen ausübt. Sein Nachteil ist, dass es die Endometriumschleimhaut stimuliert und dadurch das Risiko für ein Endometriumkarzinom geringfügig erhöht. Ferner treten bei langfristiger Anwendung von Tamoxifen gehäuft Thromboembolien auf. Raloxifen wirkt in Uterus und Brustgewebe ausschließlich als Östrogen-Antagonist.
Adjuvante endokrine Therapie
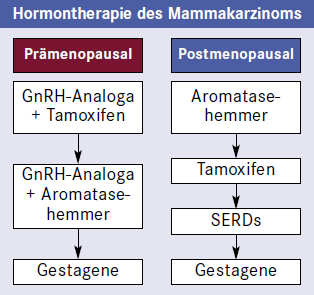
Bei prämenopausalen ER-positiven Frauen ist die Ausschaltung der Ovarialfunktion durch GnRH-Analoga in Kombination mit Tamoxifen die Therapie der ersten Wahl. Postmenopausale ER-positive Frauen erhalten fünf Jahre lang Tamoxifen. Bei Kontraindikation gegen Tamoxifen wird ein Aromatasehemmer der dritten Generation eingesetzt; aktuellen Studien (ATAC mit Anastrozol, MA17 mit Letrozol und IES mit Exemestan) zufolge erhöht die sequenzielle Gabe eines Aromatasehemmers nach 2- bis 5-jähriger Tamoxifenbehandlung die Chance für ein krankheitsfreies Überleben.
Palliative endokrine Therapie
Eine endokrine Therapie ist weniger toxisch als eine Chemotherapie und sollte daher bevorzugt eingesetzt werden. Dies gilt insbesondere für Patientinnen, die ein langes krankheitsfreies Intervall hatten oder deren Metastasen Knochen oder Weichteile betreffen. Bei positivem Rezeptorstatus ist in rund 60% mit einer Remission zu rechnen. Spricht eine palliativ behandelte Patientin auf eine endokrine Therapie an, wird diese bis zur Progression des Tumors fortgeführt. Danach können SERMs, SERDs und schließlich hochdosierte Gestagene eingesetzt werden (Abb. 3). Erst nach Ausschöpfen aller endokrinen Behandlungsmöglichkeiten wird auf eine zytostatische Therapie umgestellt, sofern die Patientin zustimmt.
Chemotherapie
Adjuvante Chemotherapie
Mammakarzinomzellen können sich über Blut- und Lymphbahnen über den ganzen Körper ausbreiten und Metastasen bilden. Nach der chirurgischen Entfernung des Tumors sollen solche Krebszellen durch eine adjuvante Chemotherapie vernichtet werden. Sie kommt vor allem bei ER-negativen Patientinnen mit erhöhtem Risiko in Frage. Bei den anderen Patientinnen kann sie mit einer endokrinen Behandlung kombiniert werden (Tab. 2). Der mögliche Nutzen einer adjuvanten Chemotherapie ist individuell verschieden:
- Frauen unter 50 Jahren (höheres Risiko) profitieren am meisten, postmenopausale Patientinnen (geringeres Risiko) weniger.
- Bei nodalnegativen Patientinnen, die ein 15%iges Rezidivrisiko aufweisen, profitieren 4 von 100 Frauen, bei nodalpositiven Patientinnen (50%iges Rezidivrisiko) 10 von 100 Frauen.
Auch zur palliativen Therapie können Zytostatika eingesetzt werden, wenn die Möglichkeiten der endokrinen Therapie ausgeschöpft sind (s.o.).
Bei der Auswahl der geeigneten Substanzen sind Zellzyklus, Zellwachstum und Wachstumskinetik zu berücksichtigen. Therapeutisch eingesetzte Zytostatika interagieren nur mit proliferierenden Zellen, also nicht mit ruhenden Zellen (G0-Phase). Bei langsamer Tumorprogression empfiehlt sich eine Monotherapie (Wirkstoffe s. Tab. 3). Da sich nicht alle Zellen eines Tumors in der gleichen Phase befinden, muss eine Monotherapie nach drei Wochen wiederholt werden. Meistens werden einige Zytostatika mit unterschiedlichem Wirkmechanismus kombiniert, um mehr Krebszellen auf einmal zu vernichten (Polychemotherapie).
Tab. 3: Häufig eingesetzte Zytostatika zur Therapie des Mammakarzinoms.
| Wirkstoff | Handelspräparat (Beispiel) | Workmechanismus | Angriffsort im Zellzyklus |
|---|---|---|---|
| Doxorubicin | Doxo-Cell® | DNA-Interkalation | S/G2-Phase |
| Epirubicin | Farmorubicin® | DNA-Interkalation | S/G2-Phase |
| Cyclophosphamid | Endoxan® | DNA- und RNA-Alkylierung | S-Phase |
| Vinorelbin | Navelbine® | Mitosehemmer | M-Phase |
| 5-Fluorouracil (5-FU) | Ribofluor®, Oncofluor® | Antimetabolit, Pyrimidinanalogon | S-Phase |
| Capecitabin | Xeloda® | Antimetabolit („orales 5-FU“) | S-Phase |
| Gemcitabin | Gemzar® | Antimetabolit | S-Phase |
| Paclitaxel | Taxol® | Spindelgift | M-Phase |
| Docetaxel | Taxotere® | Spindelgift | M-Phase |
Gängige Lehrbücher führen bereits knapp 20 verschiedene Polychemotherapien auf, daneben kommen im Rahmen von klinischen Studien weitere Kombinationen zum Einsatz.
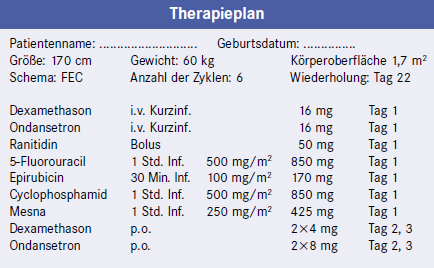
Der ehemalige "Goldstandard" CMF (Cyclophosphamid + Methotrexat + 5-Fluorouracil) wurde durch Kombinationen abgelöst, in denen Anthracycline (Epirubicin, Doxorubicin = Adriamycin u.a.) das Methotrexat ersetzen. Sie erzielen bei Patientinnen mit höherem Risiko bessere, ansonsten zumindest gleichwertige Therapieergebnisse. Ihre Überlegenheit gegenüber dem klassischen CMF-Schema ist aber nur für die sechszyklischen FEC- und FAC-Schemata (5-Fluorouracil + Epirubicin bzw. Doxorubicin + Cyclophosphamid) nachgewiesen (Abb. 4). Die vier- oder achtzyklische Gabe der Zweierkombinationen EC und AC war nicht wirksamer als CMF.
Was tun bei Resistenzen?
Nach einer längeren Therapie mit Tamoxifen können Resistenzen auftreten, die mit einer massiven Zunahme der Wachstumsfaktorrezeptoren EGFR und HER-2/neu einhergehen. Dies ist Ausdruck einer Gegenregulation der Zelle auf die ER-Blockade. In diesen Fällen wird Tamoxifen abgesetzt und die Therapie mit Aromatasehemmern oder GnRH-Analoga fortgesetzt. Des Weiteren können SERDs oder Gestagene eingesetzt werden. Ein weiterer Therapieansatz ist die Blockade der Wachstumsfaktoren mit Gefitinib (Iressa®)
Bei nodalpositiven Patientinnen kann die zusätzliche Gabe von Taxanen (Docetaxel, Paclitaxel) indiziert sein. Für Hochrisikopatientinnen kann eine dosisdichte (d. h. zweiwöchentliche) Chemotherapie in Betracht gezogen werden.
Neoadjuvante Chemotherapie Um ein lokal fortgeschrittenes oder inflammatorisches Mammakarzinom operativ entfernen zu können (evtl. sogar brusterhaltend), muss es zunächst verkleinert werden. Die neoadjuvante (präoperative) Chemotherapie verwendet zu diesem Zweck meistens Kombinationen von Anthracyclinen (Doxorubicin u.a.) mit Cyclophosphamid, neuerdings auch die sequenzielle Gabe von Taxanen und Anthracyclinen. Bei älteren ER-positiven Patientinnen ist eine endokrine Therapie gleich gut wirksam. Aufgrund der Wirkung einer neoadjuvanten Chemotherapie lässt sich abschätzen, wie die Patientin auf eine systemische Chemotherapie ansprechen wird.
(ambulante Chemotherapie). Außer den drei Zytostatika werden eingesetzt: Dexamethason und Ondansetron zur Antiemese, Ranitidin zur Stressulkusprophylaxe, Mesna zur Zystitisprophylaxe.
Chemotherapie bei metastasierendem Mammakarzinom
Das metastasierende Mammakarzinom sollte nach Möglichkeit endokrin behandelt werden, da dies weniger toxisch und belastend als eine Chemotherapie ist. Nur bei einem Tumorprogress unter der Hormontherapie ist eine zytostatische Behandlung indiziert. Hierbei wird differenziert vorgegangen: Bei langsamem Krankheitsfortschreiten wird nur jeweils ein Zytostatikum eingesetzt, u.a. Doxorubicin, Docetaxel (Taxotere®), Vinorelbin (Navelbine®), Gemcitabin (Gemzar®), Paclitaxel (Taxol®) und Capecitabin (Xeloda®). Bei raschem Fortschreiten und ausgeprägten Beschwerden ist eine Polychemotherapie angezeigt. In der Kombinationstherapie werden vorwiegend Taxane und Anthracycline eingesetzt.
Bei Patientinnen mit metastasierendem Mammakarzinom, die HER-2/neu übermäßig synthetisieren, verlängert der monoklonale HER-2/neu-Antikörper Trastuzumab (Herceptin®) sowohl in der Mono- als auch in der Kombinationstherapie die Überlebenszeit.
Psychoonkologische Hilfen
- Krankheitsverarbeitung
- Angst, Depression, Belastungserleben
- Körperbild, Selbstkonzept, Sexualität
- Soziale Beziehungen, Kommunikation
Unerlässlich: begleitende Maßnahmen
Die umfassende Betreuung der Krebspatientin beginnt mit der Aufklärung über die Diagnose und die empfohlenen Therapien, deren Chancen und Risiken, Nebenwirkungen und mögliche Spätfolgen ihr der Arzt verständlich erläutern muss. Grundsätzlich muss die Patientin ihre Zustimmung zu der empfohlenen Behandlung geben und muss auf Wunsch auch die Gelegenheit erhalten, eine Zweitmeinung einzuholen.
Der Patientin sind frühzeitig psychoonkologische Unterstützungen zur Krankheitsbewältigung anzubieten (s. Kasten). Dasselbe gilt für praktische Hilfen wie z. B. das Beschaffen von Perücken oder Rehabilitationsmaßnahmen. Zu den medizinischen Supportivmaßnahmen der Krebspatientin gehören unter anderem eine adäquate Schmerzbehandlung, Antiemese, Einsatz von Wachstumsfaktoren, antimikrobielle Prophylaxe und Therapie der Neutropenie sowie die Gabe von Bisphosphonaten [3]. Nicht zuletzt ist auf eine sinnvolle Ernährung zu achten.






















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.