Zur Erinnerung: Was ist der Ct-Wert?
Als Threshold Cycle, Ct-Wert oder kurz Ct, wird bei der Realtime-PCR (Polymerase Chain Reaction; Nukeinsäure-Amplifikationstechnik) der Amplifikationszyklus bezeichnet, bei dem die Reaktion in die exponentielle Phase eintritt und das gesuchte Nukleinsäurefragment durch eine Fluoreszenzreaktion sichtbar wird. Bei konstanten Reaktionsbedingungen ist der Threshold Cycle proportional zur Menge der untersuchten DNA oder RNA und kann zur Quantifizierung benutzt werden. Aus diesem Grunde wird die Realtime-PCR auch als quantitative PCR oder qPCR bezeichnet. Je höher der Ct-Wert, desto geringer war die eingesetzte Menge DNA/RNA.
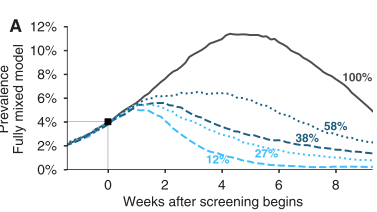
Die ermittelten Ct-Werte sind zwischen PCR-Assays verschiedener Hersteller nur mit Einschränkungen vergleichbar. Eine Ct-Schwelle, ab der eine Person infektiös bzw. nicht mehr infektiös ist, kann nicht pauschal angegeben werden, eben sowenig wie eine bestimmte Virusmenge, die zu einer Infektion bei exponierten Personen führt. Angaben für Kontagiosität reichen von Ct-Werten zwischen 20 und 30. Ein CT-Wert >30 darf als „nicht mehr infektiös“ gelten, da ab dieser Grenze SARS-CoV-2 in Studien nicht mehr kulturell anzüchtbar war (4 = Mina et al.).
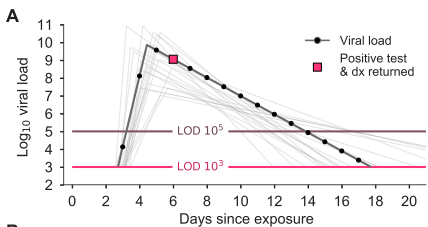
Ein Ct-Wert von 18 bis 21 spiegelt eine – mit größter Wahrscheinlichkeit kontagiöse – Viruslast von 100.000 (105) bis 1 Million (106) RNA-Kopien pro Milliliter Probe. Diese Konzentration dürfte von evaluierten Lateral-Flow-Antigentests sicher nachgewiesen werden, eine korrekte Probeentnahme und Auswertung vorausgesetzt. Ihre untere Nachweisgrenze (Limit of Detection/LOD) wird bei ca. bei 100.000 (105) Kopien/ml gezogen. PCR-Assays reagieren schon bei einer um zwei Größenordnungen niedrigeren Viruslast positiv, ab etwa 103 Kopien/ml (5 = Larremore DB et al.)





















5 Kommentare
Sensitivität, Spezifität Artikel vs. Packungsbeilage
von Stefan Pollmeier am 06.04.2021 um 11:41 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Sensitivität
von Manfred Magg am 14.03.2021 um 19:55 Uhr
» Auf diesen Kommentar antworten | 2 Antworten
AW: Sensitivität
von S. Schmidt am 23.03.2021 um 17:16 Uhr
AW: Sensitivität
von Schlenger am 06.04.2021 um 21:04 Uhr
Einspruch!
von Gunnar Müller, Detmold am 14.03.2021 um 9:49 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Das Kommentieren ist aktuell nicht möglich.