
- DAZ.online
- News
- Pharmazie
- Kritik: Erster Corona-...
Entwicklung von COVID-19-Impfstoffen
Kritik: Erster Corona-Impfstoff soll in Indien im August verfügbar sein
Remagen - 10.07.2020, 15:15 Uhr
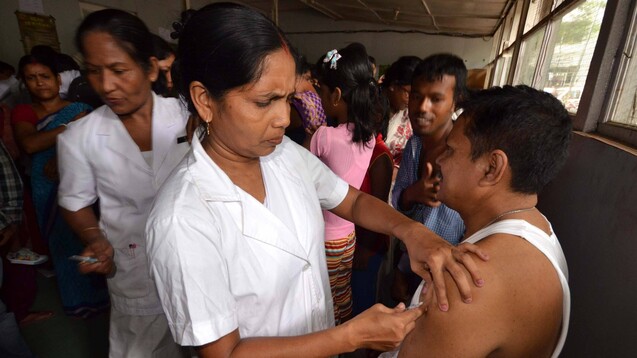
Ist die scheinbare Hektik, mit der eine indische Regierungsinstitution einen COVID-19-Impfstoff testen will, politisch motiviert? (x / Foto: Symbolbild einer Impfszene aus 2014 / imago images / ZUMA Press)
In der letzten Woche hat die indische Regierung die ersten Genehmigungen für klinische Prüfungen mit COVID-19-Impfstoffen aus der heimischen Entwicklung erteilt. Die Kandidaten „Covaxin“ und „ZyCov-D“ stammen von den Firmen Bharat Biotech und Zydus Cadila. Bereits Mitte August soll der erste Impfstoff verfügbar sein, was in der wissenschaftlichen Gemeinschaft einige Verwunderung und Besorgnis ausgelöst hat.
Derzeit entwickeln sechs indische Unternehmen Impfstoffe gegen COVID-19. Nun hat die Aufsichtsbehörde „Drug Controller General of India“ (CDSCO) zwei von ihnen, Bharat Biotech und Zydus Cadila, erstmals die Erlaubnis erteilt, klinische Studien der Phase I und II mit ihren Impfstoffen Covaxin und ZyCov-D zu beginnen.
Covaxin wurde von dem renommierten Impfstoffhersteller Bharat Biotech, Hyderabad, zusammen mit dem Indischen Rat für medizinische Forschung (ICMR) beziehungsweise dem Nationalen Institut für Virologie (NIV) in Puna entwickelt. Der ICMR ist die Spitzenorganisation in Indien für die Formulierung, Koordination und Förderung der biomedizinischen Forschung. Sie wird von der indischen Regierung finanziert. Der den inaktivierten Viruspartikeln zugrunde liegende SARS-CoV-2-Stamm wurde im Nationalen Institut für Virologie isoliert, also alles „made in India“.
Mehr zum Thema
AZD1222 bekommt „Konkurrenz“
COVID-19-Impfstoffe: ein Kandidat in Phase 3, zweiter folgt

Update COVID-19
Impfstoffentwicklung: Noch kein Land in Sicht
Für den Antrag hatte das Unternehmen die Ergebnisse aus präklinischen Studien zum Nachweis der Sicherheit und Immunantwort eingereicht. Die klinische Studie soll im Juli 2020 in ganz Indien beginnen. Für die erste Phase sind 375 Freiwillige an zwölf Standorten geplant und für die Phase II weitere 750.
Schon am 15. August auf dem Markt?
Wie das Fachjournal „Science“ durchblicken lässt, machen die Entwickler den Covaxin-Studienzentren mächtig Druck: „Es ist geplant, den Impfstoff für die öffentliche Gesundheit spätestens am 15. August 2020 nach Abschluss aller klinischen Studien auf den Markt zu bringen“, wird aus einem auf Twitter geleakten Schreiben von Balram Bhargava, Generaldirektor des Indischen Rats für medizinische Forschung (ICMR), zitiert. Er soll die Krankenhäuser dazu aufgefordert haben, die Teilnehmer „spätestens am 7. Juli 2020“ einzuschreiben.
Zeitplan birgt potenzielle Risiken
Die scheinbare Hektik, mit der eine indische Regierungsinstitution den COVID-19-Impfstoff testen will, hat laut „Science“ unter Wissenschaftlern im In- und Ausland für Aufruhr gesorgt. Es sei absurd zu glauben, Studien könnten in weniger als zwei Monaten zeigen, dass ein Impfstoff sicher und wirksam ist, meinten viele. „Meines Wissens nach wurde für keine Art von Impfstoff jemals ein derart beschleunigter Entwicklungspfad beschritten“, sagt Anant Bhan, unabhängiger Ethik- und Politikforscher und ehemaliger Präsident der „International Association of Bioethics“.
Der Zeitplan berge potenzielle Risiken und berücksichtige die erforderlichen Sicherheitsverfahren nur unzureichend. Klinische Studien könnten nicht beschleunigt werden, stimmte der indische Virologe und erfahrene Impfstoff-Forscher Thekkekara Jacob John ihm zu. Selbst wenn sie beschleunigt würden, veranschlagt Jacob John für die Phase I- und Phase II-Studien mindestens fünf Monate, und für die Phase III kämen wahrscheinlich mindestens weitere sechs Monate hinzu.
Mehr zum Thema

Die gute Nachricht des Tages
WHO hat Hoffnung auf Corona-Impfstoffe noch in diesem Jahr
Kritiker hielten das Zieldatum für politisch motiviert, schreibt „Science“. Der 15. August sei Indiens Unabhängigkeitstag, an dem Premierminister Narendra Modi traditionell die Stadtmauer des Roten Forts in Delhi erklimme, um eine lange Rede zu halten, in der er von den Erfolgen seiner Regierung berichtet und wichtige Ankündigungen macht.
ZyCoV-D ab Mitte Juli in der klinischen Erprobung
Neben Covaxin hat auch ZyCoV-D, der COVID-19-Impfstoffkandidat von Zydus Cadila mit Sitz in Ahmedabad, die präklinische Testung erfolgreich abgeschlossen und von der Central Drugs Standard Control Organization (CDSCO) die Erlaubnis für den Start einer klinischen Phase-I/II-Studie erhalten. Präklinische Toxizitätsstudien hätten gezeigt, dass die Plasmid-DNA-Vakzine gut verträglich, sicher und immunogen sei, teilt das Unternehmen mit. In beiden Phasen sollen an mehreren Standorten in Indien mehr als 1.000 Probanden teilnehmen (CTRI/2020/07/026352). Die Rekrutierung soll Mitte Juli losgehen.
Neben Bharat Biotech und Zydus Cadila, das außer ZyCoV-D noch einen weiteren Impfstoffkandidaten gegen das neuartige Coronavirus in petto hat, entwickeln in Indien auch die Unternehmen Biological E, Indian Immunologicals und Mynvax jeweils eine weitere COVID-19-Vakzine.





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.