
- DAZ.online
- News
- Pharmazie
- FDA: Fünf Hersteller ...
Nach Petition von US-Apotheke
FDA: Fünf Hersteller sollen ihr Metformin zurückrufen
Stuttgart - 03.06.2020, 16:30 Uhr
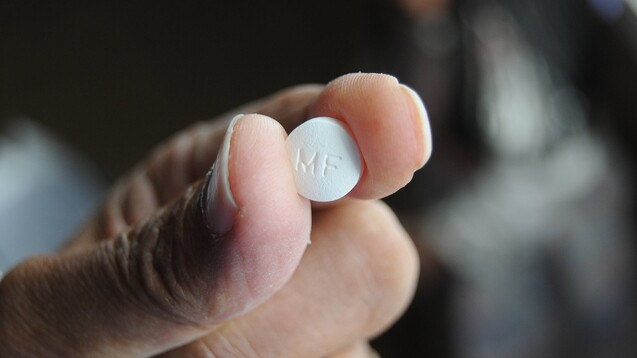
Wie kommt die Nitrosamin-Verunreinigung NDMA ins Metformin und welche Konsequenzen könnte das mit sich bingen? Es gibt noch viele offene Fragen, doch in den USA erfolgen die ersten Rückrufe. ( r / Foto: imago images / Dean Pictures)
Nur Metformin mit verlängerter Wirkstofffreisetzung betroffen?
Als die FDA Anfang Februar ihre eingangs erwähnten ersten Labor-Ergebnisse zur Prüfung von Metformin auf NDMA veröffentlicht hatte, erwähnte sie auch, dass bislang nur in Fertigarzneimitteln, nicht aber im Wirkstoff (API) selbst, NDMA nachgewiesen wurde. Dies ist nun auch in den aktuellen Untersuchungen der FDA der Fall, die nun aber zu Rückrufen führen. Zudem sind wie bereits im Februar wieder nur Metformin-Tabletten mit verlängerter Wirkstofffreisetzung betroffen.
In diesem Zusammenhang erscheint die Einschätzungen von Helmut Buschmann, Fritz Sörgel und Ulrike Holzgrabe aus der DAZ 51/2019 erneut interessant: Ein Blick auf die chemische Struktur des Metformins zeigt demnach, dass es auch zu einer nachträglichen Bildung von Nitrosamin während der Lagerung im Fertigarzneimittel kommen könnte. Unter bestimmten Lagerbedingungen könne es zudem in Abhängigkeit vom Blistermaterial zu unterschiedlichen Zersetzungskinetiken kommen. Diese nachträgliche NDMA-Bildung dürfte einige an das ebenfalls mit Nitrosaminen verunreinigte Ranitidin erinnern.
Mehr zum Thema

Auch in der EU
Wegen NDMA: Endgültiges Aus für Ranitidin?

Endgültiges Aus durch Nitrosamin-Verunreinigung?
FDA zu Ranitidin: Je älter das Präparat, desto höher der NDMA-Gehalt
Wie im Fall Ranitidin ist es auch im Fall Metformin wieder die US-Versand-Apotheke „Valisure“ mit angeschlossenem Labor, die darauf aufmerksam gemacht hat, dass die Verunreinigungen bedeutender sein könnten, als aus den Prüfungen der FDA zunächst zu schließen war.
16 von 38 Chargen kontaminiert
Nach Angaben von Valisure war es eine einzelne Person, die eine Metformin-Probe an Valisure sendete, sich besorgt über deren Reinheit äußerte und so schließlich zu weiteren Untersuchungen Valisures führte. Daraufhin untersuchte Valisure 38 Chargen von 22 Firmen, die Valisure von Lieferanten seiner Apotheke bezogen hatte. Darin enthielten 16 der 38 Chargen NDMA-Mengen oberhalb des Grenzwerts – der Maximalwert soll 16-fach erhöht gewesen sein. Anschließend reichte Valisure am 2. März 2020 (wie zuvor für Ranitidin) eine FDA-Bürgerpetition ein.
Valisure erklärt sich die abweichenden Ergebnisse zur FDA dadurch, dass die FDA auf freiwillige Proben der Industrie angewiesen sei, während Valisure Präparate am Ende der Lieferkette prüfe. Die Hersteller würden im Fall von Valisure also nicht entscheiden, was getestet werden soll.


























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.