
- DAZ.online
- News
- Pharmazie
- FDA: Fünf Hersteller ...
Nach Petition von US-Apotheke
FDA: Fünf Hersteller sollen ihr Metformin zurückrufen
Stuttgart - 03.06.2020, 16:30 Uhr
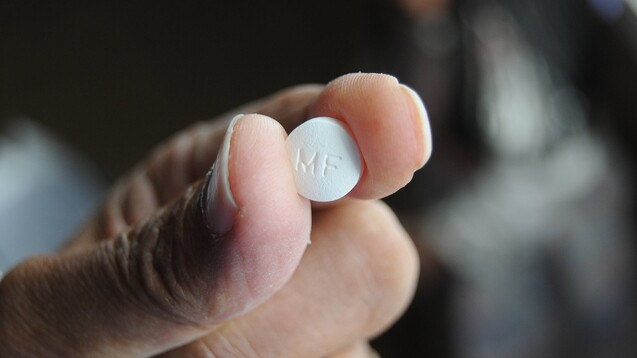
Wie kommt die Nitrosamin-Verunreinigung NDMA ins Metformin und welche Konsequenzen könnte das mit sich bingen? Es gibt noch viele offene Fragen, doch in den USA erfolgen die ersten Rückrufe. ( r / Foto: imago images / Dean Pictures)
Die Nitrosamin-Krise brodelt noch unter der Oberfläche: Während in Europa bislang zwar kein Update zur NDMA-Problematik in Metformin erschienen ist, hat sich die US-amerikanische Arzneimittelbehörde FDA nun zum zweiten Mal geäußert. Ihr vorläufiges Urteil vom Februar musste sie verschärfen und für bestimmte Metformin-Präparate fünf Firmen zu Rückrufen auffordern. Gelöst ist das „Rätsel“ von NDMA in Metformin damit aber noch nicht.
Die US-amerikanische Arzneimittelbehörde FDA hatte bereits Anfang Februar erste Labor-Ergebnisse zur Prüfung von Metformin auf das Nitrosamin NDMA veröffentlicht. Daraus ging hervor, dass bislang nur in Metformin von Actavis NDMA gefunden wurde – in Mengen zwischen 0,01 und 0,02 µg. Damit lag die Menge unter der tolerierten täglichen Aufnahmegrenze von 0,096 µg. Bis dahin hatte die FDA somit keine Rückrufaktion von Metformin für die USA empfohlen. Die Untersuchungen galten aber noch nicht als abgeschlossen.
Zuvor war es nur in Singapur (drei Metformin-Präparate), in der Schweiz und Kanada aufgrund einer Verunreinigung mit NDMA zu Metformin-Rückrufen gekommen. Das BfArM (Bundesinstitut für Arzneimittel und Medizinprodukte) hatte vergangenen Dezember betont, dass nur „Spuren einer Verunreinigung, N-Nitrosodimethylamin (NDMA)“ in einer „geringen Anzahl von metforminhaltigen Arzneimitteln außerhalb der Europäischen Union (EU) gefunden“ worden waren.
Mehr zum Thema
Erster Engpass in Deutschland
Metformin: FDA findet NDMA nur in Fertigarzneimitteln, nicht im Wirkstoff
NDMA in Metformin
Nitrosamine: Behörden wollen Versorgungsengpässe vermeiden

Relevante Engpässe laut BfArM
Die Versorgung mit Metformin ist angespannt
Doch eine angespannte Liefersituation in Deutschland und die Metformin-Rückrufe in Kanada ließen erahnen, dass im Fall Metformin noch keine endgültige Entwarnung gegeben werden kann. Zur angespannten Versorgungssituation von Metformin in Deutschland schrieb das BfArM am 14. Mai an DAZ.online: „Eine periodisch angespannte Situation ist u. a. auf die Durchführung der auf europäischer Ebene vereinbarten Maßnahmen im Zusammenhang mit Nitrosaminverunreinigungen und den daraus entstehenden in Teilen zeitlichen Verzögerungen der Chargenfreigabe zurückzuführen.“ Zudem hatten auch die Corona-Einschränkungen Probleme gemacht. Weiterhin sollten dem BfArM zwischenzeitlich belastbare Angaben vorliegen, dass die Menge der in den Verkehr gebrachten metforminhaltigen Arzneimittel im März deutlich erhöht wurde und in der Gesamtschau den Bedarf decken sollte.
Es wird also weltweit weiterhin verstärkt auf Nitrosamine geprüft. Das hat in den USA nun zum Ergebnis, dass die FDA vergangenen Donnerstag fünf Firmen dazu aufgefordert hat, Ihre Metformin-Präparate „freiwillig“ zurückzurufen: Amneal Pharmaceuticals LLC und Apotex Corp sind der Aufforderung bereits nachgekommen.
Nur Metformin mit verlängerter Wirkstofffreisetzung betroffen?
Als die FDA Anfang Februar ihre eingangs erwähnten ersten Labor-Ergebnisse zur Prüfung von Metformin auf NDMA veröffentlicht hatte, erwähnte sie auch, dass bislang nur in Fertigarzneimitteln, nicht aber im Wirkstoff (API) selbst, NDMA nachgewiesen wurde. Dies ist nun auch in den aktuellen Untersuchungen der FDA der Fall, die nun aber zu Rückrufen führen. Zudem sind wie bereits im Februar wieder nur Metformin-Tabletten mit verlängerter Wirkstofffreisetzung betroffen.
In diesem Zusammenhang erscheint die Einschätzungen von Helmut Buschmann, Fritz Sörgel und Ulrike Holzgrabe aus der DAZ 51/2019 erneut interessant: Ein Blick auf die chemische Struktur des Metformins zeigt demnach, dass es auch zu einer nachträglichen Bildung von Nitrosamin während der Lagerung im Fertigarzneimittel kommen könnte. Unter bestimmten Lagerbedingungen könne es zudem in Abhängigkeit vom Blistermaterial zu unterschiedlichen Zersetzungskinetiken kommen. Diese nachträgliche NDMA-Bildung dürfte einige an das ebenfalls mit Nitrosaminen verunreinigte Ranitidin erinnern.
Mehr zum Thema

Auch in der EU
Wegen NDMA: Endgültiges Aus für Ranitidin?

Endgültiges Aus durch Nitrosamin-Verunreinigung?
FDA zu Ranitidin: Je älter das Präparat, desto höher der NDMA-Gehalt
Wie im Fall Ranitidin ist es auch im Fall Metformin wieder die US-Versand-Apotheke „Valisure“ mit angeschlossenem Labor, die darauf aufmerksam gemacht hat, dass die Verunreinigungen bedeutender sein könnten, als aus den Prüfungen der FDA zunächst zu schließen war.
16 von 38 Chargen kontaminiert
Nach Angaben von Valisure war es eine einzelne Person, die eine Metformin-Probe an Valisure sendete, sich besorgt über deren Reinheit äußerte und so schließlich zu weiteren Untersuchungen Valisures führte. Daraufhin untersuchte Valisure 38 Chargen von 22 Firmen, die Valisure von Lieferanten seiner Apotheke bezogen hatte. Darin enthielten 16 der 38 Chargen NDMA-Mengen oberhalb des Grenzwerts – der Maximalwert soll 16-fach erhöht gewesen sein. Anschließend reichte Valisure am 2. März 2020 (wie zuvor für Ranitidin) eine FDA-Bürgerpetition ein.
Valisure erklärt sich die abweichenden Ergebnisse zur FDA dadurch, dass die FDA auf freiwillige Proben der Industrie angewiesen sei, während Valisure Präparate am Ende der Lieferkette prüfe. Die Hersteller würden im Fall von Valisure also nicht entscheiden, was getestet werden soll.
FDA findet niedrigere NDMA-Werte als Valisure
Valisure wollte nun offenbar noch einen Schritt weiter gehen und die eigenen Ergebnisse bestätigen. Dazu bat Valisure die Bevölkerung um die Einsendung von Metformin-Tabletten im „Crowdsourcing“-Stil. Nach Angaben von Valisure hätten dabei 46 von 128 Metformin-Proben aus 30 Staaten die von der FDA festgelegte NDMA-Menge überschritten. Die Ergebnisse wurden auf dem Preprint-Server medRxiv.org am 1. Juni veröffentlicht. Sie zeigen laut Valisure, dass es sofortiger Produktrückrufe bedarf. Außerdem hegt Valisure offenbar den Verdacht, dass kontaminierte Chargen mit sauberen vermengt werden und so weiter in den USA vertrieben werden. Denn es gibt offenbar hohe Schwankungen im NDMA-Gehalt.
Valisure forderte FDA bereits im März zu Rückrufen auf
Am 28. Mai hat die FDA nun auf die Petition von Valisure reagiert. In dieser war ebenfalls (wie im aktuellen Preprint von Valisure) bereits zu einem Chargenrückruf aufgerufen worden. Auffällig ist, dass Valisure anders als die FDA auch erhöhte NDMA-Werte in Metformin-Präparaten mit sofortiger Wirkstofffreisetzung gemessen hat. Die Präparate mit verzögerter Wirkstofffreisetzung waren aber auch in den Analysen von Valisure verstärkt betroffen. Die FDA hat laut ihrer aktuellsten Stellungnahme NDMA also ausschließlich in den Präparaten mit verzögerter Freisetzung gefunden – dies könnte ein Grund sein, warum es in Deutschland bislang zu keinen Rückrufen kam, denn hier sind keine Metformin-Präparate mit verzögerter Freisetzung in der Lauer-Taxe gelistet. Auch in den USA werden sie laut FDA seltener eingesetzt als die Tabletten mit sofortiger Freisetzung.
Die FDA hat nach eigenen Angaben dieselben Chargen getestet, die laut einem privaten Labor – das Valisure sein muss – erhöhte NDMA-Mengen enthalten. Merkwürdig ist dabei, dass die FDA die Ergebnisse für manche Chargen bestätigen konnte, aber nicht für alle. In anderen Beispielen habe die FDA sogar NDMA in Chargen gefunden, in denen das private Labor keines gefunden hatte. Insgesamt seien die durch die FDA gemessenen NDMA-Werte jedoch niedriger gewesen. In den USA führen sie nun dennoch zu Rückrufen.
Auf die Aufklärung der Hintergründe dieser uneinheitlichen Ergebnisse darf also mit Spannung gewartet werden.


























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.