
- DAZ.online
- DAZ / AZ
- DAZ 49/2021
- Wettlauf gegen die Zeit
Notfallmedizin
Wettlauf gegen die Zeit
Empfehlungen zur Notfalltherapie und Prophylaxe des Schlaganfalls
Ein kleiner Thrombus genügt, um das Leben im wahrsten Sinne des Wortes schlagartig auf den Kopf zu stellen. Jedes Jahr erleiden in Deutschland 200.000 Personen erstmalig einen Schlaganfall, weitere 70.000 Rezidive kommen hinzu [1]. Ein Schlaganfall ist hierzulande und weltweit die zweithäufigste Todesursache. Auch wenn die Inzidenzen und Todesraten in den letzten Jahren kontinuierlich fielen, steigen die absoluten Zahlen aufgrund der demografischen Entwicklung weiter an [2].
Man unterscheidet die nachfolgend beschriebenen ischämischen Schlaganfälle, die 80% aller Erkrankungen ausmachen von den hämorrhagischen Schlaganfällen wie Hirnblutungen und Subarachnoidalblutungen. Ischämische Schlaganfälle entstehen durch Verschlüsse von Hirnarterien durch Thromben an lokalen atherosklerotischen Plaques bzw. aufgrund von Emboli, die aus dem Herz oder anderen Arterien stammen. Mikroangiopathien der kleinen Hirngefäße stellen eine weitere Ursache dar. Die transitorische ischämische Attacke ist gekennzeichnet durch eine vorübergehende Durchblutungsstörung des Gehirns, die Symptome klingen nach einigen Minuten oder Stunden wieder ab.
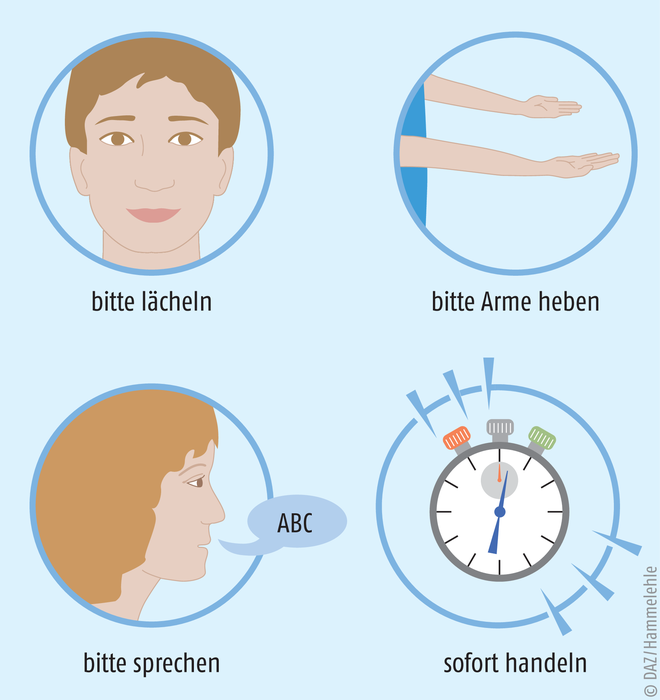
Abb. 1: Mit dem FAST-Test kann ein Schlaganfall zügig erkannt werden. FACE: Man bittet die Person zu lächeln. Herabhängende Mundwinkel deuten auf eine halbseitige Lähmung hin. ARMS: Man bittet die Person, beide Arme zu heben und die Handflächen nach oben zu drehen, um Lähmungen zu überprüfen. SPEECH: Man bittet die Person, einen Satz zu wiederholen. Ist die Person dazu nicht in der Lage oder spricht undeutlich, liegt eine Sprachstörung vor. TIME: Nicht zögern und den Notruf absetzen.
Typische Schlaganfall- bzw. Ischämiezeichen wie Taubheitsgefühle, Seh- und Sprachstörungen, Schwindel oder Kopfschmerzen treten plötzlich auf. Verschiedene Skalen wie bspw. der FAST-Test können den Sanitätern vor Ort helfen, den Schlaganfall festzustellen (s. Abb. 1). Durch die verschlossene Hirnarterie wird die Blutversorgung und damit die Sauerstoffversorgung des betroffenen Areals eingeschränkt. Das Hirngewebe stellt zunächst seine Funktion ein, stirbt dann aber mit Andauern der Ischämie ab. Ausgehend vom Kern, der innerhalb von Minuten abstirbt, greift der Infarkt auf die zunächst weniger stark betroffene, angrenzende Penumbra über (s. Abb. 2). Alle Therapieversuche zielen darauf ab, dieses Areal zu retten. Da das Penumbragewebe den durch den Schlaganfall hervorgerufenen Sauerstoffmangel nur kurz überleben kann, muss nach der Devise „time is brain“ schnell gehandelt werden. Therapeutische Maßnahmen, um den Blutfluss wieder in Gang zu bringen, ergeben deshalb vor allem in den ersten Stunden nach dem Anfall Sinn. Langfristige Folgen wie Sprachstörungen, Einschränkungen der Mobilität und Selbstständigkeit, neuropathische Schmerzen, kognitive und psychische Störungen können nicht immer verhindert werden.
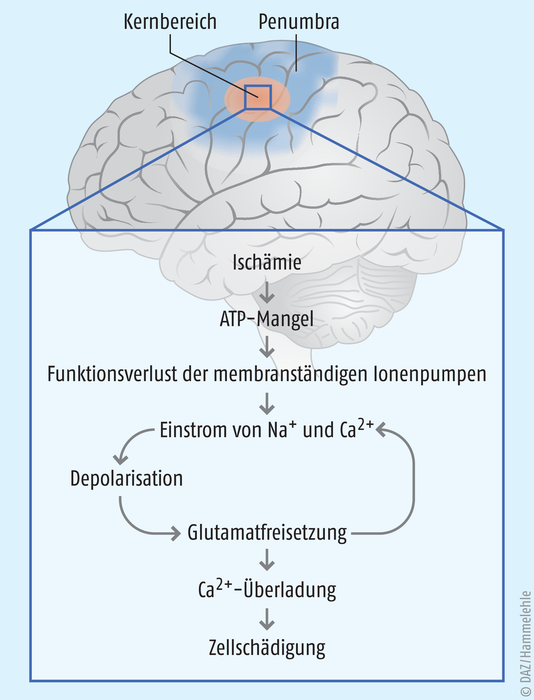
Abb. 2: Pathophysiologische Vorgänge bei einem ischämischen Schlaganfall [10]: Die Blutzufuhr durch das betroffene Gefäß wird durch das Blutgerinnsel unterbrochen. Dem unmittelbar durch die Arterie versorgten Hirnareal wird somit die Glucose- und Sauerstoffzufuhr gekappt. Aufgrund des Nährstoffmangels können die Nervenzellen kein lebenswichtiges ATP mehr produzieren, gleichzeitig steigt die Laktat-Konzentration aufgrund der anaeroben Glykolyse an. Die membranständigen (ATP-abhängigen) Ionenpumpen stellen ihre Funktion ein und der elektrochemische Gradient an der Membran bricht zusammen. Die Zellmembranen depolarisieren, da immer mehr Natrium- und Calcium-Ionen in die Zellen einströmen und Neurotransmitter werden freigesetzt. Insbesondere der exzitatorische Botenstoff Glutamat verstärkt die Depolarisation der Neuronen, sodass weitere Calcium-Ionen einströmen, die zellschädigende Vorgänge aktivieren. Weiterhin bewirkt der einwärts gerichtete Ionenflux, dass Wasser in die Neuronen einströmt und diese anschwellen. Ein zytotoxisches Hirnödem ist die Folge. Diese Prozesse spielen sich zunächst nur in unmittelbarer Nähe des Verschlusses, im Kernbereich des Ischämiebezirks ab. Angrenzende Areale - die Penumbra des Infarkts - können zumindest noch teilweise von Kollateralgefäßen versorgt werden und länger überleben. Neuronen in diesem Gebiet sind zwar auch nicht mehr elektrisch aktiv und tragen zur Symptomatik des Anfalls bei, aber sie können noch längere Zeit überleben und ihre elektrochemische Integrität erhalten. Doch mit Verstreichen der Zeit breitet sich der Kern durch die zellzerstörenden Vorgänge aus und führt zum Untergang der Penumbra, langfristig vernarbt das Infarktgewebe.
Schnittstelle Stroke Unit
Um Patienten frühzeitig und adäquat betreuen zu können, hat sich seit Mitte der 1990er Jahre das Konzept der spezialisierten Schlaganfallstationen etabliert, der sogenannten Stroke Units. Diese Abteilungen bündeln die apparativen und personellen Kompetenzen zur Diagnose und Therapie des Schlaganfalls. Leitlinien weltweit sprechen sich dafür aus, dass alle akuten Schlaganfälle und transitorischen ischämischen Attacken in einer Stroke Unit behandelt werden sollen [3]. Die Vorteile sind einem Cochrane-Review zufolge nicht von der Hand zu weisen: signifikant reduzierte Risiken für ein schlechtes Outcome, Letalität und eine spätere Abhängigkeit im Vergleich zu alternativen Einrichtungen [4]. Um als solche Einheit zertifiziert zu werden, müssen verschiedene Voraussetzungen erfüllt werden. Dazu gehören entsprechende Personalschlüssel, geeignete Betten mit umfangreichem Monitoring der Patienten, Möglichkeiten zur Bildgebung und neurologischen Ultraschall-Diagnostik. Die Bildgebung ist essenziell für die Diagnose des Schlaganfalls. Obwohl die Magnetresonanz-Tomografie (MRT) eine höhere Sensitivität liefert, hat sich in der Praxis die Computertomografie (CT) als Standard etabliert, da sie schneller durchführbar ist und eine höhere Verfügbarkeit aufweist. Eventuelle intrakranielle Blutungen lassen sich so sicher diagnostizieren. Nach Kontrastmittelgabe sind auch die Gefäße detektierbar und je nach Verfahren lassen sich infarzierte Gewebeareale lokalisieren [3]. Um das betroffene Hirnareal zu retten, muss das verschlossene Gefäß schleunigst wieder geöffnet werden. Laut Leitlinie kommen bei Schlaganfällen zwei Optionen infrage:
- die systemische Lysetherapie und
- die endovaskuläre mechanische Thrombektomie.
Systemische Lysetherapie
Als Standard in der Schlaganfalltherapie der ischämischen Schlaganfälle mit behindernden Symptomen hat sich die intravenöse Thrombolyse mit Alteplase etabliert (0,9 mg/kg Körpergewicht (maximal 90 mg), über 60 Minuten, initial 10% der Dosis als Bolus) [3]. Die selektiv wirkende Tenecteplase sollte derzeit nur in klinischen Studien verwendet werden. Die Leitlinienautoren betonen explizit die Wichtigkeit der systemischen Lyse, da dieses Verfahren immer noch in höchst unterschiedlichem Maße angewendet wird. Der rekombinante Gewebeplasminogenaktivator Alteplase wird durch Fibrin-Bindung weitgehend thrombusselektiv aktiviert und spaltet Plasminogen zum aktiven Plasmin – dem eigentlichen fibrinolytischen Agens, das das Blutgerinnsel auflöst. Trotz der Thrombusselektivität kann nicht ausgeschlossen werden, dass Alteplase auch systemisch das Fibrinolysesystem aktiviert und Blutungen hervorruft. Vor der Behandlung müssen daher unbedingt eventuelle intrakranielle Blutungen ausgeschlossen werden. Eine thrombolytische Therapie soll so schnell wie möglich erfolgen. Bei Vorstellung innerhalb von 4,5 Stunden nach Beginn der Symptome kann mittels spezialisierter Bildgebung noch rettbares Hirngewebe identifiziert und damit die Indikation zur Revaskularisation gestellt werden [3].
Mechanische Thrombektomie
Mit der endovaskulären Entfernung des verstopfenden Blutgerinnsels hat die Schlaganfalltherapie einen großen Schritt nach vorn gemacht. Hierzu wird ein sogenannter Stent-Retriever mit einem Katheter über die Leistenarterie bis zum verschlossenen Gefäß geführt. Der Thrombus verfängt sich in dem Drahtgeflecht an der Spitze des Instruments und kann entfernt werden. Besonders Patienten mit ausgeprägten Symptomen und einem in der Bildgebung nachgewiesenen Verschluss einer großen Arterie im vorderen Kreislauf der hirnversorgenden Arterien müssen dahingehend evaluiert werden, ob rettbares Risikogewebe vorliegt und die Möglichkeit einer Revaskularisation besteht. Diese Therapie sollte nur in Ausnahmefällen zurückgehalten werden, obwohl es Situationen gibt (sehr großer Infarktkern) in denen aktuell die Effektivität noch nicht gesichert ist. Bei Verschlüssen von größeren Gefäßen des hinteren Kreislaufs kann das Verfahren ebenfalls in Frage kommen [3]. Gelingt die Auflösung oder Entfernung des Gerinnsels, braucht das Gehirn vor allem Zeit, um sich zu erholen. Eine aktivierende Pflege, Ergotherapie, Logopädie und Physiotherapie zeigen positive Effekte auf die Erholung des Patienten und sollten innerhalb der ersten 48 Stunden nach dem Schlaganfall begonnen werden [3]. Langfristig erfolgt die Rehabilitation in einer entsprechenden Klinik.
Ultima Ratio: Schädeldach-Entfernung
Im Laufe der Schlaganfalltherapie drohen zahlreiche Komplikationen wie Infektionen, Thrombosen und epileptische Anfälle. Eine bisher noch wenig untersuchte und neu in die Leitlinie aufgenommene Komplikation ist das Post-Stroke-Delir, das in ca. 10 bis 48% der Fälle auftritt und oft mit einer schlechteren Prognose einhergeht [3]. Patienten sollen regelmäßig mithilfe von Scoring-Tools (z. B. der Confusion Assessment Method for the Intensive Care Unit, CAM-ICU) auf delirante Symptome überprüft werden. Präventiv wird empfohlen, Patienten zu orientieren, zu mobilisieren und den Tag-Nacht-Rhythmus zu fördern. Pharmakologisch kann bei Schlafstörungen mit Melatonin geholfen werden. Neuroleptika wie Quetiapin und Risperidon werden bei psychotischen Symptomen verwendet. Bei starker Agitation kann Haloperidol eingesetzt werden, bei Hinweisen auf eine Angstsymptomatik auch Lorazepam [3]. Infarzierte Hirnzellen schwellen im Laufe der Zeit durch die ischämischen Vorgänge an (s. Abb. 2). Dies führt bei schweren Schlaganfällen zum Entstehen eines Hirnödems, welches zusätzlich durch eine in Mitleidenschaft gezogene Blut-Hirn-Schranke befördert wird. Besonders Schlaganfallpatienten mit erfolglos behandelten Verschlüssen der inneren Halsschlagader oder der mittleren Gehirnschlagader, bei denen ein großes Infarktareal besteht, laufen Gefahr, eine solche Hirnschwellung zu entwickeln [3]. Durch den ansteigenden intrakraniellen Druck wird das Hirn eingeklemmt bzw. verschoben und irreversibel geschädigt. Zunächst kann mit intravenös zugeführten Osmotika wie Mannitol oder hypertoner Kochsalzlösung versucht werden, die Schwellung zu mindern. In schweren Fällen bleibt nur die dekompressive Hemikraniektomie, also die teilweise Entfernung der Schädeldecke, um den Hirndruck zu senken [3].
Duale antithrombotische Therapie: doppelt wirkt besser?
Wer einmal einen Schlaganfall erlitten hat, läuft Gefahr, innerhalb der nächsten Jahre einen Re-Infarkt zu erleiden. 10 bis 15% aller Schlaganfallpatienten müssen im Schnitt solch ein Ereignis durchmachen [5]. Deshalb erfolgt die antithrombotische Sekundärprävention möglichst frühzeitig. Die S2e-Leitlinie empfiehlt eine erste Gabe von 100 bis 300 mg Acetylsalicylsäure (ASS) innerhalb der ersten 24 bis 48 Stunden [3]. Bei Patienten, die eine Lysetherapie mit Alteplase erhalten haben, muss allerdings zunächst eine mögliche intrakranielle Blutung mittels geeigneter Bildgebung ausgeschlossen werden. Die antithrombotische Sekundärprävention ist in der Regel eine lebenslange Therapie. Bei Patienten mit einer ASS-Unverträglichkeit stehen Clopidogrel (75 mg) oder Ticagrelor (zweimal 90 mg) als Alternativen parat. Ein neu in die Leitlinie aufgenommenes Verfahren in der Sekundärprävention ist die frühe duale antithrombotische Therapie bestehend aus ASS und Ticagrelor über 30 Tage oder ASS und Clopidogrel über 21 Tage. Man nimmt an, dass eine Kombination zweier Thrombozytenaggregationshemmer mit unterschiedlichen Angriffspunkten die Wirkung steigern kann. Zahlreiche Inhomogenitäten zwischen den entsprechenden Studien führen allerdings dazu, dass dieser Ansatz den Leitlinienautoren zufolge entgegen den Aussagen anderer internationaler Leitlinien nur eingeschränkt empfohlen werden kann. Patienten mit einem leichten nicht kardioembolischen Schlaganfall ohne Rekanalisationsbehandlung oder einer transitorischen ischämischen Attacke mit hohem Rezidivrisiko können aber davon profitieren. Weniger nicht-tödlichen Rezidiven und einer geringfügigen Verbesserung der Behinderung und Lebensqualität stehen aber eine gleichzeitig unveränderte Mortalität und ein erhöhtes Risiko für extrakranielle Blutungen gegenüber [3].
Eine antithrombotische Therapie stellt allerdings nur einen Baustein eines langfristigen Behandlungsplans dar. Es gilt, eventuelle kardiovaskuläre Risikofaktoren zu erkennen und zu behandeln, sowohl zur Rezidivprophylaxe als auch im Rahmen der Primärprävention in der Allgemeinbevölkerung (s. Kasten „Säulen der Schlaganfallprävention“). Hierzu zählen unter anderen der Lebensstil, Rauchen, Bluthochdruck, eine Hypercholesterinämie, Diabetes und ein vergangenes kardiovaskuläres Ereignis. Je mehr Faktoren zutreffen, umso höher das Risiko für atherosklerotische Veränderungen der Gefäße und dementsprechend das Schlaganfallrisiko. Ein Mix aus Lebensstiländerungen und einer geeigneten Medikation kann die Gefahr außerordentlich eingrenzen. Die Global-Burden-of-Disease Studie bspw. kam zu dem Schluss, dass 90% aller Schlaganfälle auf beeinflussbare Faktoren zurückgeführt werden können [6]. Gerade der Einfluss des Lebenswandels, der laut den Ergebnissen der Forscher für knapp 75% aller Schlaganfälle verantwortlich ist, darf nicht unterschätzt werden.
Säulen der Schlaganfallprävention
1. Lebensstiländerung
- komplette Einstellung des Rauchens
- Kost reich an pflanzlichen Lebensmitteln, z. B. mediterrane Diät
- maximal 5 bis 6 g Salz täglich
- maximal 10 bis 12 g Alkohol pro Tag für Frauen und 20 g für Männer (entspricht ca. einem halben Liter Bier oder 200 ml Wein für Männer und knapp die Hälfte für Frauen)
- mindestens 75 Minuten intensive körperliche Aktivität oder 150 Minuten mäßige Aktivität pro Woche, zusätzlich zweimal wöchentliches Krafttraining
2. Thrombozytenaggregationshemmung
- 100 mg ASS täglich (alternativ 75 mg Clopidogrel oder zweimal 90 mg Ticagrelor)
- ein Muss in der Sekundärprävention
- in Primärprävention bei hohem Schlaganfallrisiko
- frühe duale Thrombozytenaggregationshemmung (ASS und Ticagrelor über 30 Tage oder ASS und Clopidogrel über 21 Tage) für ausgewählte Patienten in der Sekundärprävention, z. B. nach transitorischer ischämischer Attacke mit hohem Rezidivrisiko oder nach einem leichten nicht kardioembolischen Schlaganfall ohne erfolgter Rekanalisation
3. Blutdrucknormalisierung
- Zielwert: < 140/90 mmHg
- Substanzauswahl anhand persönlicher Verträglichkeit und Komorbiditäten
4. Behandlung einer Hypercholesterinämie
- Zielwert: < 100 mg/dl LDL-Cholsterol
- Zielwert: < 70 bzw. 55 mg/dl LDL-Cholsterol bei hohem bzw. sehr hohem Risiko
- Atorvastatin und Rosuvastatin bei Hochrisiko-Patienten
- Ezetimib als Kombinationspartner bei unzureichender Senkung der Werte
- keine Empfehlung für andere Lipidsenker
5. Diabetestherapie
- leitliniengerechte Therapie eines Diabetes mellitus mit HbA1c-Zielkorridor von 6,5 bis 7,5%
6. Antikoagulation bei Vorhofflimmern
- Vitamin-K-Antagonisten Phenprocoumon und Warfarin: individuelle Dosierung; INR-Zielwert von 2,5
- neue Orale Antikoagulanzien (NOAK) Dabigatranetexilat, Rivaroxaban, Apixaban und Edoxaban:
- Dosierung strikt nach Herstellerangaben, um häufig auftretende Unterdosierung zu vermeiden
Der Lebensstil ist entscheidend
Wer an den drei Stellschrauben Ernährung, Bewegung und Alkohol- sowie Zigarettenkonsum dreht, hat deshalb schon viel gewonnen. Personen mit einem erhöhten Schlaganfallrisiko sollten eine abwechslungsreiche Kost zu sich nehmen, die zum großen Teil aus pflanzlichen Lebensmitteln besteht [7]. Ein klassisches Beispiel für solch eine Ernährung ist die mediterrane Diät, die reich an Obst, Gemüse, Nüssen und Olivenöl ist. Bei einem hohen Schlaganfallrisiko sollte darüber hinaus die Salzaufnahme auf maximal fünf bis sechs Gramm täglich reduziert werden [7]. Wer rastet, der rostet. Daher gilt: 75 Minuten intensive körperliche Aktivität oder 150 Minuten mäßige Aktivität pro Woche mit zusätzlich zweimal wöchentlichem Krafttraining sind Mindestmaß [7]. Sport vermindert Risikofaktoren wie Bluthochdruck und zu hohe Blutlipidwerte und trägt zur Gewichtsabnahme bei [8]. Bekanntermaßen sollte ein eventuelles Übergewicht reduziert werden.
Die dritte Säule der Lebensstiländerungen stellt der Konsum der Genussmittel Alkohol und Zigaretten dar. Das Rauchen sollte komplett eingestellt werden. Das Schlaganfallrisiko reduziert sich so um 35 bis 50% – effektiver als jede pharmakologische Maßnahme [7]. Eine Reihe von Angeboten steht zur Verfügung, um die Entwöhnung von der Zigarette zu erleichtern, z. B. die Initiative www.rauch-frei.info.de der Bundeszentrale für gesundheitliche Aufklärung (BZgA) oder www.ohnekippe.de. der Thoraxklinik-Heidelberg. Auch beim Alkohol ist weniger mehr. Die Deutsche Gesellschaft für Allgemeinmedizin und Familienmedizin z. B. empfiehlt maximal 10 bis 12 g Alkohol pro Tag für Frauen und 20 g für Männer [7]. Letzteres entspricht ca. einem halben Liter Bier oder 200 ml Wein.
Normalisierung des Blutdrucks besonders effektiv
Nicht immer ist eine Lebensstiländerung ausreichend oder durchsetzbar. Um das Schlaganfallrisiko einzudämmen, muss nicht zuletzt auf pharmakologische Interventionen zurückgegriffen werden. Die beiden zentralen kardiovaskulären Risikofaktoren, die neben einer Behandlung eines möglichen Diabetes mellitus medikamentös kontrolliert werden können, sind der Blutdruck und die Blutlipidwerte. Eine Blutdrucknormalisierung ist dabei die wirksamste medikamentöse Maßnahme, um ischämische und hämorrhagische Schlaganfälle zu verhindern. Die verschiedenen Fachgesellschaften weltweit bewerten die Grenzwerte für einen erhöhten Blutdruck jeweils unterschiedlich. Hierzulande wird eine langfristige Blutdrucksenkung unter 140/90 mmHg angestrebt [7]. Die Auswahl der Wirkstoffe richtet sich nach dem persönlichen Komorbiditäts- und Verträglichkeitsprofil.
Reicht eine Lebensstiländerung nicht aus, um die Blutlipide zu normalisieren, können Statine eingesetzt werden. Ihr protektiver Einfluss auf das Schlaganfallrisiko in der Primär- und Sekundärprävention ist belegt. Bei Patienten mit verschiedenen kardiovaskulären Risikofaktoren sollte der Nutzen der Präparate individuell beurteilt werden, auch im Hinblick auf koronare Ereignisse. Patienten, die bereits einen Schlaganfall erlitten haben, soll aber laut Therapieleitlinie ein Statin angeboten werden [7]. In der Schlaganfallprävention gibt es noch wenig Erkenntnisse darüber, welche LDL-Cholesterol-Zielwerte angestrebt werden sollten. Die Arzneimittelkommission der deutschen Ärzteschaft z. B. empfiehlt, den LDL-Cholesterol-Wert auf unter 100 mg/dl bzw. wenigstens um 30 bis 40% abzusenken [9]. Bei Patienten mit einem hohen oder sehr hohen kardiovaskulären Risiko empfehlen die Gesellschaften für Kardiologie und Rehabilitationswissenschaften niedrigere Grenzwerte: < 70 mg/dl bei hohem Risiko und < 55 mg/dl bei sehr hohem Risiko [7]. Ezetimib kann bei einer unzureichenden Absenkung der Werte als Kombinationspartner in Frage kommen. Andere Lipidsenker wie Fibrate werden aber nicht zur Schlaganfallprophylaxe empfohlen [7].
Acetylsalicylsäure (ASS), der Grundpfeiler der Sekundärprävention, wird in der Primärprophylaxe hingegen differenzierter eingesetzt, da die Effektivität bei ansonsten gesunden Personen umstritten ist und darüber hinaus mögliche positive Effekte durch das erhöhte Blutungsrisiko aufgehoben werden [7]. Bei einem hohen Schlaganfallrisiko sollte ASS aber vorbeugend zur Thrombozytenaggregationshemmung verwendet werden. Ein wichtiger Risikofaktor für einen embolischen Schlaganfall ist das Vorhofflimmern. Durch die eingeschränkte atriale Kontraktion staut sich das Blut im linken Vorhof oder linken Vorhofohr. Die Stase kann dazu führen, dass sich Thromben bilden und mit dem Blutstrom ins Gehirn getragen werden. Um der Thrombenbildung entgegenzuwirken, werden orale Antikoagulantien eingesetzt [7]. Man unterscheidet zwei Wirkstoffklassen, die Vitamin-K-Antagonisten Phenprocoumon (Marcumar®) und Warfarin (Coumadin®) sowie die neuen oralen Antikoagulanzien (NOAK) Dabigatranetexilat (Pradaxa®), Rivaroxaban (Xarelto®), Apixaban (Eliquis®) und Edoxaban (Lixiana®). Welchem der beiden Wirkstoffgruppen der Vorzug gegeben wird, sollte von Patient zu Patient entschieden werden. Generell sind die neuen Antikoagulantien vorzuziehen, da sie das Risiko für intrakranielle Blutungen deutlich reduzieren [7]. |
Literatur
[1] Heuschmann PU et al. Schlaganfallhäufigkeit und Versorgung von Schlaganfallpatienten in Deutschland. Aktuelle Neurologie 2010:37;333-340
[2] Busch MA, Kuhnert R. 12-Monats-Prävalenz von Schlaganfall oder chronischen Beschwerden infolge eines Schlaganfalls in Deutschland. J Health Monitor 2017;2(1)
[3] Ringleb P et al. Akuttherapie des ischämischen Schlaganfalls. S2e-Leitlinie der Deutschen Gesellschaft für Neurologie (Hrsg.), Leitlinien für Diagnostik und Therapie in der Neurologie 2021, Stand: Mai 021, AWMF-Registernummer 030-046, www.dgn.org/leitlinien
[4] Langhorne P et al. Organised inpatient (stroke unit) care for stroke: network metaanalysis. Cochrane Database of Systematic Reviews 2020;4:CD000197
[5] Flach C et al. Risk and Secondary Prevention of Stroke Recurrence: A Population-Base Cohort Study. Stroke 2020;51:2435-2444
[6] Feigin VL et al. Global burden of stroke and risk factors in 188 countries, during 1990–2013: a systematic analysis for the Global Burden of Disease Study 2013. Lancet Neurol 2016;15:913-924
[7] Schlaganfall. S3-Leitlinie der Deutschen Gesellschaft für Allgemeinmedizin und Familienmedizin (DEGAM), Stand: 2020, AWMF-Register-Nr. 053-011
[8] Lee CD et al. Physical Activity and Stroke Risk - A Meta-Analysis. Stroke 2003;34:2475–2481
[9] Empfehlungen zur Therapie von Fettstoffwechselstörungen. Arzneimittelkommission der deutschen Ärzteschaft (AkdÄ) 2012, www.akdae.de/
[10] Campbell BCV et al. Ischaemic stroke. Nat Rev Dis Primers 2019;5:70
Auf dem Weg zur individualisierten Akuttherapie
An der aktualisierten S2e-Leitlinie zur Akuttherapie beim ischämischen Schlaganfall war Dr. med. univ. Christian Hametner M.Sc. von der Neurologischen Klinik und Poliklinik am Universitätsklinikum Würzburg aktiv beteiligt. Wir sprachen mit ihm darüber, wie sich die Schlaganfall-Akuttherapie in den letzten Jahren verändert hat.
DAZ: Wie hat sich die Therapie des Schlaganfalls seit dem letzten Update der Leitlinie 2015 gewandelt?
Dr. med. Christian Hametner:Die Akuttherapie des ischämischen Schlaganfalles wird schneller, präziser und individualisierter. Für die Alteplase, die einzige in der EU genehmigte medikamentöse Therapie bei akuten Schlaganfällen mit systemischer Thrombolyse, wurde die Zulassung erweitert. Seit 2018 können nun Patienten über 80 Jahren mit Alteplase behandelt werden. Die Bildgebung identifiziert immer präziser jenes Hirngewebe, das von einer Wiedereröffnung eines Gefäßverschlusses profitieren kann. Darüber hinaus entwickelt sich die mechanische Thrombektomie technisch laufend weiter. Ihre Effektivität zur Behandlung von großen, intrakraniellen Gefäßverschlüssen wurde bestätigt und hat sich als Standardtherapie etabliert.
DAZ: Die systemische Lyse mit Alteplase hat sich als wichtige Säule der Akuttherapie etabliert. Welche Vorteile könnte eine zukünftige Therapieoption mit Tenecteplase bringen?
Hametner: Tenecteplase ist ein dem humanen Tissue-Plasminogen-Aktivator ähnliches Molekül. Eine Veränderung der Proteinstruktur an drei Stellen führt zu einer höheren Fibrin-Bindung und weniger schnellen Inaktivierung des Enzyms. Ob dieser pharmakologische „Vorteil“ eine Besserung im klinischen Ansprechen und einer verminderten Blutungsrate im Vergleich zu anderen Thrombolytika bringt, gilt es in randomisiert kontrollierten Studien mit klinischem Primärendpunkt zu beweisen. Aktuell ist Tenecteplase ausschließlich für die Behandlung des akuten Herzinfarktes zugelassen. Ein aktuell bereits ersichtlicher Vorteil ist die Applikationsform – Tenecteplase wird als einmaliger Bolus (keine Dauerinfusion) verabreicht. Diese einfachere Handhabung ist zum Beispiel für Patienten mit sekundärer Verlegung in ein Thrombektomiezentrum sehr interessant.
DAZ: Ein signifikanter Anteil der Patienten erleidet Rezidive, eine Sekundärprävention ist daher unabdingbar. Welchen Stellenwert hat die duale antithrombotische Therapie?
Hametner: Die aktuelle Datenlage zeigt, dass es für sorgfältig ausgewählte Patienten in der Frühphase nach dem Schlaganfall von Vorteil sein kann, wenn zwei Thrombozytenaggregationshemmer eingesetzt werden. Ein routinemäßiger Einsatz der dualen Plättchenhemmung (ASS+Clopidogrel, ASS+Ticagrelor) kann aktuell nicht empfohlen werden – es bedarf weiterer klinischer Studien.
DAZ: Die Leitlinie geht auch auf geschlechtsspezifische Aspekte ein.
Hametner: Dies ist ein sehr wichtiges Thema, insbesondere bei der Entwicklung hin zu einer individualisierten Schlaganfalltherapie. Generell ist erfreulich, dass der Anteil an Frauen, die an Studien teilnehmen, größer geworden ist, wenngleich er immer noch meist unter 50% liegt. Die Behandlung des akuten Schlaganfalles setzt voraus, dass er erkannt wird. Hier gibt es Hinweise, dass bei Frauen häufig untypische Schlaganfallsymptome (Bewusstseins- und kognitive Störungen) auftreten. Dies mag ein Grund dafür sein, dass prähospital die Verdachtsdiagnose Schlaganfall bei Frauen seltener korrekt gestellt wird. Obgleich die Behandlung mit einer systemischer Thrombolyse bei Frauen gleich wirksam ist, wurde sie weniger häufig angewandt (-13%), als bei Männern. Aus epidemiologischer Sicht erleiden Frauen Schlaganfälle häufiger im höheren Alter. Ein Grund für den unterschiedlichen Behandlungsanteil könnte die Zurückhaltung der Thrombolyse bei älteren Patientinnen vor 2018 sein. Erfreulicherweise zeigt sich in den letzten Jahren ein Rückgang dieses Unterschieds. Hinsichtlich der mechanischen Thrombektomie, die für Frauen gleich effektiv und gleich sicher ist, zeigt sich interessanterweise ein gegengleicher Trend in den Behandlungszahlen. Frauen werden mit höherer Wahrscheinlichkeit per Thrombektomie behandelt (+26%). Insgesamt sollten aber Frauen wie Männer nach aktuellem Wissensstand in der Akuttherapie des ischämischen Schlaganfalles dem gleichen Behandlungsregimen unterzogen werden.
DAZ: Dr. Hametner, vielen Dank!

























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.