
- DAZ.online
- DAZ / AZ
- DAZ 26/2020
- Mit Darolutamid gegen ...
Arzneimittel und Therapie
Mit Darolutamid gegen Prostatakrebs
Neuer Androgenrezeptor wirkt effektiv bei Tumorpatienten
Mit Darolutamid (Nubeqa®) hat Bayer kastrationsresistentem Prostatakarzinom den Kampf angesagt. Und das mit großen Erfolgsversprechen. In jedem Fall ist es wünschenswert, denn Prostatakrebs ist inzwischen die häufigste Krebserkrankung bei Männern. In Deutschland beträgt der Anteil an Prostatakarzinomen etwa 25%. Pro Jahr treten nach einer Schätzung des Robert Koch-Instituts knapp 60.000 neue Fälle auf. Das Erkrankungsrisiko steigt ab 50 Jahren stark an. Die meisten Patienten sind älter als 70 Jahre. Prostatakrebs steht an dritter Stelle bei den zum Tode führenden Krebserkrankungen (11,3%). Jährlich versterben ca. 12.000 Männer an den Folgen der Erkrankung. Besonders heimtückisch: Prostatakrebs schreitet ziemlich lange symptomlos voran. Wird er endlich entdeckt, ist es meist schon zu spät und die Überlebenschancen sind bereits stark gesunken. Auch deshalb gehört die Prostatakrebs-Vorsorge-Untersuchung zum Standardprozedere für Männer ab 45 Jahren. Behandlungsoptionen für das organbegrenzte Prostatakarzinom sind die Operation, die Bestrahlung oder bei langsamem Wachstum das „watchful-waiting“ (beobachtendes Abwarten). Wächst der Tumor organüberschreitend, wird neben Bestrahlungs- und Chemotherapie eine Hormonentzugstherapie empfohlen [1, 2]. Grundlage dafür ist, dass acht von zehn Prostatakarzinomen testosteronabhängig wachsen. Wie wir es bereits vom Brustkrebs kennen, lässt sich auch der Prostatakrebs nach seiner Hormonempfindlichkeit einteilen. Hormonsensitive Formen werden mit klassischen Antiandrogenen behandelt. Durch Hemmung von Testosteron kommt es zur Wachstumshemmung der Krebszellen. Beim sogenannten kastrationsresistenten Prostatakrebs schreitet das Wachstum trotz der Herunterregulierung der Testosteronproduktion weiter voran. Keine guten Aussichten. Nun steht für diese Patienten eine weitere Behandlungsoption zur Verfügung: Darolutamid, das von Bayer zusammen mit Orion Corporation entwickelt wurde.
Antiandrogene – im Prinzip gleich, und doch so heterogen
Antiandrogene sind uns bereits seit den 1960er-Jahren bekannt. Als erster steroidaler Wirkstoff kam Cyproteronacetat (z. B. Androcur®) auf den Markt. Strukturell abgeleitet von Progesteron sind steroidale Antiandrogene meist weniger selektiv als die neueren Wirkstoffe und werden heute vor allem zur hormonellen Kontrazeption (z. B. Diane®-35) eingesetzt. Etwa 20 Jahre später, in den 1980er-Jahren, wurde der erste nichtsteroidale Vertreter dieser recht heterogenen Wirkstoffklasse zugelassen: Flutamid (z. B Fluta-cell®). Mit Einzug der nichtsteroidalen Antiandrogene gelang es die therapeutische Bandbreite zu vergrößern. Antiandrogene werden heute bei Prostatakarzinom, Hirsutismus oder anderen Androgenisierungserscheinungen bei Frauen eingesetzt. Etwas außergewöhnlicher ist ihr Einsatz zur Triebdämpfung beim Mann (chemische Kastration). Diese wird in Deutschland nur mit Einverständnis des Patienten durchgeführt. Anders als z. B. in den USA, wo der Einsatz auch gerichtlich angeordnet werden darf und wird.
Zur Klasse der Antiandrogene zählen neben Androgenrezeptor-Antagonisten auch Androgen-Synthesehemmer (CYP17A1-Hemmer wie Abirateronacetat, Zytiga®) sowie die zur Behandlung der benignen Prostatahyperplasie zugelassenen 5α-Reduktasehemmer (z. B. Finasterid, Proscar®). Indem man mit Gonadotropin-Releasing-Hormon-Modulatoren (z. B. Leuprorelin, Eligard®) in die Funktion des Hypothalamus als zentrales Hormon-Steuerorgan eingreift, kann ebenfalls eine antiandrogene Wirkung erzielt werden [3].
Neuester Vertreter: Darolutamid
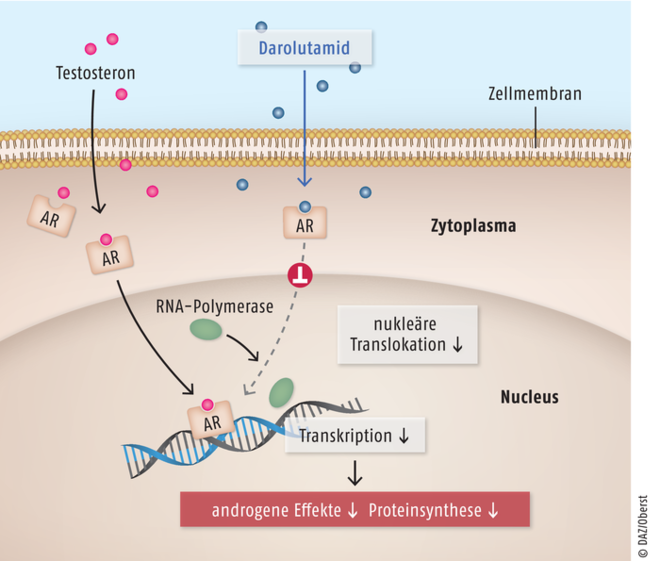
Der neueste nichtsteroidale Vertreter Darolutamid hemmt kompetitiv den Androgenrezeptor sowie die Translokation in den Zellkern und die Androgenrezeptor-vermittelte Transkription (siehe Abbildung). Ebenso trägt der pharmakologisch aktive Hauptmetabolit Keto-Darolutamid entscheidend zur antitumoralen Wirkung bei. Der neue Wirkstoff ist als Filmtablette mit einer Dosierung von 300 mg auf dem Markt. Die offizielle Indikation lautet: zur Behandlung von nicht-metastasiertem kastrationsresistentem Prostatakarzinom bei erwachsenen Männern, die ein hohes Risiko für die Entwicklung von Metastasen aufweisen. Empfohlen wird eine Dosis von zweimal täglich 600 mg zu einer Mahlzeit. Nüchtern eingenommen beträgt die absolute Bioverfügbarkeit von Darolutamid etwa 30% im Vergleich zur intravenösen Gabe. Bei Einnahme zu einer Mahlzeit erhöht sie sich um den Faktor 2 bis 2,5. Therapiebegleitend soll laut Fachinformation eine medikamentöse Kastration mit einem Gonadotropin-Releasing-Hormon-Analogon fortgeführt werden, sofern keine vorherige chirurgische Kastration (Orchiektomie) erfolgt ist. Das Nebenwirkungsprofil von Darolutamid ist typisch für die Wirkstoffklasse. Die am häufigsten beschriebene Nebenwirkung Fatigue (Erschöpfung) tritt bei 15,8% der Patienten auf (Placebo: 11,4%). Bei knapp jedem fünften Patienten verringerte sich die Neutrophilenzahl (Placebo: 9,4%) unter Darolutamid. Dies führte in den vorangegangenen klinischen Studien allerdings nur bei einem Patienten zum Absetzen des Wirkstoffes. Die Neutropenie war bei etwa 88% der Patienten vorübergehend oder reversibel und so leicht, dass kaum klinisch relevante Anzeichen oder Symptome auftraten. Generell ist unter der Therapie mit Darolutamid auf die Blutwerte zu achten: Bilirubin erhöhte sich bei 16,4% der Patienten (6,9% Placebo), eine Erhöhung des Leberfunktionswerts AST konnte bei 22,5% (13,6% Placebo) festgestellt werden. Frakturen, die für die Wirkstoffklasse recht typisch sind, traten bei 4,2% auf (3,6% Placebo). Darolutamid wird hauptsächlich über CYP3A4 oxidativ abgebaut. Daher sollte eine gleichzeitige Anwendung von CYP3A4-Inhibitoren wie Azol-Antimykotika nur unter Überwachung erfolgen. Das Sicherheitsprofil von Darolutamid bleibt unterm Strich günstig und ermöglicht Männern, auch bei längerer Anwendung ihren aktiven Lebensstil fortzusetzen [4].
Abb.: Physiologisch bindet Testosteron an den Androgenrezeptor (AR) im Zytoplasma.Erst durch die Bindung von Testosteron ist AR in der Lage, in den Zellkern einzuwandern und dort mithilfe des Enzyms RNA-Polymerase die Gen-Transkription auszulösen. Der neue Wirkstoff Darolutamid bindet an die Ligandenstelle von AR und verhindert so die nukleäre Translokation mit anschließender AR-vermittelter Transkription. Als Folge werden keine Proteine mit androgener Wirkung gebildet. Bei Prostatakarzinompatienten kann so effektiv das Wachstum des Tumors verlangsamt werden.
Wie ist die Studienlage?
Die Ergebnisse der randomisierten Phase-III-Doppelblindstudie ARAMIS (Androgen Rezeptor Antagonizing Agent for Metastasis-free Survival) haben zur Zulassung von Darolutamid geführt. Eingeschlossen wurden insgesamt 1509 Patienten, die randomisiert im Verhältnis 2 : 1 zusätzlich zur Androgendeprivationstherapie (ADT) entweder zweimal täglich 600 mg Darolutamid per os (n = 955) oder Placebo (n = 554) erhielten. Bei den Studienteilnehmern handelte es sich um Männer im Alter zwischen 48 und 95 Jahren, die während der ADT in einem mindestens einwöchigen Abstand drei ansteigende PSA-Werte hatten. Primärer Endpunkt der Studie war das metastasenfreie Überleben (engl. metastasis-free survival, MFS). Sekundäre Endpunkte umfassten Faktoren wie das Gesamtüberleben, die Zeit bis zur Schmerzprogression, Zeit bis zum Einleiten einer ersten Chemotherapie oder Zeit bis zum Auftreten erster symptomatischer Knochenereignisse (z. B. Knochenfrakturen).
Die Ergebnisse in ARAMIS sind überzeugend: Darolutamid führte insgesamt zu einer Verbesserung des MFS mit einem Median von 40,4 Monaten gegenüber 18,4 Monate unter Placebo plus ADT (HR = 0,41; 95% KI 0,34 bis 0,50; p < 0,001). Auch im Gesamtüberleben zeigte sich eine signifikante Verbesserung. Insgesamt verringerte sich das Metastasen- oder Sterberisiko unter Darolutamid um 59%. Bei guter Verträglichkeit erzielte der Wirkstoff auch in den sekundären Endpunkten gute Ergebnisse. Ein besonderer Vorteil: Darolutamid verringerte die Lebensqualität der Betroffenen nicht maßgeblich. Mit Darolutamid hat Bayer einen neuen Vertreter der Antiandrogene gefunden, der in präklinischen Studien eine geringere Toxizität und bessere Verträglichkeit gegenüber vergleichbaren Wirkstoffen (z. B. Apalutamid [Erleada®] oder Enzalutamid [Xtandi®]) zeigte. Darolutamid durchdringt aufgrund seiner besonderen Struktur nicht die Blut-Hirn-Schranke. Derzeit läuft eine weitere Phase-III-Studie, in der die Sicherheit und Wirksamkeit von Darolutamid bei Patienten mit bereits metastasierendem hormonsensitivem Prostatakarzinom untersucht wird (ARASENS, Ende voraussichtlich 2022) [5]. |
Literatur
[1] Rohde V et al. Prostataerkrankungen. Themenheft des Robert Koch-Instituts. 2007, Nr. 36
[2] Früherkennung, Diagnose und Therapie der verschiedenen Stadien des Prostatakarzinoms. S3-Leitlinie der Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften e. V. (AWMF), Deutschen Krebsgesellschaft e. V. (DKG) und Deutschen Krebshilfe (DKH). AWMF-Registernr: 043/022OL, Stand Mai 2019
[3] Geisslinger et al. Mutschler Arzneimittelwirkungen, 8. Auflage 2001, Wissenschaftliche Verlagsgesellschaft Stuttgart
[4] Fachinformation zu Nubeqa®, Stand März 2020
[5] Fizazi K et al. Darolutamide in nonmetastatic, castration-resistant prostate cancer. N Engl j Med 2019;380(13):1235-1246





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.