
- DAZ.online
- DAZ / AZ
- DAZ 13/2020
- Alte Besen kehren gut
Pandemie Spezial
Alte Besen kehren gut
Könnten Chloroquin und Hydroxychloroquin die neuen Wunderwaffen gegen COVID-19 sein?
Klinische evidenzbasierte, randomisierte Doppelblindstudien zum Einsatz von Chloroquin bzw. Hydroxychloroquin bei COVID-19-Patienten sucht man bislang vergeblich. Im Rahmen von In-vitro-Studien konnte jedoch an SARS-CoV-2-infizierten Verozellen gezeigt werden, dass die beiden Substanzen eine antivirale Aktivität aufweisen. In Zellkulturen wurde die Vermehrung des SARS-CoV-2 bei Konzentrationen (EC50 = Konzentration mit halbmaximaler Wirkung) von 1,13 µM Chloroquin gehemmt [1]. Auch während des vorherigen Ausbruchs des durch das eng verwandte SARS-CoV ausgelöste Schweren Akuten Respiratorischen Syndroms (SARS) in 2002/2003 wurde berichtet, dass Chloroquin und Hydroxychloroquin in vitro eine Anti-SARS-CoV-Aktivität besitzen [2].
Die 4-Aminochinolone Chloroquin und Hydroxychloroquin weisen keine wesentlichen Unterschiede hinsichtlich des Wirkungsmechanismus auf. Hydroxychloroquin besitzt ein günstigeres Sicherheitsprofil als Chloroquin und soll eine geringere okuläre Toxizität (Retinopathie) besitzen. Nach oraler Applikation werden die beiden Wirkstoffe rasch und vollständig aus dem Darm resorbiert und in zahlreichen Geweben angereichert. Sie werden aus diesen Depots nur langsam freigesetzt und haben somit eine lange Halbwertszeit von 30 bis 60 Tagen.
Möglicher Wirkmechanismus
Der antivirale Wirkmechanismus beider Arzneimittel ist noch nicht vollständig aufgeklärt. Da beide Arzneistoffe schwache Basen sind, von denen bekannt ist, dass sie sowohl den pH-Wert der Oberflächen als auch von sauren intrazellulären Organellen wie Endosomen und Lysosomen erhöhen, geht man davon aus, dass schon die Fusion des Virus mit der Zellmembran gehemmt wird [3]. Zusätzlich könnte der SARS-CoV-Eintritt durch Veränderung der Glykosylierung von (Angiotensin-konvertierendes Enzym 2)ACE2-Rezeptor und Spike-Protein gehemmt werden [4]. Die Ansäuerung ist für die Reifung und Funktion der Endosomen von entscheidender Bedeutung. Man vermutet, dass Chloroquin und Hydroxychloroquin die Reifung der Endosomen in Zwischenstadien der Endozytose blockieren, was dazu führt, dass der weitere Transport von Virionen zur endgültigen Freisetzungsstelle fehlschlägt. Chloroquin und Hydroxychloroquin inhibieren also neben dem Eintritt auch die Post-Entry-Stadien von SARS-CoV-2 [5].
Weiterhin geht man davon aus, dass die beiden Arzneistoffe die Produktion und Freisetzung von Zytokinen und weiteren entzündungsfördernden Faktoren (z. B. Interleukin 6) erheblich verringern können. Klinische Untersuchungen ergaben, dass im Plasma kritisch kranker Patienten, die mit SARS-CoV-2 infiziert waren, eine hohe Konzentration an Zytokinen festgestellt wurde. Was darauf hindeutet, dass die Zytokinkonzentration mit der Schwere der Erkrankung verbunden war [6]. Somit könnten Chloroquin und Hydroxychloroquin bei COVID‑19-Patienten auch zur Abschwächung der Entzündungsreaktion beitragen.
Empfehlungen der Fachgesellschaften
Mehrere medizinische Fachgesellschaften haben eine gemeinsame Empfehlung zur intensivmedizinischen Betreuung von COVID-19-Patienten veröffentlicht [8]. Darin heißt es zur medikamentösen Therapie, dass für eine spezifische antivirale Therapie bislang noch keine ausreichenden Daten vorliegen und es Therapieversuche mit einer Reihe von Substanzen wie Hydroxychloroquin und anderen gibt. Ein Einsatz kann unter Umständen nach einer Benefit-Risiko-Abwägung als Einzelfallentscheidung erwogen werden und sollte, wenn möglich, im Rahmen von Compassionate-Use-Programmen oder Studienprotokollen durchgeführt werden.
Herausforderung Dosierung
In physiologiebasierten pharmakokinetischen Modellen (PBPK) wurden für beide Wirkstoffe die Konzentrationen in der Lungenflüssigkeit unter fünf verschiedenen Dosierungsschemata simuliert, um das effektivste Schema unter Berücksichtigung des Sicherheitsprofils zu ermitteln. Basierend auf den Ergebnissen der PBPK-Modelle wird für die SARS-CoV-2-Infektion eine Initialdosis von zweimal täglich 400 mg Hydroxychloroquinsulfat oral empfohlen, gefolgt von einer Erhaltungsdosis von zweimal 200 mg täglich über vier Tage [7]. Zuverlässige Daten aus randomisierten klinischen Studien zur optimalen Therapiedauer und Dosierung fehlen jedoch. Von US-amerikanischen Ärzten werden in Einzelberichten verschiedene mögliche Therapieregime für Hydroxychloroquin genannt: 400 mg zweimal täglich als Initialdosis, gefolgt von 400 mg einmal täglich für fünf weitere Tage; 400 mg zweimal täglich als Initialdosis, gefolgt von 200 mg zweimal täglich für vier weitere Tage; 600 mg zweimal täglich als Initialdosis, gefolgt von 400 mg einmal täglich für vier weitere Tage [14].
Erste Erfahrungen aus China
Chloroquin wurde bei mehreren Hundert Patienten in über zehn Krankenhäusern in China eingesetzt. In einer Veröffentlichung der japanischen Fachzeitschrift „BioScience Trends“ wurde über eine bessere Wirkung als Placebo berichtet [9]. Konkrete Angaben zu Studienaufbau und Ergebnissen wurden bislang allerdings nicht publiziert.
Ergebnisse aus Frankreich
Die Veröffentlichung der In-Vitro-Ergebnisse veranlasste auch Forscher in Marseille dazu, eine klinische, offene, nicht randomisierte Studie zu starten. Patienten, bei denen eine Infektion mit SARS-CoV-2 bestätigt worden war, sollten Hydroxychloroquin und zum Teil Azithromycin (um bakteriellen Superinfektionen vorzubeugen) unter EKG-Kontrolle erhalten [10]. Behandelt wurden 26 Patienten, die mit 16 nicht behandelten Patienten, die auch an SARS-CoV-2 erkrankt waren (Kontrollgruppe), verglichen wurden. Allerdings wurden nur 20 Patienten der Verumgruppe bei der Analyse berücksichtigt, da bei den restlichen sechs Patienten die Behandlung nicht fortgeführt werden konnte. Bei zwölf Patienten waren die Beschwerden auf die oberen Atemwege beschränkt, zwei Infizierte waren asymptomatisch. Über zehn Tage bekamen die Patienten in der Verumgruppe 600 mg Hydroxychloroquin täglich (dreimal 200 mg). Die Viruslast in Nasopharynx-Abstrichen wurde täglich im Krankenhaus getestet. Das Vorhandensein und Fehlen des Virus an Tag 6 nach der Aufnahme wurde als Endpunkt festgelegt.
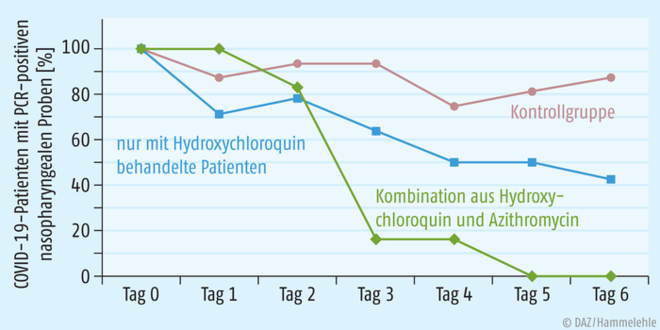
Nach sechs Tagen hatte sich die Viruslast bei den Patienten der Verumgruppe im Vergleich zur Kontrollgruppe signifikant verringert. Bei den Patienten, die zusätzlich Azithromycin erhielten, kam es zu einer noch effizienteren Virusreduktion (s. Abbildung 1).
Abb. 1: Verringerung der Viruslast unter Hydroxychloroquin ± Azithromycin im Vergleich zur Kontrollgruppe Prozentsatz der COVID-19-Patienten mit PCR-positiven nasopharyngealen Proben vom Einschlusstag bis zum sechsten Tag nach Einschluss (nach [10])
Weitere Studien gefordert
In Fachkreisen werden der Studienaufbau (nicht randomisiert und doppelblind) sowie der Surrogatparameter (Virusnachweisrate im Hals an Tag 6 nach Aufnahme) bemängelt, der in der französischen Studie statt des klinischen Ausgangs als Endpunkt gewählt wurde. Weiterhin wird angemerkt, dass die beiden Patientengruppen, die verglichen wurden, stark divergieren. Beispielsweise betrug das Durchschnittsalter der mit Hydroxychloroquin ± Azithromycin behandelten Gruppe 51 Jahre und der nicht behandelten Patienten 37 Jahre. Problematisch ist auch die Zeitskala: Aus den Studienunterlagen geht nicht klar hervor, an welchem Tag der Erkrankung die Patienten in die Studie eingeschlossen wurden. Da die Erkrankung in vielen Fällen selbstlimitierend ist, könnte es sein, dass die behandelte Gruppe im Verlauf schon weiter fortgeschritten war als die Kontrollgruppe, als sie eingeschlossen wurde.
Nicht nur die Experten plädieren für große, randomisierte Studien mit harten klinischen Endpunkten. Auch die europäische Arzneimittelagentur (EMA) macht in einer Meldung deutlich, dass sie genau diese Art von Studien fordert und forschende Hersteller bei der Durchführung unterstützt, um die Bekämpfung von COVID-19 voranzutreiben und zu beschleunigen [11].
Aktuell wird diskutiert, die klinische Anwendung von Chloroquin bei SARS-CoV-2-Patienten in Zusammenarbeit mit der Charité in Berlin zu prüfen. Zudem hat die Firma Bayer bekannt gegeben, drei Millionen Tabletten mit dem Wirkstoff Chloroquin zu spenden, um die US-Regierung im Kampf gegen COVID-19 zu unterstützen [19]. In den USA sind mehrere klinische Studien, in denen die prophylaktische bzw. therapeutische Gabe von Hydroxychloroquin zur Behandlung von SARS-CoV-2-Infektionen untersucht werden soll, geplant oder bereits kurz vor der Rekrutierung [14].
Auch die Weltgesundheitsorganisation (WHO) möchte die Wirksamkeit von Chloroquin/Hydroxychloroquin in einer globalen Studie bei Patienten mit SARS-CoV-2-Infektion untersuchen. Neben dem Malariamittel sollen in der SOLIDARITY-Studie das Virostatikum Remdesivir sowie die HIV-Kombination Lopinavir/Ritonavir ± Beta-Interferon getestet werden [15, 16].
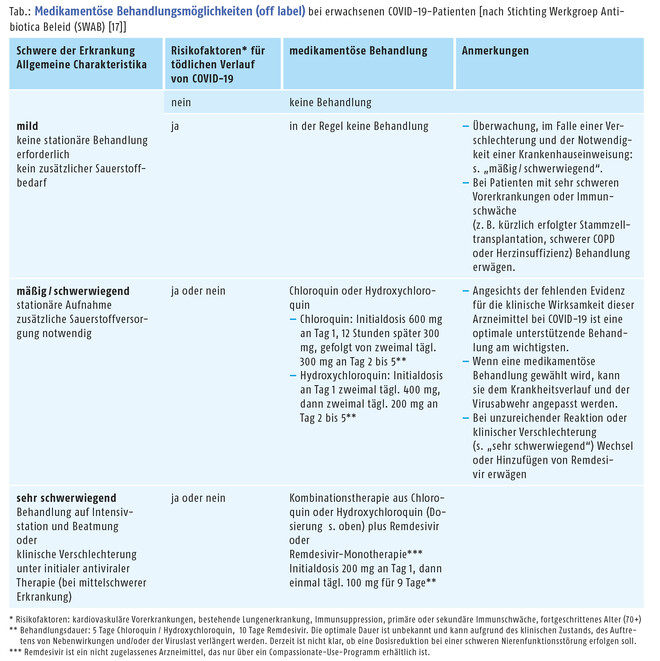
Auch wenn bislang keine belastbaren Studienergebnisse vorliegen, wird der Off-Label-Einsatz von Chloroquin und Hydroxychloroquin in der klinischen Praxis bei COVID-19-Patienten als mögliche Behandlungsoption angesehen (s. Tabelle) [17]. Aufgrund der fehlenden Evidenz gibt die europäische Gesellschaft für Intensivmedizin diesbezüglich allerdings keine konkreten Empfehlungen [18]. Generell sollten Chloroquin und Hydroxychloroquin nicht gleichzeitig verabreicht werden, da Hydroxychloroquin ein Metabolit von Chloroquin ist.
Fazit
Ob die „alten Besen“ Chloroquin und Hydroxychloroquin tatsächlich als Wunderwaffe gegen SARS-CoV-2 geeignet sind, muss sich zeigen. Die Datenlage und Empfehlungen hierzu ändern sich täglich. Gerade auch unter dem Aspekt, dass sowohl Chloroquin als auch Hydroxychloroquin nicht frei von schweren Nebenwirkungen und Wechselwirkungen sind (s. Kasten „Hydroxychloroquin und Chloroquin in der Praxis“), müssen die bisherigen Ergebnisse noch durch große klinische Studien bestätigt werden. |
Hydroxychloroquin und Chloroquin in der Praxis
Dosierung
- Hydroxychloroquin: Empfohlene Initialdosis zweimal täglich 400 mg oral, gefolgt von einer Erhaltungsdosis von zweimal täglich 200 mg über vier Tage [7]
- Chloroquin: Zweimal täglich 500 mg für zehn Tage [12]
Interaktionen
- Die Universität Liverpool hat unter www.covid19-druginteractions.org eine Aufstellung wahrscheinlicher pharmakokinetischer Interaktionen mit experimentellen Therapien bei COVID-19 veröffentlicht, die sehr hilfreich ist [13].
- Bei der Anwendung von Chloroquin und Hydroxychloroquin ist besondere Vorsicht geboten, wenn gleichzeitig Arzneimittel eingesetzt werden, die zu einer Verlängerung des QTc-Intervalls führen können. Dies sind z. B. Antiarrhythmika der Klasse IA und III, trizyklische Antidepressiva, Antipsychotika und bestimmte antimikrobielle Wirkstoffe. Aufgrund des erhöhten Risikos von ventrikulären Arrhythmien wird eine Überwachung mittels Elektrokardiogramm (EKG) empfohlen.
- Chloroquin und Hydroxychloroquin können zu einem erhöhten Digoxin-Plasmaspiegel führen und die blutzuckersenkende Therapie verstärken.
- Beide Wirkstoffe hemmen CYP2D6, daher wird von einer gleichzeitigen Anwendung von CYP2D6 hemmenden Arzneimitteln (wie Fluoxetin, Paroxetin oder Bupropion) abgeraten.
- Weiterhin kann die Krampfschwelle herabgesetzt werden. Die Wirkung antiepileptischer Arzneimittel kann bei gleichzeitiger Verabreichung mit Hydroxychloroquin beeinträchtigt werden.
Unerwünschte Arzneimittelwirkungen
- Es kann zu einer Verlängerung des QTc-Intervalls kommen. Deshalb sollte bei Patienten mit einem angeborenen stark verlängerten QTc-Intervall (> 500 ms) eine EKG-Überwachung erfolgen.
- Bei längerfristiger Gabe und Dosen von mehr als 6,5 mg/kg Körpergewicht besteht ein Risiko für Retinaveränderungen und Sehstörungen. Daher sollten, wenn möglich, ophthalmologische Verlaufskontrollen erfolgen.
- Sowohl mit als auch ohne antidiabetische Begleitmedikation können schwere Hypoglykämien einschließlich Bewusstseinsverlust auftreten. Engmaschiges Monitoring ist hier sinnvoll.
- Weiterhin sind extrapyramidale Störungen und kardiovaskuläre Nebenwirkungen wie Kardiomyopathien, Herzinsuffizienz und Erregungsleitungsstörung möglich.
Anwendung
- Chloroquin und Hydroxychloroquin sollten nach dem Essen eingenommen werden, da es gelegentlich zu Übelkeit, Diarrhö und Bauchschmerzen kommen kann.
- Sollten Schluckbeschwerden auftreten, empfehlen die meisten Hersteller nicht, die Tablette zu zerkleinern (außer Quensyl®). Trotzdem kann sowohl Hydroxychloroquin als auch Chloroquin zerkleinert und mit Joghurt, Apfelmus oder ähnlichen Lebensmitteln eingenommen oder über eine Magensonde verabreicht werden. Zur Verabreichung experimenteller Therapien gegen COVID-19 bei Patienten mit Schluckbeschwerden hat die Universität Liverpool ebenfalls eine Liste veröffentlicht [13].
Vorsichtsmaßnahmen
- In manchen Krankenhäusern wird die Abgabe von Hydroxychloroquin (Quensyl®) sehr restriktiv gehandhabt: Normale Bestellungen der Tabletten sind nicht möglich, das Arzneimittel darf erst nach Rücksprache mit dem Apotheker abgegeben werden, um die genaue Indikation, Dosierung und das Interaktionspotenzial vorher abzuklären.
Literatur
[1] Wang M et al. Remdesivir and chloroquine effectively inhibit the recently emerged novel coronavirus (2019-nCoV) in vitro. Cell Res 2020; doi:10.1038/s41422-020-0282-0
[2] Biot C et al. Design and synthesis of hydroxyferroquine derivatives with antimalarial and antiviral activities. J Med Chem 2006;49(9):2845-2849
[3] Mauthe M. et al. Chloroquine inhibits autophagic flux by decreasing autophagosome-lysosome fusion. Autophagy 2018;14:1435–1455
[4] Savarino A. et al. New insights into the antiviral effects of chloroquine. Lancet Infect Dis 2006;6:67–69
[5] Liu J et al. Hydroxychloroquine, a less toxic derivative of chloroquine, is effective in inhibiting SARS-CoV-2 infection in vitro. Cell Discov 2020;6:16
[6] Huang C. et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet 2020;395:497–506
[7] Yao X et al. In Vitro Antiviral Activity and Projection of Optimized Dosing Design of Hydroxychloroquine for the Treatment of Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-CoV-2). Clin Infect Dis 2020; doi:10.1093/cid/ciaa237
[8] Kluge S et al. MedKlin Intensivmed Notfmed 2020; doi/10.1007/s00063-020-00674-3
[9] Gao JJ et al. Breakthrough: Chloroquine phosphate has shown apparent efficacy in treatment of COVID-19 associated pneumonia in clinical studies. BioScience Trends 2020;14(1):72-73
[10] Gautret et al. Hydroxychloroquine and azithromycin as a treatment of COVID-19: results of an open-label non-randomized clinical trial. Int J Antimicrob Agents 2020; doi:10.1016/j.ijantimicag.2020.105949
[11] European Medicines Agency (EMA). Call to pool research resources into large multi-centre, multi-arm clinical trials to generate sound evidence on COVID-19 treatments. Pressemitteilung vom 19. März 2020. www.ema.europa.eu; Abruf am 22. März 2020
[12] Zhonghua Jie He He Hu Xi Za Zhi. [Expert consensus on chloroquine phosphate for the treatment of novel coronavirus pneumonia]. 2020;43(0):E019; doi:10.3760/cma.j.issn.1001-0939.2020.0019
[13] Liverpool Drug Interactions Group. www.covid19-druginteractions.org; Abruf am 22. März 2020
[14] Centers for Disease Control and Prevention (CDC). Information for Clinicians on Therapeutic Options for COVID-19 Patients. www.cdc.gov (Stand 21. März 2020); Abruf am 23. März 2020 [15] World Health Organization (WHO). WHO Director-General‘s opening remarks at the media briefing on COVID-19 - 18 March 2020. https://www.who.int/dg/speeches/detail/who-director-general-s-opening-remarks-at-the-media-briefing-on-covid-19---18-march-2020; Abruf am 24. März 2020
[16] Kupferschmidt K, Cohen J. WHO launches global megatrial of the four most promising coronavirus treatments. Science 2020;doi:10.1126/science.abb8497. www.sciencemag.org; Abruf am 24. März 2020
[17] Stichting Werkgroep Antibiotica Beleid (SWAB). Medicamenteuze behandelopties bij patiënten met COVID-19 (infecties met SARS-CoV-2). Stand 20. März 2020; https://swab.nl/nl/covid-19; Abruf am 24. März 2020
[18] Alhazzani et al. Surviving Sepsis Campaign: Guidelines on the Management of Critically Ill Adults with Coronavirus Disease 2019 (COVID-19). European Society of Intensive Care Medicine and the Society of Critical Care Medicine 2020. www.esicm.org; Abruf am 24. März 2020
[19] Bayer Partners with U.S. Government on Major Product Donation to Fight Coronavirus. Pressemitteilung vom 19. März 2020. https://bayer2019tf.q4web.com/news/news-details/2020/Bayer-Partners-with-US-Government-on-Major-Product-Donation-to-Fight-Coronavirus/default.aspx; Abruf am 24. März 2020























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.