
- DAZ.online
- DAZ / AZ
- DAZ 28/2019
- Schnell oder langsam
Technologie
Schnell oder langsam
Wie sich die Freisetzung von Arzneistoffen modifizieren lässt
Eine Modifizierung der Freisetzung ist einerseits möglich durch die Steuerung der zeitlichen Parameter (Retardierung, Beschleunigung). Andererseits kann dies auch durch die Steuerung der örtlichen Parameter (Zerfall aufgrund bestimmter Bedingungen am Zielort, z. B. pH-Wert) erfolgen. Die wichtigsten Gründe, die Freisetzung zu modifizieren, sind:
- Patientenakzeptanz (z. B. besserer Geschmack, einfacheres Schlucken)
- Applikation säureempfindlicher Wirkstoffe (Magensaftresistenz)
- verlängerte Wirkdauer (zeitkontrollierte Freisetzung)
- erhöhte Bioverfügbarkeit (z. B. durch eine bessere Wasserlöslichkeit)
- Targeting (z. B. Freisetzung im Colon)
- orale Applikation (z. B. Peptide, Proteine, Biologika)
Verzögerte Freisetzung von Arzneistoffen
Sollen Arzneistoffe verzögert bzw. retardiert freigesetzt werden, sind je nach Eigenschaft der Wirkstoffe chemische Veränderungen am Molekül möglich, wodurch der Wirkstoff schwerer löslich und dadurch schlechter resorbiert oder erst nach und nach im Organismus freigesetzt wird. Von physiologischer Seite kann bereits durch die Wahl des Applikationsortes versucht werden, zum Beispiel eine Depotwirkung zu erzielen. Auch die pharmazeutische Technologie bietet viele Möglichkeiten, die Arzneimittelwirkung zu verlängern (s. Kasten „Möglichkeiten zur Wirkungsverlängerung“).
Möglichkeiten zur Wirkungsverlängerung
am Wirkstoff chemisch durch
- Salzbildung
- Esterbildung
- Additionsverbindungen
- Komplexverbindungen
- Molekülvergrößerung
- Einführung chemischer Gruppen
an der Arzneiform pharmazeutisch-technologisch durch
- Wahl schwerlöslicher Wirkstoffmodifikationen
- Teilchengröße und -form
- Art und Menge der Hilfsstoffe
- hohen Anteil an Bindemittel
- hydrophobe Gleit- und Formentrennmittel bei Tabletten
- Wechselwirkungen mit Hilfsstoffen
- Herstellungstechnologie (große Festigkeit bei Tabletten)
- Wahl der Umhüllung oder Einbettung
- Gerüstbildung
- Bindung an Ionenaustauscher
am Individuum physiologisch bzw. pharmakologisch durch
- Applikationsort
- Applikationsart
- Reaktionshemmer
- Gefäßkonstriktoren
- Ausscheidungsblocker
Quelle: Fahr A. Voigt – Pharmazeutische Technologie für Studium und Beruf. 12. Auflage, Deutscher Apotheker Verlag Stuttgart 2015 [10]
Zu den Darreichungsformen mit veränderter Wirkstofffreisetzung zählen solche mit verlängerter Wirkstofffreisetzung (prolonged/extended release dosage forms, sustained release), wie wirkstoffhaltige Implantate oder ölige Suspensionen, die intramuskulär appliziert werden können. Oral applizierbare Formen enthalten oft eine Initial- und eine Depotdosis, die schnell dem Körper eine Dosis zugänglich macht und dann den Wirkstoff kontinuierlich freigibt und so zu einer messbaren Wirkungsverlängerung gegenüber einer normalen Einzeldosis führt (z. B. Equasym® retard). Möglich sind auch Darreichungsformen mit pulsierender Wirkstofffreisetzung.
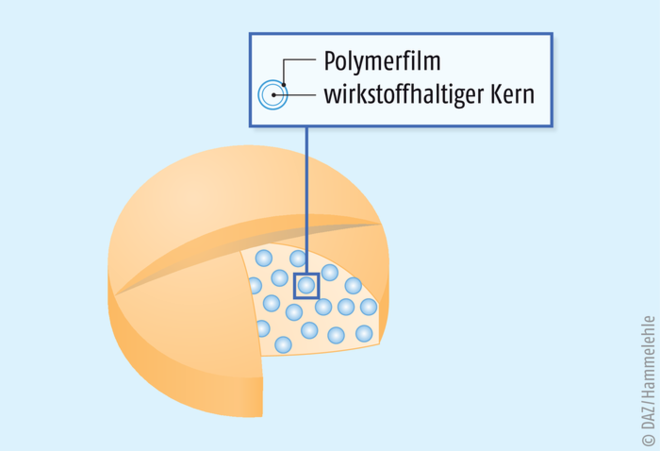
Retardarzneimittel werden häufig eingesetzt, um eine optimierte, zeitkontrollierte Freisetzung des Arzneistoffes zu erreichen. So kann die Gefahr kurzzeitig zu hoher Arzneistoffkonzentrationen im Blut minimiert werden. Ein Beispiel sind Antihypertensiva wie Metoprolol in der Beloc-Zok®-Formulierung. Dabei steht „Zok“ für Zero Order Kinetic, einer Freisetzungskinetik 0. Ordnung. Diese Zok®-Formulierung bietet im Vergleich zu Formulierungen mit einer Freisetzungskinetik 1. Ordnung den Vorteil, dass eine nahezu konstante Plasmakonzentration im Steady-State über einen möglichst langen Zeitraum des Einnahmeintervalls erreicht wird. Um die Freisetzungskinetik 0. Ordnung in Metoprolol-Präparaten zu erreichen, enthalten die Zok®-Präparate eine große Anzahl an einzelnen, kleinen Wirkstoff-haltigen Pellets. In den sogenannten Multiple-unit-Formulierungen sind diese einzelnen Pellets mit einem speziellen Retard-Polymer überzogen, das die Freisetzung des Wirkstoffes kontrolliert [2] (s. Abb. 1). Beispiele für solche Polymere sind Polymethacrylate, Ethylcellulose und Polyvinylacetat. Dabei ist insbesondere eine ausreichende Flexibilität der Polymerüberzüge eine wichtige Voraussetzung. Durch eine große Flexibilität kann verhindert werden, dass die Polymerüberzüge beim Tablettiervorgang reißen. Diese Flexibilisierung kann noch zusätzlich durch die Beimischung von Weichmachern erhöht werden. Weiterhin werden sogenannte Einbettungsmaterialien eingesetzt, die beim Pressen der multipartikulären Tabletten die Polymerüberzüge der Pellets schützen. Die Tablette selbst ist hierbei nicht mit dem Polymer überzogen, sodass sie nach der Einnahme im Gastrointestinaltrakt schnell in die einzelnen, Polymer-beschichteten Retard-Pellets zerfällt. So wird eine kontinuierliche Freisetzung des Wirkstoffes aus den einzelnen Pellets über einen längeren Zeitraum gewährleistet. Eine multipartikuläre Formulierung hat folgende Vorteile:
- Da der Magenausgang für die kleinen Pellets keine Barriere darstellt, sind Verweilzeiten im Magen geringer als bei im Magen nicht zerfallenden Arzneiformen.
- Der Einfluss von Art, Menge und Zeitpunkt der Nahrungsaufnahme auf die Wirkstofffreisetzung ist reduziert.
- Es werden besser reproduzierbare Blutspiegel erzielt und Schwankungen in der Bioverfügbarkeit reduziert.
- Selbst bei einer geringfügigen Beschädigung der Überzüge der Pellets während des Tablettierens ist nicht mit einer unerwünschten, spontanen vollständigen Wirkstofffreigabe zu rechnen.
Daher sind auch Arzneistoffe mit einer geringen therapeutischen Breite mit hoher Sicherheit auf diese Weise retardierbar. Zu beachten ist, dass multipartikuläre Retardformulierungen teilbar sind, sie dürfen aber nicht gemörsert werden.
Der größte Nachteil besteht darin, dass bei Präparaten mit einer Freisetzungskinetik 0. Ordnung idealerweise die nächste Applikation genau dann erfolgen sollte, wenn sich die Wirkung der vorherigen Applikation erschöpft. Dieser Zeitpunkt ist schwer vorhersehbar, sodass auch hier die Gefahr eines zu niedrigen bzw. zu hohen Wirkstoffspiegels besteht. Im Apothekenalltag sollte vor allem beim Austausch von Präparaten mit Freisetzungskinetik 0. Ordnung mit Präparaten mit einer anderen Freisetzungskinetik (unterschiedliche Hersteller von Metoprolol-Generika) ein sorgfältiges Monitoring durchgeführt werden, da diese Präparate nicht immer bioäquivalent sind [3].
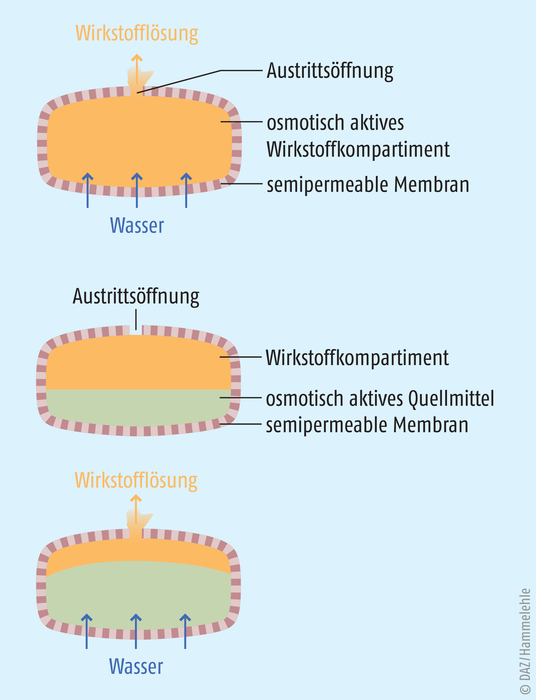
Eine Möglichkeit, die Freisetzung der Wirkstoffe zu steuern, ist das sogenannte Oros®-System (Abb. 2). Bei diesen oralen osmotischen Systemen wird der Arzneistoff mit einem semipermeablen und wasserunlöslichen Lack umhüllt, in den mittels Lasertechnik eine kleine, genau definierte Öffnung (ø 0,3 mm) gebrannt wird. Durch osmotische Prozesse kann Flüssigkeit aus dem Magen- bzw. Darmsaft eindringen und der Wirkstoff löst sich auf, bis eine gesättigte Lösung erreicht ist. Da die gesättigte Arzneimittellösung nicht den Lack passieren kann, baut sich eine osmotische Druckdifferenz auf beiden Seiten der Membran auf. Der Wirkstoff wird durch den erhöhten osmotischen Druck aus dem Innern des Systems mit konstanter Geschwindigkeit durch die Öffnung hinausgedrückt (Einkammersystem). Zusätzlich können sich in dem System ein osmotisch aktiver Hilfsstoff und ein Quellmittel befinden, das sich durch Quellung ausdehnt und so den Wirkstoff herausdrückt (Zweikammersystem). Ein Anwendungsbeispiel sind Tabletten, die Methylphenidat in einem zweistufigen Prozess freisetzen (z. B. Concerta®). Nach der oralen Einnahme am Morgen wird ein Mantel aus Methylphenidat sofort abgebaut, sodass bereits kurz nach der Applikation ein wirksamer Plasmaspiegel erreicht wird. Hat sich die Methylphenidat-Ummantelung aufgelöst, dringt Wasser durch die freiliegende, semipermeable Tablettenhülle ein. Im Inneren der Tablette baut sich ein osmotischer Druck auf, und das Quellkompartiment beginnt sich auszudehnen, so dass während des weiteren Tages der verbleibende Wirkstoff kontinuierlich aus der Tablette freigesetzt wird. Ein maximaler Plasmaspiegel wird nach sechs bis acht Stunden erreicht und eine stabile Wirkung über den gesamten aktiven Tag erzielt. Retardtabletten auf der Basis von osmotischen Systemen sowie Tabletten mit einem Funktionsüberzug dürfen nicht geteilt werden.
Modifikation am Arzneistoffmolekül
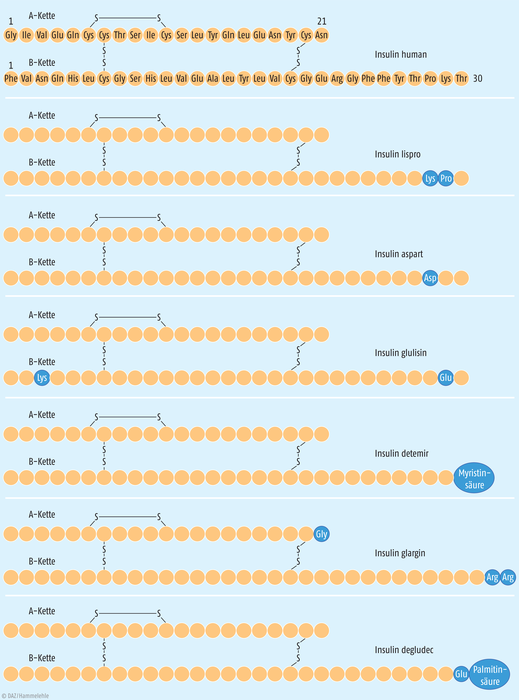
Neben Retard-Formulierungen besteht auch die Möglichkeit, durch eine direkte, chemische Modifikation des Arzneistoffes lang wirkende Präparate zu erhalten. Bedeutendstes Beispiel sind verzögert anflutende Insulin-Präparate. Kurzwirksame Insuline fluten schnell an bzw. ab, so dass sie hauptsächlich zu den Mahlzeiten oder zur Korrektur von Blutzuckerspitzen eingesetzt werden. Die sogenannten Verzögerungsinsuline decken dagegen den von den Mahlzeiten unabhängigen Grundbedarf des Körpers an Insulin. Die Wirkdauer kann durch den Zusatz von neutralem Protamin Hagedorn (NPH) verlängert werden oder auch durch den Austausch bzw. das Einfügen einzelner Aminosäuren im Insulin-Molekül. Früher wurden dazu auch kristalline Insuline durch die Verbindung von Insulin-Molekülen mit Zink-Ionen hergestellt. Sie werden heute aber nicht mehr eingesetzt. Die Verzögerung durch Protamin Hagedorn ist je nach Dosierung unterschiedlich. Normalerweise beträgt die Wirkdauer 12 (8 bis 16) Stunden. Die maximale Wirkung entfaltet sich nach vier bis sechs Stunden. Durch Veränderung der Aminiosäuresequenz lassen sich langwirksame Insulinanaloga gewinnen (z. B. Insulin glargin, Lantus®), die länger wirken als NPH-Verzögerungsinsulin, (durchschnittlich 24 Stunden). Sie haben eine gleichmäßigere Wirkung und verringern somit auch das Risiko von Unterzuckerungen. Insulin glargin hat dieselbe Primärstruktur wie humanes Insulin, es wurde lediglich in der A-Kette die Aminosäure Asparagin durch Glycin an Position 21 ausgetauscht und in der B-Kette zwei zusätzliche Arginine an Position 31 und 32 eingefügt (s. Abb. 3). Dadurch ist Insulin glargin im neutralen pH-Wert-Bereich nur gering löslich. Im sauren pH-Bereich (Lantus-Injektionslösung pH-Wert = 4) ist es vollständig löslich. Nach der subkutanen Injektion erfolgt eine Neutralisierung, die zur Bildung von Mikropräzipitaten führt. Aus diesen werden kontinuierlich geringe Mengen Insulin freigesetzt. So kann ein gleichmäßiges, vorhersehbares Konzentrations-Zeit-Profil ohne große Spitzen mit langanhaltender Wirkdauer erzielt werden [4]. Eine weitere Möglichkeit, die Wirkdauer zu verlängern, besteht im Anhängen einer Fettsäure (z. B. Insulin detemir, Levemir® Novo Nordisk). Insulin detemir hat eine identische Primärsequenz wie humanes Insulin mit Ausnahme des entfernten Threonins in Position B30 der B-Kette und einer zusätzlichen Myristinsäure am Lysin in Position B29. Durch diese Änderung wird das modifizierte Insulin im Blut verstärkt an Albumin gebunden (nur etwa 1% zirkuliert frei im Blut) und langsam wieder freigesetzt [5].
Eine weitere interessante galenische Zubereitung sind wässrige Kristallsuspensionen. Dabei enthalten wässrige, injizierbare Suspensionen zum Beispiel Hormonkristalle verschiedener Größen. Es werden vorwiegend Ester (Essig-, Propion-, Butter- oder Benzoeester) verwendet, um ein Depot zur verlängerten Wirkstofffreisetzung zu bilden (Triam®inject [Triamcinolon acetonid], Celestan® solubile [Betamethasondihydrogenphosphat Dinatrium], Volon® A [Triamcinolonacetonid]). Die Kristallsuspensionen werden meist intramuskulär appliziert, auch eine lokale Therapie (intrafokal oder subläsional) ist möglich. Die unlöslichen Kristalle in der Ampulle müssen vor Gebrauch gut aufgeschüttelt und wieder in der Lösung verteilt werden. Kristallsuspensionen werden bei einer systemischen Therapie intramuskulär verabreicht, bei einer lokalen Therapie meist intrafokal oder subläsional. Sie dürfen nie intravenös injiziert werden.
Beschleunigte Freisetzung von Arzneistoffen
Neben der Möglichkeit, die Freisetzung von Wirkstoffen zu verzögern, soll in vielen Fällen genau das Gegenteil, nämlich eine beschleunigte Freisetzung von Wirkstoffen, erreicht werden. Dazu können Wirkstoffe als Schmelz- bzw. Brausetablette formuliert werden. Schmelztabletten können aufgrund ihres Freisetzungsverhaltens der Gruppe der orodispersiblen Arzneiformen zugeordnet werden. In Brausetabletten wird der rasche Zerfall durch den Zusatz einer Brausemischung (Natriumhydrogencarbonat/Zitronensäure) erreicht. Orodispersible Arzneiformen zerfallen bereits in der Mundhöhle des Patienten schnell in eine Vielzahl kleiner Partikel. Die in orodispersiblen Tabletten am häufigsten eingesetzten Hilfsstoffe sind Zuckeralkohole wie Mannitol oder Xylitol.
Orale Lyophilisate sind feste Zubereitungen zur Anwendung in der Mundhöhle oder zur Dispergierung in Wasser vor der Einnahme, die durch Gefriertrocknung hergestellt werden. Sie werden oft als Schmelztabletten deklariert und werden auch als lyophilisierte Plättchen bezeichnet (Ascotop® Schmelztabletten [Zolmitriptan], Maxalt® lingua [Rizatriptan], Zyprexa® Velotab® [Olanzapin]). Nach Kontakt mit nur geringen Mengen an Speichel lösen sie sich innerhalb von Sekunden, und sie müssen innerhalb von drei Minuten zerfallen.
Schmelztabletten sind nicht überzogene Tabletten, die im Mund nach der Einnahme direkt auf der Zunge rasch zerfallen, bevor sie geschluckt werden. Sie werden durch Kompression oder Schmelzextrusion hergestellt und sollen innerhalb von drei Minuten zerfallen. Dabei ist der Begriff Schmelztablette eigentlich irreführend, denn die Bestandteile schmelzen nicht, die Tabletten lösen sich nach Kontakt mit Wasser rasch auf bzw. zerfallen. Oft werden Generika von Lyophilisaten wie die Originalpräparate als „Schmelztabletten“ deklariert, obwohl das Original ein Lyophilisat ist (z. B. Zofran®, Maxalt®, Ascotop®).
Tabletten zur Anwendung in der Mundhöhle sind normalerweise nicht überzogene Tabletten. Dazu gehören mit Lutschtabletten und Pastillen feste, einzeldosierte Zubereitungen zum Lutschen. Sie sollen einen lokalen oder systemischen Effekt erzielen. Sublingual- und Buccaltabletten sind ebenfalls feste, einzeldosierte Zubereitungen zur Anwendung in der Mundhöhle, die unter der Zunge (Sublingualtabletten) oder in der Backentasche (Buccaltabletten) appliziert werden und systemisch wirken [10].
Es gibt auch mukoadhäsive Sublingual- und Buccaltabletten, die auf eine Schleimhautstelle gelegt und angedrückt werden und die mit dem Speichel in 10 bis 30 Minuten ein hochvisköses, mukoadhäsives Hydrogel ausbilden. Beispiele sind Abstral® Sublingualtabletten und Breakyl® Fentanyl Buccalfilm (Fentanylcitrat) sowie Aftab® Hafttabletten (Triamcinolonacetonid).
Diese Arzneiformen können ohne Flüssigkeit eingenommen werden. Dies ist bei Patienten mit Schluckschwierigkeiten praktisch, kann aber auch bei bestimmten Erkrankungen wie bei einem akuten Migräneanfall oder chronischem Erbrechen vorteilhaft sein (Immodium® akut lingual Schmelztabletten zur Behandlung von akutem Durchfall oder Maxalt® lingua Schmelztabletten zur Behandlung von Migräneanfällen). Im Bereich der pädiatrischen Arzneiformen spielen diese orodispersiblen Arzneiformen ebenfalls eine bedeutende Rolle (z. B. Nurofen® Schmelztabletten).
Das schnelle Auflösen ohne größere Flüssigkeitsmengen ermöglicht der Herstellungsprozess: Durch Gefriertrocknung (Lyophilisation) einer Arzneistoff/Hilfsstoff-Dispersion entstehen die Plättchen. Als Matrixbildner werden bevorzugt Gelatine oder Mannitol eingesetzt. Lyophilisate haben eine hohe Affinität zu Wasser, bedingt durch die hohe Porosität und die große Oberfläche. Wegen der Hydrophilie und Zerbrechlichkeit erfordern sie eine spezielle luft- und wasserdichte Verpackung. Meist werden sie in Aluminiumblister mit abziehbarer Deckfolie (Peel-of-Blister) verpackt. Beim Entnehmen dürfen Lyophilisate aufgrund ihrer geringen Bruchfestigkeit nicht wie herkömmliche Tabletten aus dem Blister gedrückt werden, nach dem Abziehen der Folie müssen die Finger vollkommen trocken sein. Die Plättchen von Tavor® Expidet® (Lorazepam) erhalten durch den Lyophilisations-Herstellungsprozess eine Kerbe [6], die aber nicht zum Teilen des Plättchens dient. Vermehrt werden orodispersible Tabletten eingesetzt, die eine hohe mechanische Stabilität aufweisen, wodurch Weiterverarbeitung, Verpackung und Transport kaum Probleme bereiten [7].
Wünschenswerte Eigenschaften orodispersibler Arzneiformen
- schneller Zerfall in einer geringen Flüssigkeitsmenge
- akzeptabler Geschmack
- tolerierbares Mundgefühl
- Schutz des Wirkstoffes (z. B. vor Feuchtigkeit)
- Möglichkeit der Beladung mit hohem Arzneistoffgehalt
- geringe Empfindlichkeit gegenüber Feuchtigkeit bei Lagerung
- ausreichende Bruchfestigkeit
(nach [12])
Brausetabletten gelten als eine anwenderfreundliche Darreichungsform, die sehr schnell zerfällt und den Wirkstoff schnell freisetzt. Bei der Einnahme liegt der Wirkstoff dann bereits in gelöster Form vor. Brausetabletten müssen innerhalb von fünf Minuten zerfallen sein. Sie sind vorteilhaft für Patienten mit Problemen beim Schlucken von Tabletten mit größerem Durchmesser, auch die Einnahme des Wirkstoffes mit einer größeren Menge Wasser kann durch Brausetabletten sichergestellt werden. Sie gelten als besser verträglich, da punktuell keine hohen Wirkstoffkonzentrationen auftreten. Auch kann der Geschmack durch den Zusatz von Aromen verbessert werden. Brausetabletten enthalten neben dem Wirkstoff eine wasserlösliche organischen Säure (häufig Zitronensäure, Ascorbinsäure oder Weinsäure) und ein Alkalicarbonat (häufig Natriumcarbonate oder Kaliumhydrogencarbonat) als Kohlenstoffdioxid-liefernde Komponente. Damit die Tabletten im Wasser oder bei Personen mit subazidem Magensaft schnell zerfallen, werden meist Zitronensäure und Weinsäure gemeinsam verwendet. Wenn dieses Gemisch mit Wasser in Berührung kommt, wird Kohlendioxid entwickelt, der Brauseeffekt beschleunigt den Lösungsvorgang der Tablette sehr stark. Die Anwendung ist vielfältig z. B. bei Analgetika (z. B. Aspirin® plus C Brausetabletten) sowie bei Hustenlösern (z. B. ACC® akut). Noch häufiger werden sie als Nahrungsergänzungsmittel (Vitamin-Präparate) eingesetzt. Von Nachteil ist die Empfindlichkeit gegen Feuchtigkeit und ihre Zerbrechlichkeit. Anwender sollten darauf hingewiesen werden, dass die enthaltenen Hilfsstoffe zu einem hohen Natrium- und Citrat-Gehalt der Lösung führen. Diese hohen Natrium-Konzentrationen addieren sich zu anderweitig zugeführten Natrium-Ionen (Kochsalz) [11]. Es kann zu unerwünschten Natrium- bzw. Natriumchlorid-Effekten kommen, dazu gehören ein erhöhtes Risiko für arterielle Hypertonie oder andere kardiovaskuläre Effekte sowie eine verstärkte Ausscheidung von Calcium-Ionen mit Abnahme der Knochendichte [11].
Eine beschleunigte Wirkstofffreisetzung kann auch mit einer chemischen Struktur-Modifikation erreicht werden (Abb. 3). Ein Beispiel sind die schnell wirksamen Insuline (Insulin aspart [NovoRapid®], Insulin lispro [Humalog®]). Die Primärstruktur von Insulin aspart ist mit Ausnahme der neu eingeführten Asparaginsäure anstelle von Prolin in Position 28 der B-Kette identisch mit der Primärstruktur von Humaninsulin (Abb. 3). Durch den Austausch der Aminosäure wird nach der subkutanen Verabreichung eine bessere Absorption und eine schnellere Elimination erreicht [8]. Ebenfalls durch den Austausch von Aminosäuren (Position 28 und 29 der B-Kette) entsteht aus Humaninsulin Insulin lispro. Der Austausch führt zu einem raschen Wirkungseintritt, weshalb es kurz vor den Mahlzeiten verabreicht werden kann. Bei den kurz wirkenden Insulinen tritt die Wirkung sehr rasch ein (zehn Minuten nach der Injektion). Die größte Wirksamkeit entwickelt sich nach 60 (30 bis 90) Minuten. Die gesamte Wirkung hält nur zwei bis drei Stunden an [9]. |
Literatur
[1] Mäder K. Innovative Arzneiformen: Ein Lehrbuch für Studium und Praxis. 1. Auflage, Wissenschaftliche Verlagsgesellschaft Stuttgart 2009
[2] Opitz UH. Multipartikuläre Tabletten. Apothekenmagazin 2005;23:136-141
[3] Griese N et al. Austauschbarkeit von Retardpräparaten. Pharm Ztg 2010;25
[4] Lantus, INN-insulin glargine. Zusammenfassung des EPAR für die Öffentlichkeit. EMA/313727/2012, Stand: 2012
[5] Levemir Insulin detemir. Zusammenfassung des EPAR für die Öffentlichkeit. EMA/516544/2015, Stand: 2015
[6] Tavor® Fachinformation. Stand: Mai 2019
[7] Stoltenberg I. Orodispersible Minitabletten – Entwicklung und Charakterisierung einer neuen festen Darreichungsform für die Pädiatrie. Dissertation, Universität Düsseldorf, Januar 2012
[8] NovoRapid Insulinaspart. Zusammenfassung des EPAR für die Öffentlichkeit. EMA/632418/2016, Stand: 2016
[9] Humalog Insulin lispro. Zusammenfassung des EPAR für die Öffentlichkeit. EMA/640678/2014, Stand: 2014, www.ema.europa.eu/en/documents/overview/humalog-epar-summary-public_de.pdf
[10] Fahr A. Voigt - Pharmazeutische Technologie für Studium und Beruf. 12. Auflage, Deutscher Apotheker Verlag Stuttgart 2015
[11] Kircher W. Arzneiformen richtig anwenden. 4. Auflage, Deutscher Apotheker Verlag Stuttgart 2016
[12] Fu, Yourong, et al. Preparation of fast-dissolving tablets based on mannose. ACS symposium series. Vol. 924. Oxford University Press, 2006























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.