
- DAZ.online
- DAZ / AZ
- DAZ 19/2019
- Gerinnungshemmer gegen ...
Arzneimittel und Therapie
Gerinnungshemmer gegen Fettleber
Thrombozyten erweisen sich als vielversprechendes Target
Die nichtalkoholische Fettlebererkrankung ist eine der häufigsten chronischen Lebererkrankungen in den westlichen Industrienationen. Die vermehrten Fetteinlagerungen in den Leberzellen bleiben zunächst unbemerkt. Unspezifische Beschwerden wie Druckempfindlichkeit der vergrößerten Leber und Erschöpfung treten erst auf, wenn sich die Fettleber zu einer Fettleberhepatitis entwickelt. Ein weiteres Voranschreiten der Erkrankung kann zu Leberkrebs und dadurch zum Tod führen. Trotz der hohen Relevanz der Erkrankung fehlt es bislang an einer effektiven Pharmakotherapie. Als Hauptrisikofaktoren gelten Diabetes mellitus Typ 2, Übergewicht – vor allem übermäßige Fettablagerungen im Bauchbereich – und Fettstoffwechselstörungen. Dass diese Prädispositionen nur ein Aspekt des Geschehens sind, zeigen die Ergebnisse einer aktuellen Studie.
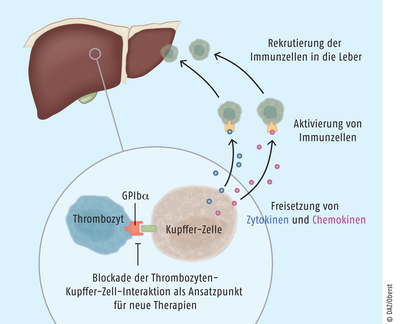
Wissenschaftler des Deutschen Krebsforschungszentrums Heidelberg sowie der Universität und des Universitätsspitals Zürich haben gezeigt, dass eine fettreiche Diät bei Mäusen zu erhöhten Thrombozytenzahlen und zu einer Ansammlung von Immunzellen in der Leber führt. Ähnliches wurde auch bei Patienten mit nichtalkoholischer Fettlebererkrankung beobachtet. Wurden die Mäuse über zwölf Monate mit Acetylsalicylsäure, Clopidogrel oder Ticagrelor behandelt, reduzierte sich die Zahl der Thrombozyten in der Leber signifikant. Die Mäuse wurden zwar weiterhin übergewichtig, entwickelten jedoch weder eine Hepatitis noch ein hepatozelluläres Karzinom. Gestützt werden diese Beobachtungen durch die Ergebnisse einer kleinen Pilotstudie an Menschen mit nichtalkoholischer Fettlebererkrankung: Durch eine Therapie mit Thrombozytenaggregationshemmern konnten sowohl der Fettanteil in der Leber als auch die Größe des Organs reduziert werden. Im Mausmodell führte die Behandlung mit Thrombozytenaggregationshemmern außerdem zu einer starken Reduktion der Kupffer-Zellen – den Makrophagen der Leber – und deren Aktivierung. Weitere Untersuchungen bestätigten die tragende Rolle der Kupffer-Zellen. Die Autoren schlagen folgenden Thrombozyten-vermittelten Mechanismus vor: Die Blutplättchen binden in der Leber über das Glykoprotein GPIbα an die Kupffer-Zellen, woraufhin diese Zytokine und Chemokine freisetzen. Immunzellen werden in die Leber gelockt und setzen dort Entzündungsprozesse in Gang (s. Abbildung). Die Blockade von GPIbα mit einem Antikörper verringerte die Menge der produzierten Botenstoffe und damit die entzündlichen Veränderungen in der Leber. Die Identifikation dieses Mechanismus eröffnet Möglichkeiten für rationale Therapieansätze zur Prävention und Behandlung der Fettlebererkrankung. Um die vielversprechenden Ergebnisse zu bestätigen und die Zusammenhänge besser zu verstehen, sind weitere Studien erforderlich. Die Ergebnisse lassen allerdings auf eine Pharmakotherapie hoffen, die in Zukunft das Risiko für fettleberinduzierten Leberkrebs senkt. |
Quelle
Malehmir M et al. Platelet GPIbα is a mediator and potential interventional target for NASH and subsequent liver cancer. Nat Med 2019;25(4):641-655





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.