
- DAZ.online
- DAZ / AZ
- DAZ 37/2017
- Ein Paradies für Pilze
Beratung
Ein Paradies für Pilze
Wie Dermatophyten und Co. von Haut und Schleimhäuten vertrieben werden können
Auf unserer Haut siedeln etwa eine Billion Mikroorganismen, darunter auch einige Pilze. Die meisten dieser Mikroorganismen sind nicht pathogen, im Gegenteil, unsere Mikrobiota schützt uns vor eindringenden Fremdkeimen. Erst wenn das Gleichgewicht innerhalb dieser Hautflora gestört oder unser Immunsystem geschwächt ist, kann es einem einzelnen Stamm gelingen, die Hautflora zu überwuchern und eine „Pilzinfektion“ auszulösen.
Nach dem „DHS-Schema“ werden die humanpathogenen Pilze in drei Gruppen unterteilt:
- Dermatophyten,
- Hefen und
- Schimmelpilze.
Letztere verursachen vor allem systemische Pilzinfektionen oder schädigen die Atemwege, sie spielen auf der Haut kaum eine Rolle. Grundsätzlich sollte die Diagnose Hautmykose vom Arzt gestellt werden, da er durch einen Erregernachweis das am besten geeignete Antimykotikum auswählen und andere Hauterkrankungen ausschließen kann. Ausnahmen sind Fußpilz und Vaginalmykosen, doch auch hier sollte bei Nichtanschlagen der Therapie ein Arzt aufgesucht werden.
Als nicht-verschreibungspflichtige topische Antimykotika stehen folgende Wirkstoffe zur Verfügung:
- Allylamine: Naftifin, Terbinafin
- Azole: Clotrimazol, Bifonazol, Econazol, Miconazol, Ketoconazol und Sertoconazol
- Hydroxypyridon: Ciclopiroxolamin
- Morpholin: Amorolfin
- Polyen: Nystatin
- Thiocarbamat: Tolnaftat
Nystatin ist ausschließlich gegen Hefepilze wirksam und wird selbst bei oraler Gabe nicht resorbiert, viele Azole und Ciclopirox sind Breitband-Antimykotika.
Hefen kommen ubiquitär vor, die meisten von ihnen sind apathogen. Pilzinfektionen werden vor allem durch Candida-Arten ausgelöst, 80% davon durch Candida albicans. Sie sind bei vielen Menschen Bestandteil der natürlichen Hautflora, bei Vorliegen disponierender Faktoren können sie diese überwuchern. Candida-Arten wachsen am besten in feucht-warmer Umgebung, vor allem auf den Schleimhäuten. Aber auch auf trockener Haut können Candidosen auftreten, wenn durch Hautfalten oder Einmalwindeln Staunässe entsteht.
Candida bevorzugt die Schleimhaut
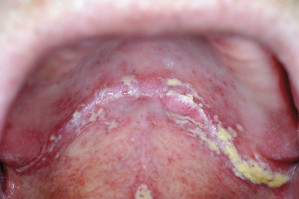
Die orale Candidose (Mundsoor, Abb. 1) tritt vor allem bei Säuglingen, bei Immunsupprimierten oder als Nebenwirkung einer Therapie mit inhalativen Glucocorticoiden auf. Erreger ist in der Regel Candida albicans. Typisch sind weiße, abstreifbare Beläge auf Mundschleimhaut und Zunge, eine Rötung unter diesen Belägen sowie starker Juckreiz. Zusätzlich kann es zur Schwellung der Mundschleimhaut, zu Schluckbeschwerden oder zu Schmerzen im Mundraum kommen. Chronische Candidosen, wie sie typischerweise bei Prothesenträgern auftreten, sind durch weiße Läsionen gekennzeichnet, die nicht abwischbar sind, zusätzlich treten oft Mundwinkelrhagaden auf.
Die topische Behandlung erfolgt meist als Mundgel oder Suspension mit Nystatin (z. B. Candio-Hermal® Mundgel, Moronal® Suspension, Mykundex® Suspension) oder Miconazol (z. B. Daktar® Mundgel, Infectosoor® Mundgel). Das Gel kann mithilfe eines Wattestäbchens auf die betroffenen Stellen aufgetragen werden. Die Zubereitung sollte mehrmals täglich nach dem Essen angewendet und einige Minuten im Mund behalten werden, bevor sie geschluckt wird.
Orale Candidose: vorbeugende und begleitende Maßnahmen
- Prothesen und herausnehmbare Zahnspangen mitbehandeln
- Sitz von Prothesen und Zahnspangen überprüfen lassen
- Zahnbürste regelmäßig wechseln, vor allem nach Beginn der Therapie
- Säuglinge: Schnuller und Sauger regelmäßig auskochen bzw. desinfizieren und wechseln; Babylöffel, Schnuller etc. nicht selbst in den Mund nehmen!
- Asthmatiker: nach Anwendung inhalativer Glucocorticoide den Mund ausspülen oder etwas trinken bzw. essen
Windeldermatitis ist eigentlich ein Oberbegriff für verschiedene Erkrankungen der Haut im Windelbereich, meist wird er jedoch für eine Candidose verwendet (Windelsoor). Betroffen sind Säuglinge, aber auch Erwachsene mit Inkontinenz. Candida albicans gelangt in der Regel über den Stuhl in die Windelregion. Die Windel wirkt dann als „feuchte Kammer“, in der sich der Hefepilz innerhalb weniger Stunden ausbreiten kann. Typisch sind gefüllte, später aufplatzende Bläschen auf geröteter, glänzender Haut, an den Rändern können sich feine Schuppen zeigen.
Für die Behandlung einer Windeldermatitis sind Dermatika mit Kombinationen aus Zinkoxid mit Nystatin (z. B. Mykoderm® Heilsalbe, Multilind® Heilsalbe) oder Miconazol (z. B. Infectosoor® Zinksalbe) sinnvoll. Gerbstoffe, Kamille oder Dexpanthenol können unterstützend eingesetzt werden.
Ebenfalls aus dem Darm erfolgt die Besiedelung der weiblichen Vagina mit C. albicans, aus der sich eine Vulvovaginal-Candidose entwickeln kann. Typische Symptome sind starker Juckreiz sowie weißliche Beläge auf den Schleimhäuten der Vagina, der Schamlippen sowie in der Perianalregion. Die Patientinnen haben weißen, teils krümeligen, geruchlosen Ausfluss. Riecht der Ausfluss unangenehm fischartig oder tritt gar kein Ausfluss auf, so sind das Hinweise darauf, dass keine Pilzinfektion vorliegt. Als weitere Beschwerden können geschwollene und gerötete Schleimhäute, Wundgefühl und Schmerzen beim Geschlechtsverkehr auftreten. Vaginal-Candidosen sind häufig, da der leicht saure pH-Wert der Scheidenflüssigkeit optimal für den acidophilen C. albicans ist, in der Regel sind sie jedoch unkompliziert zu therapieren. Problematisch ist ein zunehmender Anteil von Non-albicans-Candidastämmen, vor allem Candida crusei und C. glabrata. Letzterer führt häufig zu chronisch-rezidivierenden Vaginalmykosen und wird durch die üblichen topischen Antimykotika nicht angegriffen.
Windeldermatitis: vorbeugende und begleitende Maßnahmen
- häufiger Windelwechsel
- regelmäßig „belüften“, das heißt Kinder einige Zeit ohne Windel lassen
- Haut im Windelbereich gut pflegen, vor allem bei bettlägerigen Inkontinenzpatienten
Vaginal-Pilz: im Zweifel zum Arzt
In der Praxis ist nur ein Drittel aller Selbstdiagnosen „Vaginalpilz“ richtig, daher sollte folgenden Patientinnen zum Arztbesuch geraten werden:
- Frauen, bei denen die Symptome zum ersten Mal auftreten
- junge Frauen unter 18 Jahren
- Schwangere
- Frauen mit mehr als vier Rezidiven pro Jahr (hier sollte eine Erregerbestimmung durchgeführt sowie die Infektionsquelle gesucht werden, z. B. Biofilme auf Hormonspiralen, Intimpiercings oder ein befallener Partner)
- Nichtanschlagen der Selbstmedikation
Candidose der Vaginalschleimhaut: vorbeugende und begleitende Maßnahmen
- keine übertriebene Intimhygiene! Reinigung mit Wasser und milden Intimwaschlotionen
- richtige „Wischtechnik“ nach dem Toilettengang: von vorne nach hinten!
- Handtücher/Waschlappen täglich wechseln, bei 90 °C oder mit einem Wäschedesinfektionsmittel waschen
- Unterwäsche aus Baumwolle statt Kunstfasern tragen; täglich wechseln
- nach dem Baden die nasse Badekleidung sofort wechseln
Eine Vaginal-Candidose wird in der Selbstmedikation mit Clotrimazol (z. B. Canesten® Gyn Vaginalcreme, Kadefungin® Vaginalcreme, Canifug® Cremolum) oder Nystatin (z. B. Biofanal®) behandelt. An drei aufeinanderfolgenden Abenden (nicht während der Menstruation) werden unmittelbar vor dem Schlafengehen eine (Clotrimazol) bzw. zwei (Nystatin) Vaginal-Tabletten eingeführt. Von den Nystatin-Präparaten kann alternativ eine Vaginal-Tablette täglich über sechs Tage angewendet werden. Clotrimazol ist in einer speziellen Galenik als Vaginal-Tablette auch als Ein-Tages-Behandlung erhältlich (z. B. Canesten® Gyn once, Kombination aus Vaginal-Tablette und Vaginal-Creme). Zusätzlich sollte immer für ein bis zwei Wochen die entsprechende Vaginal-Creme äußerlich angewendet werden. Eine Schwangere sollte die Vaginal-Tabletten nicht mit Applikator sondern mit dem Finger einführen. Nystatin kann in der Schwangerschaft ohne Einschränkungen angewendet werden.
Hilfreich ist ein Hinweis an die Patientin, dass Nystatin die Wäsche gelb färben kann. Daher sollte während der Therapie ein Wäscheschutz getragen werden. Auch sollte erwähnt werden, dass die Hilfsstoffe mancher vaginal angewendeter halbfester Zubereitungen die Funktion von Latex (Kondome, Diaphragmen) beeinträchtigen können.
Der Partner, der als Infektionsquelle für Rezidive in Betracht kommt, sollte nur mitbehandelt werden, wenn er auch Symptome einer Candidose zeigt, nicht bei bloßer Besiedelung. Eine Therapie mit Laktobazillen zur Normalisierung der Vaginal-Flora ist nur nötig, wenn diese z. B. durch eine vorangegangene Antibiotika-Therapie gestört wurde. Eine antimykotische Therapie greift die Vaginal-Flora nicht an, eine zusätzliche Gabe von Laktobazillen würde den pH-Wert für das Wachstum des acidophilen C. albicans sogar optimieren.
Schließlich können Candidosen auch auf trockener Haut in schlecht belüfteten Arealen auftreten. Typisch sind Hautfalten wie unter der Brust oder in der Leiste. Diese Candidosis intertriginosa tritt vor allem bei älteren, adipösen Patienten auf, Diabetes mellitus steigert das Risiko zusätzlich. Hier ist es wichtig, den Haut-zu-Haut-Kontakt zu vermeiden, z. B. durch Einlegen von Mull- oder Leinenläppchen in die Hautfalten.
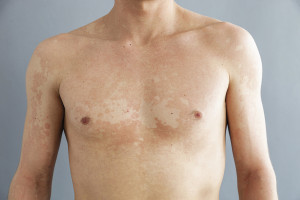
Ebenfalls zu den Hefen zählt Malassezia furfur, der Erreger der Kleienpilzflechte (Pityriasis versicolor).M. furfur ist Bestandteil der natürlichen Hautflora und besiedelt Hautareale mit hoher Talgproduktion. Vor allem am oberen Körperstamm (Brust, Rücken, Oberarme) kann es zum Ausbruch der Infektion kommen, wenn sich der Patient in einem warmen, feuchten Klima befindet, viel schwitzt und luftundurchlässige Kleidung (z. B. Badekleidung oder synthetische Sportkleidung) trägt. Typisch ist die Pityriasis versicolor als „Urlaubsmitbringsel“ nach Reisen in Länder mit heißem Klima. Charakteristisch sind runde oder ovale, 3 bis 5 mm große Flecken, die sowohl hypo- oder hyperpigmentiert sein können (Abb. 2). Bei Fortschreiten der Krankheit können sie konfluieren. Vor allem am Rand der Makulae kann eine typische „kleieförmige“ weiße Schuppung zu sehen sein, Juckreiz tritt selten auf. Therapiert wird in der Regel lokal mit Azolen, Allylaminen oder Ciclopirox-Olamin. Die Fehlpigmentierung kann auch nach Elimination des Pilzes über mehrere Monate bestehen bleiben. Eine großflächige Behandlung des Körperstamms, vor allem die Mitbehandlung der behaarten Kopfhaut wird empfohlen, da diese oft ebenfalls dicht besiedelt ist. Geeignete Formulierungen sind z. B. mit Econazol erhältlich (z. B. Epi-Pevaryl® Lösung). Die Behandlung mit der Lösung wird an drei aufeinanderfolgenden Abenden vor dem Schlafengehen durchgeführt. Ein Beutel der Lösung wird nach dem Duschen auf die komplette Haut und Kopfhaut aufgetragen und einmassiert. Der Schaum muss eintrocknen und wird am nächsten Morgen abgeduscht.
Eine wichtige Rolle wird Malassezia furfur auch bei der seborrhoischen Dermatitis der Kopfhaut zugeschrieben, die durch die Bildung von großen, fettigen Schuppen gekennzeichnet ist. Sie wird mit Azol-haltigen Shampoos therapiert (z. B. Ketoconazol in Ketozolin® oder Terzolin®), die während der Haarwäsche nur fünf Minuten einwirken müssen und zweimal wöchentlich appliziert werden. Eine Anwendung über mehr als sechs Monate wird nicht empfohlen, um die natürliche Flora der Kopfhaut nicht zu verändern.
Am häufigsten: Dermatophyten
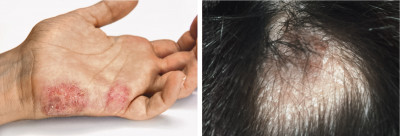
Die meisten Hautmykosen werden von Dermatophyten ausgelöst. Diese Fadenpilze vermehren sich bei einem Temperaturoptimum von 25°C und benötigen Keratin zum Wachstum. Die wichtigsten pathogenen Arten gehören zu den Gattungen Trichophyton und Microsporum. Die Infektion wird als „Tinea“ bezeichnet. Erstinfektion ist oft die Tinea pedis, der Fußpilz, der meist durch Trichophyton rubrum oder T. interdigitale verursacht wird. Die Sporen werden in Barfußbereichen von öffentlichen Sportanlagen, durch Teppiche in Hotelzimmern, in religiösen Bet- oder Begegnungsstätten, in denen barfuß gelaufen wird, oder im privaten Umfeld durch gemeinsames Benutzen von Handtüchern, Hausschuhen etc. übertragen. Zusätzliche Risikofaktoren sind z. B. enge, nicht atmungsaktive Schuhe, Durchblutungsstörungen oder Diabetes mellitus. Selbstmedikation sollte nur bei der interdigitalen Form erfolgen, die durch juckende, teils schuppende Läsionen in den Zehenzwischenräumen gekennzeichnet ist (Abb. 3). Die „Mokassin-Mykose“, bei der sich die Infektion auf die Fußsohle und die Fußkante ausbreitet, und die vesikulös-dishydrotische Form mit Blasen im Bereich von Fußgewölbe und Fußkanten gehören in die Hand des Arztes.
Die Therapie der Tinea pedis erfolgt meist durch Cremes. Für schwer erreichbare Stellen oder Patienten mit motorischen Problemen stehen auch Sprays zur Verfügung. Bei den einzelnen Wirkstoffen sind die unterschiedliche Behandlungsdauer und die Applikationshäufigkeit zu beachten.
So muss z. B. Clotrimazol zweimal täglich über etwa vier Wochen, Bifonazol einmal täglich über etwa drei Wochen oder Terbinafin einmal täglich über mindestens eine Woche appliziert werden. Von Terbinafin ist eine Zubereitung zur Einmalapplikation erhältlich (Lamisil® once). Es wird vermutet, dass Terbinafin in höheren Konzentrationen einen weiteren fungiziden Wirkmechanismus besitzt. Die gelbildende Terbinafin-Lösung muss, beginnend bei den befallenen Stellen, stets auf die gewaschene, abgetrocknete Haut beider Füße aufgetragen werden (Zehen, Fußsohle und Fußkante). Nach der Applikation dürfen die Füße 24 Stunden nicht gewaschen werden.
Begleitend zu einer Fußpilztherapie sollten Hygienemaßnahmen ergriffen werden, um eine Reinfektion zu vermeiden: Handtücher sollten täglich gewechselt und nicht von mehreren Personen verwendet werden, Handtücher und Socken sollten entweder im Kochwaschgang oder mit Hygienespüler (z. B. Canesten® Hygiene Wäschespüler) gewaschen werden, Schuhe sollten desinfiziert werden (Einwirkzeit beachten, z. B. für quartäre Ammoniumverbindungen: 30 Minuten). Die meisten Wirkstoffe greifen hauptsächlich hemmend in die Ergosterol-Biosynthese der Pilzzellmembran ein, sie wirken überwiegend auf proliferierende Pilzzellen. Um Rezidive zu vermeiden, sollte die Lokalbehandlung im Idealfall etwa drei bis vier Wochen über die klinische Heilung hinaus fortgesetzt werden.
Fußpilz: Achtung Ausbreitung!
Nach der Pflege und Behandlung befallener Füße müssen gründlich die Hände gewaschen werden, sonst kann sich in der Folge eine Tinea an anderer Stelle entwickeln, z. B. eine Tinea manuum (Abb. 4). Diese oft chronische Mykose an Händen tritt typischerweise anfangs an nur einer Hand auf. Schuppen und tiefe, schmerzhafte Rhagaden können bis zur Arbeitsunfähigkeit führen. Die Tinea inguinalis in der Leistenregion tritt bevorzugt bei Männern auf, auch sie hat ihren Ausgang häufig in einer Tinea pedis. Auch die Tinea corporis e faciei (Körper und Gesicht) wird meist durch Trichophyton rubrum ausgelöst. Typisch sind vor allem am Rand schuppende, zentrifugal wachsende, gerötete Herde. Grundsätzlich können die meisten dieser Dermatosen topisch behandelt werden.
Eine Sonderstellung nimmt Tinea capitis ein, eine Pilzinfektion der Kopfhaut (Abb. 4). Sie tritt am häufigsten im Kindesalter auf. Typisch sind runde, schuppige, stark juckende Läsionen auf der Kopfhaut, die durch Abbrechen der Haare an Stoppelfelder erinnern. Begleitend können starke Entzündungen auftreten bis hin zum Kerion celsii, einem tiefen, eitrigen, stark schmerzenden Infektionsherd. Erreger der Tinea capitis sind häufig aggressive zoophile (von Tieren übertragene) Pilzstämme. Hier tritt seit einigen Jahren vermehrt Microsporum canis als Erreger in Erscheinung, der vor allem im Mittelmeerraum von streunenden Katzen und Hunden übertragen wird. Die Infektion ist hoch ansteckend, daher muss streng darauf geachtet werden dass Bürsten, Kopfbedeckungen, Kuscheltiere, Bettwäsche etc. nach Einleitung der Therapie desinfiziert oder gekocht und unter keinen Umständen von einer anderen Person benutzt werden. Die Therapie muss in der Regel über mehrere Wochen systemisch erfolgen. Eine Kontrolle des familiären Umfelds ist sinnvoll, bei „stummen“ Trägern, die noch keine Symptome zeigen, kann eine topische Therapie mit einem antimykotischen Shampoo erfolgen. Auch Haustiere sollten untersucht werden.
Weitere Haustiere wie Meerschweinchen und andere Nagetiere, aber auch Wildtiere wie Igel können zoophile Dermatophyten übertragen. Ähnlich schwer wie die Tinea capitis verläuft die Tinea barbae, eine Pilzinfektion der Bartregion die ebenfalls durch zoophile Stämme ausgelöst und häufig bei Landwirten beobachtet wird.
Ärzte verordnen bei Hautmykosen gelegentlich auch Kombinationen aus Antimykotika und Glucocorticoiden. Sie werden bei stark entzündlichen Läsionen zur Initialtherapie eingesetzt. Der Patient sollte auf jeden Fall darauf hingewiesen werden, dass nach einigen Tagen ein Wechsel auf ein rein antimykotisches Präparat erfolgen sollte.
Für eine orale Therapie von Hautmykosen stehen dem Arzt vor allem die Wirkstoffe Fluconazol, Itraconazol, Griseofulvin und Terbinafin zur Verfügung. Hier ist bei der Abgabe sicherzustellen, dass der Patient seine individuelle Dosierung kennt, da Antimykotika in Abhängigkeit von der Art der Mykose sehr unterschiedlich dosiert werden. Da Hautmykosen oft vom Hautarzt therapiert werden, sollte abgefragt werden, ob dieser über die Medikation anderer Ärzte informiert wurde. Vor allem die Azol-Antimykotika interagieren als CYP-Induktoren oder -Hemmstoffe mit zahlreichen großen Arzneistoffgruppen, so dass Dosisanpassungen nötig sind. Einige orale Antimykotika können als Nebenwirkung Schwindel verursachen (Terbinafin, Fluconazol, Itraconazol), Griseofulvin beeinträchtigt das Reaktionsvermögen so dass die Fähigkeit am Straßenverkehr teilzunehmen eingeschränkt sein kann. Bei der Abgabe von Griseofulvin müssen noch einige weitere Beratungshinweise gegeben werden: Griseofulvin sollte mit einer fettreichen Mahlzeit und einer großen Menge Flüssigkeit, am besten Milch, eingenommen werden. Während der Therapie sollte auf Alkohol verzichtet werden, aufgrund der fotosensibilisierenden Wirkung auch auf intensive Sonnenbäder. Da Griseofulvin erbgutschädigend wirken kann, sollten Frauen bis zu einen Monat nach Therapieende konsequent verhüten, Männer bis zu sechs Monate nach Therapieende kein Kind zeugen.
Abschließend zwei Punkte, die in der Apotheke bei der Beratung zu allen Hautmykosen vermittelt werden sollten:
- Mykosen sind immer therapiebedürftig, sie heilen nicht von selbst. Versäumt man es, eine ursprünglich harmlose Pilzerkrankung zu therapieren, besteht die Gefahr der Ausbreitung auf andere Körperregionen sowie der Superinfektion. So kann eine Fußpilzinfektion Eintrittspforte für ein durch Streptokokken ausgelöstes Erysipel (Wundrose) sein.
- Die Therapie einer Mykose muss stets ausreichend lange über das Abklingen der Symptome hinaus fortgeführt werden, um den Erreger vollständig zu eliminieren. Ein vorzeitiger Therapieabbruch führt zum Wiederausbruch der Infektion. |
Literatur
Diagnose und Therapie von Candida-Infektionen. S1-Leitlinie, gemeinsame Empfehlungen der Deutschsprachigen Mykologischen Gesellschaft und der Paul-Ehrlich-Gesellschaft für Chemotherapie, Stand Juli 2016
Tinea der freien Haut. Leitlinie der Deutschen Dermatologischen Gesellschaft und der Deutschsprachigen Mykologischen Gesellschaft, Stand Oktober 2008, abgelaufen, wird zur Zeit überprüft
Die Vulvovaginalkandidose. S2-Leitlinie der Deutschen Gesellschaft für Gynäkologie und Geburtshilfe, der Arbeitsgemeinschaft für Infektionen und Infektionsimmunologie in der Gynäkologie und Geburtshilfe, der Deutschen Dermatologischen Gesellschaft und der Deutschsprachigen Mykologischen Gesellschaft, Stand Dezember 2013
Hay RJ. Tinea capitis: Current Status. Mycopathologia 2017;182:87-93
Nenoff P et al. Mycology – an update. Part 1: Dermatomycoses: Causative agents, epidemiology and pathogenesis. Part 2: Dermatomycoses: Clinical picture an diagnostics. Journal of the German Society of Dermatology; CME-Artikel 2014
Ely JW et al. Diagnosis and Management of Tinea Infections. American Family Physician 2014;90(10)
Lehnen J. Beratungspraxis Pilzinfektionen. Deutscher Apotheker Verlag 1. Auflage 2013
Hof H et al. Medizinisch relevante Pilze. aus: Medizinische Mikrobiologie, Thieme-Verlag 2017
Fachinformationen der Hersteller
weiter Literatur bei der Autorin























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.