
- DAZ.online
- DAZ / AZ
- DAZ 8/2015
- Dreifache Angiokinase-...
Arzneimittel und Therapie
Dreifache Angiokinase-Hemmung
Nintedanib verlängert beim nicht-kleinzelligen Lungenkarzinom das Leben
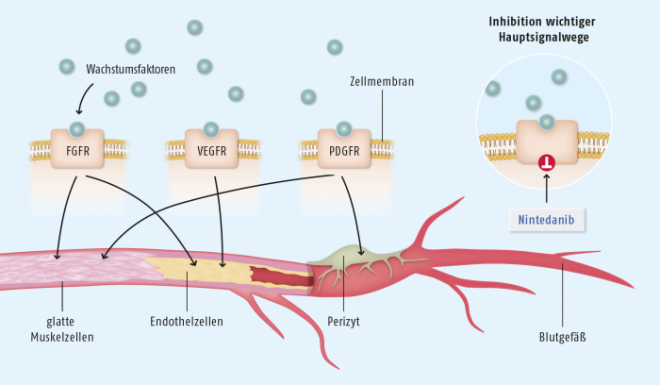
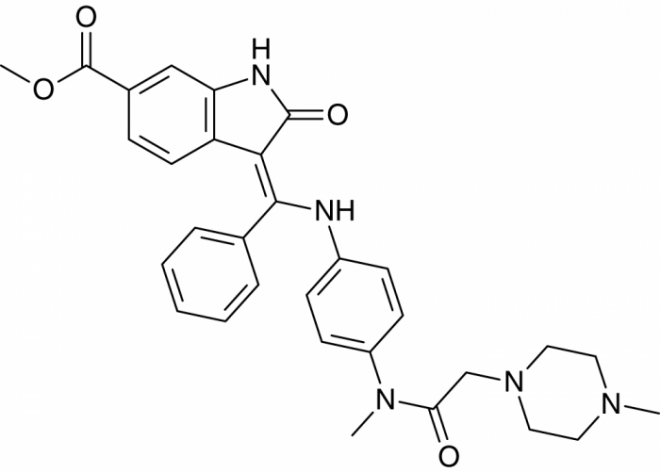
Nintedanib (Vargatef®) ist ein oral einzunehmender Angiokinase-Hemmer, der simultan die Signalweiterleitung von Wachstumsfaktoren für drei Rezeptorfamilien hemmt. Er blockiert die Tyrosinkinasen von Rezeptoren/Rezeptorfamilien für VEGF 1-3 (Vascular Endothelial Growth Factor), für FGFR (Fibroblasten-Wachstumsfaktor) sowie für PDGF alpha und beta (Platelet Derived Growth Factor). Diese Rezeptorfamilien sind an der Angiogenese sowie beim Wachstum und bei der Metastasierung von Tumoren beteiligt. Ihre Blockade kann demzufolge die Ausbreitung von Krebszellen hemmen. Nintedanib ist zugelassen in Kombination mit Docetaxel zur Zweit-Linien-Therapie des lokal fortgeschrittenen, metastasierten oder lokal rezidivierten nicht-kleinzelligen Lungenkarzinoms mit Adenokarzinom-Histologie.
Nintedanib blockiert die Kinase-Aktivität von drei für die Angiogenese wichtigen Wachstumsfaktor-Rezeptoren: FGFR (Fibroblasten-Growth-Factor-Rezeptor) auf glatten Muskelzellen, VEGFR (Vascular-Endothelial-Growth-Factor-Rezeptor) auf Endothelzellen und PDGFR (Platelet-Derived-Growth-Factor-Rezeptor) auf Perizyten. Damit wird das für die Tumorversorgung wichtige Wachstum der Blutgefäße unterdrückt.
Zulassungsstudie
Die Zulassung von Nintedanib beruht auf den Daten der multinationalen LUME-Lung-1-Studie mit mehr als 1300 Probanden. Die unabhängig von ihrem Mutationsstatus eingeschlossenen Patienten waren an einem nicht-kleinzelligen Lungenkarzinom (NSCLC) erkrankt, das nach einer Erst-Linien-Therapie weiter fortschritt. Sie erhielten randomisiert Nintedanib oral zweimal 200 mg pro Tag (außer am Tag der Chemotherapie) plus Docetaxel 75 mg/m² i. v. alle drei Wochen oder Placebo plus Docetaxel. Der primäre Studienendpunkt war das progressionsfreie Überleben, ein sekundärer Endpunkt das Gesamtüberleben. Das progressionsfreie Überleben wurde durch die Kombination von Docetaxel plus Nintedanib von 2,7 Monaten (Docetaxel-Gruppe) auf 3,4 Monate verlängert (HR 0,79; p = 0,0019). Beim Gesamtüberleben zeigte sich für die gesamte Studienpopulation ein positiver Trend zugunsten der Kombinationstherapie (10,1 Monate vs. 9,1 Monate; p = 0,272). Eine präspezifizierte Subgruppenanalyse führte beim Gesamtüberleben zu folgendem Ergebnis: Patienten mit einem Adenokarzinom [Anmerkung: Adenokarzinome sind die größte Subgruppe der nicht-kleinzelligen Lungenkarzinome] erzielten unter der Kombinationstherapie ein medianes Gesamtüberleben von 12,6 Monaten (vs. 10,3 Monaten unter der Docetaxel-Therapie; HR = 0,83; p = 0,0359). Für diese Subgruppe zeigte sich also eine Verlängerung des Gesamtüberlebens um 2,3 Monate. Eine Auswertung von Standardfragebögen zur Lebensqualität zeigte, dass die Lebensqualität in beiden Gruppen vergleichbar war. Die Verlängerung des Gesamtüberlebens ging nicht zulasten der Lebensqualität. Die Zahl der Studienabbrüche war in beiden Gruppen vergleichbar. Bei Patienten, die die Kombinationstherapie erhielten, wurden mehr Nebenwirkungen registriert als bei Probanden der Monotherapie-Gruppe. Die unerwünschten Wirkungen konnten durch Dosisreduktionen, supportive Maßnahmen und Therapieunterbrechungen kontrolliert werden.
Unerwünschte Wirkungen und Interaktionen
Die in der Zulassungsstudie am häufigsten aufgetretenen unerwünschten Ereignisse waren reversible Leberenzymerhöhungen sowie gastrointestinale Nebenwirkungen; klassenspezifische Effekte, die für eine Therapie mit Angiogenese-Hemmern charakteristisch sind (Hypertonie, Blutungen, Thrombosen), traten bei Adenokarzinom-Patienten unter der Kombinationstherapie kaum häufiger auf als unter der Monotherapie. Sehr häufig (> 1/10) traten Neutropenie, Appetitverlust, Elektrolytverschiebungen, Blutungen, periphere Neuropathie, Erhöhung der Leberenzyme, febrile Neutropenie, Sepsis, Abszesse, Übelkeit, Erbrechen, Durchfall, Abdominalschmerz und Mukositis auf; häufig wurden Dehydratation, Hypertonie, venöse Thromboembolien sowie Hyperbilirubinämie registriert. Nintedanib ist ein Substrat von P-Glykoprotein (P-gp). Die gleichzeitige Gabe des starken P-gp-Inhibitors Ketoconazol erhöht den Plasmaspiegel von Nintedanib. Bei gleichzeitiger Gabe des starken P-gp-Induktors Rifampicin sinkt der Plasmaspiegel von Nintedanib. Die Biotransformation von Nintedanib erfolgt nur in geringem Ausmaß über CYP-Stoffwechselwege, so dass auf diesem Weg mit keinen nennenswerten Interaktionen zu rechnen ist.
Dosierung
Die empfohlene Dosis von Nintedanib beträgt 200 mg zweimal täglich, die im Abstand von ca. zwölf Stunden an den Tagen 2 bis 21 eines 21-tägigen Standardbehandlungszyklus mit Docetaxel eingenommen wird. Vargatef® darf nicht am selben Tag der Anwendung der Chemotherapie mit Docetaxel (= Tag 1) eingenommen werden. Wenn eine Einnahme von Nintedanib versäumt wird, sollte die Einnahme zum nächsten geplanten Zeitpunkt mit der empfohlenen Dosis fortgesetzt werden. Die einzelnen Tagesdosen von Nintedanib sollten nicht über die empfohlene Dosis hinaus erhöht werden, um die versäumten Dosen auszugleichen. Die empfohlene maximale Tagesdosis von 400 mg sollte nicht überschritten werden. Patienten können die Therapie mit Nintedanib nach Absetzen von Docetaxel fortsetzen, solange ein klinischer Nutzen beobachtet wird oder bis eine inakzeptable Toxizität auftritt. Die Kapseln werden vorzugsweise mit einer Mahlzeit eingenommen; sie müssen unzerkaut bzw. unzerkleinert mit Wasser geschluckt werden.
Einschätzung und weitere Indikationen
Dem Leiter der Zulassungsstudie zufolge steht nun nach fast zehn Jahren Stillstand wieder eine neue Option zur Verfügung, die das Überleben von Patienten mit einem fortgeschrittenen Adenokarzinom der Lunge in der Zweit-Linien-Therapie signifikant verlängern kann. Nintedanib wird derzeit in Studien zur Therapie weiterer solider Tumoren (Ovarialkarzinom, Darmkrebs, Nierenzellkarzinom, Mesotheliom, Leberkrebs) eingesetzt. Der Wirkstoff Nintedanib ist ferner unter der Bezeichnung Ofev® seit Oktober 2014 von der FDA und seit 19. Januar 2015 von der EMA zur Behandlung der idiopathischen Lungenfibrose zugelassen. Durch die mehrfache Kinasehemmung werden Wege blockiert, die bei der Vernarbung des Lungengewebes beteiligt sein können. Sicherheit und Wirksamkeit wurden in mehreren klinischen Studien mit mehr als 1200 Patienten bestätigt. |
Quelle
Reck M et al. Docetaxel plus nintedanib versus docetaxel plus placebo in patients with previously treated non-small-cell lung cancer (LUME-Lung 1): a phase 3, double-blind, randomised controlled trial. Lancet Oncol 2014;15(2):143-155
Fachinformation Vargatef® (Stand November 2014).


















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.