
- DAZ.online
- DAZ / AZ
- DAZ 48/2015
- Von asymptomatisch bis ...
Medizin
Von asymptomatisch bis Leberversagen
Die Hepatitis B ist immer noch die häufigste Form der Virushepatitis
Da die Schutzimpfung in vielen, vor allem ärmeren Ländern bisher nicht eingeführt wurde, leiden weltweit zurzeit etwa 248 Millionen Menschen unter einer chronischen Hepatitis B. Jährlich sterben etwa 780.000 Menschen aufgrund einer HBV-Infektion, davon allein 650.000 an den Folgeerkrankungen Leberzirrhose und Leberkarzinom. Im Hinblick auf die geografische Verteilung dominieren Ostasien und die Subsahara-Regionen Afrikas mit einer Rate von fünf bis zehn, teilweise sogar bis 20 Prozent chronisch infizierter Erwachsener. Erhöhte Raten finden sich auch im Mittleren Osten sowie in Süd- und Osteuropa, vor allem in Rumänien, Bulgarien, Griechenland und der Türkei (in der östlichen Türkei über 7%).
In Deutschland niedrige Prävalenz
Demgegenüber sind im Schnitt weniger als ein Prozent der Bevölkerung in Westeuropa und Nordamerika chronisch infiziert. Auch Deutschland gehört – nicht zuletzt dank der hohen Impfquote – mit einer Rate von unter einem Prozent zu den Niedrig-Prävalenzländern; hier wurde seit 2001 ein Rückgang der gemeldeten Hepatitis-B-Erkrankungen verzeichnet. Allerdings stagniert dieser Trend mit geringen Schwankungen seit 2009, und seit 2012 steigen die Fallzahlen tendenziell wieder leicht an. Im Jahr 2014 wurden insgesamt 2374 Hepatitis-B-Erkrankungen an das Robert Koch-Institut gemeldet – 430 Fälle mehr als im Vorjahr. Vor allem in den Stadtstaaten Hamburg und Berlin sowie in Bundesländern mit großen Ballungszentren wie Nordrhein-Westfalen stieg die Anzahl im Vergleich zu den Vorjahren.
Schätzungen zufolge entfallen etwa 40 Prozent der chronischen Fälle auf Menschen, die einen Migrationshintergrund aufweisen und aus Ländern mit einer höheren Prävalenz für Hepatitis B stammen. Die derzeit stark zunehmende Migration von Menschen aus solchen Regionen dürfte die Hepatitis-B-Rate hierzulande weiterhin ansteigen lassen.
Viral verursacht, immunologisch vermittelt
Erreger der Hepatitis B ist das Hepatitis-B-Virus (HBV), ein kleines, umhülltes DNA-Virus, das zur Familie der Hepadnaviridae gehört und 1970 entdeckt wurde (s. Kasten). Man geht heute davon aus, dass das HBV keine direkte zytopathische Wirkung an den Hepatozyten (Leberzellen) zeigt, sondern dass die Organschädigung vielmehr auf eine inadäquate Immunreaktion gegen verschiedene HBV-Antigene zurückzuführen ist. Wenn zu wenig infizierte Hepatozyten zerstört werden und die Virusvermehrung zu schwach gehemmt wird, erhöht sich die Viruslast, und die Infektion persistiert.
Das Hepatitis-B-Virus (HBV)
Seine Außenhülle besteht aus einer Lipiddoppelschicht und dem darin enthaltenen HBV-Oberflächenantigen (HBV surface antigen, HBsAg), das für den serologischen Nachweis einer akuten Infektion von Bedeutung ist. Sein Genom ist eine zirkuläre, teilweise doppelsträngige DNA, die in einer aus dem HBV-Kernantigen (HBV core antigen, HBcAg) bestehenden Kapsid verpackt ist. Bei der Replikation des Virus wird das HBcAg zu HBeAg abgebaut, das als serologischer Marker der Virusvermehrung dient.
Laut Robert Koch-Institut sind derzeit mindestens neun verschiedene HBV-Genotypen (A – I), zahlreiche Subgenotypen und acht serologisch unterscheidbare HBsAg-Subtypen bekannt, deren Verbreitung in verschiedenen geografischen Regionen unterschiedlich ist. In Europa sind die Genotypen A2 und D vorherrschend.
Aufgrund seiner Außenhülle zeigt das HBV eine vergleichsweise hohe Stabilität gegenüber Umwelteinflüssen und nicht zuletzt auch eine relativ hohe Resistenz gegenüber Desinfektionsmitteln.
Hauptsächlich sexuelle Übertragung
Da das HBV insbesondere im Blut enorm hohe Konzentrationen erreichen kann (bis zu 1011 Viruspartikel pro Milliliter), genügen bereits kleinste Mengen Blut, um das Virus auch über kleinste Verletzungen der Haut oder Schleimhaut zu übertragen. Weiterhin findet sich das Virus – wenn auch in geringeren Konzentrationen – in Sperma, Vaginalsekret, Speichel, Tränenflüssigkeit, Menstruationsblut und Kolostrum (Erst- oder Vormilch).
Im Gegensatz zur fäkal-oralen Übertragung des Hepatitis-A-Virus wird das HBV hauptsächlich sexuell sowie über Blut übertragen. Das Risiko, sich über Spenderblut und Blutprodukte zu infizieren, ist aufgrund der Spendertestung in unseren Breiten inzwischen nahezu ausgeschlossen.
Schätzungen zufolge hat die Übertragung durch ungeschützten Geschlechtsverkehr in Deutschland und anderen westlichen Industriestaaten einen Anteil von 40 bis 70 Prozent an den Neuinfektionen, wobei der größte Teil akuter Hepatitis-B-Fälle bei jungen Erwachsenen beobachtet wird. Besonders gefährdet sind homosexuell aktive Männer (MSM), aber auch Prostituierte, promiskuitive Heterosexuelle sowie Reisende aus Hochprävalenz-Ländern, die dort sexuellen Kontakt hatten.
Eine weitere HBV-Risikogruppe sind i.v.-Drogenabhängige. Hauptrisikofaktoren sind der Tausch von Spritzen und Kanülen bzw. deren mehrfache Anwendung (ca. 20% aller Fälle) sowie die gemeinsame Nutzung anderen Zubehörs ohne ausreichende Sterilisation oder Desinfektion. Hinzu kommt das erhöhte Risiko für andere gravierende Infektionskrankheiten wie HIV/Aids, Tuberkulose oder Hepatitis C. In diesem Kontext sind auch Gefängnisinsassen als Risikogruppe anzusehen.
Ungewollte Risikogruppen
Trotz der Schutzimpfung wird die Hepatitis B immer noch als wichtige berufsbedingte Infektionserkrankung angesehen, vor allem im Gesundheitswesen (einschließlich Pflegeheimen und Rettungsdiensten). Nicht nur die klassische „Kanülenstichverletzung“ ist möglich, sondern auch der Kontakt infizierter Körperflüssigkeiten mit Schleimhäuten und Bagatellverletzungen. Laut Angabe der Berufsgenossenschaft für Gesundheitsdienste und Wohlfahrtspflege (BGW) wurden in den vergangenen Jahren jährlich etwa 100 Verdachtsmeldungen berufsbedingter Hepatitis-B-Erkrankungen bearbeitet (allerdings sind dort nur etwa 40% der im medizinischen Bereich beschäftigten Personen versichert).
Eine weitere Risikogruppe sind die Neugeborenen von HBV-infizierten Müttern. Diese können die Infektion – sowohl prä- als auch perinatal – an ihr Kind weitergeben, es sei denn, beim Neugeborenen wird sowohl eine aktive als auch eine passive Immunisierung durchgeführt.
Akuter Verlauf oft unbemerkt
Die Inkubationszeit ist sehr variabel und liegt zwischen 40 und 180 Tagen (s. Kasten „Diagnostische Lücke“). Bei Erwachsenen verläuft etwa ein Drittel der HBV-Infektionen asymptomatisch und daher häufig unbemerkt. Ein weiteres Drittel führt zum klinischen Bild einer akuten ikterischen Hepatitis, beim letzten Drittel der Infizierten tritt die akute Form ohne Ikterus auf.
Das Prodromalstadium kann bis zu zehn Tage dauern und zeigt eher unspezifische Symptome:
grippale Symptome wie subfebrile Temperaturen und Abgeschlagenheit,
gastrointestinale Beschwerden wie Appetitlosigkeit, Unwohlsein, Erbrechen, Druckschmerz im rechten Oberbauch (beginnende Lebervergrößerung), manchmal auch Diarrhö,
Gelenkschmerzen und flüchtiges Hautexanthem.
Diagnostische Lücke
Bei fehlender oder schwacher Immunabwehr vermehrt sich das Hepatitis-B-Virus sehr stark. Aber auch bei Immunkompetenten kann es bis zu einem halben Jahr dauern, bis eine Immunreaktion eintritt. Das bedeutet, dass eine betroffene Person bereits mehrere Wochen vor Krankheitsausbruch hochinfektiös sein kann. Zwar hängt die Ansteckungsgefahr stark von der Virämie (HBV-DNA) und der Art des Kontaktes ab. Prinzipiell muss aber jede HBsAg-positive Person als potenziell infektiös angesehen werden.
Anschließend folgt das Stadium der Organmanifestation, gegebenenfalls mit einer ikterischen Phase: Der Urin verfärbt sich dunkel, der Stuhl ist entfärbt, es entwickelt sich ein Ikterus (zuerst an den Skleren, dann an der Haut). Durch die Cholestase (Gallenstau) kommt es häufig zum Juckreiz, die Leber bleibt druckempfindlich. In bis zu 20 Prozent der Fälle zeigen sich geschwollene Lymphknoten und eine vergrößerte Milz. Insgesamt jedoch fühlen sich viele Patienten mit dem Beginn des Ikterus wieder besser. Dieser erreicht seinen Höhepunkt nach ein bis zwei Wochen und blasst dann innerhalb von zwei bis vier, manchmal auch erst nach acht Wochen wieder ab.
Etwa 0,5 bis 1 Prozent aller Infektionen verlaufen fulminant mit der Entwicklung eines akuten Leberversagens. Das klinische Bild umfasst neben dem Ikterus vor allem eine hämorrhagische Diathese durch Mangel an Gerinnungsfaktoren, eine arterielle Hypotonie durch Vasodilatation und eine hepatische Enzephalopathie mit Bewusstseinsstörungen von Somnolenz bis Koma.
Aufgrund ihrer hohen Spontanheilungsrate wird die akute Hepatitis B beim Erwachsenen allenfalls symptomatisch behandelt (Bettruhe, fettarme Kost). Nur bei eingeschränkter Leberfunktion (z. B. Quick-Wert unter 50%) ist eine antivirale Therapie indiziert (s. u.).
Chronischer Verlauf und Folgeschäden
Während die meisten akuten Hepatitis-B-Erkrankungen bei Erwachsenen vollständig ausheilen und zu einer lebenslangen Immunität führen, entwickelt sich bei bis zu zehn Prozent der HBV-infizierten Erwachsenen eine chronische Verlaufsform, wobei etwa doppelt so viele Männer wie Frauen betroffen sind. Die Chronifizierungsrate nimmt mit sinkendem Alter stetig zu, sodass die HBV-Infektion bei Kleinkindern in der Regel sofort einen chronischen Verlauf nimmt. Noch bei vierjährigen Betroffenen verläuft die Hälfte aller Infektionen chronisch. Ebenfalls gefährdet sind immungeschwächte Personen; bei Nierentransplantierten etwa beträgt das Risiko bis zu 50 Prozent.
Von einer chronischen HBV-Infektion spricht man, wenn (auch unspezifische) Symptome länger als sechs Monate persistieren und histologische sowie serologische Marker nachweisbar sind, vor allem ein persistierendes HBsAg:
- Bei etwa fünf Prozent der Betroffenen kommt es zu einer cholestatischen Verlaufsform mit starkem Anstieg des Bilirubins und der Transaminasen AST und ALT (früher: GOT, GPT).
- Viele Patienten sind asymptomatischer HBsAg-Träger: Die Virämie ist niedrig, die Leberfunktion ist nicht oder kaum eingeschränkt. Auch die Leberhistologie ist nahezu normal, HBsAg-haltige Leberzellen können als sogenannte Milchglashepatozyten nachgewiesen werden.
- Möglich ist auch ein asymptomatischer, hochvirämischer HBsAg-Trägerstatus (ohne Nachweis einer Organschädigung), der allerdings in eine manifeste chronische Hepatitis B mit Leberzellschädigung und Funktionsstörungen übergehen kann.
Mit zunehmender Viruslast steigt das Risiko für gravierende Folgeschäden. Weltweit lassen sich etwa 30 Prozent aller Fälle von Leberzirrhose und etwa 53 Prozent aller Fälle des primären Leberzellkarzinoms (hepatozelluläres Karzinom, HCC) auf eine chronische Hepatitis B zurückführen.
Viruslast wichtiger Parameter
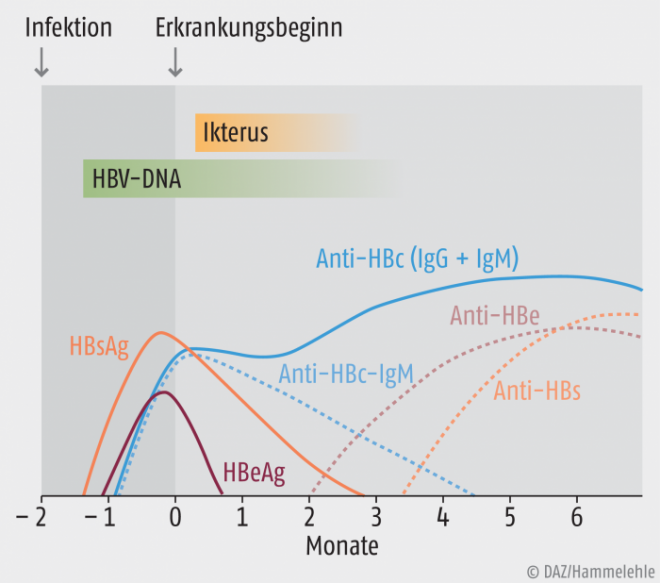
Die Konstellation der verschiedenen serologischen Marker erlaubt in der Regel die Trennung zwischen einer abgelaufenen und einer noch bestehenden HBV-Infektion (s. Abb. 1). Die Hepatitis-B-Antikörper (Immunglobuline G und M; IgG, IgM) werden nacheinander gebildet: zuerst Anti-HBc, dann Anti-HBe, zuletzt Anti-HBs (auch: HBcAK, HBeAK, HBsAK). Das Anti-HBs tritt erst auf, wenn das zugehörige Antigen HBsAg schon wieder verschwunden ist, und signalisiert die Ausheilung der Hepatitis B.
Als ergänzender Parameter einer chronischen HBV-Infektion steht seit einigen Jahren die quantitative Bestimmung der HBV-DNA zur Verfügung, um die individuelle Viruslast und Infektiosität abzuschätzen. Werte über 2000 IE/ml
- sprechen für eine manifeste chronische Hepatitis B, wenn auch die Transaminasenwerte und (meistens) das HbeAg erhöht sind, oder
- weisen auf einen hochvirämischen HBsAg-Status hin, wenn auch das HBeAg erhöht ist, aber die Transaminasenwerte normal sind.
Mit Abklingen der akuten Hepatitis-B-Erkrankung verschwindet das Anti-HBc-IgM im Verlauf von Monaten, während das Anti-HBc-IgG lebenslang persistiert. Bei chronischem Verlauf kann auch das Anti-HBc-IgM in mäßig hohen Konzentrationen nachweisbar bleiben.
Abb. 1: Serologisches Muster einer HBV-Infektion mit nachfolgender Hepatitis und Ausheilung (Ikterus bei jedem 3. Fall).
Suppression der HBV-DNA mit Virustatika
Nach der Indikation der aktuellen deutschen S3-Leitlinie sind alle Patienten mit chronischer HBV-Infektion (HBV-DNA über 2000 IE/ml) „grundsätzlich Kandidaten für eine antivirale Therapie“. Ziel ist zunächst eine dauerhafte Suppression der HBV-DNA unterhalb der Nachweisgrenze (zur Vermeidung des HCC), langfristig die vollständige Serokonversion von HBsAg zu Anti-HBs. Im Einzelfall orientiert man sich auch an der Höhe der Transaminasenwerte und am Organbefund. Eine antivirale Therapie ist indiziert bei
- Patienten mit fortgeschrittener Leberfibrose oder -zirrhose, unabhängig von der Höhe der Virämie, sowie
- Patienten ohne Leberzirrhose, aber mit einer Viruslast über 2000 IE/ml, wiederholt erhöhten Transaminasenwerten und bestimmten histologischen Befunden.
Als Virustatika stehen Interferon alpha (IFN-α) und pegyliertes Interferon alpha-2a (Peginterferon α-2a) sowie mehrere Nucleosid- und Nucleotidanaloga zur Auswahl. Anhand bestimmter Kriterien kann entschieden werden, welche Patienten für welche Substanzgruppen geeignet sind (s. Tab. 1).
Interferone |
Nucleosid- und Nucleotidanaloga |
|---|---|
|
|
Interferon hat den Vorteil, dass es sich um eine zeitlich definierte Therapiedauer handelt, in der Regel maximal 48 Wochen. Bei geeigneten Patienten beendet Interferon in 30 bis 40 Prozent der Fälle die Virusreplikation. Allerdings klagen mehr als die Hälfte der Patienten über Nebenwirkungen wie grippeähnliche Beschwerden, Haarausfall und Depressionen; auch eine Thrombozytopenie kann sich unter Interferon verstärken. Aufgrund der patientenfreundlichen Applikation (einmal pro Woche) bei mindestens äquivalenten Ansprechraten wird der Einsatz von PEG-Interferon dem des Standard-Interferons inzwischen vorgezogen.
Antivirale Therapie oft lebenslang
Lassen sich bereits Zeichen einer Leberzirrhose nachweisen, sollten Virustatika mit einer hohen genetischen Resistenzbarriere gegeben werden: Nucleosidanaloga wie Entecavir oder Nucleotidanaloga wie Tenofovir.
Alle drei bis sechs Monate sollten die HBV-DNA-Spiegel kontrolliert werden, um sowohl die Therapieadhärenz als auch das Therapieansprechen zu überprüfen. Letzteres gilt als erreicht, wenn nach sechs Monaten die HBV-DNA auf unter 200 IE/ml gesunken ist und nach zwölf Monaten nicht mehr nachweisbar ist. Da Nucleosid- und Nucleotidanaloga zunächst „nur“ die Viruslast senken, kann die Therapiedauer im Einzelfall nicht vorhergesagt werden; häufig ist sie lebenslang. Das ultimative Therapieziel einer dauerhaften Serokonversion wird unter Nucleosid- oder Nucleotidanaloga nur in bis zu zehn Prozent der Fälle erreicht.
Nucleosid- und Nucleotidanaloga können oral verabreicht werden und sind auch bei langer Therapiedauer gut verträglich. Dennoch sollte die Nierenfunktion der Patienten regelmäßig überprüft werden.
Impfung exponierter Personen
Eine effektive Prophylaxe der Hepatitis B ist nur durch eine aktive Immunisierung möglich. Hierbei schützt ein gentechnologisch hergestellter Impfstoff aus dem HBV-Oberflächenantigen (HBsAg) vor der Infektion mit HBV. In Deutschland beinhalten die Empfehlungen der STIKO nicht nur die Impfungen für Personengruppen mit einem erhöhten HBV-Infektionsrisiko (s. Tab. 2), sondern auch eine generelle Grundimmunisierung im Säuglings- und Kleinkindalter (einschließlich Nachholen der Grundimmunisierung bis dahin noch ungeimpfter Kinder und Jugendlicher möglichst vor der Pubertät, spätestens aber bis zum 18. Lebensjahr).
|
Personen, bei denen
ein schwerer Verlauf einer Hepatitis-B-Erkrankung zu erwarten ist (z. B. HIV-Positive, HCV-Positive, Dialysepatienten)
|
|
Personen mit einem erhöhten nichtberuflichen Expositionsrisiko, z. B. durch
|
|
Personen mit einem erhöhten beruflichen Expositionsrisiko, z. B.
|
|
Personen, die
|
Der Impfstoff wird zu den Zeitpunkten 0, 1 und 6 Monate jeweils intramuskulär appliziert (in den Schultermuskel M. deltoideus). Die Immunisierung gilt als erfolgreich, wenn vier bis acht Wochen nach der dritten Impfung ein Anti-HBs-Wert von mindestens 100 IE/l erreicht wurde (bei rund 96% aller Impflinge). Diese Personen sind für wenigstens zehn Jahre geschützt. Liegt der Anti-HBs-Titer jedoch unter 100 IE/l, muss die Impfung wiederholt und abermals nach vier bis acht Wochen eine Kontrolle durchgeführt werden.
Andere Schutzmaßnahmen
Nicht zu vernachlässigen sind verschiedene präventive Maßnahmen, die sowohl Hygienestandards betreffen als auch Verhaltensweisen in Risikogruppen, vor allem
- effektive Desinfektions-, Schutz- und Entsorgungsmaßnahmen in medizinischen Einrichtungen (z. B. Einmalhandschuhe, Sicherheitskanülen und -lanzetten, vorsichtiger Umgang mit Fremdblut),
- das Screening von Blutspendern auf Virusmarker und Transaminasen,
- eine räumliche Trennung von Hepatitis-Virusträgern auf (Dialyse-)Stationen,
- Verzicht auf Promiskuität und Benutzung von Kondomen,
- kein „needle sharing“ bei Drogenabhängigen,
- das strikte Einhalten häuslicher Hygiene bei Kontakt mit HBV-Infizierten in Familie oder Wohngemeinschaft (z. B. kein gemeinsames Benutzen von Nagelscheren oder Rasierapparaten),
- eine arbeitsmedizinische Vorsorgeuntersuchung und ggf. aktive Immunisierung gegen HBV bei beruflich gefährdeten Personen.
Im Falle eines Falles
Besteht der Verdacht auf eine mögliche Übertragung des Hepatitis-B-Virus durch direkten Kontakt mit Blut oder eine Verletzung (Kanülenstich), sollte bei ungeimpften Personen innerhalb von 48 Stunden eine Postexpositionsprophylaxe durchgeführt werden. Diese erfolgt in der Regel simultan als aktive Immunisierung (Impfung) und passive Immunisierung mit Hepatitis-B-Immunglobulin. Bei Personen mit nachweislich bestehendem Impfschutz genügt als Prophylaxe eine Auffrischungsimpfung. |
Literatur
[1] Cornberg M, et al. Aktualisierung der S3-Leitlinie zur Prophylaxe, Diagnostik und Therapie der Hepatitis-B-Virusinfektion. AWMF-Register-Nr. 021/011. Z Gastroenterol 2011;49:871-930
[2] Robert Koch-Institut. Hepatitis B. RKI-Ratgeber für Ärzte. Fassung vom November 2011
[3] Virushepatitiden. In: Herold G, et al. Innere Medizin, 2014: 517-521
[4] Hepatitis B. In: Herold G, et al. Innere Medizin, 2014: 522-526
[5] Schweitzer A, et al. Estimations of worldwide prevalence of chronic Hepatitis B virus infection: a systematic review of data published between 1965 and 2013. Lancet 2015;386(10003):1546-55
[6] Robert Koch-Institut. Virushepatitis B und D im Jahr 2014. Epidemiol Bull 2015;(29):271-285
[7] Robert Koch-Institut. Wissenschaftliche Begründung für die Änderung der Empfehlung zur Impfung gegen Hepatitis B. Epidemiol Bull 2013;(36/37):371-381





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.