
- DAZ.online
- DAZ / AZ
- DAZ 28/2015
- Neue Wege
Therapietreue
Neue Wege
Künftig kann mHealth die Therapietreue im Alter verbessern

Die Therapietreue eines Patienten beginnt bereits bei der Diagnose, indem der Patient seine Erkrankung als solche anerkennt. Dies ist umso wichtiger bei chronischen Erkrankungen, die ohne wahrnehmbare Symptome einhergehen und vom Patienten erst verstanden und eingeordnet werden müssen. Der zweite wichtige Schritt auf dem Weg zur Therapietreue ist die Akzeptanz der verschriebenen Arzneimittel und der Therapie insgesamt. Hierzu gehört auch, dass der Patient ein gewisses Verständnis für die Therapie entwickelt und die Arzneimittel zur jeweiligen chronischen Erkrankung zuordnen kann. Gerade mit der zunehmenden Anzahl chronischer Erkrankungen und verschriebener Arzneimittel kann das Arzneimittelmanagement durch die Apotheker entscheidend zur Therapietreue und Arzneimittelsicherheit beitragen.
Um die Therapietreue zu erreichen, ist es allerdings ebenfalls von ausschlaggebender Bedeutung, dass die Patienten sich einen Plan erstellen, wie, wann und wo sie die einzelnen Medikamente während ihres individuellen Tagesablaufs einnehmen wollen [2] und welche Erinnerungshilfen sie dabei am sinnvollsten einsetzen können [3]. Besonders Patienten mit einem geregelten Tagesablauf und einer gewissen Routine des Tagesablaufs profitieren von dieser Planung und erreichen eine hohe Therapietreue [4]. Dennoch bleibt die langfristige Aufrechterhaltung der Therapietreue eine große Herausforderung. Neben den im vorherigen Beitrag beschriebenen Anwendungsproblemen der Patienten können zahlreiche weitere Patienten- und Umgebungsfaktoren die Therapietreue negativ beeinflussen (Tab. 1).
Änderungen der Verschreibungen |
Wechselnde generische Substitution |
Auftretende Nebenwirkungen bzw. Symptome |
Patienteninduzierte Therapieoptimierung |
Krankheitsprogression |
Fortschreitendes Alter |
Nachlassende Kognition und sensomotorische Fähigkeiten |
Krankenhauseinweisung bzw. -entlassung |
Psychologische Faktoren (z. B. depressive Verstimmung) |
Medienberichte |
Gebrechlichkeit (Frailty) |
Dies gilt speziell für alte und multimorbide Patienten mit komplexen Arzneimitteltherapien und zunehmenden Einschränkungen hinsichtlich der Aufrechterhaltung einer selbstständigen Lebensführung. Eine unzureichende Therapietreue kann kurz- oder langfristig erhebliche und schwerwiegende Konsequenzen für den Patienten haben, darunter
- unveränderte Progression der Erkrankung,
- Komorbiditäten wie diabetische Retinopathie, erhöhte Sturzneigung mit bleibenden Behinderungen oder unvorhergesehenen Krankenhauseinweisungen z. B. aufgrund von Delirzuständen und
- vorzeitige Mortalität [5].
Die unzureichende Therapietreue hat damit nicht nur einen direkten Einfluss auf den Patienten, sondern verursacht auch erhebliche zusätzliche Kosten im Gesundheitswesen, die vermeidbar wären [17].
Ziel der zukünftigen ambulanten und stationären Arzneimitteltherapie muss deshalb auch die Sicherstellung der langfristigen Therapietreue sein, die nur durch ein effektives Monitoring der Arzneimitteleinnahme und Beratung der Patienten sichergestellt werden kann.
Bislang war die Überwachung der Arzneimitteleinnahme der Patienten in der ambulanten Versorgung allerdings nur bedingt möglich. Zu den direkten Überwachungsmethoden zählen etwa die Beobachtung der Einnahme durch den Patienten, die Messung von Plasmaspiegeln oder klinischen Parametern, die Befragung des Patienten zu seinen Arzneimitteln und deren Einnahme (z. B. Medication/Pills Identification Test, MIT/PIT; Self-Reported Questionnaire, SRQ) sowie ein Patiententagebuch zur Arzneimitteleinnahme. Bei den indirekten Überwachungsmethoden handelt es sich etwa um die Zählung der verbleibenden Dosen eines Arzneimittels im Besitz des Patienten, die zeitgerechte Einlösung von Rezepten und Ähnliches (Medication Possession Ratio, MPR; Cumulative Medication Gap, CMG) [6]. Diese Methoden sind allerdings schwer als Routinemessung durchführbar (z. B. Plasmaspiegelmessung, direkte Beobachtung) oder aber subjektiv und ungenau (Befragung des Patienten, Anzahl der Dosen im Besitz des Patienten).
ICT-basierte Verfahren
In den vergangenen Jahren wurden neuartige Verfahren zur Messung der Therapietreue entwickelt und erheblich vorangebracht, die nicht nur zunehmend in der medizinisch-pharmazeutischen Praxis eingesetzt werden, sondern das Potenzial haben, die Betreuung der Patienten grundlegend zu verändern. Diese Verfahren beruhen auf moderner „Information and Communication Technology“ (ICT); sie können über entsprechende Sensoren („wearable diagnostics“) nicht nur die Arzneimitteleinnahme überwachen, sondern auch die mit einer Erkrankung verbundenen biometrische Daten zu jeder Zeit und an jedem Ort des Patienten erfassen [7].
In diesem Zusammenhang ist es wichtig, sich die rasanten Entwicklung und Akzeptanz des „mobile Health“ (auch „mHealth“) bewusst zu machen, das heute in Form verschiedener Produkte (z. B. Fitbit, iHealth, Jawbone, Moves, RunKeeper, Strava, Withings) angeboten und von den großen amerikanischen Firmen vorangetrieben wird [8]. Es wird geschätzt, dass im Jahre 2012 bereits 44 Millionen Menschen ihre biometrischen Daten über mHealth aufgezeichnet haben [9].
Bei der Arzneimitteltherapie lassen sich elektronische mHealth-Applikationen für die direkte Erfassung der Einnahme eines Medikamentes und die direkte und kontinuierliche Messung von relevanten klinischen Parametern und biometrischen Daten einsetzen. Dadurch wird es möglich, Patienten in ihrer häuslichen Umgebung hinsichtlich der Therapietreue, des Behandlungserfolgs und eventueller Arzneimittelprobleme oder Gesundheitsprobleme (z. B. Sturzneigung) zu erfassen und gegebenenfalls frühzeitig einzugreifen. In England hat der National Health Service (NHS) bereits die Anwendung von „wearable diagnostics“ in der klinischen Praxis beschlossen und wird diese in den kommenden Jahren umsetzen [16]. Des Weiteren hat sich gezeigt, dass der Patient durch die Visualisierung der biometrischen Informationen seine Erkrankung besser und objektiver einschätzen kann, was wiederum seine Therapietreue verbessern kann [10].
Die elektronischen mHealth-Applikationen können das Öffnen des Verschlusses von Arzneiflaschen (z. B. MEMS®, MeadWestvaco, früher Aardex) aufzeichnen oder das Perforieren einer Blisterfolie, worauf die Daten am Computer gelesen oder per Smartphone übertragen werden können [11]. Seit 2012 steht auch ein essbarer Microchip zur Verfügung, der auf die Darreichungsform aufgebracht wird und im Kontakt mit der Magensäure ein Signal an einen am Gürtel befestigten Empfänger überträgt (Helius™, Proteus Digital Health). Diese Technologie wird bereits bei Lloyds Pharmacy in England angewendet, indem der individuellen verblisterten Tagestherapie der Patienten eine mit dem Chip ausgestattete Placebotablette beigefügt wird [12].
Die direkte Messung der biometrischen Daten eines Patienten (z. B. Blutdruck, Herzfrequenz, Blutglucosespiegel) und anderer relevanter Patientendaten (z. B. Bewegungsprofil, Sturzneigung, psychischer Zustand) stellt allerdings eine neue Dimension der Patientenbetreuung durch mHealth dar [7]. Denn hierdurch wird es möglich, auch die Wirksamkeit der Therapie zu überprüfen. Hinzu kommt, dass auch andere Parameter erfasst werden können, die Aussagen über die Gesamtkonstitution des Patienten machen und somit ein präventives Intervenieren erlauben [13]. Beispiele sind ein biometrischer Chip zur nicht-invasiven Messung des Glucosespiegels (Abb. 1) [14] und ein mit Sensoren (Wearable Motherboard™) ausgestattetes multifunktionelles Hemd (smart shirt), das z. B. Körpertemperatur, Herzschlag und Atmung kontrolliert [15].
Abb. 1: Ein kleiner biometrischer Chip (hier unter dem Auge platziert) kann kontinuierlich den Blutglucosespiegel kontrollieren.
Therapiemonitoring schließt Lücke
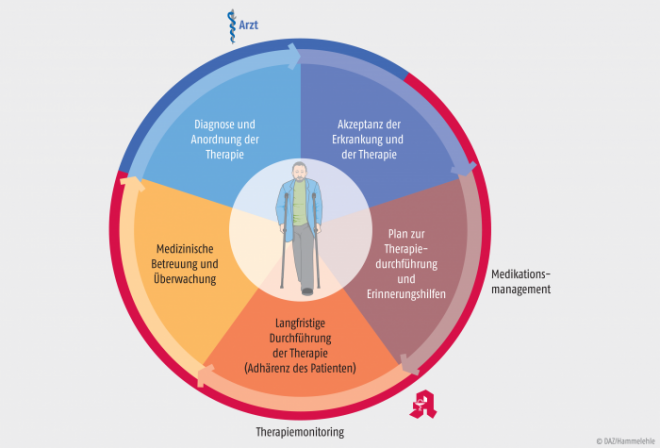
Die Anwendung eines mHealth-basierten Therapiemonitorings ist als konsequente Erweiterung des Medikationsmanagements durch den Apotheker zu sehen (Abb. 2). Durch die kontinuierliche Kontrolle der klinischen Parameter ist eine erhebliche Effizienzsteigerung der Arzneimitteltherapie zu erwarten. Des Weiteren ergibt sich ein geschlossener Kreislauf (engl. closed loop), weil das Therapiemonitoring wieder Konsequenzen für die Diagnose haben kann. Das ganze Konzept bedeutet einen Schritt von der derzeitigen reaktiven, erkrankungsorientierten Medizin hin zu einer prädiktiven, präventiven und patientenzentrierten Medizin [13].
Abb. 2: Patientenzentrierte Medizin: Effizienzsteigerung der Therapie durch die Apotheke, die zusätzlich zum Medikationsmanagement auch das Therapiemonitoring übernimmt.
Die ganz offensichtlichen Vorteile, die sich aus den Entwicklungen der ICT und dem mHealth ergeben, werden die treibende Kraft sein, die noch bestehenden technischen und gesellschaftlichen Fragestellungen zügig zu lösen. Die mit der ICT aufgewachsenen und vertrauten Generationen werden auch bei Krankheit und im Alter nicht auf die Vorteile einer „closed loop“-Medizin durch mHealth verzichten wollen. Es ist also nur eine Frage der Zeit, wann mHealth zu einem Bestandteil des Gesundheitswesens wird. Spätestens dann muss sich entscheiden, welche Disziplin im Gesundheitswesen durch ihr Engagement die Federführung beim mHealth übernimmt. Der Apotheker wäre am ehesten dafür prädestiniert, nicht zuletzt weil es sich um die logische Weiterentwicklung des Medikationsmanagements handelt (Abb. 2). |
Literatur
[1] Sabate E. Adherence to Long-Term Therapies: Evidence for Action. Geneva: World Health Organization 2003; www.who.int/chp/knowledge/publications/adherence_report/en
[2] Gollwitzer PM. Implementation Intentions – Strong Effects of Simple Plans. Am Psychologist 1999;54(7):493-503
[3] Park DC, Meade ML. A Broad View of Medical Adherence: Integrating Cognitive, Social, and Contextual Factors. In Park DC, Liu LL (Eds). Medical adherence and aging: Social and cognitive perspectives. Washington, DC: American Psychological Association 2007: 3-21
[4] Martin M, Park DC. The Martin and Park environmental demands (MPED) questionnaire: psychometric properties of a brief instrument to measure self-reported environmental demands. Aging Clin Exp Res 2003;15(1):77-82
[5] Madden JM, et al. Cost-related medication nonadherence and spending on basic needs following implementation of Medicare Part D. JAMA 2008;299(16):1922-1928
[6] Stegemann S, et al. Adherence Measurement Systems and Technology for oral medications in older patient populations. Eur Geriatric Med 2012;3:254-260
[7] Akter S, Ray P. mHealth – an ultimate platform to serve the unserved. IMIA Yearb Med Inform 2010:94-100
[8] https://developers.google.com/fit/overview; https://developer.apple.com/healthkit; http://news.microsoft.com/presskits/microsoftband
[9] Raskin R. Digital Health and the monitored life. Posted 12/14/2012; www.huffingtonpost.com/robin-raskin/digital-health-and-the-mo_b_2301222.html
[10] Baxter M. The case of the vanishing patient? Image and experience. Sociol Health Illn 2009;31(5):762-778
[11] Schreier G, et al. Design and Evaluation of a multimodal mHealth based medication management system for patient self administration. Conf Proc IEEE Eng Med Biol Soc 2013:7270-3
[13] Simmons LA, et al. Patient engagement as a risk factor in personalized healthcare: a systematic review of the literature on chronic disease. Genome Med 2014;6:16
[14] Blutzucker messen ohne Pieks; www.ims.fraunhofer.de/news, Meldung vom 3. 9. 2012
[15] Wearable Biosensors; www.mepits.com/tutorial/180/Latest-Technologies/Wearable-Biosensors, 23. 8. 2014
[16] NHS. Personalised Health and Care 2020: Using Data and Technology to Transform Outcomes for Patients and Citizens. November 2014. www.gov.uk/government/publications/personalised-health-and-care-2020
[17] Schneider KM, et al. Prevalence of multiple chronic conditions in the United States’ Medicare population. Health Qual Life Outcomes 2009;7:82





























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.