
- DAZ.online
- DAZ / AZ
- DAZ 28/2014
- Dem Druck standhalten
Arzneimittel und Therapie
Dem Druck standhalten
Mirabegron: Neuer Wirkmechanismus bei überaktiver Blase
Der neue Wirkstoff, der in den USA bereits seit zwei Jahren zugelassen ist, erhöht bei Patienten mit überaktiver Blase die Speicherkapazität bzw. das Füllungsvolumen der Blase mit einhergehender Reduktion der Miktionsfrequenz. Das „Krankheitsbild“ überaktive Blase umfasst die Symptome Pollakisurie (≥ acht Miktionen kleiner Harnmengen pro 24 Stunden), imperativer Harndrang (plötzlicher Harndrang mit Gefahr des unwillkürlichen Harnverlusts) und Nykturie (nächtliches Gewecktwerden durch Harndrang und Blasenentleerung) mit oder ohne Inkontinenz [1]. Da die Abgrenzung zu weiteren urologischen Störungen nicht immer eindeutig ist, wird zur diagnostischen Abklärung einer ÜAB neben weiteren ergänzenden Untersuchungen das Führen eines Miktionstagebuchs über zwei bis fünf Tage empfohlen. Hier werden die Miktionsfrequenz und die Miktionsvolumina objektiv erfasst, zusätzlich können der Schweregrad des imperativen Harndranges, der Leidensdruck, die Anzahl der Inkontinenzepisoden, der Vorlagenverbrauch und die Trinkmenge dokumentiert werden [1].
Therapieoptionen
Bei überaktiver Blase ist eine Stufentherapie indiziert, deren unterste Stufe aus einer Verhaltens- und Physiotherapie besteht [1]. Die Verhaltenstherapie baut auf den individuellen Erkenntnissen des Miktionstagebuchs auf. So sollte im Rahmen eines sogenannten Miktionstrainings versucht werden, die zu kurzen Miktionsintervalle zu verlängern, indem bei Auftreten von Harndrang der Beckenboden angespannt wird („bladder drill“). Ein weiterer verhaltenstherapeutischer Ansatz besteht im sogenannten Toilettentraining. Auf Grundlage der im Miktionstagebuch ersichtlichen Blasenkapazität wird der Entleerungsrhythmus so angepasst, dass bewusst vor- beziehungsweise rechtzeitig die Blase entleert wird, um einem unwillkürlichen Harnverlust zuvorzukommen. Die physiotherapeutischen Maßnahmen bestehen im Wesentlichen aus einem Beckenbodentraining. Dieses kann konservativ oder intensiviert mithilfe von Biofeedback- oder Elektrostimulationsgeräten durchgeführt werden. Zusätzlich beziehungsweise bei persistierenden Störungen trotz Verhaltens- und Physiotherapie wird in einer zweiten Stufe medikamentös behandelt. Mittel der ersten Wahl sind die anticholinerg wirkenden urologischen Spasmolytika Darifenacin, Fesoterodin, Oxybutynin, Propiverin, Solifenacin, Tolterodin oder Trospiumchlorid. Als neue Therapieoption bei Erwachsenen mit überaktiver Blase wurde nun der β3-Adrenozeptoragonist Mirabegron zur symptomatischen Therapie von imperativem Harndrang, erhöhter Miktionsfrequenz und/oder Dranginkontinenz zugelassen. Die Behandlungsoptionen umfassen bei Frauen zusätzlich noch eine lokale Östrogenisierung. Bestehen die Beschwerden trotz Pharmakotherapie weiter, kann eine Blasenwandinfiltration mit Botulinumtoxin A, eine sakrale Neuromodulation (Implantat eines permanenten Neurostimulators) und als Ultima ratio eine Blasenaugmentation (operative Blasenvergrößerung) oder ein Harnblasenersatz in Betracht gezogen werden [1].
Neuer Wirkmechanismus
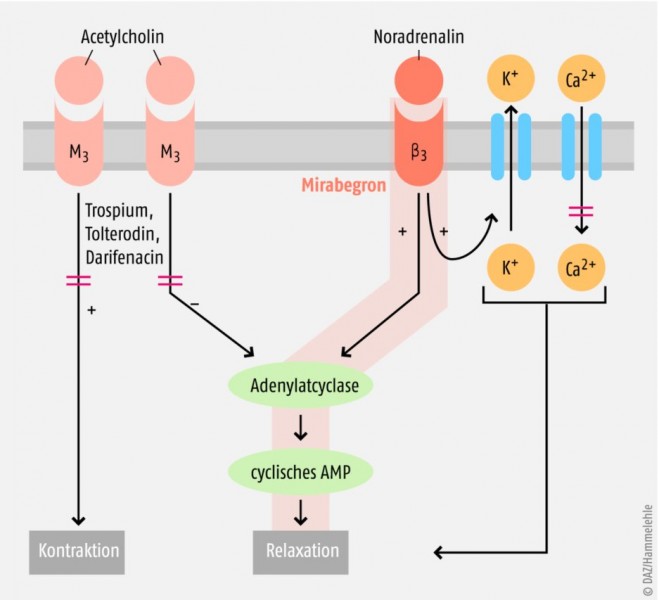
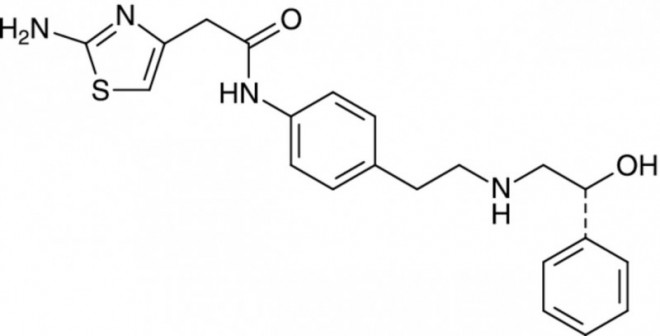
Die Funktionen der Harnblase unterliegen dem vegetativen Nervensystem und damit Sympathikus und Parasympathikus: Die Aktivierung des Sympathikus verhindert in der Harnspeicherphase unwillkürlichen Harnabgang durch Entspannung des Detrusormuskels in der Blasenwand und Kontraktion des inneren Schließmuskels. Die Aktivierung des Parasympathikus verursacht das Gegenteil, es kommt in der Harnentleerungsphase durch Kontraktion des Detrusormuskels und Entspannung des inneren Schließmuskels zur Miktion. Während die bisherigen urologischen Spasmolytika als Antagonisten auf den cholinerg kontrollierten Parasympathikus wirken, indem sie mehr oder minder selektiv Muskarinrezeptoren hemmen und dadurch unwillkürliche Kontraktionen des Detrusors mindern, weist Mirabegron einen ganz neuen Wirkmechanismus durch Angriff auf den adrenerg kontrollierten Sympathikus auf (siehe Abbildung). Der in der Harnblase vorherrschende β3-Adrenozeptor-Subtyp vermittelt bei sympathischer Stimulation die Entspannung der glatten Muskulatur und erhöht somit das Harnspeichervolumen. Mirabegron ist ein Agonist dieses Rezeptors.
In den drei zwölfwöchigen doppelblinden, placebokontrollierten Phase-III-Studien zur Untersuchung der Wirksamkeit konnte Mirabegron die primären Studienendpunkte Anzahl Inkontinenzereignisse und Miktionshäufigkeit pro 24 Stunden statistisch signifikant senken (p < 0,05) [5]. Unter 50 mg Mirabegron konnte die Anzahl der Miktionen pro 24 Stunden bei einem Ausgangswert von 11,70 um den Wert 1,75 gesenkt werden (Placebo –1,20). Die Anzahl der Inkontinenzepisoden je 24 Stunden konnte bei einem Ausgangswert von 2,71 um 1,49 gesenkt werden (Placebo -1,10). Es zeigten sich bereits nach vier Wochen Behandlungsdauer statistisch signifikante Unterschiede in den genannten Endpunkten. Von besonderem Interesse war auch der Anteil der Patienten, die unter der Behandlung keine nächtlichen Inkontinenzepisoden mehr zu beklagen hatten. Dies war bei 44,1% der mit 50 mg Mirabegron behandelten Patienten und bei 37,8% der mit Placebo behandelten Patienten der Fall. Zudem wurde die Wirksamkeit bei Patienten mit früherer Antimuskarinika-Therapie der ÜAB nachgewiesen. Hier konnte gezeigt werden, dass Patienten, die auf eine frühere antimuskarinerge Therapie nicht ausreichend angesprochen haben bzw. diese aufgrund von Nebenwirkungen abbrechen mussten, mit Mirabegron erfolgreich behandelt werden konnten. In einer Langzeitstudie mit zwölf Monaten Anwendungsdauer konnte zudem der Nachweis erbracht werden, dass die Wirksamkeit von Mirabegron über diesen Zeitraum anhielt.
Dosierung
Mirabegron wird einmal täglich, zu oder unabhängig von den Mahlzeiten eingenommen. Die Retardtablette darf weder zerkaut, zerteilt noch zerstoßen werden, um das Freisetzungsverhalten nicht negativ zu beeinflussen. Die empfohlene Tagesdosis beträgt 50 mg. Da Mirabegron renal und hepatisch eliminiert wird und seine Plasmaspiegel bei gleichzeitiger Gabe starker CYP3A-Inhibitoren wie Ketoconazol oder Makrolidantibiotika steigen, muss es bei einer Funktionseinschränkung der Eliminationsorgane und/oder bei gleichzeitiger Einnahme starker CYP3A-Inhibitoren in seiner Dosierung reduziert werden (siehe Tabelle). Bei stark eingeschränkter Nierenfunktion oder bei mäßig eingeschränkter Leberfunktion muss die Dosis um die Hälfte, auf 25 mg, reduziert werden. Werden bei diesen Funktionseinschränkungen gleichzeitig noch starke CYP3A-Inhibitoren eingenommen, wird die Anwendung von Mirabegron nicht mehr empfohlen (siehe Tabelle). Für die unterschiedlichen Szenarien steht BetmigaTM in den Einzeldosisstärken 25 und 50 mg zur Verfügung. Die Anwendung bei Patienten mit terminaler Niereninsuffizienz (GFR < 15 ml/min/1,73 m2 oder Dialysepflicht) oder stark eingeschränkter Leberfunktion wurde nicht untersucht und wird daher nicht empfohlen. Bei älteren Patienten ist keine Dosisanpassung erforderlich.
Steckbrief
Handelsname: Betmiga
Hersteller: Astellas GmbH, München
Einführungsdatum: 1. Juni 2014
Zusammensetzung: jede Retardtablette enthält 25 mg bzw. 50 mg Mirabegron
Stoffklasse: Urologika, urologische Spasmolytika, ATC-Code: G04BD12
Indikation: symptomatische Therapie von imperativem Harndrang, erhöhter Miktionsfrequenz und/oder Dranginkontinenz, die bei Erwachsenen mit überaktiver Blase auftreten können
Dosierung: die empfohlene Dosis beträgt 50 mg einmal täglich mit oder ohne Nahrung
Gegenanzeigen: Überempfindlichkeit gegen den Wirkstoff oder einen der sonstigen Bestandteile
Nebenwirkungen: häufig: Harnwegsinfektion, Tachykardie; gelegentlich: Scheideninfektion, Zystitis, Palpitation, Vorhofflimmern, Dyspepsie, Gastritis, Urtikaria, makulöser und papulöser Ausschlag, Pruritus, Gelenkschwellung, vulvovaginaler Pruritus, Blutdruck erhöht, GGT erhöht, AST erhöht, ALT erhöht; selten: Augenlidödem, Lippenödem, leukozytoklastische Vaskulitis, Purpura
Wechselwirkungen: Mirabegron ist ein Substrat von CYP3A4, CYP2D6, Butyrylcholinesterase, Uridin-Diphospho-Glucuronosyltransferasen (UGT), Efflux-Transporter P-Glykoprotein (P-gp) und Influx-Transporter für organische Kationen. Studien zeigten, dass Mirabegron ein mäßiger und zeitabhängiger Inhibitor von CYP2D6 und ein schwacher Inhibitor von CYP3A ist. Mirabegron hemmte in hohen Konzentrationen den über P-gp-vermittelten Arzneimittel-Transport. Wechselwirkungen zwischen Mirabegron und bekannten CYP2D6-Inhibitoren werden nicht erwartet und wurden nicht untersucht. Bei gemeinsamer Anwendung mit CYP2D6-Inhibitoren oder bei Gabe an langsame CYP2D6-Metabolisierer, ist keine Dosisanpassung erforderlich. Bei Kombination mit Inhibitoren von CYP3A und/ oder P-gp ist keine Dosisanpassung erforderlich.
Warnhinweise und Vorsichtsmaßnahmen: Mirabegron wird bei Patienten mit starker Einschränkung der Nierenfunktion (GFR 15 bis 29 ml/min/ 1,73 m2) oder dialysepflichtigen Patienten oder solchen mit mäßiger Einschränkung der Leberfunktion (Child-Pugh-Klasse B), die gleichzeitig starke CYP3A-Inhibitoren erhalten, nicht empfohlen. Die Anwendung bei Patienten mit schwerer, nicht behandelter Hypertonie (systolischer Blutdruck ≥ 180 mmHg und/oder diastolischer Blutdruck ≥ 110 mmHg) wird nicht empfohlen.
Keine anticholinergen Nebenwirkungen
Es ist bekannt, dass für die bisherigen urologischen Spasmolytika eine enge Wirkung-Nebenwirkung-Korrelation besteht und Patienten oft über nicht tolerable anticholinerge Nebenwirkungen wie Mundtrockenheit, Obstipation, Harnverhalt, Tachykardie und Erhöhung des Augeninnendrucks mit Gefahr eines Glaukomanfalls klagen. Aufgrund dieser Nebenwirkungen und zusätzlichen kognitiven Beeinträchtigungen werden die urologischen Spasmolytika Oxybutynin, Tolterodin und Solifenacin in der PRISCUS-Liste als potenziell altersinadäquate Medikation angesehen. Dies ist von großer praktischer Bedeutung, da die Prävalenz des Krankheitsbilds ÜAB in der Gruppe der älteren Patienten am höchsten ist, auch wenn sie in allen Altersgruppen auftritt. Schätzungen zufolge sind ungefähr 30% aller Personen über 65 Jahre betroffen. Da Mirabegron durch seinen neuartigen Wirkmechanismus keinen Einfluss auf das muskarinerge System ausübt und folglich keine anticholinergen Nebenwirkungen aufweist, empfiehlt es sich besonders für den Einsatz bei älteren Patienten und solchen, die aufgrund von nicht tolerablen Nebenwirkungen eine Therapie mit Anticholinergika abgebrochen haben oder nicht therapietreu sind. Eine weitere Zielgruppe werden auch demente Patienten sein, da Mirabegron im Gegensatz zu den meisten Anticholinergika keine negativen Auswirkungen auf die Kognition hat [3].
Nebenwirkungen
Die meisten Nebenwirkungen von Mirabegron waren in den drei Phase-III-Studien leicht bis mäßig ausgeprägt, und aufgrund unerwünschter Ereignisse brachen insgesamt ca. 4% der Teilnehmer die Studie ab. 7,5% der Patienten entwickelten unter 50 mg Mirabegron einen Bluthochdruck beziehungsweise eine Verschlechterung ihrer Hypertonie (Inzidenz vergleichbar mit der Placebogruppe), 3,9% eine Nasopharyngitis, 3,4% Kopfschmerzen, und 2,9% erlitten Harnwegsinfekte. Tachykarde Ereignisse wurden bei 3,8% der Patienten beobachtet. Die Wirkung von Mirabegron auf einen gesteigerten Blutdruck und eine erhöhte Herzfrequenz lässt sich dadurch erklären, dass β3-Adrenozeptoren nicht nur auf der glatten Harnblasenmuskulatur vorhanden sind, sondern auch am Herzen. Bei Patienten mit schwerer, nicht behandelter Hypertonie (systolischer Blutdruck ≥ 180 mmHg und/oder diastolischer Blutdruck ≥ 110 mmHg) wird Mirabegron deshalb nicht empfohlen. Es empfiehlt sich, den Blutdruck in der Einleitungsphase von Mirabegron und danach in regelmäßigen Abständen zu kontrollieren.
Fazit
Für Patienten mit überaktiver Blase steht mit Mirabegron nun ein weiterer Wirkstoff zur Linderung des belastenden Krankheitsbildes zur Verfügung. Im Vergleich zu den lang erprobten Anticholinergika, bis dato Mittel der ersten Wahl bei ÜAB, verfügt Mirabegron über ein gefälligeres Nebenwirkungsprofil und bietet sich insbesondere bei älteren und dementen Patienten an. Bei hypertensiven Patienten muss der Einfluss von Mirabegron auf den Blutdruck beobachtet werden.
Quelle
[1] Die überaktive Blase (ÜAB). S2k-Leitlinie, Deutsche Gesellschaft für Gynäkologie und Geburtshilfe e.V., Stand Juni 2010. www.awmf.org (letzter Zugriff am 24. Juni 2014)
[2] Fachinformation BetmigaTM, Stand: Januar 2014
[3] Bridgeman MB et al. Mirabegron: β3-Adrenergic Receptor Agonist for the Treatment of Overactive Bladder. Ann Pharmacother 2013;47:1029‒1038
[4] Wirkstoff Aktuell. Urologische Spasmolytika, Anticholinergika. KBV und AkdÄ. Stand 12. Juli 2013. www.akdae.de (letzter Zugriff am 24. Juni 2014)
[5] Nitti VW et al. Mirabegron for the treatment of overactive bladder: a prespecified pooled efficacy analysis and pooled safety analysis of three randomised, placebo-controlled, phase III studies. Int J Clin Pract 2013;67(7):619–632.




















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.