
- DAZ.online
- DAZ / AZ
- DAZ 16/2013
- Harter Kampf gegen ...
Immunologie
Harter Kampf gegen resistente Staphylokokken
Falls Sie sich beim letzten Krankenhausaufenthalt gewundert haben, dass ein Abstrich von Ihrer Nase genommen wurde: Dort sitzt gern dieses kugelförmige, grampositive Bakterium, das oft ganz harmlos ist, aber gelegentlich auch leichtere oder schwerere Hautentzündungen und im Extremfall lebensbedrohliche Erkrankungen wie Lungenentzündung, Endokarditis oder Sepsis verursachen kann. Ungefähr 30% aller Menschen, egal welcher ethnischen Zugehörigkeit, sind Träger dieses Bakteriums, und das meist ohne irgendwelche Probleme. Neben den eher harmlosen Varianten existieren jedoch auch Bakterien, die mit dem Kürzel "MRSA" – Methicillin-resistenter Staphylococcus aureus – bezeichnet werden; sie führen zu gefürchteten Infektionen bei stationär behandelten Patienten, die mit Antibiotika kaum noch beherrschbar sind.
Das war nicht immer so. Die berühmte Petrischale von Alexander Fleming, die zur Entdeckung des Penicillins führte, war angelegt, um Staphylococcus aureus genauer zu untersuchen [1]. Zufälligerweise war aber noch eine Pilzspore aus der Luft auf die geöffnete Kulturschale gefallen, die sich zu einem Myzel weiterentwickelte, dessen "ausgedünstetes Sekret" das Staphylokokken-Wachstum verhinderte. Damals, 1928, war das Bakterium also noch sensitiv gegen das Antibiotikum, aber bereits 1944 wurde ein Stamm isoliert, dem Penicillin nichts mehr anhaben konnte. 15 Jahre später war Methicillin das Mittel der Wahl gegen S. aureus, doch schon nach zwei Jahren war auch diese Waffe stumpf. Sobald ein neues Antibiotikum gegen das Bakterium eingesetzt wurde, wurden kurze Zeit später resistente Stämme entdeckt – ein schier hoffnungsloser Kampf gegen dieses ubiquitär vorkommende, sehr gut an den menschlichen Wirt angepasste und extrem wandlungsfähige Bakterium.
In Deutschland schätzt man jährlich ca. 140.000 MRSA-Fälle, die in Krankenhäusern und Altenheimen auftreten und als "Healthcare-associated" (HA) MRSA bezeichnet werden [2]. Der Anteil der MRSA-Stämme an allen S.-aureus -Isolaten von stationären Patienten liegt in den letzten Jahren relativ konstant bei ca. 20%.
Von den statistisch recht gut erfassten HA-MRSA-Fällen sind die in der Allgemeinbevölkerung auftretenden "Community-associated" (CA) MRSA und die bei landwirtschaftlichen Nutztieren anzutreffenden "Livestock-associated" (LA) MRSA zu unterscheiden, deren Inzidenzen nur schwer zu schätzen sind. Wahrscheinlich sind 1 bis 2% der Personen mit Hautinfektionen von CA-MRSA betroffen; ca. 30% der gehaltenen Rinder und 70% der Schweine haben LA-MRSA, und folglich haben auch bis zu 86% der Landwirte LA-MRSA [2].
"Thema mit Variation"
S. aureus hat ein zirkuläres Genom von knapp drei Millionen Basenpaaren. 2001 wurden erstmals die kompletten Sequenzen eines Methicillin- und eines Vancomycin-resistenten Stamms veröffentlicht, wodurch etwas Klarheit in die Pathomechanismen der Bakterien kam [3]. 75% der Gene gehören zur Grundausstattung und sind in allen Staphylococcus -Arten zu finden. Die restlichen 25% sind dagegen hoch variabel und unterscheiden sich von Stamm zu Stamm. Unter den variablen Sequenzen befinden sich mobile, zwischen unterschiedlichen Stämmen austauschbare Elemente wie sogenannte Pathogenitätsinseln, inserierte Bakteriophagen-DNA (Prophagen), Staphylokokken-Cassetten-Chromosomen (SCC), genetische Inseln und Plasmide [1]. Der Austausch dieses genetischen Materials kann allerdings nicht nur unter Staphylokokken stattfinden, sondern auch zwischen Staphylokokken und Bakterien anderer Gattungen wie z. B. Enterokokken. Dadurch erhöht sich die Variabilität enorm, und die verschiedenen Stämme weisen meist sehr unterschiedliche Virulenz- und Resistenzmuster auf.
Drei Gruppen von Virulenzfaktoren
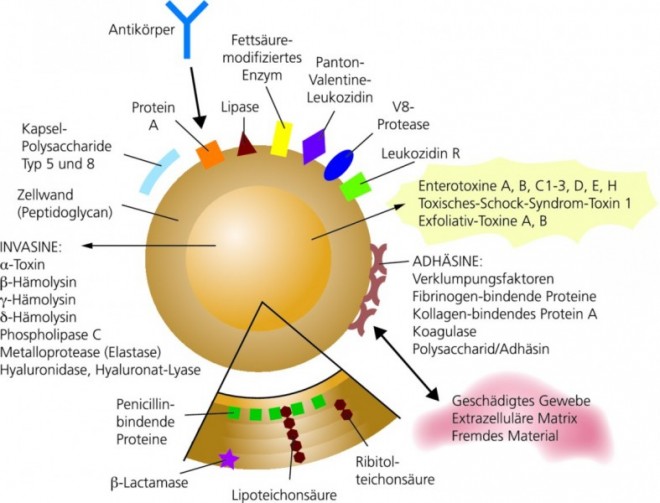
Die Virulenzfaktoren von S. aureus lassen sich in drei Gruppen einteilen (Abb. 1):
- bakterielle Strukturmoleküle,
- sezernierte bakterielle Moleküle und
- bakterielle Enzyme.
Zu den Strukturmolekülen zählt neben der Zellwand mit den integrierten Oberflächenadhäsionsproteinen auch die Polysaccharid-Kapsel, die die Bakterien vor Phagozytose schützt. Die Oberflächenadhäsionsproteine (microbial surface components recognizing adhesive matrix molecules, MSCRAMMs) dienen der Verankerung des Mikroorganismus in der extrazellulären Matrix des Besiedelungsgewebes im / am Wirt. Zu diesen MSCRAMMs gehören unter anderem Verklumpungsfaktoren, Protein A, aber auch verschiedene Proteine, die beispielsweise Fibronectin, Elastin, Kollagen oder Knochen-Sialoprotein binden können [1].
Neben den Adhäsionsmolekülen, die in der Zellwand verankert sind, sezernieren Staphylokokken weitere Adhäsionsmoleküle, die als SERAM (secretable expanded repertoire adhesive molecules) bezeichnet werden. Der Cocktail der sezernierten Proteine ist meist außerdem noch um Exotoxine und Superantigene erweitert, die die Zellen des Wirtsorganismus schädigen bzw. eine überschießende Immunantwort im Wirt induzieren.
Ein wichtiger Virulenzfaktor, der sowohl zur Zellwand als auch zu den sezernierten Molekülen zählt, ist eine Matrix aus Polysacchariden und Proteinen, die als Biofilm bezeichnet wird und von bestimmten Bakterien gebildet wird, wenn sie eine Oberfläche besiedeln. Dieser Biofilm bettet verschiedene Bakterienzellen ein und bietet einen Schutz sowohl vor Antibiotika als auch vor Abwehrmechanismen des Wirts.
Fasst man die Variabilität zusammen, können Staphylokokken verschiedenste Lebensräume im und am Menschen (bzw. Tier) besiedeln, da sie sowohl aerob als auch anaerob leben können. Sie können Biofilme entwickeln oder eine Polysaccharidkapsel ausbilden. Und sie variieren in der Zusammensetzung der verschiedenen Virulenzfaktoren und Resistenzen gegenüber unterschiedlichen Antibiotika.
Impfstoff statt Antibiotikum?
Wenn kein Antibiotikum mehr greift und die antibiotische Wirkstoff-Pipeline eher leer ist, wäre eine clevere Alternative, von vornherein die Infektion zu verhindern. Ähnliche Resistenzprobleme und einen Impfansatz als erfolgreiches Lösungskonzept hat es bereits mit Haemophilus influenzae Typ b oder Streptococcus pneumoniae gegeben, gegen die mittlerweile standardmäßig geimpft wird [4]. Allerdings ist ein derartig wandlungsfähiges Bakterium wie S. aureus ein schwieriges Ziel, um mit einem bestimmten Antigen einen möglichst umfassenden Impfschutz gegen die verschiedenen Infektionsmöglichkeiten zu erreichen.
In Analogie zu den Kapsel-Polysacchariden von H. influenzae, S. pneumoniae oder Neisseria meningitidis wurden auch von S. aureus zwei Kapsel-Polysaccharide in Form von Protein-Konjugat-Impfstoffen getestet. Allerdings waren die bisher durchgeführten Studien erfolglos. Ein anderes getestetes Kohlenhydrat-Antigen, das Poly-N-Acetylglucosamin (PNAG), ist an der Ausbildung des Biofilms beteiligt und kommt in acetylierter und deacetylierter Form vor, wobei erste Untersuchungen die deacetylierte Variante als erfolgversprechender einstuften. Auch Verklumpungsfaktoren, das Enterotoxin B und verschiedene andere Proteine wurden bereits als potenzielle Antigene untersucht. Als ein vielversprechendes Antigen wurde dabei ein Eisen-Oberflächenprotein (iron surface determinant B, IsdB) identifiziert, das nach den ersten positiven Ergebnissen unter der Bezeichnung V710 in einer großen Phase-II/III-Studie genauer getestet wurde.
Die Phase-II/III-Studie
Insgesamt 7983 Studienteilnehmer an 165 Orten in 26 Ländern erhielten entweder den Impfstoff (einmal 60 µg V710; n = 3981) oder ein Placebo [5, 6]. Alle Patienten standen kurz vor einer größeren Herz-Operation. Endpunkt der Studie war die Vermeidung von Staphylokokken-Infektionen innerhalb von zwölf Monaten nach der Operation.
Erstaunlicherweise war in der Verumgruppe die Anzahl der Todesfälle infolge einer S.-aureus -Infektion signifikant höher als in der Placebogruppe (15 vs. 4), obwohl in den Geimpften ein für eine Immunisierung (scheinbar) ausreichend hoher Antikörpertiter induziert worden war. Zudem erlitten mehr Patienten in der Verumgruppe ein Multiorganversagen oder eine MRSA-Infektion als in der Placebogruppe. Offensichtlich brachte der Impfstoff nicht nur keinen Schutz, sondern sogar ein höheres Risiko, an einer Staphylokokken-Infektion zu erkranken.
Was könnte das Problem sein?
Sicherlich ist die extreme Wandlungsfähigkeit des Bakteriums ein großes Problem bei einer Impfstoffentwicklung. Hier könnte ein Multi-Komponenten-Impfstoff erfolgversprechender sein, der aus verschiedenen S.-aureus -Molekülen zusammengesetzt wird. Eine Schwierigkeit liegt aber wahrscheinlich in einem sehr konserviert vorkommenden Oberflächenprotein von S. aureus, dem Protein A (Abb. 1).
Protein A ist in biochemischen Labors bestens bekannt als das Mittel der Wahl, um sehr selektiv Antikörpermoleküle aus einer Proteinmischung aufzureinigen. Dabei bindet Protein A sehr spezifisch an den konstanten Fc-Teil des Antikörpers, der im menschlichen Körper normalerweise eigentlich mit Rezeptoren auf Makrophagen oder Natürlichen Killerzellen interagiert, um das gebundene Antigen durch das Immunsystem zu eliminieren. Wird nun durch die Impfung mit IsdB-Antigen die Bildung schützender Antikörper induziert, könnte es sein, dass bei einer Infektion mit S. aureus genau diese Antikörper von Protein A auf der Bakterienoberfläche gebunden werden. Dann wären die Antikörper nicht mehr in der Lage, das Immunsystem zu stimulieren, dass es die Bakterien eliminiert. Man könnte sich sogar vorstellen, dass ein an Protein A gebundener Antikörper über seine beiden Antigen-bindenden Domänen an das Eisen-Oberflächenprotein IsdB anderer Bakterien bindet und dass auf diese Weise quasi Bakterienklumpen entstehen, die dann zu größeren Problemen im Körper führen.
Es ist ernüchternd, dass diese große Studie erfolglos war. Allerdings hat sie wieder einen Baustein zum besseren Verständnis einer Staphylokokken-Infektion geliefert. Wahrscheinlich müssen andere Impfstrategien entwickelt werden, die weniger die Bildung von Antikörpern als vielmehr eine zelluläre Immunantwort induzieren. Mit NDV-3, der N‑terminalen Region eines Agglutinin-ähnlichen Proteins auf der Oberfläche des Bakteriums, wird inzwischen ein neues Antigen getestet, das – zumindest in Mäusen – eine schützende T-Helferzellantwort induziert hat [4]. Wie das Antigen das menschliche Immunsystem stimuliert, müssen klinische Studien zeigen, die jetzt anlaufen.
Staphylococcus aureus ist ein schwer zu bekämpfender Feind, der in den USA bereits massive Probleme bereitet. In Deutschland ist die Situation (noch) nicht ganz so schlimm. So bleibt zu hoffen, dass wir bald entweder noch ausreichend wirksame Antibiotika oder aber geeignete Impfstoffe zur Verfügung haben.
Literatur [1] Fry DE, Barie PS. The Changing Face of Staphylococcus aureus: A Continuing Surgical Challenge. Surgical Infections 2011; 12: 191 – 203. [2] Köck R, et al. Methicillin-resistenter Staphylococcus aureus in Deutschland. Dtsch Arztebl 2011; 108: 761 – 767. [3] Kuroda M, et al. Whole genome sequencing of meticillin-resistant Staphylococcus aureus. Lancet 2001; 357: 1225 – 1240. [4] Daum RS, Spellberg B. Progress Toward a Staphylococcus aureus Vaccine. Vaccines 2012; 54: 560 – 567. [5] Fowler VG, et al. Effect of an Investigational Vaccine for Preventing Staphylococcus aureus Infections After Cardiothoracic Surgery. J Am Med Assoc 2013; 309: 1368 – 1378. [6] Malani PN. Preventing Postoperative Staphylococcus aureus Infections. J Am Med Assoc 2013; 309: 1408 – 1409.
Autoren |
Prof. Dr. Theo Dingermann ist Professor am Institut für Pharmazeutische Biologie an der Goethe-Universität Frankfurt.
Dr. Ilse Zündorf ist dort als akademische Oberrätin tätig.
Prof. Dr. Theo Dingermann,
Dr. Ilse Zündorf
Institut für Pharmazeutische Biologie
Biozentrum
Max-von-Laue-Straße 9
60438 Frankfurt/Main























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.