
- DAZ.online
- DAZ / AZ
- DAZ 31/2012
- Orphan drug Glybera
Gentherapie
Orphan drug Glybera®

Bereits seit dem 8. März 2004 besitzt Glybera® den Status als Orphan Drug, denn es sollte zur Behandlung einer sehr seltenen Lipoprotein-Lipase-Defizienz entwickelt werden. Das allein wäre kaum einer etwas ausführlicheren Erwähnung wert, handelte es sich bei Glybera® nicht um ein ausgesprochen ausgefallenes Präparat.
Glybera® ist ein Gentherapeutikum, das in Form einer Enzymersatztherapie bei Patienten mit einer Lipoprotein-Lipase-Defizienz eingesetzt werden soll. Betroffen sind nur 1 bis 2 Personen unter 1 Million Menschen. Bei diesen führt der Enzymmangel dazu, dass Triglyceride in Lipoproteinpartikeln nicht mehr zu Fettsäuren und Glycerin abgebaut werden können, um dann in der Leber und in peripheren Zielzellen weiter verstoffwechselt zu werden. Eine schwerwiegende Folge kann eine akute Pankreatitis sein, die wiederum eine erhöhte Mortalität der betroffenen Patienten bedingt. Um diesen Enzymdefekt zu korrigieren, wurde der Gentherapievektor AAV1-LPLS447X entwickelt.
Seit dem 20. Juli 2012 ist endlich der Durchbruch für die Gentherapie geschafft: Die Europäische Zulassungsbehörde EMA erteilte die Zulassung für Alipogen tiparvovec (Glybera®). Und das, nachdem eigentlich die Zulassung schon endgültig versagt worden war.
Der steinige Weg zur Zulassung
Vor gut einem Jahr, am 23. Juni 2011, hatte sich das zuständige Committee for Medicinal Products for Human Use (CHMP) bereits gegen das Produkt entschieden. Damit wollte sich allerdings der Hersteller, Amsterdam Molecular Therapeutics (AMT), nicht abfinden und beantragte eine Nachuntersuchung des Antrags. Aber auch diese führte im Oktober 2011 wieder zu einer Ablehnung. Schließlich schaltete sich im Januar 2012 die Europäische Kommission ein und forderte eine Überprüfung des Wirkstoffs bei einer definierten Patientengruppe mit schweren oder wiederholten Pankreatitis-Episoden. Nachdem aber nur Daten aus klinischen Studien an zwölf Patienten verfügbar waren, verweigerte das CHMP im April 2012 erneut die Zulassung. Dies war eine äußert umstrittene Entscheidung, denn eine Mehrheit der CHMP-Mitglieder hatte sich für eine Zulassung ausgesprochen. Allerdings reichte die Mehrheit von 16 zu 15 Stimmen nicht aus, da die Regularien des CHMPs für ein positives Votum mindestens 17 Stimmen vorschreiben. Lag es also tatsächlich am Fehlen eines der 32 CHMP-Experten, dass dieses innovative Medikament ein weiteres Mal scheitern sollte? Das zog auch heftige Reaktionen verschiedener Organisationen, darunter die Genetic Alliance UK, nach sich, deren Direktor Alastair Kent sich bei Paola Testori Coggi, der Leiterin der Generaldirektion Gesundheit und Verbraucher der Europäischen Kommission, heftigst beschwerte*.
* www.geneticalliance.org.uk/docs/policy/letter-re-glybera-25april2012.pdfSo kam es zu einer weiteren Überprüfung der Daten, die dann zeigte, dass die wenigen Studienteilnehmer tatsächlich von der Medikation zu profitieren schienen, was sich in einer Verringerung der Häufigkeit von Pankreatitis-Episoden äußerte. Insgesamt schienen die Vorteile die Behandlungsrisiken dann doch wohl zu überwiegen, sodass Glybera® seit dem 20. Juli „unter besonderen Umständen“ zugelassen ist. Eine Zulassung „unter besonderen Umständen“ bedeutet, dass der Hersteller alle Daten von behandelten Patienten sammeln und der Zulassungsbehörde vorlegen muss. Anhand dieser Daten wird dann immer wieder geprüft, ob die Zulassungsvoraussetzungen weiterhin bestehen.
Das Hin und Her im Laufe des Zulassungsverfahrens für Glybera® führte dazu, dass der Hersteller AMT Insolvenz anmelden musste. Das Medikament wird nun von der ebenfalls in Amsterdam ansässigen Firma UniQure weiterentwickelt.
Adeno-assoziierter viraler Gentherapie-Vektor
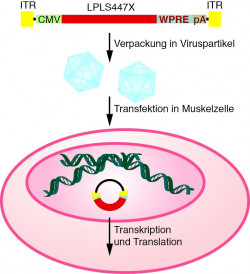
Bei Alipogen tiparvovec handelt es sich um den Adeno-assoziierten viralen Vektor AAV1-LPLS447X. Adeno-assoziierte Viren (AAV) gehören zur Familie der Parvoviridae, die kleine Viren ohne Hüllmembran umfasst und von denen bisher 14 verschiedene Serotypen bekannt sind. Die Viren haben ein einzelsträngiges DNA-Genom und treten beim Menschen häufig auf. Charakteristisch für das AAV-Genom sind u. a. die umgekehrten terminalen Wiederholungseinheiten (inverted terminal repeats, ITR) an den Enden. Dazwischen liegen im Wild-Typ-AAV zwei offene Leserahmen, rep und cap, die in dem Gentherapievektor AAV1-LPLS447X durch das Gen für die Lipoprotein-Lipase (LPL) ersetzt wurden. Für die Transkription des LPL-Gens sorgt der Promotor des Cytomegalievirus (CMV). Außerdem sind ein Element (WPRE) für die posttranskriptionelle Kontrolle und ein Polyadenylierungssignal (pA) enthalten (Abb. 5).
Alipogen tiparvovec trägt die ITRs eines AAV-Serotyps 2. Allerdings ist die DNA in ein Kapsid des Serotyps 1 verpackt. Von diesem Serotyp ist bekannt, dass er Muskelzellen besonders gut infiziert.
AAV1-LPLS447X ist als sterile Lösung mit 3 × 1012 genomischen Kopien (gc) pro ml Phosphatpuffer mit 5% Saccharose formuliert und wird unter spinaler Anästhesie an mehreren Stellen der unteren Extremitäten in einer Dosierung von 1012 gc/kg Körpergewicht intramuskulär verabreicht. Die Vektor-DNA integriert nicht in die chromosomale DNA der Muskelzelle, sondern persistiert episomal im Zellkern und wird über lange Zeit transkribiert und translatiert. Die S447X-Variante der Lipoprotein-Lipase, die von dem Gentherapievektor codiert wird, ist am C-Terminus um zwei Aminosäuren kürzer als die Wildtyp-LPL.
Zugelassen ist der Gentherapievektor bei Patienten, die trotz entsprechender fettarmer Diät unter schwerer Pankreatitis leiden.
Da Adeno-assoziierte Viren weit verbreitet sind, besteht die Gefahr, dass das Immunsystem der Patienten auf die Vektorgabe reagiert. Diese Gefahr hatte man 1999 noch folgenschwer unterschätzt. Damals hatte man den 18-jährigen Jesse Gelsinger in einem ähnlichen Ansatz, jedoch mit Adenoviren, behandelt. Gelsinger verstarb danach an immunologischen Komplikationen, was der Entwicklung der Gentherapie einen empfindlichen Rückschlag versetzte. Um die Gefahr immunologischer Komplikationen bestmöglich zu umgehen, wird die Therapie mit Alipogen tiparvovec von einer immunsuppressiven Therapie mit 3 mg/kg/d Ciclosporin und 2 g/d Mycophenolatmofetil begleitet, die mit der Vektor-Applikation begonnen und für drei Monate fortgesetzt wird. Mittlerweile liegen die Daten eines zweijährigen Follow-up vor, die zeigen, dass die Therapie sicher und wohl auch wirksam ist. Zwar scheinen die Triglycerid-Werte im Laufe der Zeit wieder anzusteigen. Allerdings blieben bisher die Pankreatitis-Episoden auf niedrigem Niveau, und die Lebensqualität der Patienten ist signifikant gestiegen.
Literatur Gaudet D, Méthot J, Kastelein J. Gene therapy for lipoprotein lipase deficiency. Curr Opin Lipidol 23 (2012), 310 – 320.
Autoren Prof. Dr. Theo Dingermann, Dr. Ilse Zündorf, Institut für Pharmazeutische Biologie, Max-von-Laue-Str. 9, 60438 Frankfurt




















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.