
- DAZ.online
- DAZ / AZ
- DAZ 31/2012
- Neues Zytostatikum ...
Arzneimittel und Therapie
Neues Zytostatikum Pixantron
Pixantron wurde unter „Besonderen Bedingungen“ zugelassen. Das bedeutet, dass der Hersteller Cell Therapeutics Pixuvri® zunächst nur befristet auf den europäischen Markt bringen darf. Die bedingte Zulassung ist jährlich befristet und gilt als vorläufig, bis die Firma weitere Nachweise für den Nutzen des Arzneimittels liefert. Zunächst sollen nur Teilnehmer eines sogenannten „Named-Patient-Programms“ das Arzneimittel bekommen. Dabei erhalten die Patienten das Mittel auf individuelle Anforderung durch den Arzt. Cell Therapeutics wird sein Produkt über ein eigenes Vertriebssystem vermarkten, also voraussichtlich nicht über die Apotheken.
Hemmt Neubildung von Blutzellen
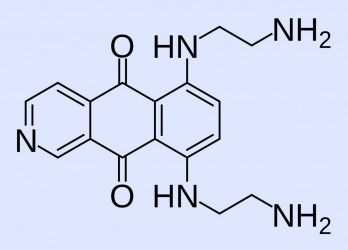
In der chemischen Struktur ähnelt Pixantron den Anthracendion Mitoxantron. Pixantron wirkt als Topoisomerase-Hemmer. Im Gegensatz zu Anthracyclinen wie Doxorubicin und anderen Anthracendionen ist Pixantron nur ein schwacher Inhibitor der Topoisomerase II. Es alkyliert außerdem direkt die DNA, bildet stabile DNA-Addukte und führt zu Doppelstrangbrüchen.
Pixantron unterdrückt das Immunsystem, indem es T-, B- und Fresszellen abtötet. Es ist zur Behandlung von Lymphomen wirksam. Außerdem kann es Entzündungsreaktionen bei der multiplen Sklerose verhindern. Zur Behandlung dieser Autoimmunerkrankung befindet es sich derzeit in dieser Indikation in Phase I und II der klinischen Entwicklung.
Dosis muss angepasst werden
Pixuvri® enthält ein Pulver zur Zubereitung einer Infusionslösung. Die Dosierung wird nach der Körperfläche unter Berücksichtung der Blutwerte des Patienten berechnet und beträgt 50 mg/m2 Körperoberfläche Pixantronbase an Tag 1, 8 und 15 von bis zu sechs 28-Tage-Zyklen.
Diese Dosis muss zu Beginn eines jeden Zyklus auf der Grundlage des Nadirs der hämatologischen Werte oder der stärksten toxischen Wirkungen des vorhergehenden Therapiezyklus angepasst werden.
Bedingte Zulassung
Grundlage der bedingten Zulassung war die multizentrische, randomisierte, aktiv kontrollierte PIX301-Studie, in der Pixantron zur Monotherapie von Non-Hodgkin-B-Zell-Lymphomen (NHL) bei 140 Patienten mit rezidiviertem oder refraktärem aggressivem Non-Hodgkin-B-Zell-Lymphomen nach mindestens zwei vorherigen Therapien bewertet wurde. Sie erhielten entweder Pixantron oder eine Einzelwirkstoff-Chemotherapie im Vergleichsarm. Das mediane Gesamtalter der Patienten betrug 59 Jahre, 76% der Patienten hatten bei Studienbeginn eine Erkrankung in einem fortgeschrittenen Stadium (III/IV nach Ann Arbor). In dieser Studie zeigten mit Pixantron behandelte Patienten signifikant höhere Ansprechraten als die Patienten der Vergleichsgruppe. 20% der Patienten erreichten eine komplette Remission im Vergleich zu 6% unter einer anderen Chemotherapie. Das Überleben verlängerte sich von 7,6 auf 10,2 Monate.
Unerwünschte Wirkungen: Neutropenie
Da Pixantron die Neubildung von Blutzellen behindert (Myelosuppression), kommt es als unerwünschte Wirkung vor allem zu einer Neutropenie, aber auch zu einer Leukopenie, Anämie, Thrombozytopenie und Lymphopenie. Bei Einhaltung der empfohlenen Dosis und des empfohlenen Dosisschemas ist die Neutropenie in der Regel reversibel. Engmaschige Blutbildkontrollen sind erforderlich; bei einem zu starken Abfall dieser Werte kann die Dosis angepasst werden; auch können rekombinante hämatopoetische Wachstumsfaktoren angewendet werden.
Während der klinischen Studien kam es zu Infektionen, Patienten mit Neutropenie waren besonders anfällig. Pixantron darf nicht angewendet werden bei Patienten mit aktiven, schweren Infektionen und bei Patienten mit anamnestisch bekannten rezidivierenden oder chronischen Infektionen oder mit Grunderkrankungen, die eine schwere Infektion zusätzlich begünstigen könnten. Eine während der Behandlung mit Pixantron vorgenommene Immunisierung bleibt möglicherweise wirkungslos. Impfungen mit Lebendviren sind wegen der therapieassoziierten Immunsuppression kontraindiziert.
Kardiotoxische Wirkungen
Pixantron kann das Herz schädigen. Ein erhöhtes Risiko besteht bei einer aktiven oder latenten Herz-Kreislauf-Erkrankung, vorausgegangener Therapie mit Anthracyclinen oder Anthracendionen, vorausgegangener oder begleitender Strahlentherapie im Mediastinalbereich oder gleichzeitiger Anwendung von anderen kardiotoxischen Arzneimitteln. Die Herzfunktion sollte vor Beginn der Behandlung mit Pixantron kontrolliert und dann in regelmäßigen Abständen überwacht werden. In Tiermodellen war Pixantron weniger kardiotoxisch als Doxorubicin oder Mitoxantron. Möglicherweise liegt das daran, dass Pixantron ein Stickstoffatom als Heteroatom in der Ringstruktur enthält und keine Ketogruppen aufweist. Dadurch hat es weniger Potenzial für die Erzeugung von reaktiven Sauerstoffarten, die Eisenbindung und die Bildung von Alkoholmetaboliten, die toxisch wirken können.
Hautverfärbung und Chromaturie sind auf die (blaue) Farbe der Substanz zurückzuführen. Die Verfärbung der Haut bildet sich im Allgemeinen im Verlauf von ein paar Tagen bis Wochen mit der Ausscheidung des Arzneimittels zurück.
In vitro hemmt Pixantron CYP1A2 und CYP2C8, daher kann der Abbau von Theophyllin oder Warfarin verlangsamt sein, ebenso der von Amitriptylin, Haloperidol, Clozapin, Ondansetron und Propranolol.
Quelle
hel
DAZ 2012, Nr. 31, S. 32




















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.