
- DAZ.online
- DAZ / AZ
- DAZ 30/2012
- Apremilast bei Psoriasis
Arzneimittel und Therapie
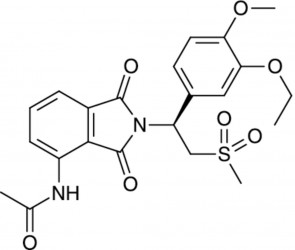
Apremilast bei Psoriasis
Die Phosphodiesterase 4 (PDE-4) katalysiert den Abbau des second messenger cAMP zu AMP. Sie besitzt in Immunzellen wie Monozyten, dendritischen Zellen und Neutrophilen, aber auch in Keratinozyten eine hohe Aktivität. Frühere Untersuchungen hatten gezeigt, dass der cAMP-Abbau zu einer erhöhten Produktion proinflammatorischer Zytokine wie TNF α, Interleukin 2, 12 und 23 führt und dass eine PDE-4-Hemmung mit Apremilast die Konzentrationen pro- und antiinflammatorischer Mediatoren modulieren kann. In einer Phase-IIb-Studie sollte nun die Wirksamkeit und Sicherheit der Substanz in verschiedenen Dosierungen geprüft werden.
Placebokontrollierte Studie mit drei Dosierungen
In der kürzlich im Fachblatt Lancet publizierten multizentrischen, randomisierten Studie hatten die Patienten (Mindestalter 18 Jahre) entweder Placebo (n = 88) oder Apremilast in den Dosierungen 10 (n = 89), 20 (n = 87) bzw. 30 mg (n = 88) zweimal täglich erhalten. Sie waren mittelschwer bzw. schwer an Plaque-Psoriasis erkrankt und Kandidaten für eine Phototherapie bzw. systemische Behandlung. Ihr PASI lag bei ≥ 12, mindestens 10% der Körperoberfläche waren von Hautläsionen betroffen. Zwischen der 16. und 24. Behandlungswoche wurde auch den Placebo-Patienten eine Behandlung mit dem Verum zuteil (mit 20 oder 30 mg Apremilast zweimal täglich). In den ersten 16 Wochen war das Studiendesign doppelblind, zwischen der 26 und der 24. Studienwoche lediglich die Dosierung unbekannt.
Primärer Studienendpunkt war der Anteil der Patienten, bei denen in Woche 16 eine mindestens 75%ige Reduktion des Baseline-PASI (psoriasis area and severity index) erreicht werden konnte.
Signifikante Überlegenheit in zwei Dosierungen
In der 16. Behandlungswoche wurde der PASI-75-Index bei fünf Placebopatienten (6%), zehn Patienten (11%) unter 10 mg, 25 (29%) unter 20 mg und 36 (41%) unter 30 mg Apremilast erreicht. Der Unterschied zwischen 20 mg sowie 30 mg und Placebo war statistisch signifikant (je p < 0,0001), während sich zwischen 10 mg und Placebo ein solcher Unterschied nicht zeigte. Darüber hinaus führte die Behandlung mit 20 bzw. 30 mg Dosierungen zu einer signifikanten Verbesserung der Lebensqualität. Die meisten (96%) der beobachteten unerwünschten Wirkungen waren mild oder moderat ausgeprägt. Mindestens 5% der Patienten litten unter Schwindel, Infektionen der oberen Atemwege, Durchfällen, Nasopharyngitis, Kopfschmerzen oder Magen-Darm-Beschwerden. Die beobachteten schwerwiegenden Nebenwirkungen (z. B. schwere Infektionen) wurden nicht auf Apremilast zurückgeführt. Urintests, Blutuntersuchungen, immunologische oder elektrokardiografische Tests beeinträchtigte der PDE-4-Hemmer nicht.
Längere Studiendauer empfohlen
Die Autoren der Studie merken kritisch an, dass die Therapiedauer mit 24 Wochen relativ kurz war. Außerdem waren überwiegend männliche, weiße und übergewichtige Patienten ohne Komorbiditäten eingeschlossen, was die Übertragbarkeit auf andere Populationen einschränkt.
Nach Ansicht der Autoren ermutigen die Studienergebnisse jedoch zu weiterführenden Untersuchungen mit längerer Behandlungsdauer. Dies ist auch die Ansicht eines Kommentators der Studie; mindestens eine einjährige Behandlungsdauer sei zur Überprüfung der Sicherheit der Substanz notwendig. Er verweist darauf, dass außerdem Vergleichsstudien mit den etablierten Therapien, insbesondere Methotrexat und Biologika, durchgeführt werden müssten.
Neben Plaque-Psoriasis wird Apremilast derzeit in klinischen Studien für die Indikationen Rheumatoide Arthritis, Arthritis psoriatica und Spondylitis ankylosans geprüft.
QuellePapp, K, et al.: Efficacy of apremilast in the treatment of moderate to severe psoriasis: a randomised controlled trial. Lancet (2012), Online publiziert am 29. Juni 2012.Van de Kerkhof, P: Apremilast: a step forward in the treatment of psoriasis. Lancet (2012), Online publiziert am 29. Juni 2012.




















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.