
- DAZ.online
- DAZ / AZ
- DAZ 38/2011
- Mit der Identitätsprü...
Reinheitsprüfung
Mit der Identitätsprüfung Verfälschungen entdecken?
Auch wenn die meisten Medikamente heutzutage als Fertigarzneimittel vertrieben werden, ist die Arzneimittelherstellung in Rezeptur und Defektur nach wie vor von großer Bedeutung im Apothekenalltag. Allein die Offizinapotheken in Deutschland stellen jährlich ca. 16 Millionen Rezepturarzneimittel her [1], und auch für die meisten Krankenhausapotheken gehört die Arzneimittelherstellung für den klinischen Bedarf zum üblichen Aufgabenbereich.
Die Anforderungen an die Arzneimittelherstellung in der Apotheke regelt die Apothekenbetriebsordnung (ApBetrO). Hiernach dürfen nur Ausgangsstoffe verwendet werden, deren ordnungsgemäße Qualität festgestellt ist. Dabei darf sich die Apotheke auf die Identitätsprüfung beschränken, wenn die Qualität der verwendeten Stoffe durch ein Prüfzertifikat nachgewiesen wird, sie trägt aber dennoch die Verantwortung für die Qualität des Arzneimittels (§ 11 Abs. 2 Satz 2 ApBetrO). Dies wirft die Frage auf, wie vertrauenswürdig die Prüf- und Analysenzertifikate der Lieferanten sind, denn dass man sich nicht "blind" auf sie verlassen kann, zeigt das folgende Beispiel.
Schwere Fälle von Fälschungen
Im Jahr 2006 machten Todesfälle in Südamerika als Folge einer Vergiftung mit Diethylenglykol (DEG) Schlagzeilen. Die toxische Substanz war in mehreren Chargen Hustensaft anstelle von Glycerol verwendet worden. Der Arzneimittelhersteller hatte auf das Analysenzertifikat vertraut, das den fraglichen Stoff als Gycerol mit einer Reinheit von 99,5% auswies [2].
In früheren Jahren wurden ähnliche Fälle von Verunreinigungen oder Vergiftungen mit DEG publik [3 – 9]. Sie sind zwar vergleichsweise selten, doch mit dem steigenden Kostendruck in der Pharmabranche und der Unübersichtlichkeit der globalen Lieferketten steigt die Wahrscheinlichkeit, dass minderwertige oder verfälschte Rohstoffe auch in Europa in den (Groß-)Handel gelangen.
Die Verwechslung eines Stoffes oder der vorsätzliche Austausch einer Substanz kann mittels geeigneter Identitätsprüfungen erkannt werden. Hingegen kann ein minderwertiger Rohstoff – im Sinne einer Substanz mit korrekter Identität, aber unzureichender Reinheit oder/und abweichendem Gehalt – in der Regel erst durch die Gesamtheit der Arzneibuchprüfungen nachgewiesen werden. In diesem Kontext kann für Apotheken die Frage interessant sein, inwieweit Identitätsprüfungen die Erkennung solcher minderwertiger Rohstoffe ermöglichen.
Identitäts- und Reinheitsprüfung
Für die Identitätsprüfung von offizinellen oder apothekenüblichen Ausgangsstoffen werden in der Apotheke die Vorschriften des Arzneibuches oder – in Ermangelung einer apothekentauglichen Methode – diejenigen des DAC herangezogen.
Glycerol ist im Europäischen Arzneibuch (EuAB) als wasserfreie Substanz und als Glycerol 85% beschrieben [10, 11]. Die Identitätsprüfungen beider Stoffe sind gleich und umfassen eine erste (instrumentelle) und eine zweite (nicht-instrumentelle) Identifikationsreihe. Die Durchführung der Prüfungen der zweiten Identifikationsreihe wird nur dann akzeptiert, wenn sichergestellt ist, dass die Substanz eindeutig einer zertifizierten Charge entstammt, die sämtlichen anderen Anforderungen der Monografie entspricht [12]. Die Anforderungen sind in beiden Monografien, mit Ausnahme der unterschiedlichen Bereiche für den Brechungsindex, identisch (Tab. 1).
Tab. 1: Identitätsprüfungen von Glycerol und Glycerol 85% gemäß Europäischem Arzneibuch [10, 11] | ||
Methode |
Glycerol |
Glycerol 85% |
A Brechungsindex |
1,470 – 1,475 |
1,449 – 1,455 |
B IR-Spektroskopie |
Übereinstimmung mit Referenzspektrum |
|
C Farbreaktion |
Entstehen eines blauen Rings, der 10 min bestehen bleibt |
|
D Acrolein-Test |
Schwärzung eines Filterpapiers |
|
Der DAC empfiehlt als alternative Identitätsprüfung von Glycerol lediglich die Messung des Brechungsindexes [13].
Als Reinheitsprüfung enthält die Arzneibuchmonografie u. a. eine gaschromatografische Bestimmung, mit der die Substanzen Ethylenglykol, DEG und Propylenglykol erfasst werden. Bei Durchführung dieser GC-Prüfung kann folglich eine Verfälschung oder ein Verschnitt des Glycerols durch die preiswerteren Glykole leicht erkannt werden. Inzwischen wird diskutiert, die GC-Prüfung durch eine HPLC-Prüfung zu ersetzen [15]. Dann könnte von den drei hier erwähnten Glykolen nur noch DEG erfasst werden.
Da die drei genannten Glykole bzw. ihre Metaboliten für den Menschen mehr oder weniger toxisch sind [14], stellt ein Verschnitt des Glycerols mit diesen Stoffen nicht nur eine erhebliche Qualitätsminderung, sondern auch eine Gesundheitsgefährdung dar.
Die US-amerikanische Food and Drug Administration (FDA) hat im Mai 2007 auf die Vorfälle in Südamerika mit der Herausgabe eines Leitfadens zur Prüfung von Glycerol auf DEG reagiert [15]. Darin wird empfohlen, dass vor der Verwendung von Glycerol als Ausgangsstoff für die Arzneimittelherstellung zusätzlich zur Identitätsprüfung eine Grenzprüfung auf DEG an allen Abpackungen jeder Charge durchgeführt wird.
Experimentelle Untersuchungen
Anhand von Testmustern wurden die im EuAB beschriebenen Identitätsprüfungen (Tab. 1) daraufhin untersucht, ob mit ihrer Hilfe Beimengungen des Glycerols erkannt werden können. Die verwendeten Muster sollten verschnittene Stoffproben simulieren und wurden durch Mischen von Glycerol (wasserfrei) mit unterschiedlichen Mengen an Glykolen (Ethylenglykol, DEG, Propylenglykol) hergestellt.
Aussehen: Da es sich bei Glycerol und den Glykolen gleichermaßen um (fast) farblose, klare, geruchlose und mehr oder weniger viskose Flüssigkeiten handelt, wird durch die Prüfung des Aussehens eine Beimischung kaum auffallen, eine Verwechslung vermutlich allenfalls bei direktem Vergleich mit einer Referenz (v. a. anhand der unterschiedlichen Viskosität).
Brechungsindex: Die Prüfung des Brechungsindexes dient vor allem zur Unterscheidung von wasserfreiem Glycerol und Glycerol 85% [17], denn mit steigendem Wassergehalt nimmt der Brechungsindex ab.
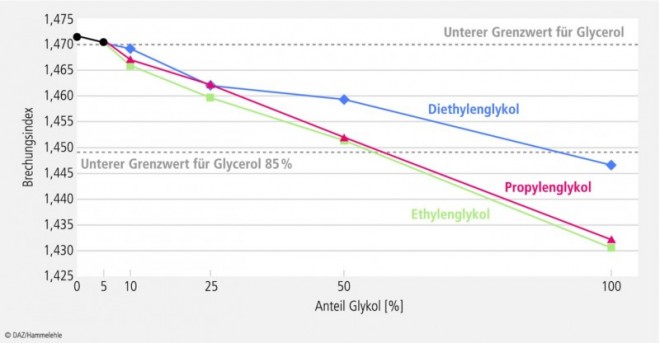
Im Vergleich zu Glycerol weisen auch die Glykole einen niedrigeren Brechungsindex (1,431 bis 1,4475) auf [18, 19], sodass dieser Wert mit steigender Konzentration an Glykolen in den Testmustern abnimmt (siehe Abb. 1).
Er unterschreitet die im EuAB festgelegten Grenzen für wasserfreies Glycerol bei einem Glykolgehalt von über 5% und diejenigen für Glycerol 85% erst bei einer Glykolkonzentration von weit über 50%.
Folglich eignet sich diese Prüfung zur Erkennung von Beimengungen des Glycerols nur bedingt, da die "Detektionsgrenze" relativ hoch liegt und so unter Umständen erhebliche Mengen an Glykol unerkannt bleiben.
Nasschemische Prüfungen: Bei der Prüfung C, einer Farbreaktion für primäre und sekundäre Alkohole, zeigt sich ab einem Zusatz von etwa 25% der getesteten Glykole ein abweichendes Verhalten von dem des reinen Glycerols. Der sich bildende blaue Farbring ist nicht mehr über die geforderte Zeitspanne (10 min) stabil, sondern diffundiert rasch in die untere Zone.
Der Acrolein-Test (Prüfung D) fällt nicht nur bei reinem Glycerol, sondern auch bei den Glykolen und ihren Mischungen mit Glycerol positiv aus. Diese Prüfung ist demnach nicht geeignet, um zwischen Glycerol und den Glykolen zu differenzieren.
Somit ergeben auch die nasschemischen Identitätsprüfungen keinen Erkenntnisgewinn über mögliche Beimengungen an Glykolen. Ohnehin werden sie in der Offizinapotheke wegen bedenklicher Reagenzien bzw. Reaktionsprodukte gern vermieden.
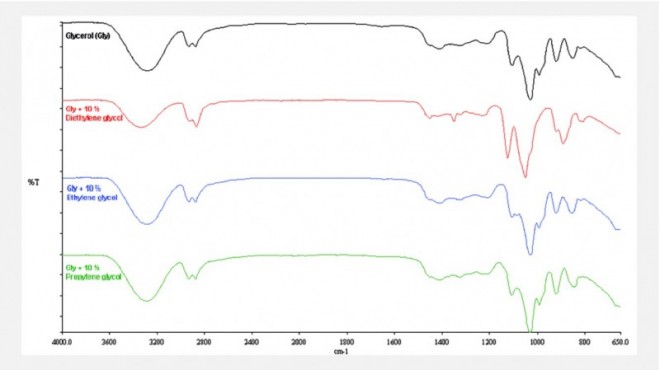
Infrarotspektrometrie: Auch die IR-Spektrometrie, die in Offizinapotheken eher selten eingesetzt wird, ist für das Aufspüren von Verunreinigungen nur bedingt geeignet. Dies gilt auch für Glycerol. Während die Spektren der Glykole als Reinsubstanzen von dem Spektrum des Glycerols relativ gut zu unterscheiden sind, fällt die Differenzierung von Mischungen deutlich schwerer. Beimischungen von ca. 10% Glykol lassen sich beim direkten Vergleich mit dem Spektrum der Referenzsubstanz nur erahnen (Abb. 2).
Die geringen Abweichungen der Valenzschwingungen sowie die kleinen Veränderungen im Fingerprint (Bandenverschiebung, Relation der Bandenintensität) sind erst ab einer Zumischung von mindestens 25% Glykol deutlich zu identifizieren.
Vergleicht man das selbst aufgezeichnete Spektrum mit dem vom Europäischen Direktorat für die Qualität von Arzneimitteln (EDQM) zur Verfügung gestellten IR-Referenzspektrum, sind signifikante Unterschiede noch viel schwerer zu erkennen. Die Abweichungen könnte man als Messungenauigkeit interpretieren oder auf Geräteunterschiede zurückführen.
Vertrauenswürdigkeit der Bezugsquellen
Die eingangs berichteten Vergiftungen in Südamerika durch DEG wären vermeidbar gewesen, wenn der Hersteller des Arzneimittels eine sorgfältige Identitätsprüfung durchgeführt hätte, denn bei dem angeblichen Glycerol handelte es sich trotz des mitgelieferten Zertifikats um reines DEG. Solch ein kompletter Austausch von Stoffen ist mit Identitätsprüfungen leicht aufzudecken. Ist der betrachtete Stoff allerdings "nur" verschnitten, stehen die Chancen der Aufdeckung bei Weitem nicht so gut. Dies gilt nicht nur für Glycerol, sondern auch für die meisten anderen pharmazeutischen Rohstoffe und ist auch nicht verwunderlich, denn das Ziel von Identitätsprüfungen gemäß Arzneibuch (oder DAC) ist die Unterscheidung von anderen Reinstoffen. Folglich werden, zumindest bei strukturell ähnlichen Verbindungen, erst relativ hohe Mengen an Verunreinigungen erkannt.
Der Apothekenleiter muss bei der Beschaffung von Rohstoffen für Rezeptur und Defektur verschiedene Aspekte berücksichtigen. Neben den pharmazeutischen Gesichtspunkten und den allgemeinen Grundsätzen der Qualitätssicherung steht auch der wirtschaftliche Aspekt im Blickfeld. Letzterer muss sorgfältig gegen die anderen beiden abgewogen werden. Wenn auf eigene Prüfungen der Ausgangsstoffe weitgehend verzichtet werden soll, ist es enorm wichtig, dass der Hersteller des Stoffes und der Lieferant vertrauenswürdig sind und nach geeigneten Qualitätsstandards arbeiten.
Die eingehende Kenntnis – und wenn möglich Kontrolle – der Lieferanten sollte Bestandteil der Qualitätssicherung in jeder Apotheke sein. Die Leitlinie für die Herstellung und Prüfung in der Krankenhausapotheke fordert daher, dass an dem Einkauf von Ausgangsstoffen "qualifiziertes Personal beteiligt sein sollte, das die Zulieferer genau kennt" [20]. Dies sollte auch für die Offizinapotheke gelten. Das bedeutet, dass sie bei einem Wechsel von Bezugsquellen für pharmazeutische Ausgangsstoffe stets die Qualifikation und Zuverlässigkeit der neuen Lieferanten prüft.
Dass die Prüfung der Ausgangsstoffe zuverlässig und kompetent erfolgen muss, spiegelt sich auch in der Apothekenbetriebsordnung wider. Laut § 11 Abs. 1 Satz 2 finden die Vorschriften des § 6 Abs. 3 zur Prüfung von Arzneimitteln entsprechende Anwendung auf die Prüfung der Ausgangsstoffe.
Den Hilfsstoffen wie Glycerol wird oft weniger Beachtung geschenkt als den Wirksubstanzen, obwohl Erstere häufig den größeren Anteil am Arzneimittel ausmachen. Allerdings ist der Pharmamarkt für Produzenten von Hilfsstoffen meistens nur ein Nebengeschäft, da der größte Anteil der Produktion in andere Märkte (z. B. Lebensmittelindustrie) fließt. Zudem findet der Handel meist über mehrere Zwischenhändler statt, sodass die Lieferkette schwer nachzuverfolgen ist. Zudem können die Zwischenhändler die Hilfsstoffe umfüllen und dabei verschiedene Chargen mischen. Umso wichtiger ist, dass die Analysenzertifikate verlässlich sind.
Die Unübersichtlichkeit der Lieferketten betrifft auch die Wirkstoffe, denn immer mehr Arzneistoffe werden im außereuropäischen Ausland hergestellt. Beispielsweise stammen schätzungsweise 80% der in Deutschland verwendeten Antibiotika aus China oder Indien [21]. Die Globalisierung der Märkte hat so auch die deutschen Apotheken erreicht.
Schlussfolgerungen
Der Verschnitt von Pharmarohstoffen kann nur dann zuverlässig erkannt werden, wenn mehr als nur Identitätsprüfungen durchgeführt werden. In Offizin- und kleineren Krankenhausapotheken ist es jedoch selten praktikabel, die gesamte Arzneibuchanalytik eines monografierten Stoffes durchzuführen. Die Verlässlichkeit des Analysenzertifikates und die Vertrauenswürdigkeit des Lieferanten sind deshalb entscheidende Faktoren, um die Qualität von Rohstoffen für Rezeptur und Defektur sicherzustellen. Kein Apotheker sollte sich ausschließlich auf mitgelieferte Zertifikate verlassen, sondern die Bezugsquelle genau kennen.
Anderenfalls läuft er Gefahr, einen falschen oder qualitätsgeminderten Stoff zu verarbeiten – mit möglicherweise unerwarteten Folgen für die Gesundheit der Patienten.
Literatur
[1] ABDA – Bundesvereinigung Deutscher Apothekerverbände. Die Apotheke – Zahlen, Daten, Fakten 2009.
[2] Megget K. To test or not to test? The glycerine debate. In PharmaTechnologist.com, 14. Juni 2007.
[3] Alfred S, et al. Delayed neurologic sequelae resulting from epidemic diethylene glycol poisoning. Clin Toxicol 2005; 43:155 – 159.
[4] Hanif M, et al. Fatal renal failure caused by diethylene glycol in paracetamol elixir. The Bangladesh epidemic. Br Med J 1995;311:88 – 91.
[5] O‘Brien KL, et al. Epidemic of pediatric deaths from acute renal failure caused by diethylene glycol poisoning. JAMA 1998;279:1175 – 1180.
[6] Singh J, et al. Diethylene glycol poisoning in Gurgaon, India, 1998. Bull World Health Organ 2001;79:88 – 95.
[7] Okuonghae HO, et al. Diethylene glycol poisoning in Nigerian children. Ann Trop Paediatr 1992;12:235 – 238.
[8] Bowie MD, McKenzie D. Diethylene glycole poisoning in children. S Afr Med J 1972;46:931 – 934.
[9] Geiling EMK, Cannon PR. Pathologic effects of elixir of sulphanilamide (diethylene glycol) poisoning. A clinical and experimental correlation. Final report. JAMA 1938;111:919 – 926. [10] Glycerol, in: Europäisches Arzneibuch, 6. Ausgabe (EuAB 6). Deutscher Apotheker Verlag / Govi-Verlag, S. 2690.
[11] Glycerol 85%, in: EuAB 6, S. 2692.
[12] Prüfung auf Identität, in: EuAB 6, 7. Nachtrag, S. 7223.
[13] Alternativverfahren zur Identifizierung von Ausgangsstoffen, in: ABDA – Bundesvereinigung Deutscher Apothekerverbände (Hrsg.). Deutscher Arzneimittel-Codex. Govi-Verlag / Deutscher Apotheker Verlag, 2009, Bd. 3, S. 221.
[14] Glycols, in: Klaassen CD (ed). Casarett and Doull‘s Toxicology, 6. Ed., McGraw-Hill, New York 2001, S. 896 – 898.
[15] Testing of Glycerin for Diethylene Glycol, Guidance for industry. Food and Drug Administration, Center for Drug Evaluation and Research, Mai 2007; www.fda.gov/cder/guidance/index.htm. [16] Glycerol. Pharmeuropa 2002;14(1):77 – 79.
[17] Glycerol, in: Böhme H, et al (Hrsg.). Arzneibuch-Kommentar, 19. Lfg. Deutscher Apotheker Verlag, 2005.
[18] The Merck Index, 14. Ed., 2006.
[19] Propylenglycol, in: EuAB 6, S. 3781.
[20] Leitlinie für die Herstellung und Prüfung in der Krankenhausapotheke. Krankenhauspharmazie 2005;26:347 – 362.
[21] Holzgrabe U, et al. Verunreinigungen in Arzneistoffen. Dtsch Apoth Ztg 2003;143:3221 – 3228.
Autoren
Dr. Susanne Belz, Regine Endler, Dr. Thorsten Gumz
Bundesinstitut für Arzneimittel und Medizinprodukte Kurt-Georg-Kiesinger-Allee 3, 53175 BonnKontakt: Dr. Thorsten Gumz, Gumz@bfarm.de

















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.