
- DAZ.online
- DAZ / AZ
- DAZ 38/2011
- Die optimale Balance ...
Arzneimittel und Therapie
Die optimale Balance finden
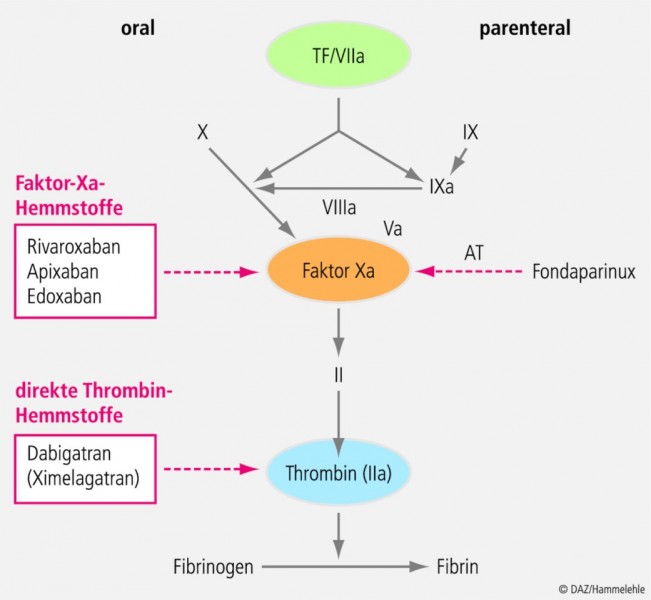
In Europa hat Edoxaban noch keine Marktzulassung. Als neue orale Gerinnungshemmer stehen hier der direkte Thrombin-Inhibitor Dabigatran (Pradaxa®, Boehringer Ingelheim) und die beiden Faktor Xa-Inhibitoren Rivaroxaban (Xarelto®, Bayer Schering Pharma AG) und Apixaban (Eliquis®, Bristol-Myers Squibb/Pfizer) zur Verfügung. Apixaban und Rivaroxaban sind zur Prophylaxe venöser Thromboembolien nach elektiven Hüft- und Kniegelenksoperationen zugelassen, Dabigatran darüber hinaus zur Schlaganfallprävention bei Patienten mit Vorhofflimmern (atrial fibrillation, AF).
Wirkprinzip von Edoxaban
Durch direkte Hemmung des Blutgerinnungsfaktors X in seiner aktivierten Form Xa verringert Edoxaban die Spaltung von Prothrombin zu Thrombin und dadurch die Umwandlung von Fibrinogen zu Fibrin. Wie Satoshi Kunitada, Tokio, auf einem von der Daiichi-Sankyo Deutschland GmbH veranstalteten Pressegespräch auf dem diesjährigen Kongress der European Society of Cardiology in Paris erläuterte, hat sich der Wirkstoff auf Basis der bislang vorliegenden Daten als effektiver Gerinnungshemmer mit vorhersehbarem pharmakokinetischem und -dynamischem Profil erwiesen. Dies ermögliche eine bequeme einmal tägliche Einnahme. Die Bioverfügbarkeit liegt bei 60%, die Elimination erfolgt nur zu etwa einem Drittel über die Nieren, zu zwei Dritteln über die Fäzes. Abgesehen von Wechselwirkungen mit potenten P-Glykoprotein-Inhibitoren sind bisher keine Interaktionen zwischen Edoxaban und anderen Arzneistoffen und nur minimale Wechselwirkungen mit Nahrungsmitteln bekannt geworden.
In bisherigen klinischen Studien in Japan zeigte sich Edoxaban im Vergleich mit Enoxaparin bei der Prävention postoperativer venöser Thromboembolien nach Knie- bzw. Hüftgelenksersatz nicht unterlegen bzw. überlegen.
Umfangreiches Studienprogramm
Das laufende Studienprogramm mit Edoxaban umfasst zwei große Phase-III-Studien: die doppelblinde randomisierte multinationale Studie HOKUSAI VTE zur Behandlung und Prävention rezidivierender VTE und ENGAGE AF-TIMI 48 (Effective anticoagulation with factor XA next generation in atrial fibrillation), eine doppelblinde, randomisierte, multinationale Studie zu Vorhofflimmern. Letztere Untersuchungen sind nach Ansicht von Experten besonders bedeutsam, weil die Zahl der Patienten mit Vorhofflimmern in den kommenden Jahren infolge der demografischen Entwicklung ansteigen wird. In den entwickelten Ländern sind zurzeit etwa 1 bis 2% der Bevölkerung betroffen. Gegenwärtiger Behandlungsstandard zur Schlaganfallprävention bei diesen Patienten sind Vitamin-K-Antagonisten. Wegen des schmalen therapeutischen Fensters sowie der Notwendigkeit einer kontinuierlichen Kontrolle der Gerinnungsparameter wird diese Therapieoption derzeit nur wenig genutzt, erläuterte Prof. Dr. Jose L. Zamorano Gomez, Madrid. Die Gerinnungshemmung sei aber bei diesen Patienten bedeutsam da sich gezeigt habe, dass einer von fünf bis sechs Schlaganfällen auf Vorhofflimmern zurückzuführen ist.
ENGAGE AF-TIMI 48 ist mit 21.105 eingeschlossenen Patienten die bisher größte Outcome-Studie zu Vorhofflimmern. Primärer Endpunkt ist das kombinierte klinische Ergebnis von Schlaganfällen und systemischen Embolien. Der primäre Sicherheitsendpunkt ist die Häufigkeit des Auftretens größerer und klinisch relevanter geringfügiger Blutungen. Edoxaban wird in zwei verschiedenen Dosierungen (30 und 60 mg, je einmal täglich) im Vergleich zur aktiven Kontrolle Warfarin untersucht. Die mediane Behandlungszeit liegt bei 24 Monaten. Robert P. Giugliano, Boston, wies auf dem Kongress darauf hin, dass für eine optimale gerinnungshemmende Therapie flexible Dosierungen notwendig sind, um die Balance zwischen der Prävention von Thrombosen und Embolien und unerwünschten Ereignissen wie etwa einer größeren Blutungsneigung finden zu können. Dennoch würden in der Entwicklung befindliche Medikamente häufig nur mit einer einzigen Dosierung getestet. Edoxaban dagegen wird in der laufenden Phase III-Studie ENGAGE AF-TIMI 48 an AF-Patienten in zwei verschiedenen Dosierungen untersucht. Dies gebe dem behandelnden Arzt die Möglichkeit, eine auf das persönliche Risikoprofil des Patienten hinsichtlich Körpergewicht, Nierenfunktion und/oder Begleitmedikation abgestimmte Dosierung auszuwählen. Die Studie wurde so angelegt, dass jederzeit eine spezifische Reduktion der Dosis bei Patienten möglich ist, bei denen ein besonderes Blutungsrisiko angenommen wird, das heißt eine Reduktion von 60 auf 30 mg bzw. 30 auf 15 mg.
Apothekerin Dr. Claudia Bruhn
Zum WeiterlesenInterpharm Kolleg 2010: Paket mit 9 Fachvorträgen zum Schwerpunkt
Interpharm Kolleg 2010 – Interaktive Kongressdokumentation auf DVD Lernen mit Fachvorträgen Paket mit 9 Fachvorträgen 90,00 Euro Deutscher Apotheker Verlag Einfach und schnell zu bestellen unter der Postadresse: Deutscher Apotheker Verlag Postfach 10 10 61 70009 Stuttgart oder im Internet unter: www.buchoffizin.de oder per Telefon unter: (07 11) 25 82 - 3 41 oder - 3 42 |


















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.