
- DAZ.online
- DAZ / AZ
- DAZ 36/2010
- Erhöhtes Sterberisiko ...
Arzneimittel und Therapie
Erhöhtes Sterberisiko nach Einsatz von Tigecyclin
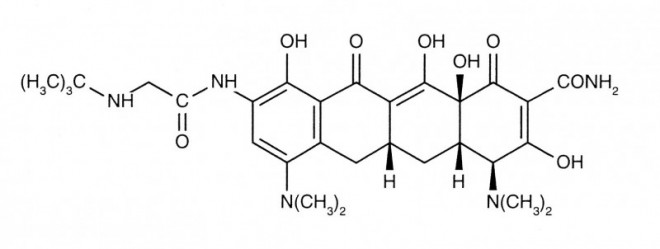
Das Reserveantibiotikum Tigecyclin (Tygacil®) gehört zur Klasse der Glycylcycline. Es handelt sich dabei um Derivate der Tetracycline mit einem sehr breiten Wirkungsspektrum, das grampositive und gramnegative, vor allem aber zahlreiche multiresistente Keime umfasst. Der Wirkstoff wurde im Jahr 2007 in Deutschland zugelassen und wird bei schweren Infektionen zur Monotherapie eingesetzt.
Wie andere Tetracycline hemmt Tigecyclin die Proteinbiosynthese, indem es die Anlagerung der Aminoacyl-tRNA an die Akzeptorstellen der 30-S-Untereinheit der bakteriellen Ribosomen und damit die Verlängerung der Peptidkette verhindert. Im Gegensatz zu den "klassischen" Tetracyclinen bindet es aber mit etwa fünffach höherer Affinität und verhindert so eine schützende Wirkung bakterieller Protektionsproteine, und es wird nicht von der Effluxpumpe aus der Zielzelle heraustransportiert.
FDA rät zu überlegtem Einsatz von Tigecyclin
Die US-amerikanische Arzneibehörde FDA hat jetzt eine Warnung zum Einsatz von Tigecyclin herausgegeben. Nach der Auswertung von 13 klinischen Studien zu unterschiedlichen Indikationsbereichen konnte zusammenfassend ein deutlich erhöhtes Sterberisiko im Vergleich zu anderen Antibiotika nachgewiesen werden. Von insgesamt etwa 3800 Patienten, die Tigecyclin erhalten hatten, starben 150 (4%). Im Vergleich dazu starben in der Kontrollgruppe von 3650 Patienten 110 (3%), die ein anderes Antibiotikum erhalten hatten. Die Auswertung ist nach unterschiedlichen Indikationen aufgeschlüsselt. Besonders prekär waren die Ergebnisse zum Einsatz bei beatmungsassoziierten Pneumonien (VAP). Während die Mortalität der mit anderen Antibiotika behandelten Patienten 12% betrug, waren es bei einem Einsatz von Tigecyclin 19%. Erhöht war das Risiko auch bei Patienten mit komplizierten Haut- und Weichgewebeinfektionen, komplizierten intraabdominalen Infektionen und Infektionen eines diabetischen Fußes.
In Deutschland hat Tigecyclin keine Zulassung für die Behandlung von ambulant erworbenen Pneumonien. Hier beschränkt sich die Zulassung von Tigecyclin auf die Behandlung komplizierter Haut- und Weichgewebeinfektionen sowie intraabdominelle Infektionen. Aber auch für diese Indikationen konnte ein leicht erhöhtes Sterberisiko bei Tigecyclin-Gabe nachgewiesen werden. Die FDA empfiehlt daher den Einsatz anderer Antibiotika bei Patienten mit schweren Infektionen.
Alternativen zu Tigecyclin gibt es allerdings häufig nicht. Das Antibiotikum ist wirksam gegen eine Vielzahl von multiresistenten Stämmen wie multiresistente Staphylokokken (MRSA), VRE (Vancomycin-resistente Enterokokken) und ESBL (extended spectrum Betalactamase)-Stämme. Auch gegen die jüngst in die Schlagzeilen geratenen NDM-1-Stämme von E. coli und Klebsiella pneumoniae war es die letzte Option. Hier zeigt sich wiederum die vom Robert Koch-Institut wiederholt dargestellte Problematik: Es fehlt bei zunehmender Zahl von multiresistenten Bakterien an Alternativen zu den derzeit noch zur Verfügung stehenden Reserveantibiotika, und es ist nicht abzusehen, wann sich diese Situation ändern wird.
Quelle FDA: Tygacil (tigecycline): Label Change – Increased Mortality Risk; Drug Safety Communication vom 1. September 2010.
Dr. Hans-Peter Hanssen




















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.