
- DAZ.online
- DAZ / AZ
- DAZ 34/2010
- Ernährung bei ...
Ernährung aktuell
Ernährung bei Mukoviszidose
Bis in die 1990er Jahre erreichten Patienten mit Mukoviszidose kaum das Erwachsenenalter [1]. Heute wird die mittlere Lebenserwartung für die Patienten auf 36 bis über 40 Jahren geschätzt [1, 2]. Mukoviszidose tritt mit einer Häufigkeit von 1:2500 auf [3]. Die Heterozygotenfrequenz liegt bei 1:20 bis 1:25 bei Kaukasiern. Somit sind 5% phänotypisch gesunde Überträger, die jedoch keine Mukoviszidose-typischen Laborbefunde aufweisen [1].
1989 war es gelungen das für die Mukoviszidose verantwortliche Gen (Cystic Fibrosis Transmembrane Conductance Regulator, CFTR) zu identifizieren [4]. Bislang konnten 1000 Mutationen beschrieben werden, die einen fehlerhaften Chloridkanal in der Membran von Epithelzellen kodieren [5]. Die häufigste Mutation (weltweit 66%) ist der Verlust von Phenylalanin in Position 508 des CFTR-Proteins. Aufgrund der Mutationen wird der Chlorid-Transport durch Zellmembranen unterschiedlich stark eingeschränkt, so dass auch das Krankheitsbild sehr variabel ist. Im Vergleich zu gesunden Personen erhöhen sich die Elektrolytkonzentrationen durch den gestörten transmembranösen Ionenfluss im Schweiß. Wegen der Chloridretention wird Natrium in sekretbildenden Drüsen verstärkt resorbiert; Wasser wird zunehmend intrazellulär zurückgehalten. Die Viskosität verschiedener Drüsensekrete nimmt zu. Dadurch werden vor allem die Funktionen der Bauchspeicheldrüse, der Bronchien, der Leber und der Gonaden eingeschränkt [4].
Welche Organe sind betroffen?
Die Lunge von Mukoviszidose-Patienten ist zum Zeitpunkt der Geburt noch gesund. Doch sehr rasch nach der Geburt können erste pathologische Veränderungen – namentlich Hypertrophie der mukösen Drüsen und Hyperplasie der Becherzellen – auftreten, die die kleinen Atemwege betreffen. Sogenanntes "Mucus Plugging" der peripheren Atemwege mit zähem purulentem Sekret führt zu einer Störung der mukozilliären Clearance. Insgesamt ist die Lungenerkrankung durch chronische endobronchiale bakterielle Infektionen und durch eine chronische Atemwegsentzündung geprägt. Bakterielle Infektionen werden in den ersten Lebensjahren durch Staphylococcus aureus und Haemophilus influenzae, später überwiegend durch Pseudomonas aeruginosa hervorgerufen. Folge sind Bronchiektasien und eine progrediente Lungendestruktion.
Auch der Gastrointestinaltrakt ist von Mukoviszidose betroffen. Aufgrund der fehlenden oder verminderten Chlorid- und Wassersekretion kann eine Eindickung des Darminhaltes beobachtet werden. 10 bis 15% aller Neugeborenen mit Mukoviszidose weisen einen Darmverschluss (Mekoniumileus) auf. Im späteren Lebensalter können ebenfalls klinische Beschwerden auftreten, etwa aufgrund eines distalen intestinalen Obstruktionssyndroms (DIOS) oder einer Darmeinstülpung bzw. einer Darmverdrehung. Zudem ist das Auftreten eines Darmvorfalls (Rektumprolaps) oder ein gastroösophagaler Reflux möglich. Auch die Bauchspeicheldrüse ist bei Mukoviszidose betroffen: bereits bei Geburt besteht bei etwa 80% der Patienten eine exokrine Pankreasinsuffizienz; mit zunehmenden Alter sind bis zu 95% davon betroffen. Durch das Fehlen von Pankreasenzymen und eine verminderte Bicarbonatsekretion kommt es zu Maldigestion, Gedeihstörungen sowie Steatorrhö. Des Weiteren können mit zunehmender fibrotischer Umwandlung des Pankreas auch die endogenen Bereiche betroffen sein und sich somit ein Diabetes mellitus manifestieren [1]. Diabetes mellitus bei Mukoviszidose gilt als die häufigste Komorbidität. Er tritt in der Regel im Alter zwischen 18 und 21 Jahren auf, verschlechtert den Allgemeinzustand der Patienten und reduziert ihre Überlebenswahrscheinlichkeit [3]. In der Leber kann eine fehlende oder verminderte CFTR-Funktion eine Cholestase bis hin zur biliären Zirrhose bewirken. Außerdem treten bei rund 15% der Erkrankten Gallensteine auf. In den Nasennebenhöhlen ist bei nahezu allen Patienten eine Pansinusitis zu beobachten, bei einem Viertel sind Nasenpolypen nachweisbar. Außerdem sind 95 bis 98% der männlichen Mukoviszidose-Patienten infertil. Schließlich liegt ein Basisdefekt in den Schweißdrüsen vor, der zu erhöhten Natrium- und Chloridkonzentrationen im Schweiß führt [1].
Husten, Durchfall, Infektanfälligkeit
Die Lungenerkrankung, Maldigestion sowie die erhöhte Natriumchloridkonzentration im Schweiß bilden die klinische Trias der Mukoviszidose. Leitsymptome der Maldigestion sind voluminöse, übelriechende Durchfälle, Steatorrhö, Blähungen, Gedeihstörung und ein vorgewölbtes Abdomen. Charakteristische pulmonale Symptome sind chronischer produktiver Husten, rezidivierende Bronchitiden und Pneumonien. Das Auftreten von Bronchiektasen führt zu bakteriellen Infektionen mit den bereits genannten Problemkeimen, die sich im Verlauf zu chronischen Erkrankungen entwickeln können. Durch die chronische Lungenerkrankung bilden sich Uhrglasnägel und Trommelschlägelfinger. Mit steigender respiratorischer Insuffizienz kommt es zu chronischer Hypoxie, Zyanose, später zu pulmonaler Hypertension und zum Cor pulmonale. Weitere Erkrankungsmanifestationen können Tabelle 1 entnommen werden [1].
Komplikationen
Es können im Rahmen der Mukoviszidose verschiedene Komplikationen auftreten (siehe auch Kasten "Komplikationen"). So kann es durch exzessives Schwitzen, etwa bei großer Hitze oder bei fieberhaften Erkrankungen zu einer Elektrolytentgleisung und hypochlorämischer Alkalose kommen. Dies kann insbesondere bei Säuglingen und Kleinkindern beobachtet werden. Des Weiteren können Pneumothoraces und Hämoptysen als Folge der progredienten Lungendestruktion sowie Diabetes mellitus durch die zunehmende fibrotische Umwandlung des Pankreas und Zerstörung der Inselzellen auftreten. Ein weiteres Beispiel ist die biliäre Zirrhose mit portaler Hypertension mit Ösophagusvarizenblutung im Rahmen der Lebermanifestation [1].
Komplikationen der Mukoviszidose
- Hämoptysen
- Pneumothorax
- Allergische bronchopulmonale Aspergillose (ABPA)
- Pulmonale Hypertension, Cor pulmonale
- Elektrolytentgleisung, hypochlorämische Alkalose
- Rektumprolaps
- Mekoniumileus, distales intestinales Obstruktionssyndrom
- Biliäre Zirrhose, portale Hypertension, Ösophagusvarizenblutung
- Cholelithiasis
- Gastroösophagealer Reflux
- Pankreatitis
- Diabetes mellitus
- Hypertrophe Osteoarthropathie
- Osteoporose, Osteopenie
Quelle: [1]
Pathophysiologie der Malnutrition
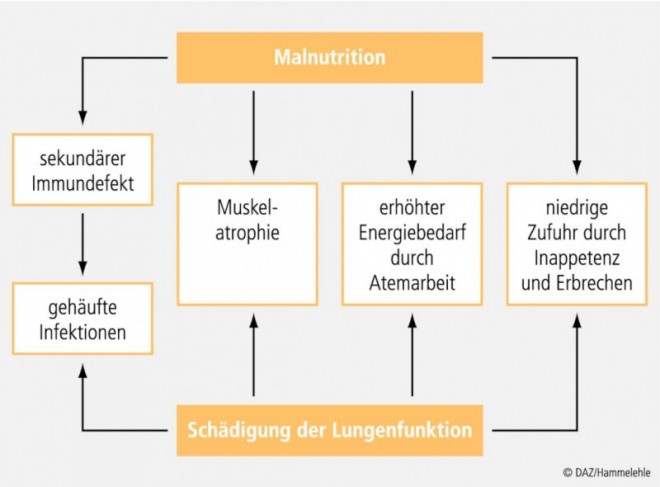
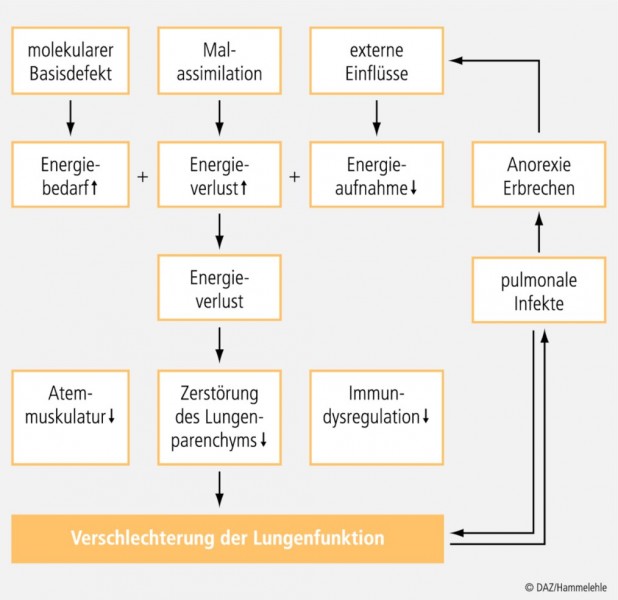
Bei vielen Mukoviszidose-Patienten liegt eine gestörte Energiebilanz und daraus resultierend ein schlechter Ernährungszustand vor. Dies lässt sich durch Malabsorption, einen erhöhten Energieverbrauch bei Infektionen, vermehrte Atemarbeit und Medikamente begründen. Zudem leiden viele Patienten aufgrund von Bauchschmerzen, Infekten, der fortgeschrittenen Lungenerkrankung, Erbrechen und teilweise auch Ernährungsfehler unter Inappetenz (siehe auch Abb. 1) [7]. Malnutrition und ein deutlich vermehrter Muskelabbau beeinträchtigen die Lungenfunktion der Patienten durch eine Schwächung der Atemhilfsmuskulatur. Aufgrund der stark verminderten respiratorischen Muskelmasse wird die Mechanik und Kraft von Atemexkursionen und Hustenstößen negativ beeinflusst. Durch die Malnutrition werden außerdem die Struktur und damit die Elastizität des Lungenparenchyms, die Synthese von oberflächenaktiven Substanzen und die Immunabwehr geschwächt. Somit ist eine durch Malnutrition geschwächte Lunge anfälliger für Atemwegsinfektionen. Das bestehende Energiedefizit wird wiederum durch Infektionen der Lunge vergrößert. Auf diese Weise entsteht ein Circulus vitiosus: Lungeninfektionen und -entzündungen können sich in einer immer schwächer werdenden Lunge weiter ausdehnen. Es überrascht daher nicht, dass die Malnutrition auch die Lebenserwartung der Patienten negativ beeinflusst. Bei stark untergewichtigen Personen halbiert sich diese im Vergleich zu Patienten mit mäßigem Untergewicht. Insgesamt zeigen Patienten mit gut funktionierender Pankreassekretion und weitgehend normaler Fettresorption im Vergleich zu pankreasinsuffizienten Patienten einen wesentlich besseren Ernährungsstatus. Auch die Lungenfunktion ist besser und die Infektionsrate mit Pseudomonas aeruginosa ist geringer, so dass für diese Personen die Lebenserwartung höher ist [4].
Ernährungstherapie als wichtiger Baustein
Seit bekannt ist, welche Bedeutung der Ernährung bei Mukoviszidose beigemessen werden muss, gehört diese zu den wichtigsten Therapiebausteinen. Zunächst sollten Mukoviszidose-Patienten eine ausgewogene Mischkost anstreben. Diese sollte zusätzlich mit Fett angereichert werden.
Die Aufteilung der Makronährstoffe verteilt sich wie folgt: 40 Energieprozent (En%) Fett, 20 En% Protein und 40 En% Kohlenhydrate. Mukoviszidose-Patienten sollten sich an diesen relativ geringen Kohlenhydratanteil halten, da bei einem überwiegenden Anteil dieser Nährstoffgruppe die Produktion von Kohlendioxid größer ist als bei einer entsprechenden Energiegewinnung aus Fett (RQ 1 vs. 0,7) wodurch das Atemminutenvolumen und die Atemarbeit gesteigert werden. Daher sollte Fett verstärkt von Patienten mit stark verminderter Lungenfunktion und Neigung zur Hyperkapnie verzehrt werden. Außerdem sollten aufgrund des niedrigen Bestands an Linolsäure vermehrt hochwertige, mehrfach ungesättigte Fettsäuren aufgenommen werden. Geeignete Quellen sind pflanzliche Fette wie Distel- und Maiskeimöl, sowie Pflanzenmargarine ohne gehärtete Fette und Nüsse [7]. Auch Fischöle, deren Omega-3-Fettsäuren auch entzündungshemmend wirken, werden empfohlen [4]. Gelingt es nicht, das Gewicht zu halten oder zu verbessern, kommen Supplementnahrungen, also enterale und parenterale Ernährung in Frage [7].
| Tab. 1: Erkrankungsmanifestationen der cystischen Fibrose in verschiedenen Lebensabschnitten | |
| Neugeborene | Mekoniummileus (10 –15%) Mekoniumpfropf Ikterus neonatorum prolongatus |
| Säuglings- und Kleinkindesalter | pulmonal:
Pneumonie, obstruktive Bronchitis, gastrointestinal:
Chronischer Durchfall, Malabsorptionssyndrom, Gedeihstörung, Rektumprolaps, großes Abdomen, Anämie, Vitaminmangel, |
| Kindesalter | pulmonal:
Bronchiektasen, Asthma, Pneumothorax, gastrointestinal:
Malabsorptionssyndrom, Wachstumsstillstand, distales intestinales Obstruktionssyndrom, |
| Jugend- und Erwachsenenalter | Verzögerte Pubertät Glucoseintoleranz Diabetes mellitus Gallensteine Biliäre Zirrhose portale Hypertension Männliche Sterilität |
| Quelle: [1] | |
Ernährungsintervention nach dem Gewicht
Die Art der Ernährungsintervention orientiert sich vor allem am Längen-Soll-Gewicht (LSG) bzw. dem BMI (vgl. Tabelle 2). Liegt z. B. das LSG unterhalb von 90% bei 2- bis 18-Jährigen, sollte die Ernährungsberatung intensiviert werden. Des Weiteren müssen Supplemente eingesetzt werden, etwa trinkbare Supplemente oder diätetische Lebensmittel mit hoher Energiedichte. Bewirken diese Supplemente keine Besserung bzw. liegt das LSG unterhalb von 85% bei den 2- bis 18-Jährigen, so wird ein invasiver Ernährungssupport unabdingbar, z. B. durch nächtliche Sondenernährung zusätzlich zur täglichen Nahrungsaufnahme, Einsatz von hoch- oder niedermolekularen Formuladiäten als ausschließliche Nahrungszufuhr oder eine kontinuierliche Sondenernährung, die evtl. mit i.v. Ernährung zusätzlich kombiniert wird [5].
Supplemente unerlässlich
Aufgrund der Maldigestion und Malabsorption sind Betroffene hinsichtlich einzelner Nährstoffe nur mangelhaft versorgt. Mithilfe von oral applizierbarer, mikroverkapselter magensaftresistenter Pankreasenzympräparate konnte die Ernährungssituation entscheidend verbessert werden. Dosiert wird in Abhängigkeit der Pankreasaktivität und der individuellen Nahrungsaufnahme. Es wird empfohlen, die Stuhlfettausscheidung zu überprüfen, um die optimale Dosis der Pankreasenzympräparate zu bestimmen [4]. Aufgrund der verminderten Bicarbonatsekretion und einem suboptimalen pH-Wert ist die Wirksamkeit dieser Präparate jedoch nicht mit der Enzymwirksamkeit eines Gesunden zu vergleichen [1]. Auch die Sekretion konjugierter Gallensäuren ist bei Mukoviszidose vermindert, wodurch die Absorption von fettlöslichen Vitaminen eingeschränkt ist. Selbst bei einer optimalen Therapie mit Pankreasenzymen, ist eine Substitution mit fettlöslichen Vitaminen notwendig (siehe auch Kasten "Empfehlungen"). Weiterhin ist der Serumspiegel des Retinol-bindenden Proteins signifikant vermindert und die Resorptionsquote für Retinol liegt lediglich bei 60%. Es ist daher möglich, dass Betroffene aufgrund eines Vitamin-A-Mangels an Nachtblindheit leiden. Daher werden täglich 5000 bis 10.000 IE Retinolpalmitat empfohlen.
| Tab. 2: Ernährungsintervention bei Mukoviszidose – Leitlinie Mukoviszidose (2005) | |||
| < 2 Jahre | 2 – 18 Jahre | > 18 Jahre | |
| Normaler Ernährungszustand, präventive Ernährungsberatung | LSG* 90 –100% | LSG 90 –110% | BMI 18,5 – 25,0 Kein Gewichtsverlust |
| Spezielle Ernährungsberatung, Supplemente | Gedeihstörung | 3.5 Grundschr LSG 85 – 89% Gewichtsverlust über Gewichtsstillstand über | BMI < 18,5 Gewichtsverlust 5% über 2 Monate |
| Invasiver Ernährungssupport | Trotz Supplement: Gedeihstörung | Trotz Supplement: LSG < 85% Gewichtsverlust 2 Perzentilen | Trotz Supplement BMI < 18,5 Gewichtsverlust 5% über 2 Monate |
* LSG: Längen-Soll-Gewicht
Quelle: [3] | |||
Auch in Hinblick auf Vitamin D scheint es eine Unterversorgung zu geben, wenngleich Rachitis, Osteomalazie oder pathologische Frakturen nur vereinzelt auftreten. Studien haben zudem gezeigt, dass bei Mukoviszidose eine Störung der Knochenmineralisation vorliegt, welche aber auch mit einer unzureichenden Calciumresorption bei Steatorrhö zusammenhängen kann.
Wird Vitamin E nicht zusätzlich zugeführt, weisen praktisch alle Mukoviszidose-Patienten mit Fettmalabsorption einen Mangel auf. Besonders betroffen sind diejenigen Patienten mit ausgeprägter Lebererkrankung und schwerer Malnutrition. Vitamin E sollte separat supplementiert werden, da keine ausreichenden Tocopherolmengen in Multivitaminpräparaten enthalten sind [4]. Eine Substitution muss in der Regel nur dann vorgenommen werden, wenn auch die Leber von der Erkrankung betroffen ist.
Wasserlösliche Vitamine müssen generell nicht supplementiert werden. Nur Vitamin B12 sollte nach einer Ileumresektion wegen Mekoniumileus supplementiert werden. Mineralstoffe und Spurenelemente sollten auch über Supplemente zusätzlich aufgenommen werden: Über den Schweiß verlieren Patienten viel Natrium und Chlorid. Für Säuglinge besteht die Gefahr einer hyponaträmischen Dehydratation bzw. hypochlorämischen Alkalose. Ein Mangel an Calcium, Phosphor, Magnesium, Zink und Selen wird im Wesentlichen nur bei Steatorrhö beobachtet. Für Zink und Selen ist ggf. eine Supplementierung notwendig. Bei einem Mangel an Vitamin E darf Selen nicht überdosiert werden, da dies fatale toxische Folgen hat. Spurenelemente sollten auf keinen Fall generell und unkontrolliert supplementiert werden [7].
Empfehlung für einzelne Altersgruppen
Auch Säuglinge mit Mukoviszidose sollten möglichst gestillt werden. Falls dies nicht möglich ist, wird eine Säuglingsmilchnahrung eingesetzt, die ggf. bei Gedeihstörung mit Supplementen energetisch aufgewertet werden kann.
Empfehlungen zur Ernährung bei MukoviszidoseEnergie- und Nährstoffzufuhr:
Besonderheiten
Allgemein zu beachten ist
|
Die Beikost sollte gemäß den Empfehlungen für gesunde Säuglinge eingeführt werden. Bei nicht ausreichendem Gedeihen kann eine Energieanreicherung vorgenommen werden. Zusätzlich benötigen Säuglinge mit Mukoviszidose extra Salzgaben, da mit dem Schweiß viel Salz verloren geht. Fettlösliche Vitamine werden wie bei allen Patienten bereits in diesem Alter supplementiert.
In der Zeit nach dem Kleinkindalter gelten die altersentsprechenden Empfehlungen der Deutschen Gesellschaft für Ernährung. Eine gezielte Lebensmittelauswahl ist wichtig, um die hohe Energiemenge aufnehmen zu können. Im Fokus der Ernährungsberatung steht die Schulung zum ausgewogenen, abwechslungs- und energiereichen Essen verbunden mit einer ausreichenden Enzymeinnahme zu den Mahlzeiten [5].
Literatur [1] Eichler, I. (2005): Zystische Fibrose (Mukoviszidose). In: Speer, C. & Gahr, M.: Pädiatrie. Springer, 2. Auflage, 619 – 627. [2] Ballmann, M. (2010): Mukoviszidose und Diabetes mellitus. Der Diabetologe 1-2010.16 – 22. [3] Palm, B. (2006): Mukoviszidose und Diabetes mellitus – Gibt es diätetische Besonderheiten? Ernährungs-Umschau 53, Heft 9. 360f. [4] Döring, G. (2004): Mukoviszidose. In: Biesalski et al.: Ernährungsmedizin. 3., erweiterte Auflage, Georg Thieme Verlag Stuttgart, 449 – 453. [5] Stern, M. Et al. (2004): Mukoviszidose – Klinik, Diagnostik, Therapie. Ernährungs-Umschau 51, Heft 9. 373 – 375. [6] Wagner, T. (2005): Mukoviszidose. In: Schölmerich, J. (Hrsg.): Medizinische Therapie. Springer, 2. Auflage. 1127 –1138. [7] Wächtershäuser et al.(2002): Ernährung bei Mukoviszidose. Ernährungs-Umschau 49, Heft 10. 380 – 385. [8] Koletzko, S. & Koletzko B. (1993): Zystische Fibrose – Normalernährung oder Ernährungstherapie. In: Koletzko, B. (Hrsg.): Ernährung chronisch kranker Kinder und Jugendlicher. Springer Verlag.167 –190.
Autorin
Katja Aue,
M. Sc. Ökotrophologie
katja_aue@web.de




















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.