
- DAZ.online
- DAZ / AZ
- DAZ 25/2010
- Magnesium Update 2010
Mineralstoffe
Magnesium Update 2010
Stoffwechselfunktionen von Magnesium
Magnesium wirkt über die Interaktion mit Phospholipiden membranstabilisierend und reguliert als Cofaktor der Na+/K+-ATPase die Erregungsleitung in Nerven- und Muskelzellen. Ein Magnesiummangel erhöht die Durchlässigkeit von K+-Kanälen für Kalium, was wiederum Auswirkungen auf das Aktionspotenzial des Herzmuskels hat. Seine antagonistische Wirkung gegenüber Calcium (NMDA-Rezeptor-Antagonist) schützt die Myokardzelle bei ischämischen Perfusionsstörungen vor einer Calciumüberladung. Aufgrund dieser Eigenschaften ökonomisiert Magnesium die kardiale Bioenergetik, wirkt antiarrhythmisch und Blutdruck-regulierend.
Aufgrund seiner vielfältigen Stoffwechselfunktionen (s. Textkasten) ist es nicht verwunderlich, dass eine unzureichende Magnesiumversorgung zu einer Vielzahl an biochemischen Störungen und klinischen Mangelsymptomen führt. Jede Modifikation des endogenen Magnesiumstatus hat Veränderungen des Gefäßtonus und damit des arteriellen Blutdrucks zur Folge.
Wichtige Stoffwechselfunktionen von Magnesium [1]
|
Magnesiumhaushalt
Der Magnesiumgesamtbestand eines 70 kg schweren, gesunden Menschen liegt etwa bei 2000 mval oder 24 g. Mengenmäßig steht damit das Magnesium nach den Alkali-Ionen Natrium und Kalium und dem anderen biologisch wichtigen Erdalkali-Ion Calcium an vierter Stelle. Legt man die Maßeinheit mval zugrunde, so beträgt der Magnesiumgehalt des Organismus etwa die Hälfte desjenigen von Natrium und Kalium. Vom Gesamtkörperbestand sind etwa 50 bis 60% im Knochen und ca. 30% in der Muskulatur lokalisiert. 1% des gesamten Magnesiums befindet sich im Extrazellularraum. Die Verteilung des Magnesiums zwischen Intra- und Extrazellulärraum verläuft im Skelettmuskel zum Teil parallel dem K+-Gradienten an der Zellmembran. Die Serum-Mg2+-Konzentration liegt zwischen 0,8 und 1,2 mmol/l. Davon liegt etwa 60% in freier Form vor, 15% sind komplex gebunden, z. B. in Form von Phosphaten oder Citraten, und 25 bis 32% sind an Proteine, insbesondere Albumine, gebunden. Der Erythrozyten/Serummagnesium-Konzentrationsgradient beträgt ca. 2,5.
In der Zelle ist Magnesium für die Aktivierung von ca. 300 Enzymen und Transportproteinen verantwortlich (s. Textkasten). Erwähnt seien hier einige zytosolische und mitochondriale Enzyme: Die Na+/K+-ATPase benötigt Magnesium ebenso wie die Ca2+-ATPase und H+-ATPase, und bestimmte Ca2+- und K+-Kanäle werden in ihrem Gleichrichtungsverhalten durch Magnesium auf der zytosolischen Seite kontrolliert.
Wichtige magnesiumabhängige Enzyme und Proteine
|
Magnesiumresorption und -exkretion
Die durchschnittliche Magnesiumzufuhr pro Tag beträgt 10 bis 15 mmol, wovon etwa 60 bis 79% wieder mit den Fäzes und 21 bis 40% im Urin ausgeschieden werden. Magnesium wird im Dünndarm resorbiert. Dies bestätigen Isotopenmessungen mit 28Mg. Welche Einflüsse die Resorption fördern bzw. verringern, ist noch nicht restlos geklärt. So führt eine gesteigerte Zufuhr an Magnesium nicht linear zu einer steigenden Magnesiumresorption und Ausscheidung durch die Nieren. Je höher die orale Zufuhr von Magnesium ist, desto geringer wird die Resorptionsrate. Von wichtiger Bedeutung ist hierbei die physiologische Ausgangslage der Magnesiumspiegel. Bei einem Magnesiummangel wird mehr, bei Absättigung mit Magnesium weniger resorbiert. So kann bei einem ausgeglichenen Magnesiumhaushalt trotz hoher oraler Magnesiumgaben keine wesentlich gesteigerte Magnesiumspeicherung über den oberen Normbereich hinaus erzielt werden.
Die Ausscheidung des im Darm resorbierten Magnesiums erfolgt überwiegend renal. Um einen signifikanten Anstieg der Serummagnesiumkonzentration im Blut zu vermeiden, erfolgt die Ausscheidung dort außerordentlich rasch. Dies erklärt unter anderem die lange Austauschzeit zwischen dem zellulären Magnesiumpool und dem extrazellulären Magnesium.
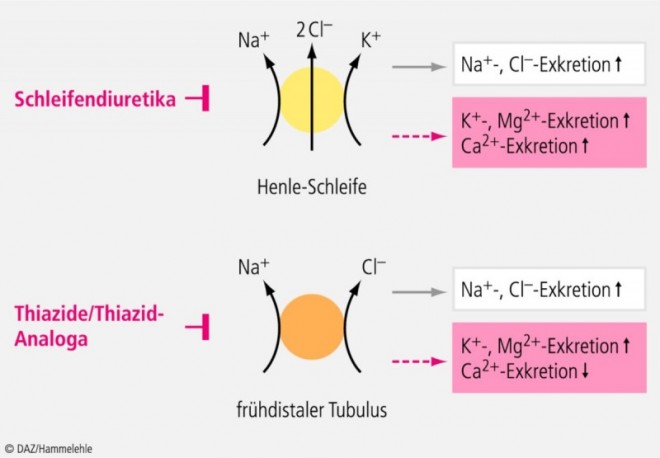
Die glomeruläre Filtration von Magnesium ist aufgrund der Proteinbindung inkomplett. Hinzu kommt durch die Gibbs-Donnan-Verteilung eine geringfügige weitere Abnahme der Konzentration auf der Bowman-Kapsel-(Filtrat-)Seite. Die Rückresorption von Magnesium im proximalen Tubulus ist an die Na+-Rückresorption gekoppelt und bei Hypovolämie gesteigert bzw. bei Hypervolämie vermindert. Hiermit hängen auch die Effekte der Mineralo- und Glucocorticoide auf die Magnesiumausscheidung zusammen. Eine vermehrte Sekretion von Mineralo- und Glucocorticoiden führt zu einer vermehrten Magnesiumausscheidung, während umgekehrt ein Mangel dieser Hormone eine Verminderung der Magnesiumausscheidung bewirkt. Die Magnesiumresorption in der Henleschen Schleife wird durch eine Zunahme der extrazellulären Ca2+-Konzentration vermindert. Man nimmt eine Kompetition zwischen Ca2+ und Mg2+ in Bezug auf die Resorption in der Henleschen Schleife an. Der Magnesiumtransport in der Henleschen Schleife ist mit dem Chloridtransport gekoppelt. Alle Diuretika, die zu einer vermehrten K+-Ausscheidung führen (Thiazide, Schleifendiuretika, Carboanhydrasehemmer), verursachen auch eine gesteigerte Magnesiumexkretion (Abb. 1), nicht dagegen K+-sparende Diuretika [17]. Die Gründe hierfür sind nicht im Einzelnen bekannt [13].
Unter den hormonalen Effekten sind neben den Steroidwirkungen die des Parathormons zu erwähnen. Das Parathormon bewirkt eine Zunahme der Magnesiumresorption, die allerdings durch die entgegengesetzten Effekte der Hyperkalzämie ganz oder teilweise antagonisiert wird. Daher erklären sich auch die unterschiedlichen Befunde hinsichtlich Magnesiumexkretion beim primären Hyperparathyreoidismus.
Die Magnesiumausscheidung ist auch beim Morbus Addison sowie bei der Gabe eines Aldosteronantagonisten (Spironolacton) geringfügig herabgesetzt. Diese Beobachtung ist allerdings in der Regel nicht von klinischer Bedeutung.
Da fast bis zu 79% des zugeführten Magnesiums mit dem Stuhlgang verloren gehen können ("Stuhlion"), ergeben sich Schwierigkeiten bei der Magnesiumresorption im Darm, z. B. bei Diarrhöen. Wenn bei einem intrazellulären Magnesiummangel eine erhöhte neuromuskuläre Erregbarkeit der glatten Muskulatur im Darm besteht, als deren Folge Diarrhö auftreten kann, zieht diese wiederum eine Minderresorption von Magnesium nach sich.
Magnesiummangel
Die klinische Bedeutung der Magnesiumüberladung oder Magnesiumintoxikation ist eher gering. Ein Magnesiummangel beim Menschen tritt jedoch häufig auf (s. Textkasten); er kann trotz normaler Ernährung nicht immer komplett ausgeglichen werden. Als primären Effekt eines Magnesiummangels beobachtet man eine Reduktion von Enzymaktivitäten mit Schrittmacheraufgaben in den Stoffwechselwegen der Energieproduktion. Die beeinträchtigte Energieproduktion wirkt sich auf die Membranfunktion, die intrazelluläre Calcium-Relokation, Elektrolytgradienten, die Bildung von sekundären Botenstoffen und auf Syntheseaufgaben der Zelle aus.
Ursachen für einen Mangel bzw. erhöhten Bedarf an Magnesium
|
Daraus resultieren Konsequenzen für die Funktion der Organe und das Ausmaß der Reaktion des menschlichen Körpers auf äußeren und inneren Stress. Ein Magnesiummangel begünstigt die Entwicklung eines Hochdruckes und steigert das Risiko für atherothrombotische Ereignisse. Im Krankheitszustand begrenzt der eingeschränkte Energiestatus die Prognose des Patienten und verstärkt klinische Zeichen der Krankheit, wie z. B. Arrhythmien, Hypertonie, Präeklampsie und allergische Reaktionen. Der Stellenwert einer oralen oder parenteralen Magnesiumtherapie ist bei einer Vielzahl von Erkrankungen gut dokumentiert. Hierzu stehen verschiedene Magnesiumpräparate oder supportive Maßnahmen zur Verfügung.
Magnesium und Hypertonie
In letzter Zeit mehren sich die Beobachtungen, dass auch Magnesiummangel neben anderen Elektrolytstörungen die Entwicklung eines Hochdruckes begünstigen kann [2 – 12]. Zahlreiche Untersuchungen liegen diesbezüglich an Erythrozyten, Lymphozyten, Thrombozyten, Zellmembranen oder glatten Gefäßmuskelzellen vor, Daten, die vielfach auch von unserer Arbeitsgruppe publiziert worden sind [2 – 9].
Bereits 1960 konnte unsere Arbeitsgruppe erstmals nachweisen, dass bei primärer essenzieller Hypertonie die intrazellulären Natriumkonzentrationen der Erythrozyten erhöht waren. Zunächst waren wir und andere Untersucher davon ausgegangen, dass diese erhöhte Natriumkonzentration, die später auch in der Gefäßwand hypertoner Ratten nachgewiesen werden konnte, für die Hochdruckentwicklung entscheidend sei. Es wurde angenommen, dass der sog. Natriumgradient der Gefäßmuskelzelle entscheidend für den Tonus der Gefäßwand und damit für die Blutdruckhöhe sei. Spätere Untersuchungen ergaben jedoch, dass bei essenzieller Hypertonie nicht nur die intrazelluläre Natriumkonzentration erhöht ist, sondern außerdem die intrazelluläre Calciumaktivität. Diese Zunahme des intrazellulären Calciums dürfte aus heutiger Sicht letztlich für den erhöhten Gefäßtonus bei Hypertonikern und damit für die Hochdruckentwicklung bedeutsam sein [12].
Als Ursache für einen Anstieg der intrazellulären Calciumaktivität bei Hypertonie kommen mehrere Faktoren in Frage. Einer dieser Faktoren dürfte eine Anreicherung von Natrium in der Zelle sein, daneben ist jedoch anzunehmen, dass auch andere Elektrolyte die intrazelluläre Calciumkonzentration beeinflussen können. Hier ist zunächst der Kaliumhaushalt zu nennen. Es ist seit langem bekannt, dass Hypokaliämie die medikamentöse Einstellung eines Hochdruckes ungünstig beeinflusst. Andererseits ließ sich tierexperimentell und auch klinisch nachweisen, dass die Zufuhr von Kalium blutdrucksenkend wirkt.
Zahlreiche Untersuchungen belegen, dass es auch bei einem Magnesiummangel nicht nur zu einer Abnahme der intrazellulären Magnesiumkonzentration kommt, sondern dass gleichzeitig die intrazellulären Natrium- und Calciumkonzentrationen ansteigen und die Kaliumwerte sinken [12].
Eine Reihe von Untersuchungen zeigen außerdem, dass, bezogen auf den Elektrolythaushalt, die intrazelluläre Calciumaktivität im Mittelpunkt der Pathogenese der essenziellen Hypertonie steht. Da eine erhöhte Calciumaktivität außer durch eine vermehrte Natriumzufuhr auch durch einen Kalium- bzw. Magnesiummangel entstehen kann, ergeben sich wichtige therapeutische Konsequenzen. An Erythrozytenmembranen konnten wir ebenso wie andere Arbeitsgruppen einen Natrium-Magnesium-Antiport beschreiben [4 – 7]. Zum einen ist danach eine Hypokaliämie bzw. Hypomagnesiämie ungünstig. Zum anderen ist denkbar, dass durch Magnesiumgaben auch bei normaler extrazellulärer Magnesiumkonzentration eine Blutdrucksenkung über die Beeinflussung der intrazellulären Calciumaktivität möglich ist, via Calmodulinkomplex und Kontraktion der Muskelfilamente, die ebenso über ATP-Verbrauch Magnesium- und Phosphat-abhängig ist, wie wir an glatten Gefäßmuskellzellen nachweisen konnten. Dann wäre Magnesium möglicherweise als physiologischer Calciumantagonist bei der Hochdrucktherapie einzusetzen. Auch wenn allein durch Magnesiumgaben eine Blutdrucknormalisierung bei Hypertonie Schweregrad II oder III nach WHO-Kriterien nicht zu erwarten ist, so könnte doch durch die gleichzeitige Gabe von Magnesium eine Verminderung der Dosierung anderer antihypertensiv wirkender Substanzen angestrebt werden. Hierdurch ließen sich zahlreiche durch die Hochdrucktherapie bedingte Nebenwirkungen vermindern.
Die Ergebnisse einer großen Metaanalyse aus dem Jahr 2002 zeigen, dass der blutdrucksenkende Effekt von oral zugeführtem Magnesium dosisabhängig ist. Mit jeder Zunahme der täglichen Magnesiumdosis um 10 mmol sank der systolische Blutdruck um 4,3 mmHg und der diastolische Blutdruck um 2,3 mmHg [18, 19]. In einer weiteren Studie, die den Einfluss von Antihypertonika auf den Magnesiumhaushalt erfasste, wurde gezeigt, dass Bluthochdruckpatienten unter einer antihypertensiven Therapie (z. B. Diuretika, ACE-Hemmer, Betablocker) im Vergleich zu Kontrollen häufig einen defizitären Magnesiumstatus aufweisen. Die Kompensation des Magnesiumdefizits durch Magnesiumsupplemente führte hierbei neben einem hoch signifikanten Anstieg des Magnesiumblutspiegels zu einer durchschnittlichen Abnahme des systolischen Blutdrucks um 15 bis 20 mmHg und des diastolischen Blutdrucks um 5 bis 9 mmHg. Auch die Häufigkeit von typischen Beschwerden wie unregelmäßiger Herzrhythmus, Herzschmerzen, Schlafstörungen oder Nervosität nahm nach Berichten der Patienten in dieser Studie unter der oralen Supplementierung von Magnesium (320 mg/d, p.o.) ab [19, 20].
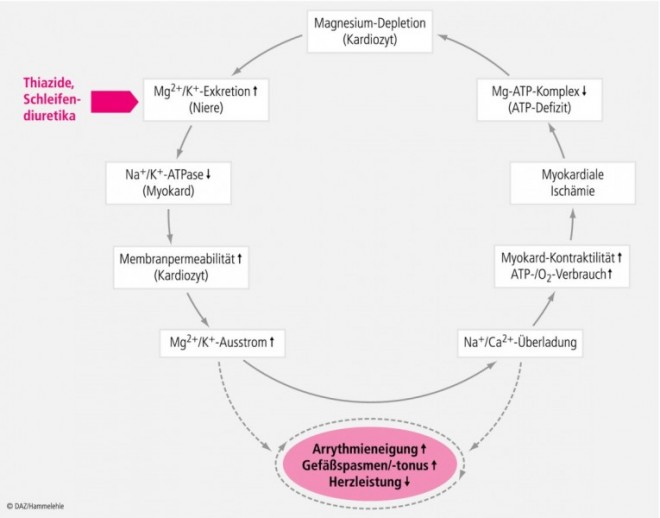
Bei einer Langzeittherapie mit Schleifendiuretika oder Thiaziden sind Magnesium- und Kaliummängel von großer klinischer Bedeutung, da eine Hypomagnesiämie und/oder -kaliämie das Auftreten kardiovaskulärer Komplikationen (z. B. Arrhythmien) sowie diuretikaassoziierter Störungen der Glucosetoleranz und des Lipidstoffwechsels begünstigt (Abb. 2).
Ebenso kann sich ein Magnesiummangel ungünstig bei der Entstehung einer Arteriosklerose auswirken. Eine vermehrte Intima-media-Dicke der Arteria carotis communis wurde von uns kürzlich beschrieben. Ein Magnesiummangel beeinflusst ferner die Höhe des Pulsdruckes (Differenz zwischen systolischem und diastolischem Blutdruck). Ein hoher Pulsdruck (z. B. > 66 mmHg) begünstigt das Auftreten von Hypertonie, Arteriosklerose, Schlaganfall oder Herzinfarkt. Auch hierbei spielt ein Magnesiummangel eine wichtige Rolle [4 – 7, 9 – 12]. In einer kürzlich veröffentlichten Studie (MACH-Studie), die an Patienten mit schwerer Herzinsuffizienz (NYHA III und IV) durchgeführt wurde, konnte gezeigt werden, dass eine orale Gabe von Magnesiumorotat (1. Monat: 6000 mg Mg-Orotat/d, p.o., 2. bis 12. Monat: 3000 mg Mg-Orotat/d, p.o.) nicht nur die Sterblichkeit infolge der Erkrankung vermindert, sondern auch die Herzfunktion im Vergleich zu Plazebo signifikant verbessert [24].
Magnesium und Diabetes mellitus
Ferner spielt ein Magnesiummangel bei der Entstehung von Diabetes mellitus eine wichtige Rolle. Eine erniedrigte intrazelluläre Magnesiumkonzentration ist eine wesentliche pathophysiologische Ursache für die Insulinresistenz. Durch Beeinflussung der Tyrosinkinase-Aktivität des Insulinrezeptors und der Signalweiterleitung ins Zytosol verbessert ein physiologischer Magnesiumspiegel die Glucoseutilisation [13]. In einer Reihe von klinischen Studien konnte gezeigt werden, dass die tägliche Supplementierung von Magnesium (z. B. 300 mg/d als MgCl2) die Insulinsensitivität sowohl bei Prädiabetikern als auch bei manifesten Diabetikern verbessert. Magnesium kann bei Diabetikern auch die Einstellung des Blutzuckerspiegels erleichtern [14, 15].
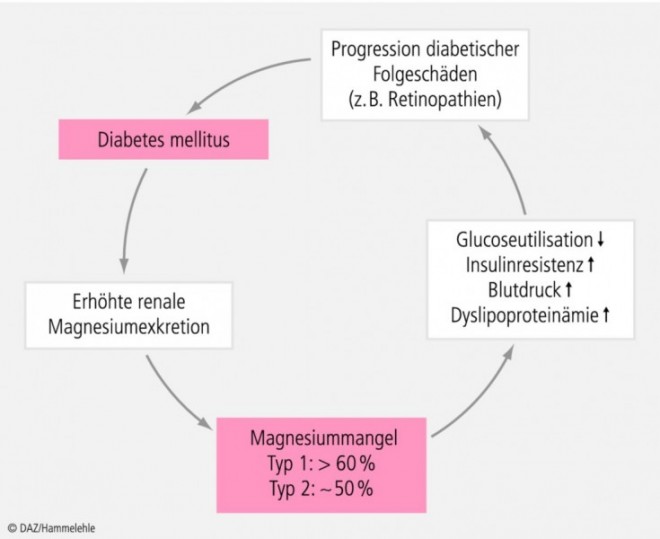
Diabetiker – besonders jene mit nicht optimaler metabolischer Kontrolle – weisen durch die erhöhte osmotische Diurese zum Teil schwere renale Magnesiumverluste auf, die zu chronischem Magnesiummangel führen [16]. Zahlreiche Studien zeigen ein deutlich häufigeres Auftreten von Hypomagnesiämien bei Diabetikern und eine erhöhte Insulinresistenz bzw. schlechtere Glucosetoleranz bei Personen mit niedriger Serum-Magnesium-Konzentrationen (Abb. 3). Bei hoher diätetischer Magnesiumzufuhr konnte hingegen eine verminderte Insulinresistenz nachgewiesen werden [13, 17].
In diesem Zusammenhang zeigen große epidemiologische Studien der letzten 10 bis 20 Jahre eine inverse Korrelation zwischen dem Risiko, an Diabetes mellitus zu erkranken, und sowohl der Serum-Magnesium-Konzentration als auch der diätetischen Magnesiumzufuhr [13, 17]. In der ARIC-Studie an 12.128 Patienten wurde bei niedriger Serum-Magnesium-Kozentration ein um 55% erhöhtes Diabetesrisiko beobachtet. Mit Bestimmung der sensitiven ionisierten Magnesiumkonzentrationen wurde bei 50% eines Diabetes-Typ-2-Kollektivs ein Magnesiummangel festgestellt.
Ferner belegen mehrere Untersuchungen, dass ein ausgeglichener Magnesiumhaushalt das Risiko für die Entwicklung von diabetischen Folgeerkrankungen signifikant verringert. Die diabetische Retinopathie ist bei Diabetikern mit niedrigem Magnesiumstatus häufiger und der Schweregrad höher als bei Diabetikern mit gutem Magnesiumstatus. Ebenso tritt die diabetische Polyneuropathie häufiger bei schlechtem Magnesiumstatus auf und bessert sich signifikant durch die Supplementierung von Magnesium [21].
Der gleiche Zusammenhang zeigt sich für das Auftreten einer Depression bei Diabetikern. Eine Supplementierung von Magnesium (450 mg/d, p.o.) war bei Diabetikern mit depressiver Symptomatik gleich wirksam wie das Antidepressivum Imipramin (50 mg/d, p.o.) [22, 23].
In der neuen Leitlinie Magnesium und Diabetes der Gesellschaft für Magnesiumforschung e.V. wird deshalb empfohlen, bereits bei Serum-Magnesium-Konzentrationen ≤ 0,80 mmol/l mit einer Magnesiumtherapie zu beginnen [13]. Empfohlen wird in diesem Zusammenhang die tägliche Substitution von 240 bis 480 mg (10 bis 20 mmol) Magnesium pro Tag (z. B. als Magnesiumorotat, ‑citrat oder -aspartat).
In Einzelfällen kann eine wesentlich höhere Dauertherapie sinnvoll sein, in vielen Fällen ist auch eine Dauertherapie erforderlich. Bei diesen Patienten ist Magnesium gut kombinierbar mit den gängigen Antidiabetika (Metformin, Glitazone, Sulfonylharnstoffe, Glinide, Insulin) und Antihypertensiva.
Resorption von Magnesiumverbindungen
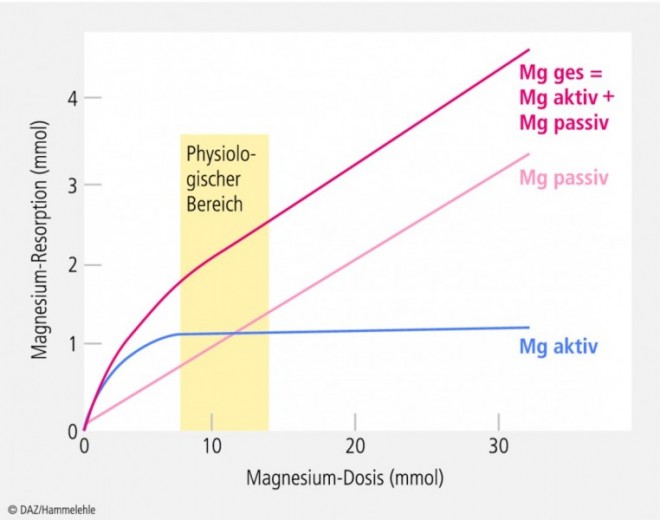
Magnesium wird im distalen Abschnitt des Dünndarms zum einen transzellulär über einen aktiven Carrier-vermittelten Prozess und zum anderen parazellulär mittels passiver Diffusion resorbiert. Untersuchungen zur familiären Hypomagnesiämie mit sekundärer Hypokalzämie zeigen, dass die Carrier-vermittelte Resorption über einen Transporter in der Darmwand, den Ionenkanal TRPM6, erfolgt. Eine TRPM6-Mutation ist mit einer Störung der intestinalen Resorption und renalen Konservierung des Mineralstoffs assoziiert. Der aktive sättigbare TRPM6-vermittelte Prozess spielt vor allem bei geringer diätetischer Magnesiumaufnahme eine Rolle, während bei höherer Zufuhr Magnesium zunehmend passiv resorbiert wird. Die passive Resorption verläuft über weite Bereiche linear in Abhängigkeit von der Magnesiumzufuhr (Abb. 4) [25, 26].
Die Resorption und Bioverfügbarkeit von Magnesium ist von zahlreichen Faktoren abhängig, wie z. B. Zusammensetzung der Nahrung (z. B. Resorptionshemmer: Oxalate, Phosphate, Phytate), Versorgungsstatus des Körpers, Dosis, Art und Löslichkeit der Magnesiumverbindungen, Darmmotilität und Flüssigkeitsaufnahme. Da die Magnesiumexkretion mit dem Urin sehr rasch verläuft und Magnesium in den Zellen nur langsam retiniert wird, entspricht der resorbierte Anteil des diätetischen Magnesiums überwiegend dem im Urin ausgeschiedenen Magnesium. Nur eine langfristige Supplementierung von Magnesium erhöht folglich die zellulären Magnesiumspiegel.
Magnesium ist aus einer gemischten Kost zu 30 bis 55% bioverfügbar. Die Bioverfügbarkeit von Magnesium aus magnesiumreichen Mineralwässern (> 110 mg Magnesium pro Liter) liegt bei etwa 45% und nimmt bei gleichzeitiger Nahrungszufuhr um bis zu 14% zu [27]. Bemerkenswert ist, dass die Resorptionsrate im Darm bei niedriger Magnesiumzufuhr oder bei einem Magnesiummangel ansteigt. Eine Untersuchung von Fine und Mitarbeitern zeigt, dass bei einer täglichen Magnesiumzufuhr von 36 mg (3 mEq) Magnesium noch 65% resorbiert werden, während bei einer täglichen Zufuhr von 973 mg (80 mEq) Magnesium mit der Nahrung nur 11% aufgenommen werden [28, 29]. Die relative Magnesiumresorption nimmt also mit zunehmender Menge ab.
In der Prävention und Therapie von Magnesiummangelzuständen werden unterschiedliche Magnesiumverbindungen eingesetzt:
- Anorganische gebundene Magnesiumsalze (z. B. Mg-Carbonat, -Chlorid, -Oxid, -Sulfat);
- Organische gebundene Magnesiumsalze (z. B. Mg-Aspartat, -Aspartat-hydrochlorid, ‑Citrat, ‑Gluconat, -Orotat).
Vergleicht man die Ergebnisse von Studien zur Bioverfügbarkeit der verschiedenen Magnesiumverbindungen, so ergibt sich insgesamt ein Bild, dass anorganische Magnesiumsalze (Ausnahme: Magnesiumchlorid) eine deutlich geringere intestinale Bioverfügbarkeit aufweisen als organische Magnesiumsalze [30 – 36].
Die Überprüfung der oralen Bioverfügbarkeit anorganischer und organischer Magnesiumsalze wird in den meisten Studien indirekt bestimmt. Gesunde Studienteilnehmer mit einem ausgeglichenen Magnesiumhaushalt nehmen dabei unter kontrollierten Bedingungen eine definierte Menge Magnesium ein (z. B. Gruppe 1: 300 mg Magnesium als Magnesiumcitrat; Gruppe 2: 300 mg Magnesium als Magnesiumoxid). Da die Ausscheidung von Magnesium nach der Resorption im Darm überwiegend mit dem Urin erfolgt, wird in den nun folgenden Stunden bei beiden Gruppen die ausgeschiedene Magnesiummenge im Urin bestimmt. Für die Überprüfung der resorbierten Magnesiummenge aus verschiedenen Magnesiumsalzen ist diese Messmethode gut geeignet. Bei einer Person mit einem ausgeglichenen Magnesiumstatus wird nämlich die überschüssige Menge an Magnesium, die im Darm aus den eingenommenen Supplementen resorbiert wurde, überwiegend wieder mit dem Urin ausgeschieden. Das bedeutet: Bei einer guten oralen Bioverfügbarkeit eines Magnesiumsalzes wird bei diesem Test Magnesium im Darm resorbiert, und die Magnesiumausscheidung im Urin steigt entsprechend an. Bei einer geringen intestinalen Bioverfügbarkeit wird wenig Magnesium über den Darm aufgenommen und entsprechend viel Magnesium, das nicht resorbiert wurde, wieder mit dem Stuhl ausgeschieden.
Walker et al. untersuchten bei 46 gesunden Personen in einer randomisierten, plazebokontrollierten Doppelblindstudie die orale Bioverfügbarkeit von drei verschiedenen Magnesiumverbindungen: Magnesiumcitrat, Magnesium-Aminosäuren-Chelat und Magnesiumoxid. Dabei wurde der Magnesiumgehalt im Urin, im Blut und im Speichel bei Studienbeginn, akut (24 h nach der ersten Magnesiumeinnahme) sowie nach 60-tägiger Einnahme von 300 mg Magnesium pro Tag (12,4 mmol/d) verglichen. Bei den Studienteilnehmern, welche die beiden organisch gebundenen Magnesiumsalze einnahmen, lag die zusätzliche Magnesium-Ausscheidung im 24h-Urin nach 60-tägiger Einnahme bei etwa 1,5 bis 2 mmol. Obwohl die durchschnittliche Magnesiumkonzentration in den Erythrozyten (Parameter, der eine Aussage über den individuellen Magnesiumstatus macht) keinen Unterschied zwischen den Gruppen aufwies, konnte nach Einnahme von Magnesiumoxid kein Anstieg der Magnesiumexkretion im Urin beobachtet werden [35].
Mühlbauer et al. verglichen in einer Studie an 24 Probanden die intestinale Resorption von Magnesium aus Magnesium-L-Aspartat-hydrochlorid (MAH) mit derjenigen aus Magnesiumoxid. Nach einer täglichen Einnahme von 720 mg (30 mmol) bzw. 1080 mg (45 mmol) Magnesium pro Tag über sieben Tage ergab sich dabei folgendes Bild: Die orale Bioverfügbarkeit von Magnesiumoxid nach siebentägiger Einnahme, gemessen anhand des Anstiegs der renalen Magnesiumexkretion, betrug nur etwa 65% bzw. 45% des Magnesiums aus Magnesium-L-Aspartat-hydrochlorid [34, 37].
Firoz und Gaber untersuchten die orale Bioverfügbarkeit von Magnesiumaspartat, Magnesiumlactat, Magnesiumchlorid und Magnesiumoxid an 16 gesunden Probanden (Magnesium-gesättigt), die täglich 255 mg Magnesium (10,5 mmol) einnahmen. Die Gesamttagesdosierung wurde wie folgt zugeführt:
3 × 1 Magnesiumoxid-Kapsel oder 2 × 2 Magnesiumaspartat-Tabletten oder 2 × 2 Magnesiumchlorid-Tabletten oder 3 × 1 Magnesiumlactat-Tablette. Dabei war die zusätzliche renale Magnesiumausscheidung unter der Einnahme von Magnesiumaspartat, Magnesiumchlorid oder Magnesiumlactat in etwa vergleichbar (25 mg/d, 30 mg/d bzw. 29 mg/d), während die Einnahme von Magnesiumoxid mit einer geringeren Magnesiumausscheidung (10 mg/d) assoziiert war [31].
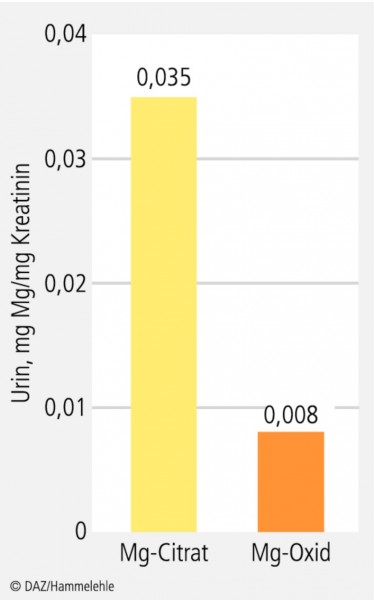
Lindberg et al. verglichen in einer Studie an 17 gesunden Probanden die intestinale Bioverfügbarkeit von Magnesiumoxid und Magnesiumcitrat. Beide Magnesiumverbindungen wurden in einer Dosierung von 608 mg Magnesium (25 mmol) oral verabreicht. Der Anstieg der renalen Magnesiumexkretion, als Maß für die orale Bioverfügbarkeit, war nach der Einnahme von Magnesiumcitrat bis zu viermal so hoch wie der Anstieg nach der Einnahme von Magnesiumoxid (während 4 h post-load: 0,022 mg vs. 0,006 mg Magnesium/mg Kreatinin; nach weiteren 2 h post-load: 0,035 mg vs. 0,008 mg Magnesium/mg Kreatinin) (Abb. 5) [36].
Bei Studien, die gerne als Hinweis auf die Gleichwertigkeit von Magnesiumoxid mit organischen Magnesiumverbindungen (z. B. Magnesiumcitrat, Magnesiumaspartat) zitiert werden [38 – 43], sollte genau auf die eingesetzten Magnesiumsalze und auf die Dosierung geachtet werden. Die orale Bioverfügbarkeit von Magnesiumoxid wurde darin häufig gar nicht untersucht, insbesondere nicht der direkte Vergleich zwischen Magnesiumoxid und Magnesiumcitrat. In einer Studie von Schütte wurden Magnesium-Diglycinat und Magnesiumoxid untersucht. Diese Studie wurde jedoch nicht an gesunden Probanden durchgeführt – wie bei Bioverfügbarkeitsstudien üblich –, sondern mit Patienten, denen ein Teil des Dünndarms entfernt worden war (Ileumresektion). Aufgrund der dadurch bedingten allgemeinen schweren Malabsorption der Studienteilnehmer besitzt diese Studie schon per se keine Aussagekraft. Zudem war bei den Patienten mit der größten Resorptionsstörung das organische Magnesium-Diglycinat signifikant besser bioverfügbar als Magnesiumoxid. Auch fand sich bei Magnesium-Diglycinat ein signifikant schnellerer Anstieg des Magnesiumspiegels im Plasma als bei Magnesiumoxid [43].
Empfehlung
Im Hinblick auf die degressive Resorption von Magnesium ist es empfehlenswert, die Gesamttagesdosis über den Tag auf kleine Einzelportionen aufzuteilen. Magnesium – wie auch Calciumsalze in Form von Brausetabletten oder Granulaten – sollten in einer gut bioverfügbaren Form mit ausreichend Flüssigkeit (z. B. 300 mg Magnesium in 750 ml Wasser) über den Tag verteilt zugeführt werden.
Zusammenfassung
- Magnesium kommt in nahezu allen Organen vor und spielt im Kohlenhydrat- und Eiweißstoffwechsel sowie bei fast allen enzymatischen Vorgängen eine wichtige Rolle.
- Als essenzielles Mineral muss es dem Körper mit der Nahrung zugeführt werden.
- Magnesiumintoxikationen sind selten.
- Ein Magnesiummangelsyndrom ist gekennzeichnet durch zerebrale Formen (Kopfdruck, Schwindel, Ataxie, Benommenheit), durch Herzrhythmusstörungen, muskulär-tetanische Formen und Spasmen der glatten Muskulatur, Bluthochdruck und Pulsdruckerhöhung sowie Arterioskleroseentstehung.
- Zur Beurteilung der Intaktheit des Magnesiumhaushalts sind Serum-Mg2+ -Spiegel nur bedingt aussagekräftig.
- Zur Behebung des Magnesiummangels sind magnesiumreiche Nahrungsmittel vorzuziehen, therapeutisch stehen auch verschiedene Magnesiumpräparate, Mineral-, Heilwässer und Spezialsalze zur Verfügung (Tab. 1).
- Von besonderer Bedeutung ist die Substitution von Magnesium bei Patienten mit Hypertonie und Diabetes mellitus, besonders wenn schwere Magnesiummangelzustände bei diesen Patienten vorliegen. Anders als früher wird hier eine höhere Dosierung von Magnesium, manchmal im Grammbereich, empfohlen.
| Tab. 1: Indikationen für eine Magnesiumtherapie (p. o., i. v.) | |
| Betroffenes Organ, Stoffwechsel | Erkrankung |
| Atemwege | Asthma bronchiale, Rhinitis allergica |
| Fettstoffwechsel | Dyslipoproteinämie (v. a. Triglyceridämie) |
| Gastrointestinaltrakt | Chronisch entzündliche Darmerkrankungen, Colon irritable, Malabsorptionssyndrome (z. B. Zöliakie, Sprue), Laxanzientherapie |
| Harnwege | Urolithiasis: Calciumoxalatsteine (Rezidivprophylaxe → Magnesiumcitrat) |
| Herz-Kreislauf-System | Hypertonie, Herzrhythmusstörungen (ventrikuläre Arrhythmien, Digitalis-assoziierte Rhythmusstörungen), ischämische Herzerkrankung, Herzinsuffizienz, Therapie mit Diuretika und/oder Herzglykosiden |
| Knochen | Osteoporose, extraossäre Verkalkungen (Myositis ossificans) |
| Kohlenhydratstoffwechsel | Diabetes mellitus Typ 1 und Typ 2, diabetische Polyneuropathie, diabetische Retinopathie (auch Kombination mit Benfotiamin), Insulinresistenz, Prädiabetes |
| Mineralstoffhaushalt | Magnesiummangel |
| Mitochondrien | Mitochondriopathien |
| Muskulatur | Muskelkrämpfe (z. B. Waden), Muskelspasmen, Gefäßspasmen (kardial, zerebral?) |
| Neurologische Erkrankungen | Migräne, Hörsturz, Neugeborenenkrämpfe, normokalzämische Tetanie |
| Neuropsychiatrische Erkrankungen | ADHS, Depressionen (auch Kombination mit DHA/EPA) |
| Weibliche Sexualorgane (Gynäkologie) | Dysmenorrhö, PMS, Eklampsie, vorzeitige Wehen (Tokolyse) |
Zum WeiterlesenMagnesium und Mg-Verbindungen in Supplementen
|
Literatur [1] Gröber U. Mikronährstoffe. Metabolic Tuning – Prävention – Therapie. Wissenschaftliche Verlagsgesellschaft, Stuttgart (in Vorbereitung). [2] Altura BM, Altura BT. Cardiovascular risk factors and magnesium: relationship to atherosclerosis, ischemic heart disease and hypertension. Magnes Trace Elem 1991;10:182 – 192. [3] Kisters K, et al. Decreased cellular magnesium concentrations in a subgroup of hypertensives – cell models for the pathogenesis of primary hypertension. Hum Hypertens 1997;11:367 – 372. [4] Kisters K, et al. Decreased cellular magnesium concentrations in a subgroup of hypertensives. Membrane model for the pathogenesis of primary hypertension. Am J Hypertens 1998;11:1390 – 1393. [5] Resnick LM, et al. Divalent cations in essential hypertension: relations between serum ionised calcium, magnesium and plasma renin activity. N Engl J Med 1983;309: 888 – 891. [6] Kisters K, et al. Importance of decreased intracellular phosphate and magnesium concentrations and reduced ATPase activities in SHR. Magnes Res 2000;13:183 – 188. [7] Seelig M. The magnesium factor. Penguin Group (USA) Inc., New York 2003. [8] Kisters K, Gremmler B, Hausberg M. Magnesium and arterial stiffness. Hypertension 2005; Epub. [9] Kisters K, et al. Magnesium und Pulsdruck bei Hypertonie. Nieren Hochdruckkrh 2005;34(10):455 – 457. [10] Kisters K, Gremmler B, Hausberg M. Disturbed Mg++ transporters in hypertension. J Hypertens 2008;26(12):2450 – 2451. [11] Kisters K. Der Magnesiumhaushalt in der Inneren- und Intensivmedizin. Nieren Hochdruckkrh 2010;39(5):182 – 194. [12] Büntzel J, Kisters K, Micke O, Mücke R. Zytoprotektion, Spurenelemente und Elektrolyte in der Tumortherapie. Dustri Verlag Dr. Karl Feistle, Oberhaching 2004. [13] von Ehrlich B, et al (Gesellschaft für Magnesiumforschung e.V.). Leitlinie Magnesium und Diabetes. Nieren Hochdruckkrh 2009;38(12):633 – 635. [14] Guerro-Romero F, et al. Oral magnesium supplementation improves insulin sensitivity in non-diabetic subjects with insulin resistance. A double-blind placebo-controlled randomized trial. Diabetes Metab 2004;30(3):253 – 258. [15] Rodriguez-Moran M, et al. Oral magnesium supplementation improves insulin sensitivity and metabolic control in type-2 diabetic subjects: a randomized double-blind controlled trial. Diabetes Care 2003;26(4):1147 – 1152. [16] Rob PM, et al. Can one really measure magnesium deficiency using the short-term magnesium loading test? J Intern Med 1999;246:373 – 378. [17] Rude RK. Magnesium deficiency and diabetes mellitus. Causes and effects. Postgrad Med 1992;92:217 – 219. [18] Jee SH, et al. The effect of magnesium supplementation on blood pressure: a meta-analysis of randomized clinical trials. Am J Hypertens 2002;15(8):691 – 696. [19] Gröber U. Antihypertensives and magnesium – update 2007. Trace Elements Electrolytes 2009;26(1):15 – 16. [20] Michón P. Level of total and ionized magnesium fraction based on biochemical analysis of blood and hair and effect of supplemented magnesium (Slow Mag B6) on selected parameters in hypertension of patients treated with various groups of drugs. Am Acad Med Stetin 2002;48:85 – 97. [21] De Leeuw I, et al. Long term magnesium supplementation influences favourably the natural evolution of neuropathy in Mg-depleted type 1 diabetic patients (T1dm). Magnes Res 2004;17(2):109 – 114. [22] Barragan-Rodriguez L, et al. Depressive symptoms and hypomagnesemia in older diabetic subjects. Arch Med Res 2007;38(7):752 – 756. [23] Barragan-Rodriguez L, et al. Efficacy and safety of oral magnesium supplementation in the treatment of depression in elderly type 2 diabetes: a randomized, equivalent trial. Magnes Res 2008;24(4):218 – 223. [24] Stepura OB, Martynow AI. Magnesium orotate in severe congestive heart failure (MACH). Int J Cardiol 2009;131: 293 – 295. [25] Walder RY, et al. Mutation of TRPM6 causes familial hypomagnesemia with secondary hypocalcemia. Nat Genet 2002;31:171 – 174. [26] Hardwick LL, et al. Magnesium absorption: mechanisms and the influence of vitamin D, calcium and phosphate. J Nutr 1991;121(1):13 – 23. [27] Sabatier M, et al. Meal effect on magnesium bioavailability from mineral water in healthy women. Am J Clin Nutr 2002;75(1):65 – 71. [28] Sabatier M, et al. Comparison of stable-isotope-tracer methods for the determination of magnesium absorption in humans. Am J Clin Nutr 2003;77:1206 – 1212. [29] Fine KD, et al. Intestinal absorption of magnesium from food and supplements. J Clin Invest 1991;88:396 – 402. [30] Benech H, Grognet JM. Recent data on the evaluation of magnesium bioavailability in humans. Magnes Res 1995;8:277 – 284. [31] Firoz M, Graber M. Bioavailability of US commercial magnesium preparations. Magnes Res 2001;14:257 – 262. [32] Kuhn I, et al. Renal elimination of magnesium as a parameter of bioavailability of oral magnesium therapy. Meth Find Exp Clin Pharmacol 1992;14:269 – 272. [33] Morris ME, LeRoy S, Sutton SC. Absorption of magnesium from orally administered magnesium sulfate in man. J Toxicol Clin Toxicol 1987;25:371 – 382. [34] Mühlbauer B, et al. Magnesium-L-aspartate-HCl and magnesium-oxide: bioavailability in healthy volunteers. Eur J Clin Pharmacol 1991;40(4):437 – 438. [35] Walker AF, et al. Mg Citrate found more bioavailable than other Mg preparations in a randomized, double-blind study. Magnes Res 2003;16(3):183 – 191. [36] Lindberg J, et al. Magnesium bioavailability from magnesium citrate and magnesium oxide. J Am Coll Nutr 1990;9(1):48 – 55. [37] Classen HG. Magnesium-L-Aspartat Hydrochlorid: Experimentelle und klinische Studienergebnisse. J Mineralstoffwechsel 2002;9(2):28 – 34. [38] Bøhmer T, et al. Bioavailability of oral magnesium supplementation in female students evaluated from elimination of magnesium in 24-hour urine. Magnes Trace Elem 1990;9(5):272 – 278. [39] Gegenheimer L. Bioäquivalenz von Magnesium aus Kautabletten und Granulat. Magnesium Bulletin 1994;16:6-8. [40] Lücker PW, et al. Zur therapeutischen Verwertbarkeit von Magnesiumzubereitungen. Magnesium Bulletin 1985;2: 62 – 65. [41] Martin RW, et al. Oral magnesium for tocolysis: a comparison of magnesium gluconate and enteric-coated magnesium chloride. J MSMA 1998;180 – 182. [42] Morris ME, et al. Absorption of magnesium from orally administered magnesium sulphate in man. Clin Toxicol 1987;25:371 – 382. [43] Schütte SA, et al. Bioavailability of magnesium diglycinate vs mg oxide in patients with ileal resection. J Parenteral Enteral Nutrition 1994;18:430 – 435.
AutorenProf. Dr. med. Klaus Kisters ist Chefarzt an der Medizinischen Klinik I am St. Anna-Hospital in Herne und seit 2001 Professor an der Universität Münster. Tätigkeitsschwerpunkte: Innere Medizin, Nephrologie, klinische Geriatrie und Hypertonie. Zahlreiche Publikationen, vor allem zu Magnesium. Präsident der Gesellschaft für Magnesium-Forschung, Herausgeber der Fachzeitschrift "Trace elements and electrolytes", Gründungsmitglied der Akademie für Mikronährstoffmedizin. Seit 2009 Leiter des "Centre of Excellence for Hypertension and Cardio-Metabolic Research". Mit der Auszeichnung "European Centre of Excellence" würdigt die Europäische Hypertonie Gesellschaft (ESH) die Leistungen Kisters bei der ambulanten und stationären Behandlung von Bluthochdruckpatienten sowie seine wissenschaftlichen Forschungsergebnisse. Prof. Dr. med. Klaus Kisters, Medizinische Klinik I, St. Anna Hospital Herne, Hospitalstr. 19, 44649 Herne Apotheker Uwe Gröber ist Leiter der Akademie für Mikronährstoffmedizin, Autor zahlreicher Publikationen, Fachbücher und Buchbeiträge sowie Herausgeber der "Zeitschrift für Orthomolekulare Medizin". Spezialgebiete: Mikronährstoffmedizin, Wechselwirkungen zwischen Arzneimitteln und Mikronährstoffen, Ernährungs- und Präventivmedizin sowie komplementäre Verfahren in der Diabetologie und Onkologie. Er ist aktives Mitglied der "Arbeitsgemeinschaft Supportive Maßnahmen in der Onkologie, Rehabilitation und Sozialmedizin" (ASORS) und des "Arbeitskreis Komplementäre Onkologische Medizin" (AKKOM) der Deutschen Krebsgesellschaft. Zudem ist er in der Aus- und Fortbildung von Ärzten, Apothekern und Ernährungswissenschaftlern tätig. Apotheker Uwe Gröber, Akademie für Mikronährstoffmedizin, Zweigertstr. 55, 45130 Essen, www.mikronaehrstoff.de |




















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.