
- DAZ.online
- DAZ / AZ
- DAZ 9/2009
- Wie die MS-Therapie ...
Arzneimittel und Therapie
Wie die MS-Therapie verbessert werden soll
Sklerotische Läsionen in der weißen Substanz von Rückenmark und Gehirn haben der neurodegenerativen Erkrankung multiple Sklerose (MS) ihren Namen gegeben. Die multiple Sklerose ist eine Autoimmunerkrankung mit einem komplexen genetischen Hintergrund. Neben einer genetischen Prädisposition spielen für die Entstehung Umweltfaktoren und virale Infektionen eine wichtige Rolle. Die multiple Sklerose ist geprägt durch Entzündungsreaktionen, Entmarkungen von Nervenzellen und axonalen Schäden, ausgelöst durch aktivierte T-Lymphozyten, die in das ZNS eindringen.
Erste Symptome sind häufig Sehstörungen infolge einer Sehnervenentzündung. Daneben zählen Müdigkeit, Gefühls- und Koordinationsstörungen, Spastik oder Lähmungen zu den typischen Erkrankungszeichen. Die Betroffenen leiden zudem verstärkt unter Depressionen. Die Suizidrate ist erhöht.
Klinisch werden vier Verlaufsformen unterschieden:
- CIS: Beim ersten Auftreten eines MS-typischen Symptoms spricht man von einem klinisch isolierten Syndrom (CIS).
- RR-MS: Nach Diagnosesicherung mithilfe der Kernspintomographie zeigen 85% der Patienten einen schubförmig remittierenden Krankheitsverlauf (relapsing remitting MS; RR-MS). Nach einem Schub erholen sie sich weitgehend. Doch diese Form geht bei vielen Betroffenen nach zehn bis 15 Jahren in eine sekundär chronisch-progrediente Form über (secondary progressive MS; SP-MS),
- SP-MS: Bei der sekundär chronisch-progredienten Form verschlechtern sich die neurologische Symptomatik und die damit verbundenen Behinderungen mit und ohne Schübe ständig.
- PP-MS: 10% aller Multiple-Sklerose-Patienten leiden von Anfang an an einer chronisch progredienten Form (primary progressive MS; PP-MS).
Zur Therapie steht während eines akuten Schubs Cortison zur Verfügung. Mit einer Basistherapie mit Interferon beta oder Glatirameracetat wird versucht, die Schubrate bei RR-MS zu senken. Bei sekundär chronisch progredientem Verlauf mit mehr als zwei Schüben pro Jahr kann auf Mitoxantron zurückgegriffen werden, bei dem jedoch eine dosislimitierende Kardiotoxizität zu berücksichtigen ist. Zudem häufen sich Berichte über sekundäre Leukämien unter der Mitoxantronbehandlung.
Natalizumab, ein monoklonaler Antikörper, der ein Zelladhäsionsmolekül auf den T-Lymphozyten blockiert und damit das Eindringen aktivierter T-Lymphozyten in das ZNS verhindern soll, ist wegen tödlicher Nebenwirkungen in die Schlagzeilen geraten. In den USA wurde Natalizumab im November 2004 eingeführt, musste aber im Februar 2005 vorübergehend vom Markt genommen werden, weil drei Patienten unter der Behandlung an einer progressiven multifokalen Leukonenzephalopathie (PML) erkrankt waren, die in zwei Fällen tödlich endete. Seit Juli 2006 steht Natalizumab in den USA wieder zur Verfügung, in der Europäischen Union ist es seit Juni 2006 zugelassen. In der Zwischenzeit sind vier weitere Fällen einer PML unter Natalizumab bekannt geworden. Darüber hinaus sind schwere Leberfunktionsstörungen beobachtet worden, die eine Kontrolle der Leberwerte erforderlich machen und eine erhöhte Aufmerksamkeit auch von Seiten der Patienten erfordern. Sie sollen bei ersten Anzeichen wie einer Gelbfärbung der Haut oder einer ungewöhnlichen Dunkelfärbung des Urins umgehend ihren Arzt aufsuchen.
Suche nach oralen Arzneistoffen
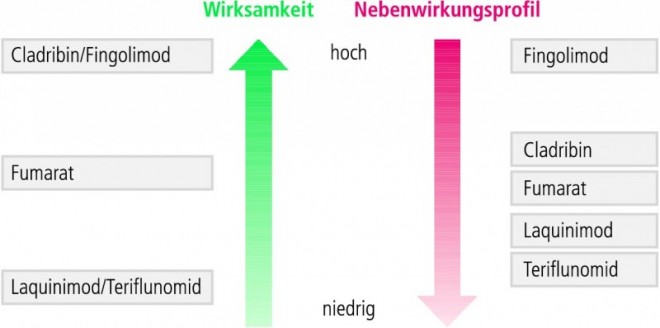
Insgesamt ist die Behandlungssituation nicht zufriedenstellend. Alle zugelassenen Arzneistoffe müssen injiziert werden, so dass intensiv nach oral zu verabreichenden Arzneistoffen gesucht wird. In klinischer Phase II und III befinden sich zur Zeit Statine, Cladribin, Fingolimod, Laquinimod, Teriflunomid und Fumarat (Abb. 1).
Die beste Wirksamkeit wurde bislang mit Cladribin und Fingolimod erzielt.
Cladribin ist ein Purinanalogon, das schon zur Behandlung der Haarzellleukämie zugelassen ist und CD4+ - sowie CD8+ -T-Zellen ausschaltet. Nach einem Behandlungszyklus hält diese Wirkung über 18 Monate an. Ergebnissen einer Phase-III-Studie zufolge reduziert Cladribin die Schübe in einer Größenordnung von 60%.
Fingolimod ist ein unspezifischer Agonist der Sphingosinrezeptoren, der die jährliche Schubrate in einer Größenordnung von 55% reduzieren soll, aber ein hohes Nebenwirkungspotenzial besitzt. Besonders beunruhigend ist das Auftreten schwerer Infektionen, die in zwei Fällen schon tödlich geendet sind. Am besten verträglich erwies sich bislang Teriflunomid.
Neue monoklonale Antikörper
Neben der Suche nach oral zu verabreichenden Arzneistoffen konzentriert sich die Forschung auf weitere Immunmodulatoren wie Alemtuzumab, Rituximab und Daclizumab (Abb. 2).
Alemtuzumab ist ein monoklonaler Antikörper, der spezifisch an das Glykoprotein CD52 auf Immunzellen bindet und deren Zerstörung in Gang setzt. Es befindet sich in Phase III der Entwicklung. Ergebnisse aus einer Phase-II-Studie lassen auf eine effektive Reduzierung der Schubrate und ein Aufhalten andauernder und zunehmender Behinderungen hoffen. Allerdings traten bei sechs Patienten schwere Nebenwirkungen in Form einer idiopathischen thrombozytopenischen Purpura auf, bei der es durch Abnahme der Thrombozytenzahl zu einer abnormen Blutungsneigung kommt, die tödlich enden kann.
Mit Rituximab werden B-Zellen ausgeschaltet. In einer Phase-II-Studie konnten mit diesem monoklonalen Antikörper Schubrate und MRT-Läsionen reduziert werden.
Daclizumab hemmt den Interleukin-2-Rezeptor alpha. Veränderungen von Genen, die für Rezeptoren der Interleukine 2 und 7 kodieren, stehen in einem engen Zusammenhang mit dem Auftreten einer multiplen Sklerose. Möglicherweise führen diese Genmutationen zu einer gestörten Interaktion von Interleukin-Rezeptoren auf der T-Zelloberfläche mit Interleukin, so dass die T-Zellen ihre regulierende Funktion nicht mehr wahrnehmen können und körpereigenes Gewebe angreifen. Unter Daclizumab kommt es zu einer Expansion von Killerzellen, deren Konzentration bei MS-Patienten verringert ist. In einer Phase-II-Studie konnten erste Erfolge in Form einer Reduktion von MRT-Läsionen und der Schubrate sowie einer Besserung der Symptomatik erzielt werden.
Zelltherapie: Das kranke Immunsystem löschen
Große Hoffnungen ruhen auch auf der autologen hämatopoetischen Stammzelltransplantation. Dazu werden dem Patienten hämatopoetische Stammzellen aus dem Knochenmark entnommen, die autoreaktiven Immunzellen mithilfe einer Chemotherapie zerstört und anschließend die entnommenen Stammzellen wieder injiziert. Auf diese Weise werden die für die autoimmunen Angriffe verantwortlichen Entzündungszellen vollständig eliminiert und der Körper kann ein neuen Immunsystem aufbauen. Autoimmune Entzündungsprozesse sollen so lang anhaltend unterbrochen werden. Doch noch sind viele Fragen offen, so zum Beispiel, ob sich durch die Erneuerung des Immunsystems der Prozess der multiplen Sklerose tatsächlich stoppen lässt, welche Patienten am besten für eine solche Zelltherapie geeignet sind und in welchem Stadium die Behandlung erfolgen sollte. Eine hohe Nebenwirkungsrate mit teilweise letalem Ausgang steht einer breiten Anwendung bislang entgegen.
Ermutigende Ergebnisse bei schubförmiger MS
Mut machen allerdings die soeben in The Lancet Neurology veröffentlichten Ergebnisse einer Phase-Ib/IIa-Studie. Bei 21 Patienten mit schubförmiger multipler Sklerose (RR-MS; mittleres Alter 33 Jahre, mittlere Krankheitsdauer fünf Jahre) wurde im Rahmen einer autologen hämatopoetischen Stammzelltransplantation das gestörte Immunsystem mit Cyclophosphamid und Alemtuzumab bzw. Antithymozytenglobulin ausgeschaltet. Es handelt sich dabei um ein nicht-myeloablatives Verfahren, das bedeutet, das Knochenmark selber wird nicht zerstört. Nach drei Jahren hatte sich bei 81% der Patienten der Behinderungsgrad um einen Punkt auf der Behinderungsskala EDSS gebessert. 62% der Patienten hatten weder klinische noch kernspintomographische Zeichen einer Krankheitsaktivität. Es traten weder schwerwiegende Nebenwirkungen noch Todesfälle auf. Allerdings erlitten 21% der Patienten sechs bis 16 Monate nach der Transplantation einen neuen Schub. Damit wurde die autologe hämatopoetische Stammzelltransplantation erstmals in einer prospektiven Studie bei jüngeren MS-Patienten untersucht. Zur Verifizierung dieser positiven Ergebnisse sind jetzt größere randomisierte Studien notwendig, die auch Aufschluss über das kurz- und langfristige Nebenwirkungspotenzial geben. Die Deutsche Gesellschaft für Neurologie betont daher in einer Stellungnahme zu der Studie, dass es sich bei dieser Behandlung zur Zeit noch um ein experimentelles und nicht um ein Routineverfahren handelt.
Quelle
Prof. Dr. Roland Martin,Hamburg: Therapie der multiplen Sklerose – State of the Art und Zukunftsperspektive. Vortrag Pharmacon Davos, 10. Februar 2009.
EMEA concludes new advice to doctors and patients for Tysabri (natalizumab) needed. Pressemitteilung vom 20. März 2008
Stammzellentransplantation bei schubförmiger MS. Stellungnahme der Deutschen Gesellschaft für Neurologie. 19. Februar 2009.
Burt RK et al.: Autologous non-myeloablative haematopoetic stem cell transplantation in relapsing-remitting multiple sclerosis. Lancet Neurology 2009; 8:244-253.
du





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.