
- DAZ.online
- DAZ / AZ
- DAZ 11/2009
- Orale Therapie mit Fumars...
Arzneimittel und Therapie
Orale Therapie mit Fumarsäureester in der Entwicklung
Multiple Sklerose (MS) wird als eine Autoimmunerkrankung des Zentralnervensystems angesehen und ist bei jungen Erwachsenen die häufigste nicht-traumatische neurologische Erkrankung. Durch ein besseres Verständnis des Pathomechanismus dieser Erkrankung konnten in den letzten Jahren zahlreiche neue therapeutische Ansatzpunkte identifiziert werden. Aktuell befinden sich mehrere oral verfügbare Wirkstoffe zum Einsatz bei schubförmig-remittierender multipler Sklerose in verschiedenen Phasen der klinischen Prüfung. Ob diese Wirkstoffe zur Marktreife gelangen, wird von der Balance aus Wirksamkeit, Sicherheit und Anwendungsfreundlichkeit abhängen. Orale Arzneiformen werden von den meisten Patienten bevorzugt, solange Wirksamkeit und Sicherheit den injizierbaren Wirkstoffen vergleichbar sind.
Wirkungsmechanismus bis heute nicht geklärt
Einer dieser Kandidaten für eine orale Therapie ist Dimethylfumarat. Dimethylfumarat ist ein Ester der Fumarsäure und seit 1995 in Deutschland als ein Gemisch aus Dimethylfumarat und Ethylhydrogenfumarat (Fumaderm®) zur Behandlung von mittelschweren bis schweren Formen der Psoriasis vulgaris, wenn eine alleinige äußerliche Therapie nicht ausreichend ist, zugelassen. Es ist ein Zwischenprodukt im Zitronensäurezyklus und Nebenprodukt im Harnsäurezyklus. Der Wirkungsmechanismus der Fumarsäureester ist bis heute nicht geklärt. Diskutiert werden immunmodulatorische und neuroprotektive Wirkungen. Durch die vermehrte Bildung antiinflammatorischer Zytokine könnten die Entzündungsreaktionen im Gehirn, die zu einer Schädigung der Myelinscheiden und Axone von Nervenzellen führen, abgemildert werden. An Rattenhirn wurden neuroprotektive Wirkungen über Aktivierung endogener antioxidativer Faktoren nachgewiesen.
In einer randomisierten, doppelblinden Phase-II-Studie wurde Dimethylfumarat (BG00012) in drei verschiedenen Dosierungen bei Patienten mit schubförmig-remittierender MS untersucht. 257 Patienten erhielten 24 Wochen lang randomisiert entweder 120 mg BG00012 einmal täglich, 120 mg dreimal täglich, 240 mg dreimal täglich oder Placebo. Die Studie gliederte sich in zwei Phasen: Eine placebokontrollierte, doppelblinde Phase über 24 Wochen und eine daran anschließende dosisblinde Phase über weitere 24 Wochen zur Erfassung von Sicherheitsaspekten.
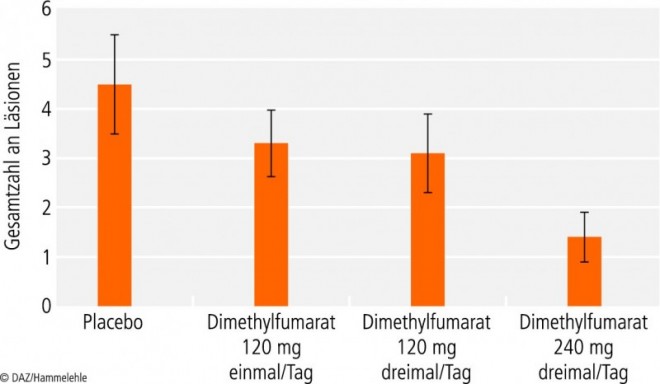
Primärer Endpunkt war die mittlere Gesamtzahl der mittels Gadolinium-verstärkter, T1-gewichteter Magnetresonanztomographie (MRT) dargestellten neuen Läsionen nach 12, 16, 20 und 24 Wochen.
Die höchste Dosis Dimethylfumarat reduzierte die Zahl dieser Läsionen verglichen mit Placebo um 69% (1,4 vs. 4,5, p < 0,0001) (siehe Abbildung). Auch verschiedene andere, mittels MRT ermittelte Parameter, die die Krankheitsaktivität beschreiben, wurden durch Dimethylfumarat in der höchsten Dosierung signifikant reduziert, während die niedrigeren Dosierungen im Vergleich zu Placebo keinen Effekt auf die MRT-Endpunkte hatten. Es stellt sich daher die Frage, ob 240 mg dreimal täglich die wirksamste Dosis ist oder ob höhere Dosierungen, eine gute Verträglichkeit vorausgesetzt, möglicherweise einen größeren Effekt haben könnten. Die jährliche Schubrate wurde von Dimethylfumarat in der höchsten Dosis im Vergleich zu Placebo um 32% reduziert, allerdings war die Studie auf klinisch relevante Endpunkte wie die Schubrate nicht angelegt. Die häufigsten unerwünschten Wirkungen waren Hitzegefühl und Erröten (Flush) sowie gastrointestinale Beschwerden.
| Einige Ergebnisse der Phase-II-Erweiterungsstudie [nach Kappos L, et al. 2006] | ||||
| Placebo und Fingolimod 1,25 mg | Placebo und Fingolimod 5 mg | Fingolimod 1,25 mg | Fingolimod 5 mg | |
| mittlere Gesamtzahl neuer Läsionen ± SD | 0,5 ± 1,0 | 0,9 ± 1,5 | 1,1 ± 4,6 | 0,6 ± 1,1 |
| Patienten ohne neue Läsionen (Monat 12) | 86 % | 69 % | 85 % | 88 % |
auf ein Jahr bezogene Schubrate, Monate 0 bis 6 auf ein Jahr bezogene Schubrate, Monate 7 bis 12 | 0,7 0,21 | 0,69 0,10 | 0,36 0,29 | 0,32 0,23 |
| SD: Standardabweichung | ||||
Fazit
Ob das oral verfügbare Dimethylfumarat im Vergleich zur derzeit üblichen Therapie bei multipler Sklerose ein akzeptables Nutzen-Risiko-Profil hat, kann erst nach Veröffentlichung laufender Phase-III-Studien abgeschätzt werden. Bei der Anwendung von Fumarsäureestern bei Psoriasis sind auch schwerwiegende unerwünschte Wirkungen (z. B. Nierenversagen) aufgetreten.
Quelle
Kappos L, et al. Efficacy and safety of oral fumarate in patients with relapsing-remitting multiple sclerosis: a multicentre, randomised, double-blind, placebo-controlled phase IIb study. Lancet 2008; 372: 1463 –1472.
Sorensen PS, Sellebjerg F. Oral fumarate for relapsing-remitting multiple sclerosis. Lancet 2008; 372: 1447–1448.
Apothekerin Dr. Birgit Schindler


















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.