
- DAZ.online
- DAZ / AZ
- DAZ 4/2008
- Diabetes mellitus – ...
Arzneistoffporträt
Diabetes mellitus – Metabolic Tuning mit Benfotiamin
Das Schicksal des Diabetikers wird maßgeblich von Mikro- und Makroangiopathien bestimmt (siehe Kasten). Sie führen zu schwerwiegenden Beeinträchtigungen der Lebensqualität und sind Ursache der im Mittel um 30% verringerten Lebenserwartung.
Diabetische Gefäß- und Organschäden entwickeln sich schon Jahre vor der Diagnosestellung. Das Gesamtsterblichkeitsrisiko für 36- bis 45-jährige Männer mit Typ-2-Diabetes ist 5,1-fach, für Frauen 7-fach höher als bei der Normalbevölkerung.
Folgeschäden an den kleinen Gefäßen der Augen, Nieren oder Nerven können vor allem bei multimorbiden Patienten mit Typ-2-Diabetes zu Erblindung, chronischem Nierenversagen und Neuropathien führen. Makroangiopathien sind die Hauptursache für die extrem hohe Inzidenz von atherothrombotischen Ereignissen (z. B. Herzinfarkt). Mikro- und Makroangiopathien sind zu 80 Prozent die Todesursache bei Diabetikern (zwei Drittel tödlicher Myokardinfarkt, ein Drittel Tod durch Urämie).
Die Prävention diabetischer Folgeerkrankungen ist beim Typ-1-Diabetes besser möglich als beim Typ-2-Diabetes, da sich bei diesem bereits das prädiabetische metabolische Syndrom schädigend auf das vaskuläre System, die Gewebe und Organe ausgewirkt hat. Bei Typ-2-Diabetikern sind daher zum Zeitpunkt der Diagnosestellung häufig mikro- oder makrovaskuläre Schäden nachweisbar (s. Tab. 1).
Tab. 1: Relative Häufigkeit von Folgeschäden bei der Erstdiagnose von Diabetes mellitus | |
Folgeschäden |
in % |
Endothelschäden |
80 – 100 |
Dyslipoproteinämie |
50 – 80 |
Hypertonie |
30 – 40 |
Retinopathie |
20 – 30 |
Anzeichen einer Neuropathie |
20 – 30 |
Mikroalbuminurie |
10 – 20 |
Diabetische Folgeerkrankungen in ZahlenNeuropathie: Etwa 60 bis 90% aller Diabetiker sind von Neuropathien betroffen. Häufigste Form ist die distal symmetrische Polyneuropathie mit strumpf- und handschuhförmig verteilten Sensibilitätsstörungen. Daneben treten motorische Störungen (z. B. Muskelatrophie) sowie Neuropathien des autonomen Nervensystems (z. B. Obstipation, Impotenz, stummer Myokardinfarkt, Ruhetachykardie) auf. Mikroangiopathien (Nephro-, Retinopathien): Die diabetische Nephropathie ist die häufigste Ursache für eine Nierenersatztherapie. Etwa 40% der Typ-1- und 20% der Typ-2-Diabetiker entwickeln innerhalb von zehn Jahren ein chronisches Nierenversagen. In den westlichen Industrienationen ist die diabetische Retinopathie die häufigste Ursache zu erblinden. Im Vergleich zum Stoffwechselgesunden haben Diabetiker ein etwa 25-fach höheres Erblindungsrisiko. Die Diagnose eines Typ-2-Diabetes erfolgt häufig beim Augenarzt, wenn bereits Hyperglykämie-bedingte Endothelschäden am Auge nachweisbar sind.
Diabetischer Fuß: Bei einem jahrelang schlecht eingestellten Diabetes können die Neuro- und Angiopathien im schlimmsten Fall zur Entwicklung des diabetischen Fußsyndroms führen. In Deutschland kommt es pro Jahr zu etwa 36.000 Neuerkrankungen und 28.000 Fußamputation. Die 5-Jahres-Überlebensrate der Patienten liegt – nach unterschiedlichen Schätzungen – bei 39 bis 68%. Makroangiopathien (Myokardinfarkt, Schlaganfall): Zwei Drittel der Diabetiker sterben an atherothrombotischen Ereignissen. Allgemein ist das Herzinfarkt- und Schlaganfallrisiko im Vergleich zur Normalbevölkerung um das Sechsfache erhöht. Neben der autonomen Neuropathie trägt hierzu das AGE-Protein N-Carboxymethyl-Lysin (CML), das sich als extremer Gefäßstressor beim Diabetiker in den Arterien und Arteriolen des Herzgewebes anreichert, maßgeblich bei. |
Oxidativer Stress und Mitochondrien
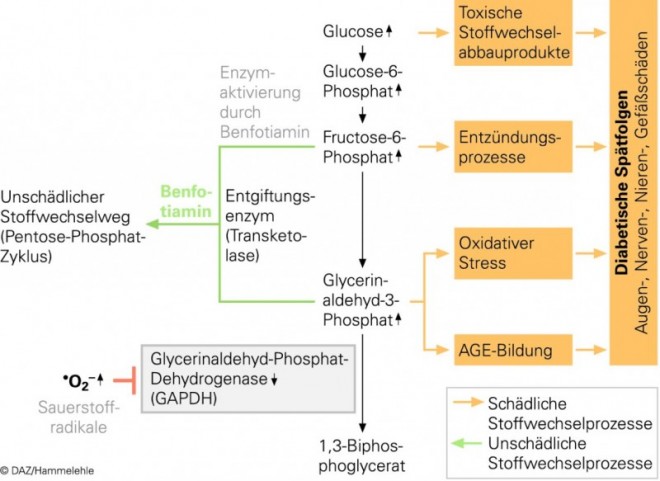
Die Überladung der Gefäß- und Nervenzellen mit Glucose (Hyperglykämie) oder Fettsäuren (Dyslipoproteinämie) lässt bei diabetischer Stoffwechsellage den mitochondrialen Elektronentransport in einem Ausmaß ansteigen, dass der kritische Grenzwert für das Membranpotenzial überschritten wird und reaktive Sauerstoffspezies (ROS) gebildet werden. Die ROS aktivieren diabetesspezifische Stoffwechsel- und Signalwege, die wesentlich zur Pathogenese der Hyperglykämie-bedingten Gefäß-, Nerven- und Organschäden beitragen. Dazu zählen:
- die Aktivierung des Aldose-Reduktase-Weges mit der toxischen Akkumulation von Sorbitol in den Nervenzellen (Polyolstoffwechsel),
- die Aktivierung des Hexosamin-Weges, die über Blockade des Pentose-Phosphat-Weges zu einer mitochondrialen Mehrproduktion von Superoxidradikalen (O2 –•) und einer zellulären Glutathion-Depletion führt,
- die Aktivierung der Proteinkinase C durch intrazelluläre Akkumulation von Diacylglycerol (DAG),
- die gesteigerte nicht-enzymatische Glykierung von Proteinen (Proteinglykosylierung) und Bildung von AGEs (Advanced Glycation End products) sowie
- die Aktivierung des Redox-sensitiven Transkriptionsfaktors NFκB, der die Synthese proinflammatorischer Zytokine wie TNF-α stimuliert (Abb. 1 und 2).
AGEs – Schlüssel für diabetische Folgeschäden
Der französische Biochemiker Louis Maillard entdeckte im Jahre 1912, dass Zucker mit Eiweißmolekülen unter Bildung von Glykierungsprodukten reagiert. Die braune Kruste des Brotes oder die knusprige Haut gebratener Hähnchen sind alltägliche Beispiele für die Maillard-Reaktion, die auch im menschlichen Körper abläuft und hier für die Bildung von AGEs verantwortlich ist. Das bekannteste AGE ist der glykierte rote Blutfarbstoff Hämoglobin (HbA1C), dessen Wert bei Diabetikern ein Maß für die Güte der Blutzuckereinstellung darstellt.
AGEs verlieren ihre physiologische Funktion oder wirken unphysiologisch. Sie stellen Blutgefäße enger und sind der Schlüssel für die diabetischen Mikro- und Makroangiopathien. Möglicherweise sind sie für die erhöhte postprandiale Inzidenz kardiovaskulärer Ereignisse bei Typ-2-Diabetikern verantwortlich.
Da bei der Glykierung von Eiweißen vermehrt freie Radikale gebildet werden, kommt es zu Entzündungen an Gefäßen und Nerven und zu den diabetischen Spätfolgen wie Herzinfarkt, Nierenversagen, Trübungen der Augenlinse und Nervenschmerzen mit Taubheitsgefühl.
AGE-Bildung – die "chemische Zeituhr" im Körper
Nahrungsmittel, die über längere Zeit gekocht, gebraten oder gegrillt wurden, sind besonders reich an AGEs. Frisches Obst und Gemüse ist dagegen ausgesprochen AGE-arm. Mit Hilfe der Laser-Doppler-Flowmetrie wurde nachgewiesen, dass eine AGE-belastete Nahrung (z. B. Schnitzel mit Pommes frites und Cola) die mikrovaskuläre Funktion bei Typ-2-Diabetikern stundenlang verschlechtert und dass die vorherige Einnahme von Benfotiamin diesen Effekt komplett verhindert.
Vergleicht man verschiedene Spezies mit unterschiedlicher Lebensdauer, zeigt sich eine direkte Korrelation zwischen der Lebensdauer und der Rate der AGE-Bildung. Die AGE-Bildung wird deshalb auch als "chemische Zeituhr" des Körpers betrachtet.
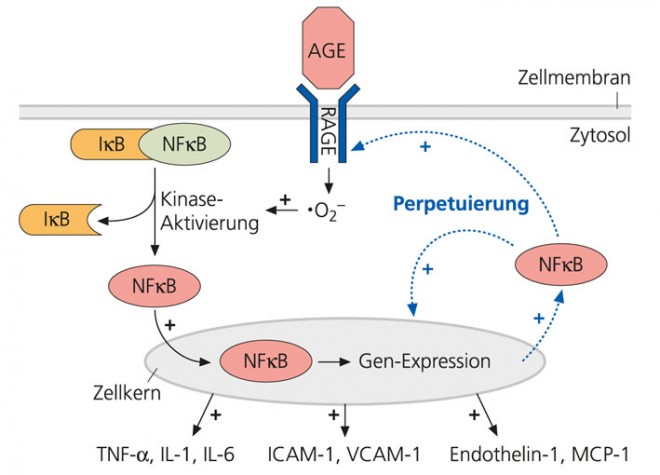
AGEs fördern entzündliche Prozesse, indem sie an den AGE-Rezeptor (RAGE) binden, der nahezu auf allen Zellen des menschlichen Organismus vorkommt. Der durch AGEs aktivierte RAGE setzt im Zytosol Sauerstoffradikale frei, die den Transkriptionsfaktor NFB aktivieren, indem sie ihn aus seiner Bindung an den Proteinkomplex IκB freisetzen; darauf gelangt NFκB über ein spezifisches Signal in den Zellkern, wo er die Synthese von Zytokinen stimuliert (Abb. 2).
Benfotiamin – das Mittel gegen AGEs
B-Vitamine spielen eine zentrale Rolle im Energie- und Kohlenhydratstoffwechsel. Ihre Aufgaben in unserem Körper reichen von der Steuerung der Nerven- und Herzfunktion über die Blutbildung und Energiegewinnung in unseren Körperzellen bis zur Abwehrfunktion und Gesunderhaltung von Haut und Haaren. Da die B-Vitamine wasserlöslich sind, gehen sie bei Diabetikern vermehrt über den Urin verloren. Eine aktuelle Studie belegt, dass bei Diabetikern eine um 75% reduzierte Konzentration von Vitamin B1 im Blut vorliegt und die renale Ausscheidung 16- bzw. 24-fach (Typ-2 bzw. Typ-1) erhöht ist [2]. Eine vielversprechende Option zur Vermeidung diabetischer Komplikationen ist die Supplementierung von Benfotiamin, einem fettlöslichen Prodrug des wasserlöslichen Thiamins (Vitamin B1). Benfotiamin aktiviert das Entgiftungsenzym Transketolase und beugt den oben geschilderten Hyperglykämie-bedingten Schäden vor (Abb. 1).
Steckbrief BenfotiaminBenfotiamin = S-Benzoylthiamin-O-monophosphat; fettlösliches, hochbioverfügbares Vitamin-B1-Prodrug. Resorption: Benfotiamin wird im Unterschied zu wasserlöslichen Vitamin-B1-Verbindungen dosisproportional resorbiert. Bioverfügbarkeit: Benfotiamin besitzt aufgrund seiner Lipidlöslichkeit eine über 8,5-fach höhere Bioverfügbarkeit im Vergleich zu wasserlöslichen Thiaminsalzen. Wirkspektrum/Wirkmechanismus: Antineuropathisch, analgetisch und endothelprotektiv. Dosierung (oral): 150–600 mg pro Tag, sowohl als Monotherapie als auch in Kombination mit Vitamin B6. Präventiv ist die Einnahme von täglich 50 mg Benfotiamin empfehlenswert. Einnahmedauer: Benfotiamin sollte zur Erzielung therapeutischer Effekte wenigstens sechs Wochen lang täglich eingenommen werden, um eine Aussage bezüglich der therapeutischen Response zu treffen. Anwendungsgebiete: Neuropathien (z. B. diabetische, alkoholtoxische), Karpaltunnel-Syndrom. Präparatebeispiel: milgamma® protekt (300 mg Benfotiamin pro Tablette). |
Gute Wirksamkeit von Benfotiamin bei diabetischen Neuropathien
Benfotiamin ist orales Mittel der Wahl in der Therapie schmerzhafter peripherer Neuropathien. Die gute Wirksamkeit und Verträglichkeit wird auch durch die Ergebnisse der bisher größten mit Benfotiamin durchgeführten Anwendungsbeobachtung unterstrichen (BEDIP-Studie, Benfotiamine in the Treatment of Diabetic Polyneuropathy). Dabei wurden die Befunde von Patienten mit diabetischer Polyneuropathie unterschiedlicher Schweregrade durch eine offene, multizentrische Befragung während neun Wochen dokumentiert. 86% der Patienten (n = 1154, Durchschnittsalter 63 Jahre) hatten einen Typ-2-Diabetes, 14% einen Typ-1-Diabetes; die durchschnittliche Krankheitsdauer betrug zehn Jahre.
Die therapeutischen Ergebnisse waren beeindruckend: Der Anteil der Patienten mit typischen Neuropathiebeschwerden wie Brennen, Taubheitsgefühl und Parästhesien im Fuß und Unterschenkel verringerte sich von 97,2% bei Beginn auf 33,6% nach neunwöchiger Therapie mit Benfotiamin. Dabei zeigte sich eine deutliche Abhängigkeit des Effekts von der Dosierung: Die Gabe von zweimal täglich 150 mg Benfotiamin (p. o.) erbrachte signifikant bessere Resultate als die Gabe von nur einmal 150 mg pro Tag [1].
Fazit
Erfahrungen aus der eigenen Beratungspraxis bestätigen immer wieder die hervorragende Wirksamkeit von Benfotiamin in der Prävention und Therapie diabetischer Neuropathien. Dabei wird der protektive Effekt von Benfotiamin durch die Optimierung des antioxidativen Schutzes nochmals verbessert. Neben Antioxidanzien sollten Diabetiker insbesondere auf eine gute Versorgung mit Magnesium, B-Vitaminen, Zink und Chrom achten, um krankheitsbedingten Mangelzuständen vorzubeugen, den Glucosestoffwechsel zu optimieren und diabetischen Folgeerkrankungen vorzubeugen.
Literatur
[1] Gröber, U.: Benfotiamin und Diabetes. Dtsch. Apoth. Ztg. 2005;145:4951 – 4953.
[2] Thornalley PJ, et al. High prevalence of low plasma thiamine concentration in diabetes linked to a marker of vascular disease. Diabetologia 2007;50: 2164 – 2170.
Anschrift des Verfassers:
Uwe Gröber
Akademie & Zentrum für Mikronährstoffmedizin
Zweigertstraße 55
45130 Essen


















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.