
- DAZ.online
- DAZ / AZ
- DAZ 32/2008
- Soja-Isoflavone bei ...
Gynäkologie
Soja-Isoflavone bei Wechseljahresbeschwerden
Soja ist für einen großen Teil der Weltbevölkerung ein Grundnahrungsmittel. Schätzungen gehen davon aus, dass Lebensmittel wie Tofu bei mindestens 1,5 Milliarden Menschen lebenslang nahezu täglich auf dem Speiseplan stehen. Entsprechend haben Fragen nach Ernährungseffekten und Lebensmittelsicherheit von Soja schon frühzeitig das Interesse der Wissenschaft geweckt.
Soja kann heute hinsichtlich der Langzeitsicherheit als eines der bestuntersuchten Lebensmittel gelten. Eine sehr langfristig angelegte japanische Studie zeigte über 40 Jahre hinweg einen durchschnittlichen Verzehr von ca. 65 g Soja pro Tag [1]. Diese Menge entspricht einer täglichen Zufuhr von 26 bis 54 mg Isoflavonen (berechnet als Aglyka), mit Spitzenwerten um 100 mg/Tag bei mindestens 150 Millionen Menschen.
Hoher Sojakonsum und insbesondere die Zufuhr von Isoflavonen wird in den umfangreichen epidemiologischen Untersuchungen und Fall-Kontroll-Studien an Zehntausenden von Teilnehmern regelmäßig mit einer geringeren Rate von Prostata-, Brust- und Endometriumkrebs assoziiert [2]. Dieses spannende Thema würde den Rahmen der Diskussion von Nutzeffekten bei Frauen mit Wechseljahresbeschwerden sprengen und soll daher Gegenstand eines eigenen Beitrags sein.
Nutzen von Soja-Isoflavonen bei Wechseljahresbeschwerden klinisch belegt
Hitzewallungen und nächtliche Schweißausbrüche zählen neben Hauttrockenheit, Stimmungsschwankungen und Antriebslosigkeit zu den auffälligsten Symptomen der Wechseljahre. Schon frühzeitig wurde der Einfluss einer sojareichen Ernährung auf die Häufigkeit von Hitzewallungen untersucht, mit zunächst wenig einheitlichen Ergebnissen – ein Umstand, auf den regelmäßig in Übersichtsarbeiten und Metaanalysen verwiesen wird. In der Tat gelang es in einer ganzen Reihe von Studien vor allem älteren Datums nicht, einen Vorteil von Soja bei Wechseljahresbeschwerden nachzuweisen. Daraus den Rückschluss eines fehlenden Nutzens zu ziehen, wäre jedoch verfehlt, weil die meisten dieser Studien vom Design und der Qualität der untersuchten Zubereitung her große Unterschiede aufwiesen. Die Studien der jüngeren Zeit zeigen dagegen regelmäßig einen statistisch signifikanten Effekt der Isoflavongruppe. Diese offensichtliche Diskrepanz erfordert eine genauere Betrachtung.
Wie bei allen Beschwerdebildern mit hoher psychosomatischer Komponente gehen Wechseljahresbeschwerden mit einem hohen Placeboeffekt einher. Entsprechend kann bereits das Studienumfeld einen wesentlichen Beitrag zum Effekt leisten. Bei stark streuenden Symptomen wie Hitzewallungen muss diesem statistischen Phänomen durch eine ausreichende Fallzahl und eine Berücksichtigung der aktuellsten Standards für die Planung klinischer Studien begegnet werden.
Dies war vor allem in der Frühphase der klinischen Untersuchungen an Frauen in den Wechseljahren ganz offensichtlich nicht der Fall [3–7] – in diesen Arbeiten wurde zum Teil zwar eine positive Tendenz oder gar Überlegenheit von Soja bei anderen Symptomen gesehen, für die Bewertung der Hitzewallung aber war die Zahl der Studienteilnehmerinnen zu niedrig gewählt. Zudem waren die Beschwerden in mehreren Studien sehr gering ausgeprägt, sodass eine deutliche Verbesserung retrospektiv auch aus dieser Sicht nicht zu erwarten war.
Sojastudien, die die FDA-Kriterien erfüllen, haben positive Ergebnisse
Über das Problem der ausreichenden Probandinnenzahl hinaus hat die US-amerikanische FDA im Jahr 2003 Kriterien für das Design von Menopausenstudien definiert. Wendet man diese Kriterien auf die Sojastudien an, so geben die Mängel im Studiendesign klare Hinweise auf die Gründe des Scheiterns der Studien.
Ein typisches und aktuelles Beispiel ist die Langzeitstudie von Khaodiar et al. (2008), die keinen statistisch signifikanten Unterschied zwischen Placebo und Verum in Bezug auf die Beeinflussung von Hitzewallungen ergeben hatte [8]. Betrachtet man die Details aber näher, so wird rasch klar, dass diese pauschale Negativaussage nicht stimmt. Khaodiar et al. hatten die Studie dreiarmig angelegt, wobei 48 Frauen mit 40 mg Isoflavonen, 49 Frauen mit 60 mg Isoflavonen (jeweils in Form von Sojaextrakt) und 45 Frauen mit Placebo supplementiert wurden. Bei der Auswertung fand sich in den Verumgruppen eine Verringerung der Beschwerden um 51 bzw. 52%, in der Placebogruppe dagegen um 32%. Diese Unterschiede zwischen Verum und Placebo erwiesen sich aber nicht als signifikant (p = 0,07 bzw. 0,09). Wurden dagegen die beiden Verumgruppen kombiniert ausgewertet, erreichte das Ergebnis die statistische Signifikanz gegenüber Placebo (p < 0,05). Dies deutet auf eine Unterschätzung des Placeboeffektes und eine zu klein gewählte Gruppenbesetzung.
Wendet man retrospektiv die FDA-Studienkriterien aus dem Jahr 2003 auf die klinischen Arbeiten bei Wechseljahresbeschwerden an, so ist festzustellen, dass immerhin vier Arbeiten, die vor dem Jahr 2003 erschienen sind, diese Kriterien erfüllen. Alle vier Arbeiten zeigen eine statistisch signifikante Überlegenheit der jeweiligen Sojazubereitung (42–100 mg Isoflavone, berechnet als Aglyka) gegenüber Placebo [9–12]. Diese Studien wurden in Übersichtsarbeiten und Konsensuskonferenzen als Beleg für die Effekte von Soja-Isoflavonen gewertet [13, 14]. Seither sind weitere Studien mit positivem Ergebnis veröffentlicht worden, die nicht nur den Effekt auf Wechseljahresbeschwerden, sondern auch auf die Anwendungssicherheit der täglichen Zufuhr von 50 bis 100 mg Isoflavonen bestätigen [15–21], darunter auch eine placebokontrollierte Langzeitstudie über die Anwendungsdauer von zwei Jahren [22, 23]. Aktuell wurde eine europäische Studie vorgestellt, bei der 176 Frauen in den Wechseljahren placebokontrolliert über zwölf Wochen ein Supplement mit 100 mg Isoflavonglykosiden entsprechend 60 mg Aglyka pro Tag erhielten (Prüfpräparat: Alsifemin), gefolgt von einer offenen Nachbeobachtungsphase unter Verum von weiteren zwölf Wochen Dauer. Diese Studie zeigte nicht nur das Fehlen eines Risikos an Schilddrüse, Leber und Uterus, sondern auch eine statistisch signifikante Verbesserung der Wechseljahresbeschwerden, ermittelt anhand der Frequenz von Hitzewallungen und der Greene Climacteric Scale [19].
Effekt von Soja-Isoflavonen in Metaanalysen statistisch gesichert
Die Wirkung von Soja-Isoflavonen auf vasomotorische Beschwerden der Wechseljahre ist in Metaanalysen statistisch abgesichert und erreicht damit den Grad 1a, also den höchsten Grad auf der Evidenzskala. Dabei stammen die aktuellsten Analysen noch aus dem Jahr 2006 und konnten daher die neuesten Studien aus den Jahren 2007 und 2008 gar nicht berücksichtigen [24–26].
Zu dieser positiven Aussage im scheinbaren Widerspruch steht, dass die Metaanalyse von Nelson et al. (2006) schon im Abstract die Effekte von Isoflavonen in Abrede stellt. Wer die Lektüre der Arbeit bereits an dieser Stelle beendet, muss zwangsläufig zu einer falschen Schlussfolgerung kommen. Der Grund für diese Diskrepanz liegt darin, dass sich die Autoren im Abstract auf eine Gesamtbewertung von Studien beziehen, die neben den Menopausenbeschwerden auch Untersuchungen an Frauen einbezogen, bei denen die Hitzewallungen medikamentös durch Einnahme von Tamoxifen ausgelöst waren. Diese Nebenwirkung von Tamoxifen kann aber nicht einfach mit den natürlich bedingten Hitzewallungen der Wechseljahre gleichgesetzt werden.
Tatsächlich wurde in bislang allen Studien an Krebspatientinnen festgestellt, dass Isoflavone keinen Einfluss auf Tamoxifen-induzierte Hitzewallungen haben [27–29]. Daraus kann aber nicht die Schlussfolgerung gezogen werden, dass dies auch bei den natürlichen Wechseljahresbeschwerden der Fall sei. Nelson et al. (2006) haben dies durch getrennte Bewertung der Studien zu Wechseljahresbeschwerden und zur Bekämpfung von Tamoxifennebenwirkungen berücksichtigt. Ein unklares oder negatives statistisches Resultat ergab sich nur dann, wenn die Tamoxifenstudien in die Bewertung einflossen – in den Analysen der natürlichen Wechseljahresbeschwerden, und insbesondere von den Studien mit adäquatem Design, wurde ein statistisch eindeutig positives Signal zugunsten einer Überlegenheit von Isoflavonen gegenüber Placebo gefunden!
Auf der Basis der ausführlichen statistischen Berechnungen von Nelson et al. (2006) ist somit der Nutzen der Soja-Isoflavone für Frauen in den Wechseljahren eindeutig bestätigt.
Rezeptorabhängige Schutzwirkungen
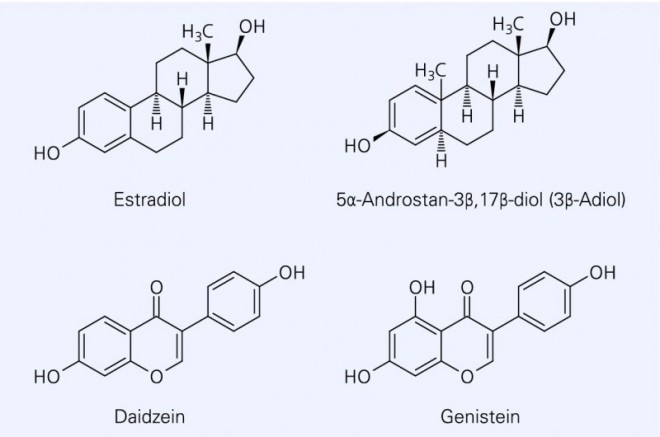
Soja-Isoflavone werden als "Phytoöstrogene" bezeichnet. Diese Bezeichnung ist irreführend, weil sich der Wirkmechanismus der Isoflavone von den typischen Östrogen-vermittelten Effekten klar unterscheidet. Isoflavone wirken nicht wie das Östrogen Estradiol, sondern eher wie Androstane – sie greifen modulierend in die komplexe Steuerung der hormonellen Effekte ein.
Vor etwa zehn Jahren hat die schwedische Arbeitsgruppe von Jan-Åke Gustafsson zusätzlich zu dem bereits bekannten Östrogenrezeptor einen weiteren Rezeptor entdeckt, der zur Unterscheidung des eigentlichen Östrogenrezeptors ER-α die Bezeichnung ER-β erhielt [30]. Die Entdeckung des zweiten Östrogenrezeptors wurde gar mit einem Paradigmenwechsel in der Hormonbiologie gleichgesetzt [31] und hat wesentlichen Einfluss auf die Krebsforschung und die Entwicklung neuer Wirkstoffe für die Behandlung von Krebs, Erkrankungen mit Ursprung im zentralen Nervensystem, Entzündungen oder Erkrankungen der Knochen und des Herz-Kreislauf-Systems – Organe, bei denen dem ER-β eine wesentliche protektive Rolle zukommen könnte [32–34].
In aktuellen Studien werden regelmäßig neue Funktionen und Zusammenhänge des Wechselspiels zwischen ER-α und ER-β erkannt. Während der klassische Östrogenrezeptor ER-α die Proliferation an Brust und Uterus und dadurch bedingt auch das Krebsrisiko fördert, hat der ER-β diesen Effekt nicht – diskutiert wird eher das Gegenteil, ein krebsprotektiver Effekt [33].
Derzeit wird intensiv an der Entwicklung selektiver ER-β-Agonisten geforscht. Strukturelles Vorbild war dabei Genistein – das Hauptisoflavon in Soja [35]. Die Affinität von Genistein zu ER-β wurde bereits kurz nach der Entdeckung des neuen Rezeptors veröffentlicht [36]. Heute können viele der epidemiologischen und klinischen Beobachtungen mit Soja zwanglos über die Effekte der Isoflavone am ER-β erklärt werden [37].
ER-β dient als Gegenspieler zu ER-α. Er hat im Organismus eine nachgeordnete Funktion und wird vor allem dann verstärkt exprimiert, wenn ER-α-vermittelte Prozesse aus dem Ruder laufen. ER-β könnte die Funktion einer "Notbremse" zukommen: Der Rezeptor wird durch hohe Estradiolkonzentrationen, wie sie z. B. in der Schwangerschaft vorliegen, aktiviert und trägt so zur Selbstlimitierung östrogener Effekte bei. Estradiol ist jedoch nicht das einzige Substrat dieses Rezeptors: Ein weiterer endogener Aktivator ist 5α-Androstan-3β,17β-diol (kurz: 3β-Adiol), ein Hormon, das bereits vor der Produktion von Östrogenen in der Pubertät im weiblichen Organismus nachweisbar aktiv ist [38, 39]. Die Hormonspiegel von 3β-Adiol gehen über die Dauer der gebärfähigen Phase mit denen von Estradiol parallel. Für beide Hormone sinken die Spiegel in den Wechseljahren erheblich ab [40, 41]. Das Auftreten von Wechseljahresbeschwerden korreliert nicht nur mit den erniedrigten Estradiol-, sondern auch mit den abgesenkten 3β-Adiolspiegeln [42].
Die bislang bekannten Zusammenhänge zwischen Estradiol und 3β-Adiol sowie den Rezeptoren ER‑α und ER-β können zwanglos einige scheinbare Widersprüche erklären, zum Beispiel die Frage, warum die hohen Estradiolspiegel der reproduktiven Phase der Frau nicht zu einem Anstieg des Risikos für Brust- und Gebärmutterkrebs führen, dagegen aber in den Wechseljahren die erniedrigten Hormonspiegel mit einem Anstieg der Krebshäufigkeit einhergehen.
Dieser Zusammenhang zwischen Estradiol und 3β-Adiol bzw. den Östrogenrezeptoren ER-α und ER-β ist wahrscheinlich auch einer der Hintergründe für die Hitzewallungen der Wechseljahre. Medikamentös werden diese Beschwerden durch Östrogengabe behandelt. Scheinbar paradox ist dagegen, dass übergewichtige menopausale Frauen, die über die Estradiolbiosynthese im Fettgewebe über höhere Estradiolspiegel verfügen als Normalgewichtige, dennoch stärker unter Hitzewallungen leiden [43]. Ohne Berücksichtigung der Effekte von 3β-Adiol am ER-β wäre dies ein schwer erklärbares Phänomen. Tatsächlich ist bereits seit vielen Jahren bekannt, dass Hitzewallungen wie auch Depressionen (ebenfalls ein typisches Symptom der Wechseljahre) mit dem sogenannten HPA-System (der Hypophysen-Hypothalamus-Adrenocorticalen Achse, also dem Stresshormonsystem) in direktem Zusammenhang stehen [44, 45]. Dieses System wird, wie in einer aktuellen Arbeit dargestellt, über den ER-β gesteuert [34]. Der eigentliche Bindungspartner ist 3β-Adiol, aber auch Estradiol kann bei ausreichender Konzentration den Effekt am ER-β auslösen. Dies erklärt, warum die Gabe von Östrogenen wie auch die Gabe anderer ER‑β-Agonisten wie Isoflavone gleichsinnig Hitzewallungen bekämpfen können – es erklärt aber auch, warum die Isoflavone nicht auch die dem Estradiol eigenen proliferationsfördernden Effekte ausüben.
ÖstrogeneÖstrogene oder Follikelhormone fördern das Wachstum der weiblichen Geschlechtsorgane, beeinflussen den Stoffwechsel in Leber und Knochen und haben zahlreiche weitere physiologische Wirkungen. Die drei Vertreter Estron, Estradiol und Estriol unterscheiden sich strukturell durch die Anzahl der OH-Gruppen. Von ihnen ist Estradiol das bei Weitem wirkungsvollste Hormon; es wird deshalb oft mit "Östrogen" (engl. Estrogen) gleichgesetzt. |
Isoflavone: Selektive ER-β-Agonisten
Die Isoflavone aus Soja, insbesondere Genistein und Daidzein, wurden schon frühzeitig als selektive ER-β-Agonisten erkannt. So hat Genistein am ER-α nur 4% der Affinität von Estradiol, am ER-β dagegen 87% [46]. Dieser Effekt wird in Anwesenheit auch kleiner Mengen an Estradiol (wie es auch im Organismus der Frau in den Wechseljahren der Fall ist) überadditiv verstärkt [47]. Die mit typischen Sojazubereitungen zugeführten Isoflavonmengen reichen für eine Aktivierung des ER‑β, nicht aber des ER-α aus [47]. Mit diesem Mechanismus stehen nicht nur die beobachteten Effekte der Isoflavone bei Wechseljahresbeschwerden, sondern auch die postulierte Senkung des Risikos hormonabhängiger Tumoren in den Wechseljahren im Zusammenhang [48].
In Übereinstimmung mit einer deutschen gynäkologischen Expertenmeinung hat die Internationale Menopausegesellschaft auf Basis der jüngsten Erkenntnisse erst kürzlich eine Empfehlung zugunsten des Einsatzes von Isoflavonen als "wirkungsvolle Alternative und Ergänzung zur Behandlung der Symptome von Menopause und Prämenopause" ausgesprochen, als alleinige Gabe oder in Kombination mit Hormonen [49, 50].
Rezeptorunabhängige Mechanismen
Neben der Aktivierung des ER-β durch Isoflavone wird auch eine Reihe unabhängiger, Enzym-vermittelter Mechanismen diskutiert. So gibt es Hinweise darauf, dass Phytoöstrogene im Brustgewebe die Biosynthese von Estradiol aus Testosteron oder Estron hemmen können – ein in der Summe nicht sehr stark ausgeprägter Effekt, der aber möglicherweise bei Brustkrebs zu einer Verringerung des Proliferationsrisikos durch Soja-Isoflavone beiträgt [51].
Hemmeffekte sind für die 17β-Hydroxysteroidhydrogenase HSOR-I bekannt, ein Enzym, das an der Umwandlung von Estron zu Estradiol beteiligt ist. Die für die Isoflavone in vitro gefundenen IC50 -Werte bewegen sich dabei mit 0,1 bis 1 μM in einer Größenordnung, die im Organismus bei Soja-reicher Ernährung relevant sein könnte [52].
Deuten In-vitro-Untersuchungen auf ein Risiko hin?
Basierend auf den östrogenen Effekten von Isoflavonen wird in aktuellen Übersichtsarbeiten regelmäßig auf die Möglichkeit proliferationsfördernder Effekte hingewiesen [53]. Diese Ableitung stützt sich auf Untersuchungen an MCF-7-Brustkrebszellen in vitro oder auf das Modell der gentechnisch veränderten ovarektomierten athymischen Maus ohne ER-β. Beide Systeme wurden entwickelt, um östrogene Effekte am ER-α zu detektieren. MCF-7-Zellen benötigen Estradiol als Auslöser der Proliferation und verfügen nicht über ER‑β-Rezeptoren. Substanzen mit östrogenen Effekten, also solche mit agonistischer Aktivität am ER-α, vermögen die Zellproliferation zu induzieren. Dies funktioniert zwangsweise auch mit selektiven ER‑β-Agonisten, weil auch hier immer auch eine geringe Restaktivität am ER-α vorliegt. Nach der Definition von Harris sollte ein selektiver ER-β-Agonist am Betarezeptor mindestens eine 70‑fach höhere Aktivität aufweisen als am Alpharezeptor [33]. Dies ist bei dem Soja-Isoflavon Genistein der Fall. Die geringe Restaktivität am ER-α genügt, um in den Modellen die Proliferation der Krebszellen zu steigern – aber nur, wenn weder Estradiol noch der Betarezeptor zugegen sind. Dies ist eine Situation, die im menschlichen Organismus nicht anzutreffen ist. Entsprechend wurde bereits mehrfach darauf hingewiesen, dass die Daten aus den In-vitro-Versuchen und Tierexperimenten nicht auf die Verhältnisse im Menschen übertragbar sind [33, 54, 55].
In einer aktuellen Studie wurde untersucht, welchen Einfluss Isoflavone im Modell der MCF-7-Zellen haben, wenn gleichzeitig Estradiol zugegen ist. Dabei ergaben sich neue Erkenntnisse: die getesteten Isoflavone waren in der Lage, die durch Estradiol ausgelöste Zellproliferation zu einem gewissen Grad zu verhindern. Erstmals wurden in dieser Studie auch Blutproben von Frauen eingesetzt, die zuvor mit Isoflavonen supplementiert worden waren. Hier zeigte sich der protektive Effekt besonders ausgeprägt: Selbst bei Einnahme einer Kombination aus Isoflavonen und Estradiol wurde der proliferationsfördernde Effekt von Estradiol an den Krebszellen komplett aufgehoben [56].
Klinische Studien: Bislang keine relevanten Hinweise auf Anwendungsrisiken
Umgekehrt wurde bisher kein relevantes Risiko am Menschen beobachtet, obwohl die Frage der Sicherheit am Endometrium und am Brustgewebe bereits Gegenstand umfangreicher Untersuchungen war, darunter epidemiologische Arbeiten, Fall-Kontroll-Studien und klinische Studien mit Abfrage von Sicherheitsparametern neuesten Datums [18, 23, 57]. In der Studien zur Anwendungssicherheit wurden ohne negative Auswirkungen Dosen bis zu 900 mg Isoflavonen pro Tag verabreicht [58].
Hinweise auf ein potenzielles Risiko schienen sich aus drei Einzelstudien zu ergeben. Alle drei lassen aber bei genauer Betrachtung die Ableitung eines Risikos nicht zu:
In einer offenen, unkontrollierten Anwendungsstudie an 37 Frauen wurden bei insgesamt sieben Frauen nach sechs Monaten der Einnahme von Sojaprotein mit ca. 38 mg Isoflavonen pro Tag Hyperplasien des Brustgewebsepithels festgestellt. Allerdings hatten mehrere Teilnehmerinnen parallel zur Einnahme des Sojaproduktes Hormone zugeführt. Nicht zur These proliferationsfördernder östrogener Effekte der Isoflavone passte zudem, dass die beobachteten Hyperplasien selbst bei Einnahme von Estradiol reversibel waren [59]. Die Autoren schlugen die Überprüfung in einer systematischen Studie vor. Solche Studien wurden mittlerweile ohne Hinweis auf ein Risiko vorgestellt.
Eine weitere unkontrollierte Studie an 48 Frauen mit einer Vorgeschichte von Brustkrebs deutete auf proliferationsfördernde Effekte einer 14-tägigen Einnahme von 45 mg Isoflavonen pro Tag hin [60]. Offenbar handelte es sich hier aber um ein statistisches Artefakt, denn kurz darauf wurde durch die Autoren bei Auswertung der Gesamtzahl von 84 Teilnehmerinnen Entwarnung gegeben – die Vermutung proliferationsfördernder Effekte auf das Brustgewebe konnte ausdrücklich widerlegt werden [61].
Die am häufigsten als Beleg für ein Risiko zitierte Studie ist die Untersuchung von Unfer et al. (2004). In dieser fünfjährigen Studie erhielten 298 Frauen eine Dosis von 150 mg Isoflavonen pro Tag. Am Ende der Studie berichteten die Autoren über einen Anteil von 3,37% Teilnehmerinnen mit einer Hyperplasie des Endometriums, während kein einziger Fall unter Placebo auftrat [62]. Dies allein ist angesichts der natürlichen Häufigkeit von Endometriumhyperplasien bei menopausalen Frauen bereits ein unwahrscheinlicher Befund. Die Studie wies aber noch wesentlich größere Schwächen auf, auf die andere Wissenschaftler deutlich hingewiesen haben [63, 64]: Bereits zu Beginn der Studie waren in der Sojagruppe bei 26,8% und in der Placebogruppe bei 24,8% der Teilnehmerinnen keine auswertbaren Untersuchungsergebnisse am Uterus verfügbar, und auch am Ende der Studie waren 19,5% (Verum) bzw. 24,8% (Placebo) der Biopsien nicht auswertbar. Somit konnten Unfer et al. (2004) weder sicherstellen, dass die beobachteten Fälle von Hyperplasie nicht schon zu Beginn der Studie vorlagen, noch konnten sie bestätigen, dass in der Placebogruppe tatsächlich kein einziger Fall aufgetreten ist. Vor dem Hintergrund dieser und weiterer Mängel sowie der Vielzahl von Studien, welche die Sicherheit von Soja-Isoflavonen an Brust und Uterus belegen, kann die Studie von Unfer et al. (2004) nicht als Bestätigung eines Risikos herangezogen werden.
Nach der gegenwärtigen Datenlage und auf der Basis der Wirkung der Isoflavone über den ER-β ist ein Risiko der Förderung hormonabhängiger Tumoren äußerst unwahrscheinlich – die klinische und epidemiologische Datenlage lässt eher das Gegenteil, nämlich einen Schutzeffekt erwarten.
Die sonstigen Risiken durch Sojapräparate sind eher überschaubar. Die vorliegenden Fallberichte beziehen sich zum größten Teil auf gastrointestinale Unverträglichkeitsreaktionen. Dies spiegelt sich auch in Übersichtsarbeiten klinischer Daten und Gesellschaftsstellungnahmen, in denen explizit auf das positive Sicherheitsprofil der Isoflavone hingewiesen wurde [65, 66].
Die bekannteste potenzielle Nebenwirkung von Sojapräparaten ist die allergische Reaktion. In der Praxis kommt diese bei Anwendung isoflavonhaltiger Zubereitungen durch Frauen in der Menopause nur sehr selten vor. Da die Packungen eindeutig als Sojazubereitungen gekennzeichnet sind, werden Allergiker mit Sojaunverträglichkeit die Einnahme entsprechender Zubereitungen meiden.
Schließlich ist noch die Frage der Anwendungssicherheit bei Schilddrüsenunterfunktion anzusprechen. Aus pharmakologischen Studien am Tier – nicht aber aus Studien am Menschen – wurde die theoretische Möglichkeit abgeleitet, dass Isoflavone eine Schilddrüsenunterfunktion durch Hemmung der Aufnahme von Schilddrüsenhormonen oder eine beschleunigte Ausscheidung von Thyroxin verstärken könnten. Diese Frage wurde in einer aktuellen Übersichtsarbeit betrachtet – mit dem Ergebnis, dass selbst Frauen mit Schilddrüsenunterfunktion keinen Anlass haben, Soja zu meiden [67]. Auch wenn es bislang keinen Hinweis auf eine relevante Beeinflussung des Schilddrüsenstoffwechsels am Menschen gibt, sollte den Patienten sinnvollerweise der Hinweis auf eine ausreichende Iodversorgung und ggf. das Wahrnehmen der regelmäßigen ärztlichen Überwachungstermine gegeben werden.
Fazit
Während einerseits der Nutzen der Isoflavone bei Wechseljahresbeschwerden nachgewiesen und statistisch in Metaanalysen gesichert ist, hat sich die Anwendungssicherheit bislang regelmäßig als sehr gut erwiesen. Das aus speziell für den Nachweis auch kleiner östrogener Effekte konzipierten Untersuchungen abgeleitete theoretische Risiko einer Verstärkung hormonabhängiger Tumoren kollidiert nicht nur mit der umfangreichen Datenlage zur Anwendungssicherheit, sondern auch mit dem Wirkmechanismus.
Selektive ER-β-Agonisten wie Genistein lösen nach heutiger Erkenntnis nicht Krebs aus. Im Gegenteil erhofft man sich von der gezielten Weiterentwicklung solcher Wirkstoffe neue Ansatzpunkte gegen hormonabhängige Tumoren und andere Erkrankungen. Entsprechende Hinweise liegen für Soja aus epidemiologischen Studien schon lange vor.
Bei der Betrachtung der vorrangig in Deutschland geführten Risikodiskussion zu Soja fällt auf, dass den Befunden aus den In-vitro- und tierexperimentellen Untersuchungen mit Hinweisen auf proliferationsfördernde Effekte ein höherer Stellenwert eingeräumt wird als der Vielzahl klinischer und epidemiologischer Befunde sowie experimenteller Daten mit gegenläufigem Ergebnis. Betrachtet man die derzeit vom US-amerikanischen NIH geförderten Forschungsprojekte, so drängt sich der Eindruck auf, dass die Sicherheit der Isoflavone dort längst nicht mehr in Frage gestellt wird – dort stehen die möglichen protektiven Effekte bei verschiedenen Erkrankungen im Vordergrund. Einen Schwerpunkt bilden dabei hormonabhängige Tumoren wie Brust- oder Prostatakrebs.
Es wäre bedauerlich, wenn die Ableitung theoretischer Risiken, extrapoliert aus In-vitro-Versuchen und Tiermodellen mit fraglicher Relevanz für die Situation am Menschen, in der Nutzen-Risiko-Betrachtung Vorrang bekäme vor den extrem umfangreichen Sicherheitsbelegen am Menschen. Der Gesundheit und dem Wohlergehen – nicht nur von Frauen in den Wechseljahren – wäre damit kein Gefallen getan.
Literatur
[1] Kobayashi S. Trends in national nutritional survey of Japan. Nutr Health 1992;8(2-3):91-96.
[2] Yamamoto S, et al. Soy, isoflavones, and breast cancer risk in Japan. J Natl Cancer Inst 2003;95(12):906-913.
[3] Campagnoli C, et al. Polyunsaturated fatty acids (PUFAs) might reduce hot flushes: an indication from two controlled trials on soy isoflavones alone and with a PUFA supplement. Maturitas 2005;51(2):127-134.
[4] Secreto G, et al. Soy isoflavones and melatonin for the relief of climacteric symptoms: a multicenter, double-blind, randomized study. Maturitas 2004;47(1):11-20.
[5] Penotti M, et al. Effect of soy-derived isoflavones on hot flushes, endometrial thickness, and the pulsatility index of the uterine and cerebral arteries. Fertil Steril 2003;79(5):1112-17.
[6] Balk JL, et al. A pilot study of the effects of phytoestrogen supplementation on postmenopausal endometrium. J Soc Gynecol Investig 2002;9(4):238-242.
[7] Khaodhiar L, et al. Daidzein-rich isoflavone aglycones are potentially effective in reducing hot flashes in menopausal women. Menopause 2008;15(1):125-132.
[8] Burke GL, et al. Soy protein and isoflavone effects on vasomotor symptoms in peri- and postmenopausal women: the Soy Estrogen Alternative Study. Menopause 2003;10(2):147-153.
[9] Drapier Faure E, et al. Effects of a standardized soy extract on hot flushes: a multicenter, double-blind, randomized, placebo-controlled study. Menopause 2002;9(5):329-334.
[10] Han KK, et al. Benefits of soy isoflavone therapeutic regimen on menopausal symptoms. Obstet Gynecol 2002;99(3):389-394.
[11] Upmalis DH, et al. Vasomotor symptom relief by soy isoflavone extract tablets in postmenopausal women: a multicenter, double-blind, randomized, placebo-controlled study. Menopause 2000;7(4):236-242.
[12] Albertazzi P, et al. The effect of dietary soy supplementation on hot flushes. Obstet Gynecol 1998;91(1):6-11.
[13] Clementi W, et al. Konsensus: Phytoöstrogene. Frauenarzt 2005;46(11):996-999.
[14] Messina M, Hughes C. Efficacy of soyfoods and soybean isoflavone supplements for alleviating menopausal symptoms is positively related to initial hot flush frequency. J Med Food 2003;6(1):1-11.
[15] Nahas EAP, et al. Efficacy and safety of a soy isoflavone extract in postmenopausal women: A randomized, double-blind, and placebo-controlled study. Maturitas 2007;58(3):249-258.
[16] Gocan A, et al. Placebo-controlled clinical study of soy-isoflavone exhibits significant relief for menopausal symptoms. 7th Congress of the Turkish-German Gynaecological Association (TGGA), Antalya May 16-20 2007.
[17] D‘Anna R, et al. Effects of the phytoestrogen genistein on hot flushes, endometrium, and vaginal epithelium in postmenopausal women: a 1-year randomized, double-blind, placebo-controlled study. Menopause 2007;14(4):648-655.
[18] Cheng G, et al. Isoflavone treatment for acute menopausal symptoms. Menopause 2007;14(3 Pt 1):468-473.
[19] Petri Nahas EA, et al. Benefits of soy germ isoflavones in postmenopausal women with contraindication for conventional hormone replacement therapy. Maturitas 2004;48(4):372-380.
[20] Crisafulli A, et al. Effects of genistein on hot flushes in early postmenopausal women: a randomized, double-blind EPT- and placebo-controlled study. Menopause 2004;11(4):400-404.
[21] Kaari C, et al. Randomized clinical trial comparing conjugated equine estrogens and isoflavones in postmenopausal women: a pilot study. Maturitas 2006;53(1):49-58.
[22] Chantre P. Étude d‘innocuité évaluant les effets d‘un extrait standardisé en isoflavones de soja (Phyto Soys®) sur le sein et l‘endomètre. Phytothérapie 2007;5(4):24-226.
[23] Marini H, et al. Effects of the phytoestrogen genistein on bone metabolism in osteopenic postmenopausal women: a randomized trial. Ann Intern Med 2007;146(12):839-847.
[24] Howes LG, Howes JB, Knight DC. Isoflavone therapy for menopausal flushes: a systematic review and meta-analysis. Maturitas 2006;55(3):203-211.
[25] Nelson HD, et al. Nonhormonal therapies for menopausal hot flashes: systematic review and meta-analysis. JAMA 2006;295(17):2057-2071.
[26] Williamson-Hughes PS, et al. Isoflavone supplements containing predominantly genistein reduce hot flash symptoms: a critical review of published studies. Menopause 2006;13(5): 831-839.
[27] MacGregor CA, et al. A randomised double-blind controlled trial of oral soy supplements versus placebo for treatment of menopausal symptoms in patients with early breast cancer. Eur J Cancer 2005;41(5):708-714.
[28] Van Patten CL, et al. Effect of soy phytoestrogens on hot flashes in postmenopausal women with breast cancer: a randomized, controlled clinical trial. J Clin Oncol 2002;20(6):1449-1455.
[29] Quella SK, et al. Evaluation of soy phytoestrogens for the treatment of hot flashes in breast cancer survivors: A North Central Cancer Treatment Group Trial. J Clin Oncol 2000;18(5):1068-1074.
[30] Kuiper GG, Gustafsson JA. The novel estrogen receptor-beta subtype: potential role in the cell- and promoter-specific actions of estrogens and anti-estrogens. FEBS Lett 1997;410(1):87-90.
[31] Koehler KF, et al. Reflections on the discovery and significance of estrogen receptor beta. Endocr Rev 2005;26(3):465-478.
[32] Heldring N, et al. Estrogen receptors: how do they signal and what are their targets. Physiol Rev 2007;87(3):905-931.
[33] Harris HA. Estrogen receptor-beta: recent lessons from in vivo studies. Mol Endocrinol 2007;21(1):1-13.
[34] Handa RJ, et al. An alternate pathway for androgen regulation of brain function: Activation of estrogen receptor beta by the metabolite of dihydrotestosterone, 5alpha-androstane-3beta, 17beta-diol. Horm Behav 2008;53(5):741-752.
[35] Sarkar FH, et al. The role of genistein and synthetic derivatives of isoflavone in cancer prevention and therapy. Mini Rev Med Chem 2006;6(4):401-407.
[36] Kuiper GG, et al. Comparison of the ligand binding specificity and transcript tissue distribution of estrogen receptors alpha and beta. Endocrinology 1997;138(3):863-870.
[37] McCarty MF. Isoflavones made simple – Genistein‘s agonist activity for the beta-type estrogen receptor mediates their health benefits. Med Hypotheses 2006;66(6):1093-1114.
[38] Remer T, et al. Urinary markers of adrenarche: reference values in healthy subjects, aged 3-18 years. J Clin Endocrinol Metab 2005;90(4):2015-2021.
[39] Mishra RG, et al. Metabolite ligands of estrogen receptor-beta reduce primate coronary hyperreactivity. Am J Physiol Heart Circ Physiol 2006;290(1):H295-H303.
[40] Wright F, et al. Urinary 5 alpha-androstane-3 alpha,17 beta-diol radioimmunoassay: a new clinical evaluation. J Clin Endocrinol Metab 1978; 47(4):850-854.
[41] Labrie F, et al. Marked decline in serum concentrations of adrenal C19 sex steroid precursors and conjugated androgen metabolites during aging. J Clin Endocrinol Metab 1997; 82(8):2396-2402.
[42] Barbaccia ML, et al. Plasma 5alpha-androstane-3alpha,17betadiol, an endogenous steroid that positively modulates GABA(A) receptor function, and anxiety: a study in menopausal women. Psychoneuroendocrinology 2000;25(7):659-675.
[43] Thurston RC, et al. Adiposity and Reporting of Vasomotor Symptoms among Midlife Women: The Study of Women‘s Health Across the Nation. Am J Epidemiol 2008;167(1):78-85.
[44] Butareva LB, I‘lina EM, Balan VE. [Pathogenetic mechanisms of the development of "hot flushes" in patients with climacteric disorders of the sympathetic-adrenal type]. Akush Ginekol (Mosk) 1989;(10):30-33.
[45] Thomson F, Craighead M. Innovative Approaches for the Treatment of Depression: Targeting the HPA Axis. Neurochem Res 2008;33:691-707.
[46] Gruber CJ, et al. Production and actions of estrogens. N Engl J Med 2002;346(5):340-352.
[47] Harris DM, et al. Phytoestrogens induce differential estrogen receptor alpha- or Beta-mediated responses in transfected breast cancer cells. Exp Biol Med (Maywood) 2005;230(8): 558-568.
[48] Harris HA. Preclinical characterization of selective estrogen receptor beta agonists: new insights into their therapeutic potential. Ernst Schering Found Symp Proc 2006;1: 149-161.
[49] Positionspapier der Internationalen und Österreichischen Menopausegesellschaft. Sekretariat Österreichische Menopausegesellschaft 2007.
[50] Schindler AE. Wie sinnvoll ist die Kombination von Sexualsteroiden und Phytohormonen? Gyne 2006;(4):82-84.
[51] Rice S, Whitehead SA. Phytoestrogens and breast cancer – promoters or protectors? Endocr Relat Cancer 2006;13(4): 995-1015.
[52] Mäkelä S, et al. Inhibition of 17beta-hydroxysteroid oxidoreductase by flavonoids in breast and prostate cancer cells. Proc Soc Exp Biol Med 1998;217(3):310-316.
[53] Duffy C, Perez K, Partridge A. Implications of phytoestrogen intake for breast cancer. CA Cancer J Clin 2007;57(5):260-77.
[54] Cheng G, et al. Letter to the Editor. Menopause 2007;14(5): 958-959.
[55] Messina M, McCaskill-Stevens W, Lampe JW. Addressing the soy and breast cancer relationship: review, commentary, and workshop proceedings. J Natl Cancer Inst 2006;98(18):1275-1284.
[56] Imhof M, Molzer S, Imhof M. Supplementation of soy isoflavones protects from 17b-estradiol-induced proliferation of MCF-7 breast cancer cells. Tox in vitro 2007;submitted.
[57] Palacios S, et al. Endometrial safety assessment of a specific and standardized soy extract according to international guidelines. Menopause 2007;14(6):1006-1011.
[58] Pop EA, et al. Effects of a high daily dose of soy isoflavones on DNA damage, apoptosis, and estrogenic outcomes in healthy postmenopausal women: a phase I clinical trial. Menopause 2008;15(4):684-692.
[59] Petrakis NL, et al. Stimulatory influence of soy protein isolate on breast secretion in pre- and postmenopausal women. Cancer Epidemiol Biomarkers Prev 1996;5(10):785-794.
[60] McMichael-Phillips DF, et al. Effects of soy-protein supplementation on epithelial proliferation in the histologically normal human breast. Am J Clin Nutr 1998;68(6 Suppl):1431S-1435S.
[61] Hargreaves DF, et al. Two-week dietary soy supplementation has an estrogenic effect on normal premenopausal breast. J Clin Endocrinol Metab 1999;84(11):4017-4024.
[62] Unfer V, et al. Endometrial effects of long-term treatment with phytoestrogens: a randomized, double-blind, placebo-controlled study. Fertil Steril 2004;82(1):145-8, quiz.
[63] Foth D, Nawroth F. Effect of phytoestrogens on the endometrium? Fertil Steril 2005;83(1):256-257.
[64] Mahady GB. Do soy isoflavones cause endometrial hyperplasia? Nutr Rev 2005;63(11):392-397.
[65] Huntley AL, Ernst E. Soy for the treatment of perimenopausal symptoms – a systematic review. Maturitas 2004;47(1):1-9.
[66] Treatment of menopause-associated vasomotor symptoms: position statement of The North American Menopause Society. Menopause 2004;11(1):11-33.
[67] Messina M, Redmond G. Effects of soy protein and soybean isoflavones on thyroid function in healthy adults and hypothyroid patients: a review of the relevant literature. Thyroid 2006;16(3):249-258.
Anschrift des Verfassers:
Dr. Mathias Schmidt, Herbresearch Germany, Wartbergweg 15, 86874 Tussenhausen-Mattsies




















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.