
- DAZ.online
- DAZ / AZ
- DAZ 20/2008
- Thalidomid zur ...
Arzneimittel und Therapie
Thalidomid zur Erstlinientherapie zugelassen
In Australien und den USA wurde Thalidomid zur Behandlung von Patienten mit multiplem Myelom bereits in den Jahren 2003 und 2006 zugelassen, in Deutschland soll es Mitte des Jahres auf den Markt kommen.
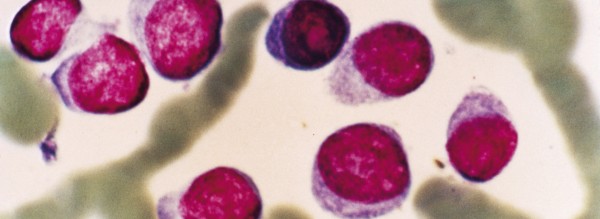
Die Plasmazellen sind betroffen
Das multiple Myelom ist eine Form von Krebs, die eine bestimmte Art von Lymphozyten, die sogenannten Plasmazellen, befällt. Im gesunden Körper sind diese für die Produktion von Antikörpern zuständig. Die Plasmazellen von Myelompatienten sind bösartig entartet und produzieren daher entweder nur noch einen Typ von Antikörper oder auch nur Bruchstücke (sogenannte Leichtketten) davon. Das entsprechende Protein wird Paraprotein genannt und kann bei 99% der Patienten im Blut und/oder Urin nachgewiesen werden. Das Paraprotein (insbesondere die Leichtketten) kann die kleinen Filtrationseinheiten in den Nieren schädigen, weil es sich dort ablagert. Zusätzlich dazu führt die reduzierte Antikörperproduktion bei Myelompatienten zu einer starken Anfälligkeit gegenüber Infektionen.
Die Bezeichnung "multiple" rührt daher, dass der Körper der meisten Patienten mehrere Krankheitsherde an verschiedenen Stellen des Skeletts aufweist, die zu einem Zerfall der Knochenstruktur führen. Der Grund: Die erhöhte Aktivität der bösartigen Plasmazellen im Knochenmark verschiebt das Gleichgewicht zwischen den Knochen aufbauenden Osteoblasten und den Knochen abbauenden Osteoklasten zugunsten der Osteoklasten. Weil das Knochengewebe reich an Calcium ist, wird dieses durch den Abbau in großen Mengen in die Blutbahn freigesetzt. Ein Überangebot an Calcium – Hyperkalzämie – kann die Nieren schädigen.
Verbesserte Erstlinientherapie
Durch die Integration der oral zu verabreichenden Substanz Thalidomid in die bislang üblichen Therapieschemata lässt sich die Erstlinientherapie bei älteren Myelom-Patienten erheblich verbessern. Dies wurde in drei großen randomisierten Studien, in denen Patienten zusätzlich zu Melphalan und Prednison Thalidomid erhielten, mit einer signifikanten Verlängerung des ereignisfreien Überlebens sowie des Gesamtüberlebens belegt. Die Kombination von Melphalan, Prednison und Thalidomid ist damit die neue Standardtherapie in der ersten Behandlungslinie für nicht vorbehandelte Myelom-Patienten in höherem Lebensalter oder bei Kontraindikationen für eine Hochdosistherapie.
Thalidomid wurde von der Celgene Corporation im Rahmen von umfangreichen präklinischen und klinischen Studien erforscht und entwickelt. Im Mai 2006 erhielt die Substanz von der US-Amerikanischen Arzneimittelbehörde (FDA) die Zulassung als orale Therapie in Kombination mit Dexamethason für Patienten mit neu diagnostiziertem multiplem Myelom. Die Australische Zulassungsbehörde (Australian Drug Evaluation Committee – ADEC) erteilte Thalidomide PharmionTM 2008 die Zulassung für eine Kombinationstherapie mit Melphalan und Prednison für Patienten mit multiplem Myelom, die nicht vorbehandelt sind oder für eine Hochdosis-Chemotherapie nicht in Frage kommen. Zudem wurde Thalidomide PharmionTM für eine vorausgehende Induktionstherapie bei einer Hochdosis-Chemotherapie mit autologer Stammzellentransplantation bei nicht vorbehandelten Myelom-Patienten in Kombination mit Dexamethason zugelassen. 2003 erteilte die australische Zulassungsbehörde Thalidomide PharmionTM zudem die Zulassung als Monotherapie für die Behandlung von Patienten mit multiplem Myelom, bei denen Standardtherapien versagt haben.
Thalidomid darf nur im Rahmen eines strengen Sicherheitsprogramms abgegeben und verwendet werden – vor allem in Hinblick auf die Schwangerschaftsprävention. Dieses Sicherheitsprogramm ist Bestandteil der Zulassungen sowohl durch die europäischen wie auch nationalen Zulassungsbehörden.
Auf keinen Fall für Schwangere
Derzeit bereitet Celgene die Einführung von Thalidomid in den deutschen Markt vor, die voraussichtlich im Sommer dieses Jahres erfolgen wird. Ein umfassendes Sicherheitsprogramm, das mit der Einleitung und Durchführung einer Thalidomid-Behandlung verbunden sein wird und das unter anderem den Kontakt Schwangerer mit dem Wirkstoff verhindern soll, ist Bestandteil der Zulassung.
Quelle
Pressemitteilung der Celgene GmbH, München, 21. April 2008.
hel

























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.