
- DAZ.online
- DAZ / AZ
- DAZ 14/2008
- Vorsicht beim Austausch ...
Schilddrüsenhormone
Vorsicht beim Austausch von Levothyroxin
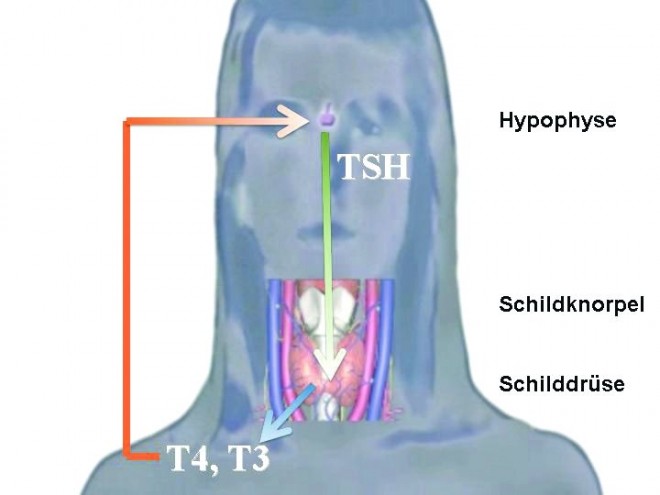
Die Schilddrüse (Thyreoidea) – unterhalb des Schildknorpels am Hals gelegen – ist ein sehr wichtiges Organ, das von den ersten Anfängen des Embryonalstadiums bis zum Lebensende in praktisch alle Funktionen des Organismus eingreift. Die Schilddrüse wirkt über die Produktion der Schilddrüsenhormone Tetraiodthyronin = Levothyroxin (kurz T4 oder Thyroxin) und Triiodthyronin (auch T3 oder Liothyronin). Pro Tag werden etwa 100 µg T4 und 10 µg T3 ins Blut abgegeben (Abb. 1). Dabei ist das T4 eine Art Prohormon, aus dem in der Leber oder den Nieren das eigentliche Wirkhormon T3 durch Abspaltung eines Iodatoms gebildet wird. Gesteuert wird die Schilddrüse durch die Hirnanhangsdrüse (Hypophyse), die über einen Regelkreis mit negativer Rückkopplung die Schilddrüsenhormonproduktion durch die Ausschüttung des Hypophysenhormons TSH (= Thyreoida stimulierendes Hormon) anregt (s. Abb. 1).
Ausreichende Iodversorgung essenziell
In allen Lebensphasen werden Schilddrüsenhormone für die ordnungsgemäße Funktion des Stoffwechsels, der Wärmeproduktion, des Sauerstoffverbrauchs, der Funktion von Nervensystem, Herz und Kreislauf, Muskeln, Keimdrüsen sowie der Ausbildung der Haut und ihrer Anhangsgebilde benötigt.
Voraussetzung für eine ordnungsgemäße Funktion der Schilddrüse ist die ausreichende Zufuhr des Hormonbausteins Iod mit dem Trinkwasser und der Nahrung. Nach aktuellen Erhebungen zur Iodversorgung in den alten und neuen Bundesländern ist davon auszugehen, dass in Deutschland nur etwa 70% der Bevölkerung ausreichend mit Iod versorgt sind, so dass die Bundesrepublik weiterhin als ein Land mit mäßigem Iodmangel zu betrachten ist [2].
Folgen des Iodmangels in Deutschland
Folge des endemischen Iodmangels ist das gehäufte Auftreten von Schilddrüsenvergrößerungen (Strumen) mit und ohne Knoten. Nach einer Screening-Untersuchung in den Jahren 2001 und 2002 [3] an fast 100.000 Freiwilligen finden sich mittels Ultraschall Schilddrüsenauffälligkeiten bei rund einem Drittel der Bevölkerung. Dabei handelt es sich in etwa 10% der Fälle um rein diffuse Vergrößerungen, in rund 15% um Knoten in normal großen Schilddrüsen sowie in weiteren 10% um knotig veränderte vergrößerte Schilddrüsen. Es besteht eine starke Altersabhängigkeit der Auffälligkeiten; sie sind bei über 45-Jährigen etwa dreimal so häufig wie bei unter 30-Jährigen. Eine früher vermutete vier- bis fünfmal größere Häufigkeit von Schilddrüsenauffälligkeiten bei Frauen im Vergleich zu Männern konnte durch die großangelegte Ultraschallstudie nicht bestätigt werden. Auch die früher regional beobachtete Häufung von Schilddrüsenvergrößerungen in gebirgigen Regionen Deutschlands entspricht nicht mehr dem aktuellen Stand der wissenschaftlichen Untersuchungen [3].
Schilddrüsenfunktionist häufig normal
In den allermeisten Fällen gehen die beschriebenen Auffälligkeiten mit einer normalen Schilddrüsenfunktion einher. Bei eigenen epidemiologischen Untersuchungen in Unterfranken fanden sich Schilddrüsenüberfunktionen bei 5% der untersuchten Freiwilligen, wobei unterschwellige, latente Formen der Hyperthyreose im Verhältnis zu symptomatischen, manifesten Formen im Verhältnis 10: 1 standen. Schilddrüsenunterfunktionen sind dem gegenüber nach den Daten aus Unterfranken mit rund 2,5% seltener; diese traten immer als latente Hypothyreosen auf. Auch bei Schilddrüsenfunktionsstörungen besteht eine starke Altersabhängigkeit; typisch ist, dass sich Schilddrüsenüberfunktionen in lange bestehenden knotig veränderten Schilddrüsen aufgrund der sich dort entwickelnden funktionellen Autonomie ("heiße Knoten") manifestieren.
Mittel der Wahl: Levothyroxin
Nach den Ergebnissen der aktuellen epidemiologischen Untersuchungen verwundert es nicht, dass Medikamente zur Behandlung der Iodmangelstruma sehr häufig eingesetzt werden. Levothyroxin zählt mit rund 1 Milliarde definierten Tagesdosen pro Jahr [4] zu den am häufigsten verschriebenen Wirkstoffen in Deutschland. Im Rahmen der Strumatherapie kann es bei normaler Funktion (= Euthyreose) als Monopräparat oder in Kombination mit Iodid effektiv zur Verkleinerung diffuser Schilddrüsenvergrößerungen eingesetzt werden. Bei knotigen Schilddrüsenvergrößerungen dient es in erster Linie dazu, das Knotenwachstum aufzuhalten. Nach Operation von Knotenstrumen wird Levothyroxin zur Rezidivprophylaxe eingesetzt. Dabei erscheint es als sinnvoll, im Falle von iodmangelbedingten Schilddrüsenerkrankungen Kombinationspräparaten mit Levothyroxin und Iodid den Vorzug zu geben [1].
Eine weitere, allerdings wesentlich seltenere Indikation für die Verwendung von Levothyroxin besteht in der Behandlung der Schilddrüsenunterfunktion (Hypothyreose) mit etwa 100 bis 200 µg täglich. Besonders wichtig ist das Thyroxin zur Nachbehandlung des Schilddrüsenkrebses nach Operation und Radioiodtherapie. Bei dieser Indikation wird Levothyroxin als Monopräparat ohne Iodid eingesetzt (ca. 150 bis 300 µg täglich). Bei der Strumatherapie und im Rahmen der Nachsorge des Schilddrüsenkarzinoms geht es darum, das Hypophysenhormon TSH (Abb. 1) zu unterdrücken, das die Schilddrüse nicht nur zur Hormonausschüttung, sondern auch zum Wachstum anregt. Dieser Suppressionseffekt muss bei der Strumatherapie (ca. 75 bis 200 µg täglich) weniger ausgeprägt sein als bei der Nachbehandlung des Schilddrüsenkrebses, wo es sehr darauf ankommt, dass das TSH lebenslang im Zielbereich liegt. Die Lebenserwartung der Schilddrüsenkarzinom-Patienten hängt nämlich – zumindest bei den Patienten mit den Hoch-Risikoformen dieser Erkrankung – eindeutig von der korrekten Einstellung der Levothyroxin-Medikation ab [5].
Individuelle Dosierung ein Muss
Dosiert wird die Levothyroxin-Behandlung immer individuell; d. h. die obigen Angaben zu Tagesdosen können nur zur Orientierung dienen, denn die benötigte Dosis hängt ab von Indikation, Alter, Körpergewicht und Begleiterkrankungen (Fachinformation Levothyroxin). Zielgröße ist das Serum-TSH, dessen Zielbereich bei der Substitution der Hypothyreose bei 0,4 bis 4,0 mU/l, der Strumatherapie bei 0,4 bis 4,0 mU/l und bei der Nachbehandlung des Schilddrüsenkarzinoms bei 0,1 bis 0,5 mU/l liegt. Vier bis sechs Wochen nach Aufnahme oder Änderung der Levothyroxin-Medikation muss das TSH im Serum kontrolliert werden; bei richtig eingestellter Dosierung ist darüber hinaus in der Regel mindestens jährlich eine Kontrolle erforderlich [1].
Im Gegensatz zum Levothyroxin spielt Liothyronin in der Behandlung der Struma und auch der Nachbehandlung des Schilddrüsenkrebses weder als Monopräparat noch in Kombination mit Levothyroxin eine wesentliche Rolle.
Problem: Geringe therapeutische Breite
Levothyroxin ist ein chemisch nicht sehr stabiles Hormon. Die Stabilität ist abhängig von Temperatur, Luft, Licht und Feuchtigkeit. Die Resorption im Darm wird durch bis zu 20 verschiedene Zusatzstoffe in den Präparaten beeinflusst. Bei Einnahme des Levothyroxins 30 bis 60 Minuten vor einer Mahlzeit sind üblicherweise 80% bioverfügbar, bei Einnahme mit der Mahlzeit nur 35%. Die Bioverfügbarkeit ist allerdings abhängig von der galenischen Zubereitung. Der Wirkungseintritt ist nach drei bis fünf Tagen festzustellen, die pharmakologische Halbwertszeit liegt bei etwa sieben Tagen (Fachinformation Levothyroxin).
Jeder Mensch hat – alters- und gewichtsabhängig – einen individuellen "optimalen" Schilddrüsenhormonspiegel, der nur am TSH-Wert im Blut erkennbar ist; dies gilt insbesondere für Kinder, Schwangere, alte Menschen und Schwerkranke. Levothyroxin ist ein Medikament mit geringer therapeutischer Breite [6]; ernsthafte Über- oder Unterdosierungserscheinungen können schon bei Abweichungen von der optimalen Dosis um den Faktor 2 auftreten. Dosierungsempfehlungen – wie oben aufgeführt – stellen aus diesem Grunde nur Anhaltspunkte für die Therapie der verschiedenen Schilddrüsenerkrankungen dar; die individuelle Kontrolle der Einstellung erfolgt über die TSH-Bestimmung (Fachinformation Levothyroxin).
Unerwünschte Wirkungen der Levothyroxin-Therapie können einerseits bei Überdosierung Zeichen der Hyperthyreose mit negativen Auswirkungen insbesondere am Herz-Kreislauf-System und am Skelett und andererseits bei Unterdosierung unter Umständen Zeichen der Hypothyreose – wie Gewichtszunahme und Obstipation – sein. Zu den Wechselwirkungen zählen eine Wirkungsverstärkung von Cumarinen sowie die Wirkungsverminderung von oralen Antidiabetika; andererseits können Colestyramin, Rifampicin, aluminium- und eisenhaltige Präparate sowie Calciumcarbonat die Levothyroxin-Wirkung verringern. (Fachinformation Levothyroxin).
Als Kontraindikationen gelten der akute Herzinfarkt (absolute Kontraindikation) sowie Herzrhythmusstörungen, die koronare Herzkrankheit oder die Myokarditis (relative Kontraindikation).
Latente Hyperthyreose verkürzt Lebenserwartung
Nach einer Untersuchung in England und Wales [8] kann ein erniedrigtes TSH im Sinne der latenten Hyperthyreose bei Patienten mit kardiovaskulären Erkrankungen zu einer deutlichen Verkürzung der Lebenserwartung führen. So zeigte sich in dieser Patientengruppe mit normalem TSH ein Zehn-Jahres-Überleben von etwa 85%, wohingegen dies bei Patienten mit supprimiertem TSH nur bei etwa 70% lag. Kommt es unter Levothyroxin-Medikation zu einer (unerwünschten) kompletten TSH-Suppression, entwickeln sich auch morphologisch Zeichen der Überdosierung am Herzen (wie Wandverdickung), die nach Dosiskorrektur wieder verschwinden [9]. Nach einer aktuellen Metaanalyse [10] findet sich auch bei latenter Hypothyreose eine Korrelation des TSH mit dem kardialen Risiko in der Form, dass Patienten mit einem erhöhten TSH-Wert signifikant häufiger an kardiovaskulären Ereignissen versterben, als Patienten mit normalem TSH. Die Substitution der latenten Hypothyreose wirkt sich nach einer kürzlich publizierten englischen Studie günstig auf die Risikofaktoren für kardiovaskuläre Erkrankungen aus [11]. Diese Studien machen deutlich, wie wichtig es ist, dass das TSH unter der Levothyroxin-Medikation immer im Zielbereich liegt.
Die Arzneimittelzulassungsbehörde der USA beschloss 1997 nach Problemen mit der Bioverfügbarkeit bzw. dem Wirkstoffgehalt verschiedener Levothyroxin-Zubereitungen, dass alle Präparate wie neue Arzneimittel einzustufen sind [7]. Auch in Deutschland auf dem Markt befindliche Levothyroxin-Präparate können sich in ihrer Bioverfügbarkeit unterscheiden. Bei Umstellung von einem auf ein anderes Präparat müssen oben beschriebene Kontrollen des TSH-Spiegels im Blut zum Nachweis der angemessenen Wirksamkeit der Levothyroxin-Medikation zunächst engmaschiger erfolgen. Dies ist bei häufigerem Präparatewechsel mit nicht unerheblichen Kosten verbunden [13].
Levothyroxin-Therapie und Aut-idem-Regelung
Der Begriff "aut idem" stammt aus dem Lateinischen und bedeutet "oder das Gleiche". Im Apothekenrecht wird damit die Möglichkeit des Apothekers beschrieben, statt eines vom Arzt verordneten Arzneimittels ein anderes (kostengünstigeres) wirkstoffgleiches Präparat (Generikum) an den Patienten abzugeben. Das Generikum muss in Dosierung und Verpackungsgröße mit dem verordneten Arzneimittel identisch und für das gleiche Krankheitsbild zugelassen sein. Im Zuge des GKV-Wettbewerbsstärkungsgesetzes sind Apothekerinnen und Apotheker angehalten, nur die Arzneien abzugeben, für die die Krankenkasse des Patienten einen Rabattvertrag mit den Arzneimittelherstellern abgeschlossen hat. Wenn der Arzt allerdings "aut idem" auf dem Kassenrezept angekreuzt hat, darf nur das rezeptierte Präparat abgegeben werden.
Als Generikum bezeichnet man ein Arzneimittel, das eine wirkstoffgleiche Kopie eines bereits unter einem Markennamen zugelassenen, auf dem Markt befindlichen Originalpräparats ist. Voraussetzung für die Zulassung des Originalpräparats ist der Nachweis der Wirksamkeit und Unbedenklichkeit an großen Stichproben "einschlägig" Kranker (in der Regel Stichprobenumfänge deutlich größer als 100 Patienten).
Ein Generikum kann sich bezüglich der Galenik vom Originalpräparat unterscheiden; es darf aber nicht weniger als 80% und nicht mehr als 125% der Bioverfügbarkeit des Originalpräparates haben. Ein Generikum soll dem Originalpräparat therapeutisch äquivalent sein, d. h. es soll ihm in Wirksamkeit und Sicherheit entsprechen [12]. Nachgewiesen werden muss aber nur die Äquivalenz der Bioverfügbarkeit an kleinen Stichproben Gesunder (Stichprobenumfang von 12 ausreichend). Die verfügbaren Bioäquivalenztests für Schilddrüsenhormone sind in ihrer Aussage problematisch, da hierbei unrealistische Dosierungen von 400 bis 600 µg eingesetzt werden müssen.
Experten-Empfehlungen
Die Levothyroxin-Medikation hat – wie dargestellt – unter Kontrolle des Serum-TSH zu erfolgen. Wechselt man das Präparat und fällt der Patient aus dem TSH-Zielbereich, ist die Effektivität der Therapie fraglich und unter Umständen mit Nebenwirkungen zu rechnen. Deswegen sehen amerikanische Fachgesellschaften die Kontrolle des Serum-TSH vier bis sechs Wochen nach einem Präparatewechsel als obligat an [7].
Derartige unverzichtbare Kontrollen machen aber die geringe Ersparnis von jährlich knapp 2 Euro zunichte, die man derzeit erreichen kann, wenn etwa das preiswerteste Levothyroxin (Generikum mit 100 µg) statt eines gleich dosierten Originalpräparates verordnet wird (Unterschied pro Tablette ca. 0,5 Cent). Eine ärztliche Kontrolle mit TSH-Bestimmung kostet die Krankenkassen nämlich 10 bis 25 Euro. Solche Kontrollen könnten auch mehrfach im Jahr fällig werden, wenn immer andere Präparate am preiswertesten sind und dann verordnet werden.
Aus den Darstellungen wird deutlich, dass ein "Präparate-Hopping" in der Therapie von Schilddrüsenerkrankungen mit Levothyroxin aufgrund seiner geringen therapeutischen Breite äußerst problematisch ist. Patienten sind verunsichert; Ärzte müssen kontrollieren [14], ob Patienten das verordnete Präparat oder ein anderes erhalten haben (etwa dadurch, dass sie sich die Packung zeigen lassen). Alternativ können sie natürlich durch ein Kreuz im Feld "aut idem" ausschließen, dass der Patient ein anderes als das verordnete Medikament erhält. Wird aber – warum auch immer – das Präparat gewechselt, muss das TSH kontrolliert werden [15].
Literatur:
[1] Gärtner R, Reincke M: Substitution von Schilddrüsenhormonen. Internist 2008: 1-6
[2] Arbeitskreis Jodmangel: Daten und Fakten zum Stand des Jodmangels und der Jodversorgung in Deutschland, Ausgabe 2007
[3] Reiners C, Wegscheider K, Schicha H, Theissen P, Vaupel R, Wrbitzky R, Schumm-Draeger P: Prevalence of thyroid disorders in the working population of Germany: Ultrasonography screening in 96.278 unselected employees. Thyroid 2004; 14:926-923
[4] Ziegler R, Schwabe U: Schilddrüsentherapeutika. In: Arzneiverordnungsreport 2006. Hrsg. R Schwabe, D Paffrath, Springer Berlin – Heidelberg 2007, 884-892
[5] Cooper DS, Specker B, Ho M, Sperling M, Ladenson PW, Brierley JD, Haugen BR, Klein I, Robbins J, Maxon HR 3rd: Thyrotropin suppression and disease progression in patients with differentiated thyroid cancer: results from the National Thyroid Cancer Treatment Cooperative Registry. Thyroid 1998; 8:737-744
[6] Hennessey JV: Levothyroxine a new drug? Since when? How could that be? Thyroid 2003;13:279-280
[7] American Thyroid Association, The Endocrine Society, and American Association of Clinical Endocrinologists: Joint statement on the U.S. Food and Drug Administrations decision regarding bioequivalence of levothyroxine sodium. Thyroid 2004;14:486-487
[8] Parle JV, Maisonneuve P, Sheppard MC, Boyle P, Franklyn JA: Prediction of all-cause and cardiovascular mortality in elderly people from one low serum thyrotropin result: a 10-year cohort study. Lancet 2001;358:861-865
[9] Mercuro G, Panzuto MG, Bina A, Leo M, Pigliaru F, Mariotti S: Cardiac function, physical exercise capacity, and quality of life during long-term thyrotropin-suppressive therapy with levothyroxine: effect of individual dose tailoring. J Clin Endocr Metabol 2000;85:159-164
[10] Singh S, Duggal J, Molnar J, Maldonado F, Barsano CP, Arora R: Impact of subclinical thyroid disorders on coronary heart disease, cardiovascular and all-cause mortality: a meta-analysis. Int J Cardiol 2008;125:41-48
[11] Razvi S, Ingoe L, Keeka G, Oates C, McMillan C, Weaver JU: The beneficial effects of L-thyroxine on cardiovascular risk factors, endothelial function, and quality of life in subclinical hypothyroidism: randomized, crossover trial. J Clin Endocr Metabol 2007; 92:1715-1723
[12] European Agency for the Evaluation of Medicinal Products: Note for Guidance on the investigation of bioavailability and bioequivalence. London 2001
[13] Hennessey JV: Levothyroxine dosage and the limitations of current bioequivalence standards. Nature Clin Pract Endocrinol Metabol 2006;2:474-475
[14] Diercks C: Auch die unerwünschten Arzneimittelwirkungen der Aut-idem-Präparate sollten Kollegen im Blick halten. Ärzte-Zeitung 140, 2007
[15] Reiners C: Präparate-Hopping ist bei Thyroxin nicht ohne – und spart nichts. Ärzte-Zeitung 142, 2007
Anschrift des Verfassers:
Prof. Dr. Christoph Reiners
Klinik und Poliklinik für Nuklearmedizin
Universität Würzburg
Josef-Schneider-Str.
97080 Würzburg




















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.