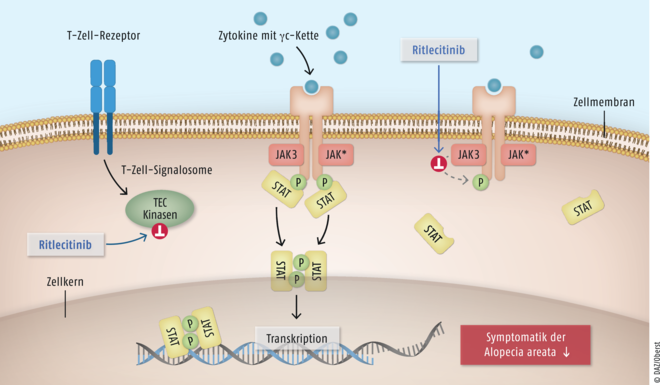
Zulassungsstudie ALLEGRO
Die Zulassung von Ritlecitinib beruht auf der randomisierten, doppelblinden Phase-IIb/III-Studie ALLEGRO mit 718 Erwachsenen und Jugendlichen ab zwölf Jahren [2]. Die Teilnehmer litten seit mehr als zehn Jahren unter einer schweren Alopecia areata mit mindestens 50%igem Kopfhaarverlust. Sie erhielten Ritlecitinib in verschiedenen Dosierungen oder Placebo. In die Auswertung wurden 261 Patienten einbezogen, die mit der therapeutisch relevanten Dosis von 50 mg Ritlecitinib oder Placebo behandelt worden waren. Primärer Endpunkt war das Erreichen eines Wertes von maximal 20 auf der Skala „Severity of Alopecia Tool“ (SALT), entsprechend einer mindestens 80%igen Bedeckung der Kopfhaut mit Haaren.
Innerhalb von 24 Therapiewochen wurde dieser Endpunkt bei etwa 23 % der Patienten aus der Verumgruppe erreicht, im Vergleich zu 1,6 % unter Placebo, entsprechend einer hochsignifikanten Überlegenheit der Ritlecitinib-Therapie (p < 0,0001). Bei mehr als 13 % der Teilnehmer aus der JAK3/TEC-Inhibitor-Gruppe war sogar eine Bedeckung von mindestens 90 % feststellbar, was als Remission eingestuft wurde. Der entsprechende Wert für eine Bedeckung der Kopfhaut von mindestens 80 bzw. 90 % lag in der Placebogruppe bei 1,5 %. Nach 24 Wochen berichteten 49 % der Teilnehmer aus dem Ritlecitinib-Arm, dass sich ihr Erkrankungszustand nach eigener Einschätzung mäßiggradig bis stark verbessert hatte, im Vergleich zu 9 % der Patienten unter Placebo.


























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.