Wirkmechanismus nicht vollständig geklärt
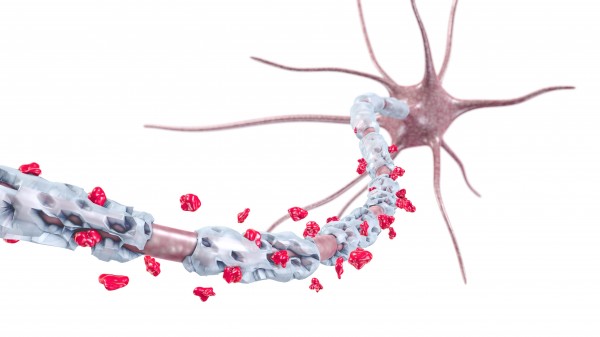
Alemtuzumab ist ein humanisierter monoklonaler IgG-Antikörper mit der Zielstruktur CD52. Der exakte Wirkmechanismus des humanisierten CD52-Antikörpers bei MS ist nicht vollständig geklärt. Vor allem CD3-T-Lymphozyten und CD19-B-Lymphozyten exprimieren das Glykoprotein. Durch Bindung von Alemtuzumab an die CD52-positiven Lymphozyten lösen sie eine komplementvermittelte Zytolyse aus. Die Forschung weist „in Richtung immunmodulatorischer Wirkung“, schreibt die Fachinformation zu Lemtrada®. Hierdurch kommt es wohl zu einer Senkung der zirkulierenden B- und T-Zellen und einer sich anschließenden Repopulation, was die Wahrscheinlichkeit eines erneuten Schubs bei Multipler Sklerose verringert.
Die initiale Behandlung mit Alemtuzuamb umfasst zwei Behandlungsphasen: In der ersten erhalten die MS-Patienten je 12mg Alemtuzumab an fünf aufeinanderfolgenden Tagen. Die zweite Behandlungsphase mit je 12mg Alemtuzumab, nun nur noch an drei aufeinanderfolgenden Tagen, schließt sich ein Jahr später an. Laut Fachinformation können weitere Behandlungsphasen, drei und vier, jeweils weitere zwölf Monate später erfolgen. Auch im dritten und vierten Zyklus erhält der Patient Alemtuzumab je nur an drei Tagen.

























5 Kommentare
MS
von Roswitha Lüer am 08.01.2020 um 16:29 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
MS Anfang
von Roswitha Lüer am 08.01.2020 um 14:41 Uhr
» Auf diesen Kommentar antworten | 1 Antwort
AW: MS Anfang
von Lisa am 24.01.2020 um 12:24 Uhr
Lemtrada-Neueinstellung
von Maria am 07.05.2019 um 17:35 Uhr
» Auf diesen Kommentar antworten | 1 Antwort
AW: Lemtrada-Neueinstellung
von Annemarie am 07.11.2019 um 10:02 Uhr
Das Kommentieren ist aktuell nicht möglich.