
- DAZ.online
- DAZ / AZ
- DAZ 23/2022
- Kleiner als die anderen
Medizin
Kleiner als die anderen
Kleinwuchs bei Kindern und Jugendlichen kann viele Gründe haben
Etwa 3% der in Deutschland geborenen Kinder sind kleinwüchsig. Ein erster Verdacht auf eine Wachstumsstörung kann aufkommen, wenn sich in den ersten ein bis zwei Lebensjahren größere Abweichungen von der Altersperzentile ergeben. Neben Wachstumshormonmangel kommen zahlreiche weitere Ursachen dafür infrage (s. Tab. 1). Kleinwuchs kann aber auch erst im späteren Kindesalter durch zu langsames oder zu früh endendes Wachstum verursacht werden. Lässt sich keine Ursache finden, wird die Diagnose idiopathischer Kleinwuchs gestellt. Dabei liegt die Körperhöhe mindestens zwei Standardabweichungen unterhalb der Norm, die Wachstumsgeschwindigkeit ist normal oder verringert.
Kleinwuchs durch Wachstumshormon-Defizit
Wenn der Kinderarzt andere Ursachen für die Diskrepanz zwischen Körpergröße und dem chronologischen Alter ausgeschlossen hat, erfolgt in der Regel eine Überweisung zum Kinder- und Jugendendokrinologen zwecks Abklärung eines Wachstumshormonmangels (hypophysärer Kleinwuchs). Die Prävalenz dieser Erkrankung wird auf 1 : 4000 bis 1 : 30.000 geschätzt. Der Hormonmangel kann angeboren oder erworben sein, zum Beispiel infolge Traumata, Infektionen, Tumoren, Bestrahlungen des Gehirns oder chirurgischen Eingriffen. Betroffene Kinder haben oft kleine Hände und Füße sowie ein im Verhältnis zum Hirnschädel kleines Gesicht (Puppengesicht). Die Körperproportionen sind jedoch weitgehend normal, sodass die Diagnostik häufig erst mit Verzögerung eingeleitet wird. Die Diagnostik des Wachstumshormonmangels ist komplex. Zu den wichtigsten Laboruntersuchungen zählen Stimulationstests, bei denen die Hypophyse des Kindes beispielsweise durch Insulin oder Arginin zur Ausschüttung von Somatropin angeregt wird. Somatropin ist außer zur Therapie des Wachstumshormonmangels auch bei anderen Grunderkrankungen indiziert, die zu Kleinwuchs führen, wie beispielsweise Prader-Willi- oder Ullrich-Turner-Syndrom (s. Tab. 1). Über die Stimulation des Längenwachstums und der Wachstumsrate hinaus besitzt Somatropin vielfältige Wirkungen auf den Fett-, Kohlenhydrat-, Protein-, Wasser und Mineralstoffwechsel sowie den Knochenmetabolismus. Aus diesem Grund ist das Hormon auch für Erwachsene zugelassen. Außerdem wird es missbräuchlich als Dopingmittel angewendet. Im April dieses Jahres neu eingeführt wurde der Wachstumsfaktor Somatrogon (Ngenla®), der für Kinder und Jugendliche ab drei Jahren zugelassen ist. Es muss nur einmal wöchentlich appliziert werden. Bezüglich der Wachstumsgeschwindigkeit nach sechs Monaten (Aufholwachstum) war Somatrogon dem Somatropin überlegen [9].
Ursache | Charakteristika |
|---|---|
familiärer Kleinwuchs | keine krankhafte Ursache; Wachstumskurve verläuft unterhalb, aber parallel zu Kindern mit Normalgröße |
konstitutionelle Verzögerung von Wachstum und Pubertät | Kleinwuchs nur vorübergehend; erblich bedingte Endgröße wird erreicht, Knochenalter entspricht biologischem Alter |
intrauteriner Kleinwuchs/SGA | SGA sind circa 5% aller Neugeborenen, häufig Aufholwachstum intrauteriner Kleinwuchs: Erkrankungen, Rauchen, Alkoholkonsum der Mutter (fetale Alkoholspektrumstörung), Plazenta-Funktionsstörung oder kindliche Ursachen wie z. B. Infektion |
Skelettdysplasien | Hypo- und Achondroplasie: veränderte Körperproportionen bereits bei Geburt; Probleme durch Gelenkfehlstellungen, u. a. im Erwachsenenalter |
Phosphat-Diabetes: geringe Knochenfestigkeit, typische O-Beinstellung, Nieren- und Zahnprobleme | |
Pseudoachondroplasie: verschobene Körperproportionen mit stark verkürzten Armen und Beinen | |
Spondyloepiphysäre Dysplasie: auffällige Veränderungen an Wirbelsäule und Knochenenden | |
chromosomale Störungen | Ullrich-Turner-Syndrom (nur bei Mädchen/Frauen): fehlendes oder verändertes X-Chromosom, zahlreiche Körperregionen und Organe betroffen |
Down-Syndrom (Trisomie 21), unterschiedlich ausgeprägte Einschränkungen und Behinderungen | |
Veränderungen im Short-stature Homeobox Gene (SHOX-Gen) | |
syndromale Erkrankungen | Noonan-Syndrom: ähnelt Ullrich-Turner-Syndrom, aber normaler Chromosomensatz |
Prader-Willi-Syndrom: defektes Gen auf Chromosom 15, Kleinwuchs, Muskelhypotonie, geistige Behinderung | |
sekundärer Kleinwuchs | Wachstumsstörung hat organische Ursache: Herzinsuffizienz, schweres Asthma, gastrointestinale, renale, muskuläre, neurologische oder chronisch-entzündliche Erkrankungen, auch schwere Unter- oder Fehlernährung |
endokrin (hormonell) bedingter Kleinwuchs | Wachstumshormonmangel, Cushing-Syndrom |
Hypothyreose | |
Diabetes mellitus | |
unzureichende Sexualhormonspiegel (hypogonadaler Kleinwuchs) | |
Laron-Syndrom (Wachstumshormonrezeptor-Defekt) | |
primärer IGF-1-Mangel | |
metabolische Störungen | Störungen des Metabolismus von Kohlenhydraten, Proteinen, Lipiden, Calcium und Phosphat |
psychosoziale Ursachen | psychosoziale Deprivation, Anorexia nervosa, Depression |
iatrogene (ärztlich bedingte) Ursachen | hochdosierte lokale (Inhalationen, intestinale Klysmen) oder systemische Glucocorticoid-Therapie, Schädel- oder Ganzkörperbestrahlung, Chemotherapie |
IGF-1 Mangel kann viele Ursachen haben
Der Insulin-ähnliche Wachstumsfaktor 1 (IGF-1) ist ein Peptidhormon, dessen strukturelle Ähnlichkeit zu Insulin namensgebend war. Er wird von der Leber nach Bindung von Somatropin an seinen dortigen Rezeptor (growth factor receptor, GFR) freigesetzt. Nach Bindung an den IGF-1-Rezeptor stimuliert IGF-1 in verschiedenen Geweben Wachstumsprozesse. Aufgrund dieser Hormonkaskade kann es zu einem IGF-1-Mangel nicht nur durch Mutationen im IGF-1-Gen, sondern beispielsweise auch durch Mutationen beim GFR kommen. Eine Behandlung mit Wachstumshormon würde dann nicht zum Erfolg führen. Für diese Kinder (im Alter zwischen zwei und 18 Jahren) steht mit Mecasermin (Increlex®) eine Therapieoption zur Verfügung. Zu den Voraussetzungen zählt unter anderem, dass die basale IGF-1-Konzentration unterhalb der 2,5ten Perzentile für Alter und Geschlecht liegt und ausreichend Wachstumshormon produziert wird. Außerdem müssen vor der Behandlung sekundäre Formen des IGF-1-Mangels wie Unterernährung, Hypophysenvorderlappen-Insuffizienz, Schilddrüsenunterfunktion oder eine Dauerbehandlung mit Steroiden ausgeschlossen werden.
Phosphat-Diabetes behandeln
Unter den Störungen des Knochenstoffwechsels als Ursache von Kleinwuchs gehört die X-chromosomale Hypophosphatämie (Synonyme: hypophosphatämische Rachitis, Phosphat-Diabetes) zu den medikamentös behandelbaren Erkrankungen. Phosphat-Diabetes tritt mit einer Häufigkeit von 1 : 20.000 auf. Er wird zwischen dem ersten und zweiten Lebensjahr, wenn die meisten Kinder frei laufen können, sichtbar. Zusätzlich zur geringen Körpergröße ist das Gangbild dieser Kinder breitbeinig-watschelnd, außerdem können Knochenschmerzen sowie eine gestörte Zahnentwicklung auftreten. Häufigste Ursache des Phosphat-Diabetes ist die Veränderung eines Gens auf dem kurzen Arm des X-Chromosoms, das ein Protein zur Regulation des Fibroblasten-Wachstumsfaktor 23 (FGF-23) kodiert. FGF-23 hemmt die renale Phosphat-Reabsorption und die renale Vitamin-D-Synthese. Eine Überaktivität von FGF-23 führt zu erhöhter renaler Phosphat-Ausscheidung und damit zur Hypophosphatämie. Die Calcitriol-Sekretion ist ebenfalls beeinträchtigt. Dadurch wird die Knochenmineralisation gestört. Die Diagnose erfolgt hauptsächlich durch Röntgenuntersuchungen, Bestimmung von Laborparametern wie beispielsweise Phosphat, Kreatinin und FGF-23 im Blut bzw. Urin. Auch ein molekulargenetischer Nachweis ist möglich. Vor der 2018 erfolgten Zulassung von Burosumab (Crysvita® Injektionslösung), einem rekombinanten humanen monoklonalen Immunglobulin(Ig)1-Antikörper gegen FGF-23, wurden die Kinder mit oralen Phosphat-Präparaten und Vitamin-D3-Derivaten behandelt. Burosumab ist indiziert bei Kindern und Jugendlichen im Alter von einem bis 17 Jahren mit röntgenologischem Nachweis einer Knochenerkrankung sowie auch bei Erwachsenen. Er bindet an das überaktive FGF-23 und hemmt dessen Aktivität. Dadurch wird die tubuläre Rückresorption von Phosphat gesteigert, auch die Serumkonzentration von Calcitriol nimmt zu. Defekte im Knochenwachstum und -umbau werden positiv beeinflusst.
Angeborene Krankheit Achondroplasie
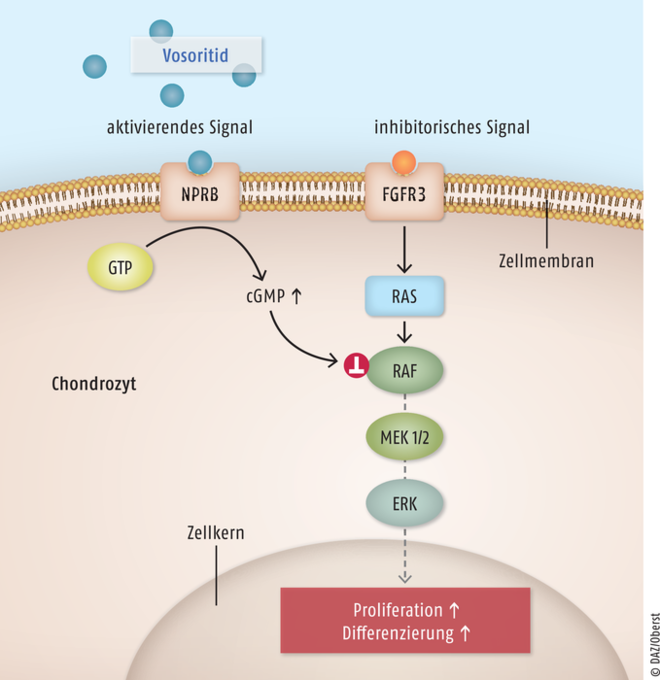
Auch die Achondroplasie zählt mit einer Prävalenz von 0,4 bis 0,6 pro 10.000 Geburten zu den seltenen Erkrankungen. Unbehandelt wird im Erwachsenenalter nur eine Körpergröße von 125 bis 140 cm erreicht. Zusätzlich treten beispielsweise Disproportionen (z. B. großer Schädel), Achsenfehlstellungen der Gliedmaßen und Wirbelkanalstenosen auf. Die betroffenen Kinder fallen bereits bei der Geburt durch einen großen Kopf, kurze Arme und Beine sowie eine stark überstreckte Lendenwirbelsäule auf. Außerdem können die Hüftgelenke und Ellbogen nicht ganz gestreckt werden, bei Knie- und Handgelenken ist dagegen eine Überstreckung möglich. Ursache der Achondroplasie ist eine Punktmutation im Gen für den Fibroblasten-Wachstumsfaktor-3 (FGFR3) auf Chromosom 4. FGFR3 ist eine Rezeptor-Tyrosinkinase, die hemmend in die Proliferation und Differenzierung von Chondrozyten eingreift. Durch die Mutation kommt es zur übermäßigen Hemmung und damit zu Störungen im Knochenwachstum, insbesondere der Röhrenknochen. Seit Oktober 2021 ist Vosoritid (Voxzogo® Injektionslösung) zur Behandlung von Achondroplasie bei Patienten ab dem zweiten Lebensjahr zugelassen. Es handelt sich um ein Analogon des natürlichen natriuretischen Peptids vom Typ C (CNP), einem Regulator des endochondralen Knochenwachstums. Vosoritid hemmt wie das natürliche Peptid durch Bindung an den natriuretischen Peptidrezeptor B (NPR-B) die nachgeschaltete FGFR3-Signalübertragung (s. Abb. 2). Dadurch werden die Proliferation und Differenzierung der Chondrozyten gefördert, eine Zunahme des Längenwachstums ist die Folge. Vosoritid wird bei Patienten ab zwei Jahren angewendet, bei denen die Epiphysenfugen noch nicht geschlossen sind.
Eine andere Mutation im FGFR3-Gen führt zur Hypochondroplasie, die der Achondroplasie ähnelt, jedoch weniger schwerwiegend ist. Für diese Kleinwuchsform steht noch keine Therapie zur Verfügung.
Abb. 2: Vosoritid bindet als Analogon des C-natriuretischen Peptids (CNP) an den Rezeptor B für natriuretische Peptide (NPRB) auf der Oberfläche von Chondrozyten (Knorpelzellen). Es kommt zu einer verstärkten Bildung von zyklischem Guanosinmonophosphat (cGMP), das die inhibitorische Fibroblasten-Wachstumsfaktor-Rezeptor-3(FGFR3)-Signalisierung durch Hemmung des MAP-Kinase-Signalwegs auf der Ebene von RAF-1 (Rapidly-Accelerated-Fibrosarcoma-1) antagonisiert. Als Folge wirkt Vosoritid wie endogenes CNP stimulierend auf die Proliferation und Differenzierung von Chondrozyten und damit auf das endochondrale Knochenwachstum.
Unterstützung bei der Anwendung
Durch die Beratung in der Apotheke können die Familien bei der richtigen Anwendung der Arzneimittel gegen Kleinwuchs vielfältig unterstützt werden. Somatropin-Präparate werden in Deutschland von verschiedenen Herstellern angeboten (s. Tab. 2). Dabei handelt es sich um Einmalpens (Fertigpens) oder wiederbefüllbare Pens mit auswechselbaren Kartuschen. Diese Kartuschen sind teilweise Zweikammer-Patronen für die getrennte Aufbewahrung von Lyophilisat (weißes Pulver) und Lösungsmittel. Beim Zusammenschrauben des Injektionsgerätes fließt das Lösungsmittel in die Kammer mit dem Pulver und löst dieses auf. Zum besseren Auflösen kann der Pen vorsichtig geschwenkt werden. Ein Schütteln ist aber unbedingt zu vermeiden, um die Denaturierung des Wirkstoffes zu verhindern.
Wichtig ist auch der Hinweis, das Wachstumshormon täglich etwa zur gleichen Zeit zu verabreichen. Ideal ist die Zeit vor dem Schlafengehen, da auch die physiologische Ausschüttung von Wachstumshormon vorwiegend nachts erfolgt. Die Injektionsstelle muss täglich gewechselt werden, um eine Lipatrophie in diesem Bereich zu vermeiden.
Bei Vosoritid schreibt die Fachinformation vor, dass die Behandlung von einem Arzt begonnen und geleitet werden muss, der im Management der Achondroplasie und skelettalen Dysplasien qualifiziert ist. In Deutschland haben sich an verschiedenen Unikliniken (z. B. Berlin, Köln, Leipzig, Ulm, Tübingen) sowie weiteren Krankenhäusern (z. B. Klinikum Bremen Nord, Ev. Klinikum Bethel, Bielefeld) Ärzte auf diese Behandlung spezialisiert und setzen Vosoritid ein. Sie sind in einer Liste auf der Website des Bundesverbands Kleinwüchsige Menschen und ihre Familien e. V. (BKMF, www.bkmf.de) zu finden. |
Präparat (Beispiele) | Firma | Indikationen im Kindes- und Jugendalter |
|---|---|---|
Genotropin® Injektionslösung Genotropin Miniquick® | Pfizer | Wachstumshormonmangel, Ullrich-Turner-Syndrom, chronische Niereninsuffizienz, SGA, Prader-Willi-Syndrom |
Humatrope® für Pen | Lilly | Wachstumshormonmangel, SGA, Ullrich-Turner-Syndrom, chronische Niereninsuffizienz, Wachstumsstörung infolge SHOX-Mangel (durch DNA-Analyse bestätigt) |
Norditropin® Flexpro | Novo Nordisk | Wachstumshormonmangel, SGA, Ullrich-Turner-Syndrom, chronische Niereninsuffizienz, Wachstumsstörung aufgrund eines Noonan-Syndroms |
NutropinAq® | Ipsen Pharma | Wachstumshormonmangel, Ullrich-Turner-Syndrom, chronische Niereninsuffizienz |
Omnitrope® Injektionslösung (Biosimilar) | Sandoz | Wachstumshormonmangel, SGA, Ullrich-Turner-Syndrom, chronische Niereninsuffizienz, Prader-Willi-Syndrom |
Saizen® Injektionslösung | Merck | Wachstumshormonmangel, SGA, Ullrich-Turner-Syndrom, chronische Niereninsuffizienz, |
Zomacton® Injektionslösung | Ferring Arzneimittel | Wachstumshormonmangel, Ullrich-Turner-Syndrom |
Literatur
[1] Diagnostik des Wachstumshormonmangels im Kindes- und Jugendalter. S2e-Leitlinie der Deutschen Gesellschaft für Kinderendokrinologie und –diabetologie (Kurzfassung), Stand 24. Juli 2021, AWMF-Registernr. 174/004
[2] Geisslinger G, Menzel S, Gudermann T, Hinz B, Ruth P. Mutschler - Arzneimittelwirkungen. Pharmakologie Klinische Pharmakologie Toxikologie. 11. Auflage, Wissenschaftliche Verlagsgesellschaft Stuttgart 2020
[3] Hereditäre hypophosphatämische Rachitiden. S1-Leitlinie der Deutschen Gesellschaft für Kinderendokrinologie und -diabetologie (DGKED) e. V. u. a. Fachgesellschaften, Stand März 2016, AWMF-Registernr. 174/008
[4] Kleinwuchs. S1-Leitlinie der Deutschen Gesellschaft für Kinderendokrinologie und -diabetologie (DGKED) e. V. in Zusammenarbeit mit der Deutschen Gesellschaft für Kinder- und Jugendmedizin (DGKJ) e. V., Stand Dezember 2016 (Gültigkeit abgelaufen), AWMF-Registernr. 174/004
[5] Phosphatdiabetes. Doccheck-Flexikon, www.flexikon.doccheck.com/Phosphatdiabetes
[6] Neubeck M. Vosoritid (Voxzogo®). Neue Arzneimittel 2022;1:2-4, www.deutsche-apotheker-zeitung.de/pharmazie/arzneimittel1
[7] Informationen des Bundesverbands Kleinwüchsige Menschen und ihre Familien e. V. (BKMF), www.bkmf.de
[8] Informationen des „Forum Wachsen“, www.forumwachsen.de, unterstützt von Ferring Arzneimittel GmbH, Lilly Deutschland GmbH, Merck Healthcare Germany GmbH, Novo Nordisk Pharma GmbH, Pfizer Pharma GmbH, Hexal AG (Sandoz Deutschland)
[9] Ngenla® 24 mg/ 60 mg Injektionslösung im Fertigpen. Fachinformation der Pfizer Pharma GmbH, Stand: März 2022























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.